Prevalencia de Trypanosoma cruzi en triatominos silvestres de Nuevo León, México
Trypanosoma cruzi in triatomines from Nuevo Leon, Mexico
Zinnia Judith Molina-Garza, Dra en CI; José Luis Rosales-Encina, Dr en CII; Lucio Galaviz-Silva, Dr en CI; Daniel Molina-Garza, MCPI
ILaboratorio de Patología Molecular, Facultad de Ciencias Biológicas, Universidad Autónoma de Nuevo León. Monterrey, México
IIDepartamento de Patología Experimental, Centro de Investigación y Estudios Avanzados del Instituto Politécnico Nacional. México
RESUMEN
OBJETIVO: Determinar la prevalencia de Trypanosoma cruzi en triatominos Triatoma gerstaeckeri de Nuevo León, mediante la estandarización de una técnica inmunoenzimática.
MATERIAL Y MÉTODOS: Se colectaron 52 chinches en General Terán, N.L. desde julio hasta septiembre de 2005, las cuales se analizaron por microscopía óptica (MO) y reacción en cadena de la polimerasa (PCR) como estándares de referencia para establecer una técnica de detección del parásito por el ensayo inmunoabsorbente ligado a enzimas (ELISA).
RESULTADOS: Por MO y PCR, 31 triatominos fueron positivos y 21 negativos; por ELISA los resultados difieren con 27 positivos y 25 negativos (100% de especificidad, 87% de sensibilidad, 84% de valor predictivo negativo y 100% de valor predictivo positivo). Por MO y PCR, la prevalencia de triatominos infectados fue de 59.61% y por ELISA, de 51.92%; por lo que se confirmó la utilidad, rapidez y elevado índice de confianza del ensayo de ELISA.
CONCLUSIÓN: Los resultados obtenidos por la técnica de ELISA son útiles para enfocar los nuevos estudios epidemiológicos con un mayor número de vectores, ya que fue posible analizar simultáneamente la mayor cantidad de muestras, con niveles de sensibilidad y especificidad elevados y a menor costo que el PCR; por lo tanto, se recomienda para programas de vigilancia epidemiológica preventiva como primera prueba de tamizaje, antes de realizar análisis confirmatorios por PCR.
Palabras clave: Trypanosoma cruzi; Triatoma gerstaeckeri; ELISA; PCR; Nuevo León; México
ABSTRACT
OBJECTIVE: To determine the prevalence of Trypanosoma cruzi in triatomines from Nuevo León using the standardization of an improved enzyme-linked immunosorbent assay test. ]]>
MATERIALS AND METHODS: From July to September 2005, 52 triatomines were captured in General Terán, a municipality located in Nuevo León. They were analyzed using optical microscopy (OM) and a polymerase chain reaction (PCR), as standards of reference, to develop a technique for detecting the parasite using enzyme-linked immunosorbent assay (ELISA).
RESULTS: Using OM and PCR, 31 triatomines were found to be positive and 21 negative. Using ELISA, 27 samples were identified as positive and 25 negative (specificity 100%, sensitivity 87%, negative predictive value 84%, and positive predictive value 100%). The prevalence of infected triatomines was 59.61% with OM and PCR, and 51.92% with ELISA. Our data confirm that the ELISA assay in triatomines is a fast, reliable and useful tool.
CONCLUSIONS: Since it was possible to simultaneously analyze a large number of samples with high sensibility and specificity values, the ELISA test proves to be useful for new epidemiologic studies having a high number of vectors. It is also less expensive than PCR. It is therefore recommended for epidemiological and preventive surveillance programs as a first screening test before conducting a confirmatory test using PCR.
Key words: Trypanosoma cruzi; Triatoma gerstaeckeri; ELISA; PCR; Nuevo Leon; Mexico
La enfermedad de Chagas es una zoonosis causada por Trypanosoma cruzi, un hemoprotozoario flagelado transmitido a vertebrados susceptibles por hemípteros hematófagos de la subfamilia Triatominae. Está restringida al área continental de América, por lo que se denomina también tripanosomiasis americana.1 Infecta aproximadamente de 16 a 18 millones de individuos en América Latina y es la mayor causa de enfermedades cardiacas en áreas endémicas. La mayoría de los individuos permanecen infectados a lo largo de su vida. De 30 a 40% de los pacientes chagásicos desarrollan una enfermedad crónica inflamatoria que comúnmente resultan en cardiomiopatías y disfunciones del tracto gastrointestinal.2
La transmisión natural de T. cruzi en la que interviene el vector se lleva a cabo en tres ciclos: el doméstico, en el cual el vector infesta de manera exclusiva la vivienda humana en áreas rurales y suburbanas; el peridoméstico, donde se mantienen alrededor de núcleos de población humana, y el enzoonótico, que se presenta alejado de asentamientos humanos y con participación exclusiva de reservorios silvestres y ecotopos naturales.3
En México, la distribución geográfica de las especies de Triatominos colectados entre 1993 y 1999 abarca la mayoría de los estados de la República.4 En Nuevo León, los vectores incluyen a Triatoma gerstaeckeri (Stål), T. neotomae (Neiva), T. lecticularia (Stål) y T. protracta (Uhler), de las cuales T. protracta y T. neotomae se han colectado en hábitats silvestres, mientras que T. gerstaeckeri y T. lecticularia han sido detectados a nivel peri e intradomiciliarios.5
El papel de Triatoma gerstaeckeri como vector primario de T. cruzi en Nuevo León fue dado a conocer en 1947;6 sin embargo, los hábitos domiciliarios y predomiciliarios apenas se estudiaron recientemente.5 La importancia de la cepa neolonesa (cepa NL) de T. cruzi, ha sido demostrada por el comportamiento histotrópico y patogenicidad, y se caracteriza como cepa miotrópica, debido a que se aloja y reproduce en músculo estriado, fibra de miocardio y músculo liso principalmente, ocasionando así daños severos a nivel tisular y celular de los hospederos inoculados experimentalmente, corroborados por microscopía óptica (MO) y microscopía electrónica de transmisión (MET).7
]]> Dada la importancia de la enfermedad, elaboramos una estrategia para la detección y diagnóstico de la cepa NL de Trypanosoma cruzi en triatominos, con base en las técnicas inmunológicas, como el ensayo inmunoenzimático (ELISA) para conocer la sensibilidad y especificidad, y se emplearon MO y PCR como estándares de referencia para la evaluación. Además, este estudio permite actualizar los datos del nivel de infección natural por T. cruzi en triatominos, ya que los anteriores datan de 1992.5,8Consideraciones éticas: el presente trabajo se realizó de acuerdo con el Reglamento de la Ley General de Salud en Materia de Investigación, el cual establece que los estudios deberán diseñarse de tal manera que eviten al máximo el sufrimiento de los animales. El Comité de Ética de la Facultad de Ciencias Biológicas aprobó el protocolo del estudio.
Material y métodos
El ejido de San Juan de Vaquerías está constituido por las comunidades de Vaquerías, Nuevo Vaquerías, La Gloria, Huizachito, Las Delicias y El Maguey, donde se distribuyen 125 domicilios habitados por 650 personas, aproximadamente, y se ubica en General Terán del estado de Nuevo León. Las casas son de adobe; algunas tienen techos de carrizo o palmito y otras de lámina acanalada; el piso es de tierra con puertas y ventanas de madera o leños. Sólo en Nuevo Vaquerías las casas son de block y cemento.9
Población estudiada
Por disección de nidos de ratas de campo Neotoma micropus, se capturaron 52 chinches T. gerstaeckeri desde julio hasta septiembre del 2005. Se colectaron las heces de cada una de las chinches, por separado, en microtubos cónicos de 1.5 mL, y se examinaron en un microscopio óptico (MO) de campo claro para identificar la infección natural en cada una de ellas. Las fotografías representativas de los tripomastigotes se digitalizaron con una videocámara miniVID (Image Driving Software, LW Scientific, Inc.) de frotis teñidos con Giemsa (CTR Scientific).
Preparación de las muestras
Las heces de los triatominos se diluyeron en 200 µL de agua; se hirvieron 10 min. y se centrifugaron a 8 000 g durante 10 min.; se recuperó el sobrenadante (SN1) en dos tubos por separado, uno para la técnica de ELISA y otro para la amplificación del DNA por la técnica de PCR, y se conservaron a -70ºC. El precipitado se resuspendió en 100 µL de solución de lisis NETN (Tris-HCl 10mM, pH 7.4, 1mM EDTA, 1.0% de Nonidet 40, 0.01% de dodecil sulfato de sodio), enriquecida con urea 10mM y fenilmetanosulfonil fluoruro (PMSF 1mM), y se incubó por 10 min. a 37ºC.10 Posteriormente, éste se centrifugó a 10 000 g y se colectó el sobrenadante 2 (SN 2). Después se adicionó a los SN1 y SN2 un volumen (100µL) de buffer de carbonatos 2X, pH 9.8 y se conservó a 4ºC para la técnica de ELISA.11
Preparación del extracto antigénico de T. cruzi
]]> Para estandarizar la técnica de ELISA se usó un extracto antigénico proporcionado por el doctor Rosales-Encina (jefe del Laboratorio de Patología Experimental del Cinvestav-IPN), obtenido de cultivos de epimastigotes de la cepa Y de T. cruzi. El extracto soluble se colocó en cada pozo de las placas de poliestireno (Costar, Hybond-Cambridge, MA, EUA), aforado a 50 mL con buffer de carbonatos (0.1 M, pH 9.6) a una concentración final de 10, 20 y 50 µg/mL, determinados con el estuche de BIO-Rad, usando como estándar albúmina sérica bovina (Bio-Rad Hercules, CA, EUA) para estandarizar la concentración más apropiada. Estas mismas concentraciones se usaron como controles positivos en los ensayos.Preparación del primer anticuerpo
El primer anticuerpo antiepimastigote se obtuvo inoculando ratones por vía intraperitoneal con el extracto total del parásito citado anteriormente. Después, el suero de los ratones se diluyó por duplicado de 1/500 hasta 1/128 000 con buffer de fosfatos-(NaCl 0.15 M, NaH2 PO4 10 mM, pH 7.2) y albúmina sérica bovina al 1% (PBS-BSA). En la estandarización, el primer anticuerpo en la dilución 1/500 µL en PBS registró una densidad óptica de 1.861 (0.1 mg/mL). La dilución 1/1000 presentó una absorbancia de 1.543 (0.050 mg/mL) y disminuyó proporcionalmente con las diluciones hasta alcanzar una lectura 0.093 en la de 1/128 000 (0.0003306 mg/mL). La dilución seleccionada para el primer anticuerpo correspondió a 1/8000, con 0.432 de absorbancia.
Procedimiento del ELISA
Se colocaron 50 µL de la mezcla SN1+SN2 por duplicado en los pozos de la microplaca, y se incubaron a 4ºC durante toda la noche. Después, los pozos se lavaron con PBS/Tween 20 al 0.05% (PT) tres veces y se bloquearon con PBS-BSA 1% por 1 hora, a 37ºC. Posteriormente se lavaron tres veces con PT y se agregaron 50 µL del anticuerpo antiepimastigote en cada pozo, a la dilución establecida, y se incubaron durante dos horas, a 37ºC. Los pozos se lavaron tres veces con PT para colocar 50 µL del segundo anticuerpo, que consistió en IgG+IgA+IgM antirratón, unida a la enzima peroxidasa (Zymed Lab. Inc., San Francisco, CA, EUA), diluido 1:4000 (según las recomendaciones del fabricante) en PBS-BSA, y se incubaron durante 1 hora, a 37ºC. Después de lavar los pozos tres veces con PT, se agregó el substrato OPD (0.04% ortofenilendiamina en buffer citrato pH 5 y 0,04% v/v de H2O2 al 30%) para el desarrollo de color de la reacción. Luego de incubar a temperatura ambiente y en la oscuridad por 30 min., la reacción se detuvo con 50 µL/pozo de H2SO4 1 N.11 Los valores de absorbancia fueron registrados de igual forma que los controles positivos, a 492 nm, con un lector de microplacas (Bio-Rad, CA). La lectura de corte se estableció mediante una curva de calibración con diluciones del extracto antigénico de la cepa Y, y se ubicó en una absorbancia de 0.130, equivalente a 10 µg/mL del extracto.
Extracción del DNA total
De los 100 µL del SN1 conservados a -70ºC, se realizaron extracciones de ácidos nucleicos totales con DNAzol (Molecular Research Center Inc.) o con la técnica de fenol/cloroformo,10 conservando el DNA en 50 µL de buffer TE (10mM tris-HCl pH 7.4, 1 mM EDTA). Para la obtención de los fragmentos de los minicírculos del DNA del kinetoplasto, 18 µL del DNA total se digirieron con 0.5 µL de la enzima Nsi I diluida 1:5, para liberar fragmentos de 380 pares de bases (pb) descritas en la literatura.12,13
Amplificación del kDNA por PCR
Se amplificó el kDNA de las 52 muestras digeridas con Nsi I, utilizando el kit de PCR de alta fidelidad (Expand High Fidelity PCR System, Roche Molecular Biochemicals), que incluye amortiguador de PCR (20mM TrisHCl pH 7.5; 100mM KCl, 1mM DTT, 0.1mM EDTA, 0.5% Tween 20, 0.5% glicerol v/v), mezcla de enzima Taq DNA polimerasa (2.6 U por reacción) y 1.5 mM de MgCl2. Los dNTP's se mezclaron a una dilución de trabajo de 10mM. Se sintetizaron primers de la región hipervariable de los minicírculos del kinetoplasto a 0.2 µM, con base en los descritos previamente por Monteón-Padilla y colaboradores,12 con secuencia KNS1 5' GGG GTT CG A TTG GGG TTG GTG TA-3' y KNS2 5'-AAA (G/T)TT GAA CGC CCC TCC CAA A-3', los cuales amplifican productos de 293-340 (pb).12 Las secuencias se verificaron con las registradas en el GenBank (Nº acceso AJ747944.1).
El programa de amplificación consistió en 35 ciclos, cada uno de 94ºC/1 min., 56/1 min. y 72/1 min.;12,13 se utilizó el termociclador JM Resarch. Posteriormente los productos amplificados fueron electroforados en geles de agarosa al 1% y teñidos en bromuro de etidio para visualizarse con la luz UV del transiluminador (Fotodyne, Inc.).
]]> Análisis estadísticoPara comparar las técnicas diagnósticas entre sí, y determinar el grado de confiabilidad estadística, se utilizó un análisis de ji-cuadrada (c2), mediante una tabla de contingencia de 3 x 2 (P> 0.05) con dos grados de libertad, con el paquete estadístico SPSS (Statistical Package for Social Sciences, ver 10.0, SPSS Inc., Chicago, Illinois, EUA). Se definió la hipótesis nula como la falta de dependencia entre las técnicas y resultados.14 La sensibilidad, especificidad, el valor predictivo positivo (VPP) y el valor predictivo negativo (VPN) de la técnica de ELISA, se determinaron con base en el análisis recomendado.15,16
Resultados
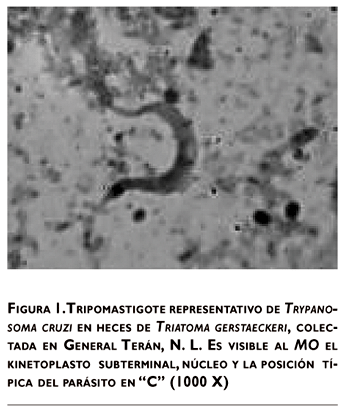
Se capturó un total de 52 triatominos (Triatoma gerstaeckeri) en Vaquerías, General Terán, N. L., de las cuales en 31 se identificó T. cruzi en las deyecciones por medio de la técnica de MO, y se observaron en los frotis teñidos con Giemsa, los tripomastigotes alargados, con extremos agudos, kinetoplasto oval, alargado, cerca del extremo posterior y el núcleo en posición media (figura 1).

Por PCR se confirmó la identificación de T. cruzi en las 31 muestras que provenían de los sobrenadantes SN1 de los mismos triatominos previamente identificados por MO. Se obtuvieron los productos esperados de 313 pb en 12 muestras (figuras 2A y 2B) y 293 pb en 19 de las deyecciones (10 de estos amplicones se presentan en la figura 2C), correspondientes a la amplificación de la región hipervariable del kDNA. Los resultados de MO y PCR aquí citados se consideraron como estándares de oro para la comparación posterior con los resultados del inmunoensayo por ELISA.
]]>
Detección de la cepa NL de Trypanosoma cruzi por medio de la técnica de ELISA
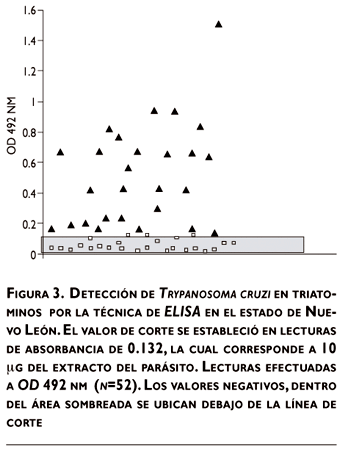
Con la lectura de corte a una absorbancia de 0.130, la cual corresponde a 10 µg/mL de extracto antigénico, se identificaron 25 triatomas como negativas, con valores desde 0.02 hasta 0.130 y 27 muestras positivas de la cepa NL de T. cruzi (cuadro I), en un rango de absorbancias entre 0.133 y 1.594, los cuales se presentan en la figura 3, donde se omite la lectura de los controles positivos de los extractos antigénicos de la cepa Y, utilizada para la obtención del primer anticuerpo para el inmunoensayo aquí descrito.
]]>

Análisis estadístico de la técnica de ELISA
En la tabla de contingencia se obtuvo la c2= 1.231 < c2 0.05= 5.99. Debido a que el valor de la ji cuadrara con dos grados de libertad fue menor que la de las tablas, se aceptó la hipótesis nula de que la ocurrencia de positivos y negativos no depende de la técnica utilizada (cuadro I). La sensibilidad y especificidad de MO y PCR fue de 100%, en ambos casos, al igual que VPP y VPN. Para la técnica de ELISA, la sensibilidad fue de 87%, y una especificidad con VPP de 100% y un VPN de 84% (cuadro II).
]]>

El índice de infección natural en T. gerstaeckeri por T. cruzi fue de 59.61% con base en los resultados obtenidos por MO y PCR, mientras que la técnica de ELISA detectó el 51.92%.
Discusión
Hasta hace algunos años, era necesario inocular animales experimentales o bien efectuar xenodiagnósticos para la identificación de T. cruzi o confirmar el diagnóstico clínico.17 Asimismo, el examen de las deyecciones de triatominos silvestres se realizaba en forma cotidiana en los programas epidemiológicos de la enfermedad de Chagas.18 Actualmente, las técnicas inmunológicas y de biología molecular facilitan esta labor, y disminuyen el tiempo requerido de aproximadamente 21 días o más a algunas horas.
Este trabajo confirma la utilidad y beneficios de las técnicas de ELISA y PCR en comparación con los estudios tradicionales, ya que los resultados obtenidos demuestran que la metodología desarrollada mediante la técnica de ELISA detecta T. cruzi en muestras de heces de triatominos naturalmente infectados, con elevados porcentajes de sensibilidad (87%) y especificidad (100%). Al aplicar la técnica de ELISA utilizando como extracto antigénico la cepa Y, se indica que los anticuerpos antiepimastigote producidos en ratón detectan de igual forma la cepa NL. Los estudios sobre las aplicaciones de técnicas inmunoenzimáticas para diagnóstico de T. cruzi en sueros humanos y los nuevos antígenos recombinantes son numerosos.19,20
Avances recientes también se han conseguido con los antígenos recombinantes obtenidos por la clonación de varios genes de T. cruzi para usarlos en el diagnóstico de la enfermedad de Chagas en pacientes, con lo que se obtuvo hasta 99% de especificidad cuando se utilizaron dos péptidos sintéticos de T. cruzi en combinación;19-21 sin embargo, se ha logrado obtener una especificidad de 84% en sueros de pacientes chagásicos, utilizando un antígeno recombinante obtenido por clonación de un fragmento de DNA de T. cruzi que codifica un antígeno inmunodominante repetitivo llamado H49. El péptido H49 reaccionó en el ensayo de ELISA con pacientes de tripanosomiosis americana, pero no con los sueros de pacientes que padecían alguna otra enfermedad parasitaria como leishmaniasis.22
En este estudio con ELISA obtuvimos valores de sensibilidad de 87% con base en la lectura de corte de absorbancia establecida. Sin embargo, este valor no afecta la utilidad de la prueba por ser de 13% de casos positivos no detectados, si se comparan el tiempo y esfuerzo que ahorra el investigador, con los análisis tradicionales al MO, examinando una a una las deyecciones de los triatomas, por lo que se considera aceptable. El valor de 100% de especificidad y VPP significa que el análisis de ELISA no detectó falsos positivos con el valor de corte de absorbancia antes citado, y aumenta el beneficio de la aplicación de esta técnica.
El VPN de 84% es aceptable, si se considera que cuantifica los triatominos que no presentaron el parásito y, al igual que el VPP, es altamente influenciable por la prevalencia, ya que, si ésta se incrementa, el VPP también aumenta y el VPN disminuye.15 En otro trabajo similar, pero con sueros humanos, se comparó la sensibilidad, especificidad, VPP y VPN en inmunoflorescencia, hemaglutinación y ELISA para detectar anticuerpos anti-T. cruzi, y se menciona que ELISA es el método de elección por tener resultados más altos y sólo requerir pequeñas cantidades de eluido o suero, además de procesar diariamente una gran cantidad de muestras.23
]]>Conclusión
El método inmunoenzimático desarrollado para la detección de T. cruzi en heces de triatominos es rápido y simple, y permite el análisis simultáneo de numerosas muestras con elevados índices de especificidad y sensibilidad. Sin embargo, no se encontraron antecedentes sobre la aplicación de técnicas inmunoenzimáticas para la detección de T. cruzi en triatominos, por lo que se considera de gran utilidad por el ahorro de tiempo y esfuerzo para el análisis de triatominos silvestres, peridomiciliarios o domiciliarios en los estudios de vigilancia epidemiológica que se desarrollan en América Latina.
La estrategia en el diseño de la presente investigación fue dirigido para determinar la efectividad de la técnica de ELISA en la detección de T. cruzi en heces de triatomas, por lo que no se realizó una colecta representativa de triatominos en la localidad de estudio, lo cual podría ser una limitante en el diseño de la investigación, aunque existen reportes previos sobre los índices entomológicos en el área de colecta.5,8
En cuanto a la técnica de PCR, se detectaron cuatro muestras positivas más que la técnica de ELISA, debido a que se seleccionó la lectura de corte más alta dentro del intervalo o rango de absorbancia (0.132% A). Estas cuatro muestras se obtuvieron con lecturas cercanas a este valor, oscilando entre 0.110-0.132% A, y se registraron como negativas. El resultado corrobora la utilidad de ELISA como una técnica de barrido o de monitoreo para estudios epidemiológicos y la técnica de PCR como confirmatoria.16 Si se hubiera definido un límite de corte más bajo en ELISA, habríamos excluido todos los resultados sospechosos,23 ya que los valores negativos con densidad óptica mayor de 0.1 fueron positivos por PCR, lo cual puede indicar que el punto de corte de 0.1-0.13 son valores indeterminados. También podría ser que las muestras del presente estudio estuvieron más diluidas, pues no se obtuvieron en un cultivo puro como en la cepa Y, sino que se tomaron de las heces directamente. De acuerdo con el análisis estadístico, no existe diferencia para el diagnóstico en las técnicas aplicadas, aunque cabe aclarar que el examen efectuado por microscopía óptica se realizó varias veces durante dos semanas y fue necesario extraer las heces de los triatomas en repetidas ocasiones para corroborar si éstas eran o no positivas al diagnóstico.
En relación con el PCR, fue posible amplificar el DNA de T. cruzi, con la utilización de los oligonucleótidos KNS1 y KNS2, debido a que se diseñaron para una región hipervariable del kinetoplasto, presente entre diversas variedades de T. cruzi.12 Estos primeros fueron diseñados originalmente para detectar la cepa Y, AWP CL y la cepa Ninoa mexicana, debido a que existe una alta homología en la secuencia nucleotídica.12,13 Los minicírculos corresponden a un DNA satélite que codifica para una proteína teórica que une calcio.12 Cada minicírculo presenta cuatro regiones de secuencias repetidas. Un solo parásito contiene de 10 000 a 20 000 minicírculos, y se presenta desde 40 000 hasta 80 000 veces la secuencia repetida en cada parásito,12 lo que lo convierte en un excelente templado para la reacción de PCR.
Por ser una región satelital hipervariable, los amplicones presentan tallas esperadas de 293 de acuerdo con las secuencias analizadas en el GenBank, y entre 313 a 340 pb, tal como ha sido reportado.12 En este estudio, en 19 muestras la técnica de PCR amplificó productos de 293 pb, pero en 12 deyecciones se encontraron productos de 313 pb, lo que, probablemente, indique la presencia de dos cepas diferentes o distinto linaje de T. cruzi, que pretenden analizarse en estudios futuros.
La secuencia de primers utilizada, descrita originalmente por Monteón-Padilla y colaboradores,12 fue verificada previamente con los registros existentes de los minicírculos del kDNA en el GenBank, y se encontró una elevada homología con la cepa brasileña P209 del parásito, aislada del roedor Dasyprocta aguti (Nº acceso AJ747944.1) y corresponde al linaje I de T. cruzi. Esta secuencia contiene 293 nucleótidos y la talla coincide con los resultados citados en este estudio. También pueden encontrarse variaciones con tallas menores a las obtenidas, como es el caso particular de la secuencia AJ748069 registrada en el GenBank, que corresponde al linaje II e de T. cruzi, la cual amplificaría con amplicones de 282 pb.
Resultados similares sobre la aplicación del PCR para la detección de T. cruzi en vectores por PCR y la identificación de distintas cepas del parásito han sido descritos previamente en la literatura;24 pero la metodología utilizada refiere menor capacidad de detección. En heces de T. infestans, Rhodnius pictipes y Triatoma sordida, en 1995 se reportó 85.3% de concordancia respecto a la detección por MO.24 Asimismo, análisis recientes del kDNA muestran un alto grado de variabilidad en T. cruzi, y acentúan el intenso polimorfismo que presentan las formas clínicas del parásito.25,26,*
La caracterización molecular de las cepas mexicanas de T. cruzi ha avanzado enormemente en los últimos años. Se han analizado 17 cepas mexicanas y cinco sudamericanas y se ha demostrado la heterogeneidad génica dentro de las mismas cepas que permiten la formación de grupos relacionados con el origen geográfico. Además, sugirieron que el análisis del DNA del kinetoplasto puede representar un método simple para diagnóstico en monitoreos epidemiológicos.27
]]> En Nuevo León, es necesario crear conciencia en las personas acerca de la importancia de salud pública que tiene la enfermedad, y de mantener una vigilancia permanente en muestras de bancos de sangre debido a que es una zona con un flujo creciente de inmigrantes del sur de México y Centroamérica. Es necesario, además, tomar medidas de control para el vector; disminuir su colonización en áreas suburbanas y urbanas y realizar fumigaciones periódicas en las viviendas con insecticidas de efecto residual, pues el índice de infección natural en los triatomas silvestres es alto (59.61%), tal como se ha reportado en estudios realizados en la misma localidad.5,7 En estos estudios, hubo una oscilación entre 14 y 80%, y se confirmó la importancia de T. gerstaeckeri como vector en el estado. El índice de infección natural es incluso más elevado que el que ocurre en otros estados del país reconocidos por su endemicidad a la enfermedad de Chagas, como Guerrero, donde alcanza 32.4% en T. pallidipennis.13,18,26
Referencias
1. Benenson AS. El control de enfermedades transmisibles en el hombre: Informe oficial de la Asociación Estadounidense de Salud Pública. 15a. edición. Pub Cient 1992;538. [ Links ]
2. Duthie MS, Kahn M, White M, Kapur RP, Kahn SJ. Critical proinflammatory and anti-inflammatory functions of different subsets of CD1d-restricted natural killer T cells during Trypanosoma cruzi infection. Infect Immun 2005;73:181-192. [ Links ]
3. Pinto-Días JC. Epidemiology of Chagas' disease. En: Wendel S, Brener Z, Camargo ME, eds. Chagas' disease (American Tripanosomiasis): Its impact on transfusions and clinical medicine. A ISBT Brazil'92 1992:49-80. [ Links ]
4. Vidal-Acosta V, Ibáñez-Bernal S, Martinez-Campos C. Natural Trypanosoma cruzi infection of triatominae bugs associated with human habitations in Mexico. Salud Pública Mex 2000;42:496-503. [ Links ]
5. Martínez-Ibarra A, Galaviz-Silva L, Trujilla C. Distribución de los triatominos asociados al domicilio humano en el municipio de General Terán, Nuevo León, México. Southwestern Entomol 1992;17:261-265. [ Links ]
6. Aguirre-Pequeño E. Una nueva distribución geográfica de los triatomas naturalmente infectados por Trypanosoma cruzi en la República mexicana. Arch Med Mex 1947;8:350-358. [ Links ]
7. Galaviz-Silva L, Ramírez E, Vázquez V. Histotropismo y patogenicidad de Trypanosoma cruzi en ratón albino (NHI) aislado de triatominos en Nuevo León, México. Bol Chil Parasitol 1992;47:3-10. [ Links ]
8. Galavíz-Silva L, Arredondo JM, Ramírez V. House Triatomineae at the San Juan de Vaquerías Comunal Land ("Ejido") in Nuevo León, México. J Border Health 1991;7:16-25. [ Links ]
9. Instituto Nacional de Estadística, Geografía e Informática. Disponible en://www.inegi.gob.mx/est/contenidos/espanol/proyectos/censos/ce2004 [consultado el 22 de noviembre, 2005]. [ Links ]
10. Sambrook J, Russell DW. Molecular Cloning. A laboratory Manual. 3rd edition. Nueva York: Cold Spring Harbor Laboratory Press, 2001; vol.3:18.67-18.68. [ Links ]
11. Maizels RM, Blaxter ML, Robertson BD, Selkirk ME. Parasite antigens, parasite genes. A laboratory manual for molecular parasitology. Cambridge: University Press, 1988. [ Links ]
12. Monteón-Padilla VM, Reyes PA, Rosales JL. Detección de Trypanosoma cruzi en muestras experimentales por el método de reacción en cadena de la ADN polimerasa. Arch Inst Cardiol 1994;64:135-143. [ Links ]
13. Sosa-Jurado F, Mazariego-Aranda M, Hernández-Becerril N, Garza-Murillo V, Cárdenas M, Reyes PA, et al. Electrocardiographic findings in Mexican chagasic subjects living in high and low endemic regions of Trypanosoma cruzi infection. Mem Inst. Oswaldo Cruz 2003;98:605-610. [ Links ]
14. Fleiss JL. Statistical methods for rates and proportions. 2a. edition. New Cork: John Wiley and Sons, 1981. [ Links ]
15. Thrusfield M. Veterinary Epidemiology. 2a. edition. UK: Blackwell Science Ltd, 1995:22-179. [ Links ]
16. Altman DG. Practical statistics form medical research. Londres: Chapman and Hall, 1991. [ Links ]
17. Goldsmith RS, Zarate RJ, Zárate LG, Kagan I, Jacobson LB, Morales G. Estudios clínicos y epidemiológicos de la enfermedad de Chagas en Oaxaca, México, y un estudio complementario de siete años, Cerro del aire. Bol of Sanit Panam 1986;100:145-166. [ Links ]
18. Becerril-Flores M, Valle-de la Cruz A. Descripción de la enfermedad de Chagas en el valle de Iguala, Guerrero, México. Gac Med Mex 2003; 139:539-544. [ Links ]
19. Franco da Silveira J, Umezawa ES, Luquetti AO. Chagas disease: recombinant Trypanosoma cruzi antigens for serological diagnosis. Trends Parasitol 2001;17:286-290. [ Links ]
20. Gruber A, Zingales B. Trypanosoma cruzi: characterization of two recombinant antigens with potential application in the diagnosis of Chagas' disease. Exp Parasitol 1993;76:1-12. [ Links ]
21. James MB, Shreffler WG, Rosman DE, Sleath PR, March CJ, Reed SG. Identification and synthesis of a major conserved antigenic epitope of T cruzi. Proc Natl Acad Sci 1992;9:1239-1243. [ Links ]
22. Paranhos-Bacalla GS, Santos MR, Cotrim PC, Rassi A, Jolivet ME, Camargo M, et al. Detection of antibodies in sera from Chagas' patients using a Trypanosoma cruzi immunodominant recombinant antigen. Parasit Immunol 1994;16:165-169. [ Links ]
23. Zicker F, Smith PG, Luquetti A, Oliveira OS. Detección de Infectados por Trypanosoma cruzi mediante inmunofluorescencia, ELISA y Hemaglutinación en suero y eluidos de sangre seca. Bol of Sanit 1991; 110:489-497. [ Links ]
24. Breniere SF, Obsceno MF, Telleria J, Carrasco R, Vargas F, Yasik N, et al. Field application of polymerase chaín reaction diagnosis and strain typing of Trypanosoma cruzi in Bolivian triatomines. Am J Trop Med Hyg 1995;53:179-184. [ Links ]
25. Lages-Silva E, Ramírez LE, Pedroza AL, Crema E, da Cunha LM, Junho Pena SD, et al. Variability of kinetoplast DNA gene signature of Trypanosoma cruzi II strains from patients with different clinical forms of Chagas' disease in Brazil. J Clin Microbiol 2006;44:2167-2171. [ Links ]
26. Segura EL, Escobar-Mesa A. Epidemiología de la enfermedad de Chagas en el estado de Veracruz. Salud Pública Mex 2005;47:201-208. [ Links ]
27. Zavala-Castro J, Velasco O, Hernández R. Molecular characterization of mexican socks of Trypanosoma cruzi using total DNA. Am J Trop Med Hyg 1992;47:201-209. [ Links ]
Fecha de recibido: 9 de marzo de 2006
Fecha de aceptado: 23 de agosto de 2006
Solicitud de sobretiros: Dra. Zinnia Judith Molina. Unidad B, Laboratorio de Patología Molecular, Facultad de Ciencias Biológicas, Universidad Autónoma de Nuevo León. Av. Universidad s/n, col. Universitaria. 66451 San Nicolás de los Garza, Monterrey, Nuevo León, México. Correo electrónico: molinazinnia@hotmail.com
* Telleria J, Lafay B, Virreina M, Barnabe C, Tibayrenc M, Svoboda M. Trypanosoma cruzi: sequence analysis of the variable region of kinetoplast minicircles. Exp Parasitol 2006. En prensa.