
Compactabilidad como un parámetro de funcionalidad del excipiente GalenIQ 720
Compactibility as a functionality parameter of the excipient GalenIQ 720
Liliana Samayoa-Sandoval, Leopoldo Villafuerte-Robles
Departamento de Farmacia, Escuela Nacional de Ciencias Biológicas, Instituto Politécnico Nacional
]]>Correspondencia:
Dr. Leopoldo Villafuerte Robles
Departamento de Farmacia, Escuela Nacional de Ciencias
Biológicas, Instituto Politécnico Nacional de México
Av. Wilfrido Massieu s/n esq. M. Stampa, Unidad
Profesional Adolfo López Mateos.
Col. Industrial Vallejo, C. P. 07738, D. F. México.
E-mail: lvillaro@encb.ipn.mx;
lvillarolvillaro@hotmail.com
Fecha de recepción: 18 de diciembre de 2012.
Fecha de recepción de modificaciones: 18 de junio de 2013.
Fecha de aceptación: 23 de julio de 2013.
Resumen
Los valores específicos de las propiedades tecnológicas permiten establecer parámetros estadísticos y límites para el uso de los excipientes. El propósito del trabajo es la evaluación de la compactabilidad de GalenIQ 720 como excipiente para compresión directa. El excipiente se valora individualmente y en mezclas con metronidazol y con estearato de magnesio, comparándose contra Helmcel 200. Los parámetros determinados son curvas de compactabilidad utilizando la resistencia a la ruptura y resistencia a la tensión. La compactabilidad de Helmcel 200 es 2-3 veces mayor que la de GalenIQ 720. Sin embargo, GalenIQ 720 muestra una mejoría de la compactabilidad en mezclas con un lubricante, contra la conocida pérdida de compactabilidad de la celulosa microcristalina. La mejora de una característica del fármaco, por un excipiente, puede ser usada como parámetro de funcionalidad.
Palabras clave: Resistencia a la ruptura, Resistencia a la tensión, Características tecnológicas, Metronidazol, lubricantes.
Abstract
]]> Specific values of technological properties of excipients allow the establishment of statistical parameters and limits for their use. The purpose of the work is the evaluation of GalenIQ 720 as direct compression excipient. The excipient is evaluated individually and in mixtures with metronidazole and magnesium stearate, comparing against Helmcel 200. The assessed parameters include compactibility curves using the crushing strength and tensile strength. The compactibility of Helmcel 200 is 2-3 times higher than that of GalenIQ 720. However, GalenIQ 720 exhibits an increased compactibility in mixtures with a lubricant, against the known fall of compactibility of microcrystalline cellulose. The improvement of a drug characteristic by an excipient can be used as a parameter of functionality.Key words: Crushing strength, Tensile strength, Technological characteristics, Metronidazole, lubricants.
Introducción
Las formas de dosificación de medicamentos pueden ser sistemas muy complejos. La calidad de los medicamentos no sólo depende de los principios activos y procesos de producción, sino también de los excipientes.1 Por esta razón, es de importancia conocer la funcionalidad de los excipientes en la etapa previa a la formulación ya que de este modo se puede estimar cuál sería su desempeño en la forma farmacéutica.2
Las sustancias activas difícilmente poseen las propiedades físicas deseadas para su procesamiento y la adición de excipientes se vuelve una necesidad. La mayoría de las formas de dosificación requieren de la adición de excipientes para apoyar su fabricación y su administración. En las tabletas se incluyen diluentes, aglutinantes, lubricantes, desintegrantes y deslizantes. Los excipientes se utilizan en cantidades variables para ajustar la funcionalidad de las formulaciones. Su función va más allá del concepto tradicional de ser inertes, para progresivamente ser materiales más específicos y funcionales.3,4
Actualmente, es reconocido que el desempeño de una forma de dosificación está íntimamente ligado a las propiedades tecnológicas, físicas y químicas de todos los ingredientes en la formulación. Las formas farmacéuticas están constituidas, a menudo, en su mayor parte por excipientes. De hecho, los excipientes regularmente suelen constituir hasta el 90% en peso de la formulación y, por tanto, pueden influir de manera importante en el desempeño de los fármacos. De ello, se deduce que el desempeño de una forma de dosificación no se puede separar de la funcionalidad de los excipientes que la constituyen.5
Un concepto fundamental de los excipientes es que el desempeño de una forma farmacéutica depende de su estructura. El objetivo del control del proceso de manufactura es el acomodar todos los componentes del producto dentro de esa estructura. Las propiedades mecánicas, la velocidad de disolución y la estabilidad física y química están determinadas por las propiedades de las materias primas y de cómo ellas se distribuyen y se mantienen unidas dentro de la forma farmacéutica. Por lo tanto, para obtener resultados satisfactorios en las propiedades de las formas farmacéuticas se controlan los atributos de las materias primas y de los productos intermedios, durante cada etapa del proceso de producción. El control tiene como finalidad el mantener los atributos mencionados dentro de un intervalo específico, p. e., operando dentro del espacio de diseño de los atributos de cada material.6
La compactación, referida a los polvos farmacéuticos, consiste de procesos simultáneos de compresión y consolidación de un sistema de dos fases (partículas sólidas-gas) debido a la aplicación de una fuerza. El término compactación de los polvos se usa, generalmente, para describir una situación en la cual estos materiales se someten a la aplicación de algún nivel de fuerza mecánica.7
Las propiedades de compactación de los polvos farmacéuticos se caracterizan a través de su compresibilidad y su compactabilidad. La compresibilidad es la capacidad de los polvos para deformarse o disminuir su volumen cuando se someten a una presión. La compactabilidad se define como la capacidad de un material para formar aglomerados coherentes o compactos mecánicamente fuertes después de su compresión. Sin embargo, para fines prácticos, se entiende como la capacidad de un polvo para ser transformado en un comprimido de una resistencia específica. La compactabilidad se ha cuantificado de diversas maneras; con mayor frecuencia se expresa como la pendiente de una curva de resistencia a la tensión o de resistencia a la ruptura contra la presión de compactación (perfil de compactabilidad).8,9
]]> Uno de los procedimientos para caracterizar y clasificar las propiedades mecánicas de los materiales farmacéuticos es una combinación de pruebas sobre los compactos y sobre la compresión del polvo.Otro procedimiento utiliza las pruebas en los compactos como un medio para derivar una serie de índices de la habilidad para la formación de las tabletas. La compresión de los polvos es un método atractivo para el análisis, desde el punto de vista estadístico así como desde el punto de vista del consumo de material. Sin embargo, se ha reconocido que las variaciones en las condiciones de aplicación de la carga durante la compresión así como en el manejo de los datos pueden afectar el resultado de los parámetros de compresión que de ello se deriven. De esta manera, la estandarización tanto de las variables experimentales así como del manejo de los datos sería crítico para la reproducibilidad de los datos de compresión de los polvos. Además, el uso de las ecuaciones de compresión basadas en la porosidad de las tabletas representa un problema especial para el análisis de las propiedades de las partículas granuladas.10
Durante el estudio de la evolución de la resistencia la tensión de las tabletas, conforme se incrementa la presión de compactación, se ha observado que la resistencia a la tensión aumenta hasta un cierto límite. Posteriormente, con mayores aumentos en la presión de compactación la resistencia a la tensión de las tabletas se nivela. El perfil de compactabilidad completo tiende hacia una forma sigmoidea.11
Los perfiles de compactabilidad con una forma sigmoidea se han descrito con una ecuación basada en la distribución de Weibull (Ec. 1).12,13 Recientemente, este modelo se ha utilizado para describir la compactabilidad de celulosas, como un indicativo de su funcionalidad como excipientes para tabletas.14

Dónde: D es la dureza o Resistencia a la ruptura de las tabletas, Dmax es la dureza máxima alcanzada por las tabletas, Pc es la presión de compactación, n es la pendiente de la curva e I es el intercepto de la curva.
La compactabilidad de los materiales estudiados se ha definido con los parámetros de regresión obtenidos con la Ec. 1. Las curvas de compactabilidad así obtenidas describen la relación entre la dureza o resistencia a la ruptura de las tabletas y la presión de compactación usada para obtenerlas.
Otro parámetro importante para la caracterización del comportamiento mecánico de comprimidos farmacéuticos es la resistencia a la tensión. En las pruebas de compresión diametral, las tabletas cilíndricas se comprimen diametralmente hasta que estas se rompen o colapsan. La fuerza de compresión se registra y la resistencia a la tensión se calcula a partir de la fuerza de compresión y de las dimensiones de los comprimidos. En este caso, la compactibilidad se describe como la resistencia a la tensión (σ) de la tableta y se expresa con la ecuación:15
σ = 2D/(π * d * h) Ec. 2
Dónde: D es la dureza o resistencia a la ruptura, d es el diámetro y h es la altura o grosor de la tableta.
]]> El logaritmo de la resistencia a la tensión contra la densidad relativa de la tableta daría una relación lineal. Este tratamiento de los datos experimentales permite calcular la compactabilidad como la resistencia a la tensión de tabletas con una porosidad de cero o con una densidad relativa de 1 (σmax) y con la pendiente (k). Esta última, se dice que es indicativa de la capacidad del polvo considerado para formar enlaces entre las partículas. Un valor alto de k correspondería a una unión fuerte de las partículas primarias.16La relación del logaritmo de la resistencia a la tensión contra la densidad relativa antes mencionada se deriva de la ecuación de Ryshkewitch-Duckworth (1953) (Ec. 3), en la cual la resistencia a la tensión de un aglomerado (S) es igual a la resistencia a la tensión a un valor de la porosidad igual a cero (So) multiplicada por la base de los logaritmos naturales elevada un exponente con signo negativo, de una constante k multiplicada por la porosidad del aglomerado (ε). 16,17
S = So * e-kε Ec. 3
En la relación exponencial anterior el valor de la constante k cambiaría su valor cuando la ecuación se linealiza con logaritmos de base natural o de base 10. Sin embargo, la relación entre las variables seguiría siendo lineal y los valores calculados de resistencia a la tensión para tabletas de una porosidad igual a cero o con una densidad relativa de 1 serían los mismos.
Las tabletas deben tener suficiente resistencia mecánica para resistir el desgaste o ruptura durante su manipulación o procesamiento, particularmente durante el empaque. Por esta razón, la dureza de las tabletas tiene importancia y relevancia práctica.18
El desempeño funcional de los excipientes para tabletas está relacionado con sus propiedades físicas, químicas y tecnológicas. Este desempeño se puede determinar con los excipientes como polvo, como forma de dosificación de los excipientes puros y como una formulación de un fármaco dado conteniendo los excipientes. Los primeros dos niveles corresponden a una funcionalidad subrogada que pertenece a la fase de preformulación. El conocimiento de la funcionalidad subrogada (excipientes puros) permite predecir si es que un excipiente particular tiene o no los requisitos funcionales para fabricar un producto que cumplirá con las especificaciones de un producto terminado, en todos los aspectos. El tercer nivel corresponde a la funcionalidad explicita útil para desarrollar una formulación adecuada de un fármaco y un proceso de manufactura efectivo para una tableta.14
Los valores específicos en las propiedades físicas, químicas y tecnológicas de los excipientes identifican la funcionalidad del material. Estos valores concretos permiten el establecimiento de parámetros estadísticos y de límites de corte para el uso de los excipientes. La determinación cuantitativa de la funcionalidad de los excipientes tiene el propósito de controlar su calidad entre lotes, de determinar la consistencia en la fabricación de dicho material y de predecir y comparar la funcionalidad de los materiales obtenidos de diferente fabricante o con diferente marca comercial.19
La selección de los excipientes requiere de un balance entre la eficiencia en tiempo, costo y desempeño esperado en el producto. Los excipientes se incluyen en una formulación por sus propiedades, las cuales en conjunto con los procesos permiten la obtención de formas de dosificación con las especificaciones requeridas. Las propiedades que son deseables en un excipiente se refieren como su desempeño funcional o funcionalidad.
La isomaltosa es un sustituto del azúcar con propiedades fisicoquímicas que permite prever un amplio uso en la industria farmacéutica. Este excipiente se ha evaluado en sus propiedades como vehículo para compresión directa, utilizando diferentes presentaciones y marcas. Entre los productos evaluados se encuentran el Palatinit F, el C, el P.F. y el Palatinit molido. La compactabilidad de dichos materiales se evaluó a través de las gráficas de Heckel que representan la densificación de los polvos contra la presión aplicada, para interpretar el comportamiento del polvo a la deformación. Los resultados obtenidos indicaron que el material sufre fragmentación y una recuperación elástica rápida. Los estudios se realizaron en un espacio limitado del perfil de compactabilidad.20
En el 2009 se consideró que la isomaltosa, a pesar de estar descrita en las principales farmacopeas, era un excipiente más bien desconocido. Se estudiaron las propiedades de compactación de la isomaltosa tamizada, la molida y dos formas aglomeradas, GalenIQ 720 y GalenIQ 721. Se encontró que la compactabilidad de GalenIQ 720 fue algo mejor que la GalenIQ 721 y que ambos tipos de isomaltosa presentan una pequeña pero significativa reducción de la resistencia a la ruptura de sus tabletas después de la adición de estearato de magnesio. La compactabilidad se estudió presentando sólo un perfil de compactabilidad limitado sin concluir nada más que uno es superior o que el otro es inferior, sin ninguna valoración particular.21
]]> En el 2010 y 2011 se estudió la compactabilidad de la isomaltosa no para compresión directa sino en su efecto sobre la granulación húmeda de paracetamol. La compactabilidad se estudió a través de la medición del desplazamiento de la fuerza de compactación ejercida por el punzón superior, en función del tiempo y de su recorrido. La investigación del proceso de compactación se limitó a la aplicación de un diseño factorial para evaluar la bondad del excipiente en la granulación y su optimización en una cierta formulación. 22,23En estas circunstancias, el propósito de este trabajo es la determinación de la compactabilidad del GalenIQ 720 como un parámetro para definir su funcionalidad subrogada, explicita y comparativa, como excipiente para compresión directa.
Material y métodos
Material
Los materiales utilizados en este estudio fueron: celulosa microcristalina tipo 102, Helmcel 200, del proveedor Helm de México, número de lote: 50463 y de número de partida: 17649; isomaltosa aglomerada (Ph Eur., BP, USP-NF), GalenIQ 720, proveedor BENEO-Palatinit GmbH, número de lote: L906; estearato de magnesio, lote A47043 del proveedor Helm de México; metronidazol, del proveedor Química Alkano S.A. de C.V., número de lote: 03121402, con una pureza de 99.31%. El fármaco y los excipientes fueron usados tal como se recibieron.
Métodos
Elaboración de las mezclas
Se pesan las cantidades correspondientes de los materiales para obtener 30g de las mezclas de metronidazol con diferentes proporciones de cada excipiente: 50%, 75%, 62.5%, 25%, 37%, 85% y 95% y se transfieren a un mezclador de pantalón adaptado a un motor de velocidad variable Roto-Torque de Cole-Parmer, modelo 7637, para llevar a cabo la mezcla a 33 rpm, durante 20 minutos. Para las mezclas de metronidazol con GalenIQ 720 se agregó adicionalmente el 1% de estearato de magnesio, para disminuir su adherencia a las herramientas de compresión. Las mezclas de GalenIQ 720 con estearato de magnesio se realizaron a proporciones del lubricante de 0.4, 0.8, 1.0, 1.2, 1.6 y 2.0% y con 20 minutos de mezclado.
Obtención de las tabletas.
]]> Se pesan 150 mg del polvo correspondiente en una balanza analítica y se comprimen durante 10 s en una prensa hidráulica. Los punzones utilizados son circulares, planos y de 8 mm de diámetro. Para cada presión de compactación se hacen 3 tabletas y los resultados se registran como el promedio. Las presiones de compactación utilizadas están en el intervalo de 27-345 MPa.Determinación de la resistencia a la ruptura (D).
Las tabletas se colocan diametralmente en un medidor de dureza o de resistencia a la ruptura, marca Erweka TBH 30, el cual medirá además de la dureza en Newton, el diámetro de las tabletas en milímetros. La prueba se hace por triplicado para cada presión y el promedio servirá como dato para obtener los perfiles de compactación.
Determinación de la resistencia a la tensión (σ).
Con la ayuda de un vernier marca Mitutoyo con capacidad de medición de 0 a 1pulgadas y un margen de error de 0.00005 pulgadas se mide el grosor de cada una de las tabletas. El diámetro de las tabletas se determinó como se describe en la medición de la compactabilidad. El valor de la resistencia a la tensión se determina de acuerdo a la ecuación 2, a partir de las dimensiones de las tabletas y de su resistencia a la ruptura.
Las dimensiones de las tabletas se utilizaron también para determinar su volumen y después su densidad. La densidad relativa de las tabletas se calcula dividiendo la densidad de las tabletas entre la densidad de los materiales individuales y de sus mezclas.
Resultados y discusión
Compactabilidad de GalenIQ 720
La compactabilidad se ha definido en la industria farmacéutica como la dureza de las tabletas. Esta prueba se utiliza ampliamente en la industria farmacéutica para examinar las formas farmacéuticas sólidas desde la década de 1970. Aunque la resistencia de las tabletas en las pruebas usuales de compresión se conoce comúnmente como la dureza, un término más apropiado sería la resistencia mecánica. Este término se asocia con un mecanismo de colapso o destrucción, destrucción por compresión, corte o tensión. De aquí que la resistencia mecánica se equipare a la resistencia a la tensión. La resistencia mecánica se determina presionando las tabletas diametralmente por medio de placas planas, registrando la fuerza necesaria para romperlas.24-25
]]> La compactabilidad de diferentes materiales farmacéuticos o diferentes presentaciones físicas de los mismos se ha definido con los parámetros de regresión de la Ec. 1. 19 De acuerdo al ambiente regulatorio actual y al paradigma de calidad a través del diseño (QbD) la funcionalidad de un excipiente tiene un énfasis en su desempeño. Se busca identificar, evaluar y controlar los atributos críticos de los materiales, para asegurar un desempeño consistente en el producto.26 Las curvas de compactabilidad obtenidas y que describen la relación entre la dureza o resistencia a la ruptura de las tabletas y la presión de compactación utilizada para obtenerlas se puede considerar que sirvan a este propósito.La figura 1 muestra los datos experimentales y la curva de compactabilidad calculada para tabletas planas de 8 mm de diámetro de GalenIQ 720 pesando 150 mg. En la misma figura se muestra, como referencia, los datos experimentales y la curva de compactabilidad calculada para Helmcel 200. La caída de la dureza de las tabletas de GalenIQ 720, a presiones de compactación intermedias, se atribuye a cierta laminación de las tabletas debido a que utilizó el excipiente puro, sin el lubricante necesario.

En la figura 2 se muestra el uso del modelo de la Ec. 1 para linealizar los datos de compactabilidad, en este caso tomando como ejemplo al Helmcel 200. Con los parámetros de regresión obtenidos desde gráficas como la de la figura 2 se calculan los valores de la curva de regresión trazada en la figura 1.

En una primera instancia, la máxima resistencia a la ruptura alcanzada en el perfil de compactabilidad provee de una medida del potencial de enlazamiento del material referido. Esta información se puede utilizar como un parámetro de funcionalidad para caracterizar los excipientes. El valor de Dmax se puede obtener como el promedio de las tres determinaciones realizadas a la presión de compactación a la cual la resistencia a la ruptura se ha estabilizado. Sin embargo, de manera más fehaciente se puede obtener como el valor calculado por regresión ya que estaría apoyado por el perfil de compactabilidad completo.
De esta manera, la compactabilidad se describe como un parámetro operational, en términos de un proceso específico o disposición de pruebas utilizadas para determinar su presencia y cantidad. Esto es, utilizando un procedimiento, una geometría de las tabletas y un peso de las tabletas definidos. La compactabilidad, descrita de esta manera, es suficientemente accesible para que cualquier otra persona diferente del que la define la pueda medir o probar de manera independiente. De esta manera, La compactabilidad de GalenIQ 720 se puede definir con los parámetros de regresión de la curva o simplemente con el valor de la máxima dureza alcanzada por las tabletas, Dmax=134 N.
Las pendientes de las curvas de compactabilidad (n) son características de los materiales, de su comportamiento durante la compresión. Esto es, de los mecanismos que ocurren durante las transformaciones del material que se compacta. Es un parámetro indicativo de la facilidad o capacidad de un polvo para reducir su volumen y alcanzar un mínimo en su porosidad, cuando se comprime. De otra manera, refleja la facilidad o capacidad del polvo para alcanzar la máxima extensión de los enlaces interparticulares, cuando este se compacta. En el presente trabajo, este parámetro no se ha contemplado como parte de la definición de la capacidad aglutinante de los materiales en estudio.
]]> Otra manera de determinar la compactabilidad sería relacionándola a un material que se tomaría como referencia, la celulosa microcristalina tipo 102 (Helmcel 200). Como se puede observar en la figura 1, la compactabilidad de Helmcel 200 es 2-3 veces mayor, Dmax=357 N. De esta manera, la compactabilidad relativa del GalenIQ 720 sería de 0.375 veces la de Helmcel 200. La dureza de las tabletas es función de la geometría y del peso de las tabletas. Por esta razón, en ocasiones podría ser más fehaciente el usar la compactabilidad relativa ya que compara tabletas fabricadas y medidas de la misma manera, esto es, tabletas de la misma geometría, el mismo peso y el mismo método de medición de la dureza.Se ha mencionado que no hay un solo valor de la dureza o resistencia a la ruptura de las tabletas de un polvo sino más bien un intervalo de valores, el cual depende de diversos factores. En este caso, la compactabilidad puede ser referida a cada una de las mediciones de la resistencia a la ruptura a lo largo del perfil de compactabilidad. Sin embargo, el valor de la dureza máxima es uno que se ha estabilizado, teóricamente, a un valor máximo que ya no cambia y que corresponde a tabletas con cero o cerca de cero de porosidad.25
En una segunda instancia, la compactabilidad de las tabletas se puede determinar como la resistencia a la tensión (σ). La resistencia a la tensión es un parámetro que también caracteriza el comportamiento mecánico de las tabletas farmacéuticas. En la prueba de compresión diametral las tabletas se comprimen hasta que se rompen o se destruyen; la carga utilizada se registra y a partir de ella y de las dimensiones de las tabletas se puede calcular la resistencia a la tensión (Ec. 2). 16,27
En la figura 3 se muestran los datos experimentales y las líneas de regresión calculadas para la relación entre la resistencia a la tensión de las tabletas de GalenIQ 720 y de Helmcel 200 y la presión de compactación utilizada para obtenerlas.
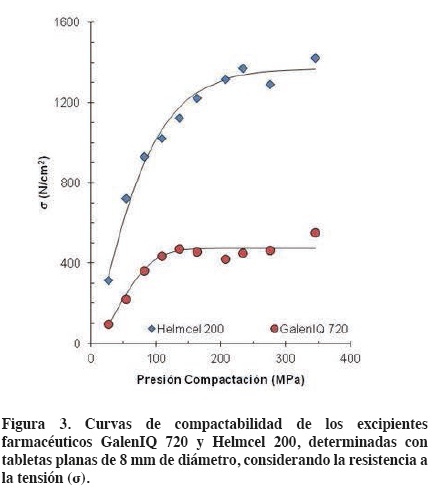
Los valores experimentales de σ contra la presión de compactación se linealizan con el modelo de la ecuación 1 cambiando los valores de D por los σ y los de Dmax por valores de σmax.
Los valores de σmax se obtienen de la relación lineal entre el logaritmo de σ y la densidad relativa, tal como se muestra en la figura 4 para el caso de GalenIQ 720. La ecuación de regresión así obtenida permitió calcular los valores de σmax, apoyados por la curva completa, como aquellos correspondientes a una densidad relativa de 1.

La compactabilidad de GalenIQ 720, determinada como la resistencia a la tensión (σ), tiene un valor absoluto calculado por regresión de σmax=473 N/cm2, mientras que el Helmcel 200 tiene una compactabilidad de σmax=1357 N/cm2. Por lo tanto, la compactabilidad relativa de GalenIQ 720 es de 0.348 veces la de Helmcel 200. Como se puede ver, la compactabilidad relativa de GalenIQ 720 obtenida con los valores de resistencia a la tensión σ y aquella obtenida con los valores de la resistencia a la ruptura D, aunque son diferentes en sus magnitudes, reflejan una diferencia proporcional en las compactabilidades de los dos excipientes estudiados. La compactabilidad relativa de GalenIQ 720 es de 0.375 para el caso de Dmax y de 0.348 para el caso de σmax. Se puede decir que ambos métodos para determinar la compactabilidad dan resultados semejantes.
Una desventaja de la determinación de la dureza máxima sería que estos valores no siempre se encuentran dentro de los límites de los medidores de dureza de las tabletas. Sin embargo, la extrapolación de σ hasta valores de densidad relativa de 1 podría darnos valores ficticios que no serían alcanzables debido a problemas en el tableteo, p. e. laminación. En este sentido, ambos métodos tendrían ventajas y desventajas. Sin embargo, cualquier de los dos métodos permitiría determinar la compactabilidad de los materiales de manera suficiente.
Efecto del estearato de magnesio sobre la compactabilidad de GalenIQ 720
Dado que GalenIQ 720 se adhiere a las matrices y punzones en la elaboración de las tabletas, se hicieron diferentes mezclas de este excipiente con el lubricante estearato de magnesio para evitar dicha adherencia. Sin embargo, este lubricante podría afectar la compactabilidad del excipiente por lo que es necesario determinar este posible efecto. Para este fin se utilizaron curvas de compactabilidad semejantes a las antes mencionadas.
Si se toma como parámetro de compactabilidad de las tabletas de estas mezclas a la dureza máxima obtenida se obtendría una gráfica como la mostrada en la figura 5. Aquí se observa que la dureza (Dmax) de las tabletas de GalenIQ 720 aumenta ligeramente cuando se le adiciona 0.4% de estearato de magnesio. La adición de mayores cantidades del lubricante (0.4% - 2%) muestran una ligera tendencia a disminuir la compactabilidad del GalenIQ 720. De cualquier manera, la compactabilidad de las mezclas del excipiente con estearato de magnesio fue igual o mayor que la del excipiente solo.

El aumento en la compactabilidad de los excipientes, debido a la presencia de un lubricante, se atribuye a una mayor facilidad de las partículas del excipiente para densificar bajo el efecto de la presión de compactación. Este efecto se pierde gradualmente por la debilidad mecánica propia del lubricante, al aumentar su proporción en las mezclas. En el caso particular de GalenIQ 720, el aumento o mantenimiento de la coherencia de las tabletas también se puede atribuir a su fragmentación durante el proceso de compactación, lo que genera superficies del excipiente libres del lubricante.
Los resultados mostrados difieren de otros obtenidos usando prensas hidráulicas, igual que en este estudio, pero utilizando una sola fuerza de compactación (20 kN) y no el perfil completo ni la Dmax. En ese estudio se encontró una pequeña disminución de la resistencia a la ruptura de las tabletas de GalenIQ 720 al adicionar diferentes proporciones de estearato de magnesio (0.5, 1.0 y 2.0%).21
]]> La Figura 6 muestra el efecto conjunto de la presión de compactación y la proporción de estearato de magnesio sobre la compactabilidad de tabletas obtenidas con las mezclas con GalenIQ 720. En esta figura sólo se consideran las proporciones de estearato de magnesio entre 0.4 % y 2.0 %.
Como se puede observar, al aumentar la presión de compactación aumenta de manera sigmoidea la resistencia a la ruptura de las tabletas. Tal como antes se ha mostrado en la figura 5, el aumento en la proporción del estearato de magnesio provoca una disminución de la resistencia a la ruptura de las tabletas. Una proporción de estearato de magnesio de 2.0 % permite alcanzar un valor calculado de la dureza o resistencia a la ruptura máxima de las tabletas de 138 N, a una presión de compactación de 200 MPa. Este valor es similar al obtenido en el perfil o curva de compactabilidad de GalenIQ 720 puro (Figura 1).
En la figura 7 se presentan los datos experimentales obtenidos para la resistencia a la tensión (σmax) para el GalenIQ 720, en función de la proporción de estearato de magnesio en sus mezclas. Como se puede observar, los resultados muestran la misma tendencia ya observada en la figura 5.

Esto es, los valores de la máxima resistencia a la tensión (σmáx) muestran un incremento con la primera adición de estearato de magnesio, para después disminuir gradualmente. Aunque con valores diferentes, la resistencia a la tensión de las tabletas representa también satisfactoriamente a la compactabilidad de los excipientes estudiados.
En términos generales, se puede decir que la compactabilidad del GalenIQ 720 es insensible a la adición del lubricante estearato de magnesio, en las proporciones aquí estudiadas. En este sentido, GalenIQ 720 es un mejor excipiente que la celulosa microcristalina (Helmcel 200), la cual es conocido que sufre un importante deterioro en su compactabilidad por la presencia de lubricantes como el estearato de magnesio.28,29
La sensibilidad a los lubricantes es dependiente de las características fisicoquímicas del lubricante y de otros componentes de las formulaciones para tabletas. Efectos mínimos de los lubricantes, tal como los muestra el GalenIQ 720, se han atribuido a una superficie irregular en los excipientes y a sus propiedades de compactar con fragmentación. La superficie irregular evitaría la formación de una película continua del lubricante mientras que los materiales que fragmentan, al hacerlo, generarían nuevas superficies libres de lubricante.29
]]> Funcionalidad de GalenIQ 720 como un excipiente de compresión directaPara determinar el desempeño de GalenIQ 720 para mejorar la compactabilidad de un producto farmacéutico o su funcionalidad explicita como un excipiente de compresión directa, se escogió el metronidazol como un fármaco de referencia debido a su pobre compactabilidad. Para este fin, se hace uso de los perfiles de compactabilidad para examinar el comportamiento de los excipientes en estudio en una formulación de ese fármaco.
La funcionalidad del GalenIQ 720 para mejorar la compactabilidad de metronidazol, expresada como la máxima resistencia a la ruptura (Dmax), se describe en la figura 8. La figura describe la máxima resistencia a la ruptura (Dmax) que pueden alcanzar las tabletas, para cada una de las diferentes mezclas que se realizaron del excipiente con el fármaco metronidazol.

Como ya se ha observado en la literatura, la compactabilidad de mezclas de polvos muestra valores de Dmax divididos en dos partes.12,13,30,31 En la relación de Dmax contra la proporción de GalenIQ 720 en las mezclas con metronidazol se observan 2 partes. La primera de ellas, a bajas proporciones del excipiente, es una fase continua de metronidazol que tiene dispersas partículas del excipiente GalenIQ 720. Después de una inversión de fases, la segunda parte es una fase continua formada por GalenIQ 720 con partículas dispersas del fármaco metronidazol. El mismo comportamiento se observa para las mezclas del fármaco con Helmcel 200. El punto de inversión de fases para las mezclas con Helmcel 200 ocurre a una proporción aproximada del 64% de este excipiente mientras que para el GalenIQ 720 este punto se da a una proporción aproximada del 68%.
En la figura 8 se observa también que a proporciones bajas de Helmcel 200, con una fase continua de metronidazol, el aumento progresivo de la proporción del excipiente produce un incremento en la dureza de las tabletas de las mezclas. Sin embargo, esto no ocurre en las mezclas con GalenIQ 720. Una fase continua de metronidazol no permite apreciar prácticamente ningún efecto del GalenIQ 720 para aumentar la compactabilidad de las mezclas.
Después del punto de inversión de fases, cuando se observa una fase continua del excipiente con partículas de metronidazol dispersas, en ambos casos ocurre un aumento progresivo de la compactabilidad conforme aumenta la proporción del excipiente. Si comparamos la mejoría en la compactabilidad de los dos excipientes, cuando forman una fase continua en sus mezclas con metronidazol, se observa una compactabilidad promedio de 276 N para Helmcel 200, comparada con una compactabilidad promedio de 87.5 N para GalenIQ 720. La compactabilidad relativa de las mezclas con GalenIQ 720 es 0.317 veces la compactabilidad de las mezclas con Helmcel 200. Este valor es de la misma magnitud que el valor observado para tabletas de los excipientes puros, 0.35-0.37.
De lo anterior, se puede concluir que la compactabilidad subrogada o de los excipientes puros se refleja en su desempeño en una formulación, en este caso de metronidazol. Sin embargo, esto ocurre sólo cuando la fase continua de la tableta está conformada por el excipiente. Esto significa que el desempeño del excipiente para mejorar la compactabilidad de una formulación podría predecirse con el conocimiento de la funcionalidad subrogada o desempeño tecnológico de los excipientes puros.
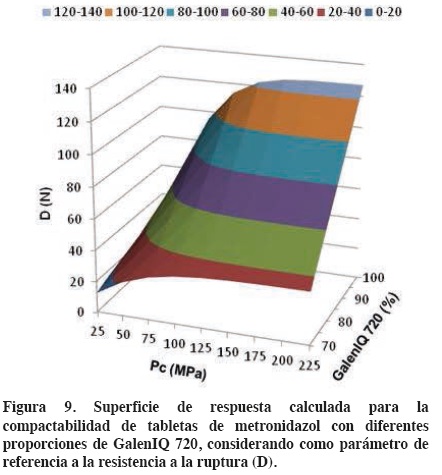
En la figura 9 se puede observar el efecto conjunto de la presión de compactación y de la proporción de GalenIQ 720 sobre la compactabilidad de tabletas de metronidazol. En este caso tomando como parámetro de compactabilidad a la resistencia a la ruptura de las tabletas (D). Las proporciones del excipiente que se consideraron son las que forman una fase continua del mismo (70-95%).
]]>
En la figura 10, se muestra un comportamiento similar al antes descrito para la figura 8, en este caso considerando como parámetro de compactabilidad la resistencia máxima a la tensión (σmáx). Aunque los parámetros de compactabilidad son diferentes en cada figura, el resultado es similar. Aunque en la figura 10 los puntos de inversión de fases son algo diferentes, para Helmcel 200 y GalenIQ 720, 48% y 71% de la proporción del excipiente respectivamente.
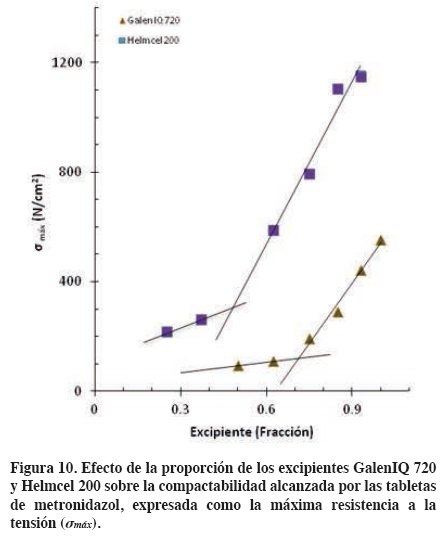
Nuevamente, se observa que la adición de Helmcel 200 genera un incremento en la resistencia a la tensión (s) de las tabletas de sus mezclas con metronidazol, desde la menor proporción del excipiente. Esto no ocurre así en el caso del GalenIQ 720, ya que este genera este efecto sólo después del punto de inversión de fases.
La compactabilidad relativa promedio de GalenIQ 720 en sus mezclas con metronidazol, de acuerdo a la máxima resistencia a la tensión de las tabletas (σmax), es de 0.41 veces la de las mezclas con Helmcel 200.
El efecto conjunto de la presión de compactación y de la proporción de GalenIQ 720 sobre la resistencia a la tensión (σ) de tabletas de Metronidazol se observa en la figura 11. La superficie de respuesta calculada muestra la porción del sistema formado por metronidazol-GalenIQ 720 correspondiente a la fase continua del excipiente (75-95% de GalenIQ 720).
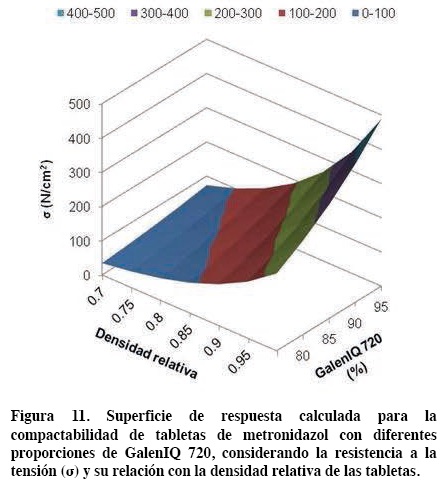
Conclusiones
Aunque por definición la funcionalidad de un excipiente está ligada al producto en el cual será usado, desde el punto de vista del excipiente la funcionalidad es una propiedad tecnológica del material, la cual puede definirse independientemente de la formulación en la que será usado. Un aglutinante sigue siendo aglutinante sin importar en que formulación se utilice o si funciona bien o no en dicha formulación. Los dos parámetros calculados (Dmax y σmax) permiten la reducción del concepto de compactabilidad hasta un valor numérico que se puede utilizar para caracterizar la funcionalidad de un material.
El uso de la celulosa microcristalina tipo 102 (Helmcel 200) como referencia permite la estimación de la compactabilidad como un valor relativo. La compactabilidad de un material puede definirse como un porcentaje o fracción de la compactabilidad de la celulosa microcristalina tipo 102.
El excipiente farmacéutico Helmcel 200 presenta una mayor compactabilidad, expresada como resistencia a la ruptura (D) y como resistencia a la tensión (s), que el excipiente farmacéutico GalenIQ 720. Sin embargo, GalenIQ no ve afectada su compactabilidad por la presencia de un lubricante graso mientras que es conocido que la celulosa microcristalina pierde compactabilidad, de manera importante, al adicionarse de ese lubricante. No obstante, ambos excipientes farmacéuticos, Helmcel 200 y GalenIQ 720, podrían satisfacer la funcionalidad de aglutinante para compresión directa del fármaco Metronidazol.
Referencias
1. Pifferi G, Restani P. The safety of pharmaceutical excipients. II Farmaco. 2003; 58(8):541-550. [ Links ]
]]>2. Monsuur F, Poncher J, Grace W. Raising expectations of excipients. Chemistry today. 2010; 28(5):5-6. [ Links ]
3. The new era of functional excipients - An innovative approach in design of dosage forms. Disponible en: http://www.pharmpro.com/articles/2011/05/raw-materials-Functional-Excipients/ Lunes Mayo 2, 2011. Acceso 09 Diciembre 2011. [ Links ]
4. Strydom SJ, Otto DP, Liebenberg W, Lvov YM de Villiers MM. Preparation and characterization of directly compactible layer-by-layer nanocoated cellulose. Int J Pharm. 2011; 404:57-65. [ Links ]
5. Chamarthy S, Pinal R, Carvajal M. Elucidating Raw Material Variability–Importance of Surface Properties and Functionality in Pharmaceutical Powders. AAPS Pharm Sci Tech. 2009; 10(3):780-788. [ Links ]
6. Michaels JN, Bonsignore H, Hudson-Curtis BL, Laurenz S, Lin HH, Mathai T, Pande G, Sheth A, Sprockel O. Attribute-based design space: materials-science-based quality-by-design for operational flexibility and process portability. J Pharm Innov. 2011; 6:193-201. [ Links ]
]]>7. Odeku OA. The compaction of pharmaceutical powders. Pharmainfo.net. Disponible en: http://www.pharmainfo.net/reviews/compaction-pharmaceutical-powders. 2007. Acceso 19 Noviembre 2009. [ Links ]
8. Santl S, Ilic I, Vrecer F, Baumgartner S. A compressibility and compactibility study of real tableting mixtures: The impact of wet and dry granulation versus a direct tableting mixture. Int J Pharm. 2011; 414:131-139. [ Links ]
9. Leuenberger H, Rohera BD. Fundamentals of powder compression. I. The compactibility and compressibility of pharmaceutical powders. Pharm Res. 1986; 3 (1):12-22. [ Links ]
10. Nordstrom J, Klevan I, Alderborn G. A protocol for the classification of powder compression characteristics, Eur J Pharm Biopharm. 2011, 80 (1):209-216. [ Links ]
11. Fichtner F, Mahlin D, Welch K, Gaisford S, Alderborn G. Effect of Surface Energy on Powder Compactibility. Pharm Res. 2008; 25 (12):2750-2760. [ Links ]
]]>12. Castillo S, Villafuerte L. Compactibility of binary mixtures of pharmaceutical powders. Eur J Pharm Biopharm. 1995; 41 (5):309-314. [ Links ]
13. Castillo S, Villafuerte L. Compactibility of ternary mixtures of pharmaceutical powders. Pharm Acta Helv. 1995; 70:329-337. [ Links ]
14. Díaz Ramírez CC, Villafuerte Robles L. Surrogate functionality of celluloses as tablet excipients. Drug Dev Ind Pharm. 2010; 36 (12):1422-1435. [ Links ]
15. Fell J, Newton J. The prediction of the tensile strength of tablets. J Pharm Pharmacol. 1970; 22 (3):247-248. [ Links ]
16. Wu Ch, Best SM, Bentham AC, Hancock BC, Bonfield W. A simple predictive model for the tensile strength of binary tablets. Eur J Pharm Sci. 2005; 25:331-336. [ Links ]
]]>17. Van Veen B, van der Voort Maarschalk K, Bolhuis GK, Zuurman K, Frijlink HW. Tensile strength of tablets containing two materials with a different compaction behavior. Int J Pharm. 2000; 203 (1-2):71-79. [ Links ]
18. Ilića I, Kása P, Dreua R, Pintye-Hódi K, Srčiča S. A modification of the Pr value equation for measuring the compactibility of pharmaceutical materials. Chem Eng Proc: Process Intensification. 2010; 49 (8):881-884. [ Links ]
19. Villafuerte Robles L. The excipients and their functionality in pharmaceutical solid products. Rev Mex Cienc Farm. 2011; 42 (1):18-36. [ Links ]
20. Ndindayino F, Henrist D, Kiekens F, Vervaet C, Remon JP. Characterization and evaluation of isomalt performance in direct compression. Int J Pharm. 1999; 189:113-124. [ Links ]
21. Bolhuis GK, Engelhart JJP, Eissens AC. Compaction properties of isomalt. Eur J Pharm Biopharm. 2009; 72:621-625. [ Links ]
]]>22. Sáska Zs, Dredán J, Balogh E, Luhn O, Shafir G, Antal I. Effect of isomalt as novel binding agent on compressibility of poorly compactable paracetamol evaluated by factorial design. Powder Technol. 2010; 201:123-129. [ Links ]
23. Sáska Zs, Dredán J, Balogh E, Luhn O, Shafir G, Antal I. Evaluation of the impact of mixing speed on the compressibility and compactibility of paracetamol-isomalt containing granules with factorial design. Powder Technol. 2011; 213:132-140. [ Links ]
24. Lee J. Structural heterogeneity of pharmaceutical compacts probed by micro-indentation. J Mater Sci: Mater Med. 2008; 19:1981-1990. [ Links ]
25. Davies PN, Worthington HEC, Podczeck F, Newton JM. The determination of the mechanical strength of tablets of different shapes. Eur J Pharm Biopharm. 2007; 67:268-276. [ Links ]
26. Sheehan C, Amidon GE. Compendial Standards and Excipient Performance in the QbD Era: USP Excipient Performance Chapter <1059>. Am Pharm Rev. September/October 2011:10-18. [ Links ]
]]>27. Bacher C, Olsen PM, Bertelsen P, Sonnergaard JM. Compressibility and compactibility of granules produced by wet and dry granulation. Int J Pharm. 2008; 358:69-74. [ Links ]
28. Muzíková J. The firmness of Avicel PH 102 and Avicel PH 301 compression and the effect of magnesium stearate. Ceska Slov Farm. 2001; 50(2):92-94. [ Links ]
29. Rashid I, Daraghmeh N, Al-Remawi M, Leharne SA, Chowdhry BZ, Badwan A. Characterization of the impact of magnesium stearate lubrication on the tableting properties of chitin-Mg silicate as a superdisintegrating binder when compared to Avicel® 200. Powder Technol. 2010; 203:609-619. [ Links ]
30. Garzón-Serra ML, Villafuerte-Robles L. Compactibility of mixtures of calcium carbonate and microcrystalline cellulose. Int J Pharm. 2002; 231 (1):33-41. [ Links ]
31. Garzón-Serra ML, Villafuerte-Robles. Compactibility of agglomerated mixtures of calcium carbonate and microcrystalline cellulose. Int J Pharm. 2003; 258 (1, 2):153-163. [ Links ]
]]>