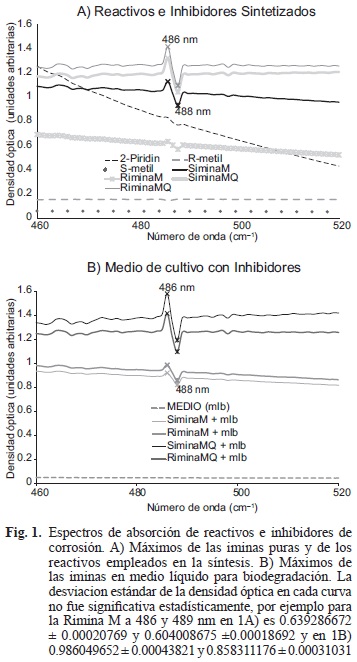
Bacterial biodegradability of inhibitors of chiral imine type corrosion and catabolic prediction
José Epigmenio Bautista García1, José Luis Imbert Palafox1*, María Aurora Veloz Rodríguez2, Rosa Ángeles Vázquez García2 y Juan Vicente Gómez Gomez1
1 Área Académica de Medicina, Instituto de Ciencias de la Salud, Universidad Autónoma del Estado de Hidalgo. Ex-hacienda la Concepción S/N, Tilcuautla, Municipio de San Agustín Tlaxiaca, Hidalgo, México, C.P. 42160 *Autor para correspondencia: imbertox@hotmail.com
2 Área Académica de Ciencias de la Tierra y Materiales, Instituto de Ciencias Básicas e Ingeniería, Universidad Autónoma del Estado de Hidalgo. Carretera Pachuca-Tulancingo Km 4.5, Municipio de Mineral de la Reforma, Hidalgo, México, C.P. 42074
]]> Recibido junio 2014;
Resumen
Dado que el uso de inhibidores de corrosión provoca en muchos casos contaminación de efluentes debido las características no biodegradables de dichos compuestos, en este trabajo se sintetizaron dos compuestos quirales S(-) y R(+) del tipo base de Schiff denominados (Simina, Rimina, SiminaM, y RiminaM) derivados de la condensación del 2-piridincarboxaldehído con las dos respectivas aminas quirales S(-)-a-metilbencilamina y R(+)-a-metilbencilamina. Estos compuestos fueron sintetizados por mecanosíntesis y química convencional. Para evaluar su carácter biodegradable se aislaron e identificaron cinco bacterias Gram negativas de aguas residuales de la ciudad de Pachuca, Hidalgo, México: Psychrobacter phenylpyruvicus, Alcaligenes faecalis, Aeromonas caviae, Citrobacter freundii y Pseudomonas pseudoalcaligene. El procedimiento consistió en hacer crecer los cultivos con las S(-) y R(+)-iminas en tubos y en matraces. La biodegradación fue evaluada por espectroscopia UV-Vis y FTIR (siguiendo la desaparición de los grupos imino y anillos aromáticos, indicativos del rompimiento de la estructura molecular de los agentes). Se encontró que los inhibidores se biodegradan tanto de manera individual como en mezclas, pero el grado de descomposición depende de su quiralidad S(-) o R(+), la cual se ve favorecida por el método de mecanosíntesis. De hecho, la bacteria Citrobacter freundii demostró tener la más alta capacidad de biodegradación para todos los compuestos, siendo la base de Schiff (SiminaM) la que sufrió la mayor degradabilidad, probablemente por su mayor afinidad biológica con la bacteria y la posible diferencia en el arreglo S(-) estructural de la molécula. Del resultado obtenido y mediante el análisis in silico se planteó una posible vía catabólica.
Palabras clave: bases de Schiff, descomposición, Psychrobacter phenylpyruvicus, Alcaligenes faecalis, Aeromonas caviae, Citrobacter freundii, Pseudomonas pseudoalcaligenes.
Abstract
Due that the use of common corrosion inhibitor agents usually causes pollution on effluents, because of their non-biodegradability character, in this work we synthesized two chiral compounds of Shiff type base S(-) and Hereafter labelled as Simina, Rimina, SiminaM and RiminaM, derived from the condensation reaction between the 2-pyridincarboxaldehyde and the S(-)-a-methylbenzylamine and the R(+)-a-methyl-benzylamine. These compounds were synthesized by mechanosynthesis and conventional chemical methods. In order to evaluate their biodegradable character, five Gram negative bacteria were previously isolated and identified from a waste water effluent in Pachuca, Hidalgo, Mexico: Psychrobacter phenylpyruvicus, Alcaligenes faecalis, Aeromonas caviae, Citrobacter freundii and Pseudomonas pseudoalcaligenes. The evaluation consisted in cultivating the bacteria in tubes and flasks in presence of the S(-)- and R(+)-imines, while the biodegradation was monitored by UV-Vis and FTIR spectroscopies (by following the intensity decrease of the signals of both the imine and aromatic rings, which are indicative of the loss of the molecular structure). It was found that the inhibitor agents are either individually or in mixture degraded depending on their S(-)- or chirality, being the most susceptible to degradation those compounds synthesized by mechanochemistry. Actually, the Citrobacter freundii bacteria showed the highest ability to degrade all these imines, while the SiminaM compound was the must degraded agent, probably due to its affinity to the bacteria and to the S(-) intramolecular arrangement. On the basis of the results obtained and by applying the analysis in silico, a possible catabolic pathway was predicted.
Key words: Schiff bases, decomposition, Psychrobacter phenylpyruvicus, Alcaligenes faecalis, Aeromonas caviae, Citrobacter freundii, Pseudomonas pseudoalcaligenes.
]]>
INTRODUCCIÓN
La biodegradabilidad se define como el grado de eficacia que tiene un producto para ser degradado por diferentes microorganismos en el ambiente como bacterias, hongos, protozoarios o algas. Este proceso puede tardar horas, días o incluso años y está determinado principalmente por la estructura química del producto (Félix-Soto et al. 1998, Jones et al. 2008).
Los productos o sustancias con alto grado de degradación microbiana bajo condiciones ambientales naturales son denominados biodegradables e indican que éstos se convierten o descomponen a formas moleculares más sencillas mediante procesos de transformación química. Por otro lado, aquellas sustancias que no cumplen con dicha propiedad y que por el contrario permanecen en el medio por muchos años o décadas se les llama recalcitrantes (Kalwasinska et al. 2011, Vasdev 2011).
Se ha demostrado que hay comunidades microbianas dominadas por cianobacterias involucradas de manera muy activa en el proceso de degradación del petróleo y sus derivados, ya que tiempo después de ocurridos los derrames petroleros se encuentra una gran colonización formada por extensos aglomerados de dichas cianobacterias, que se correlaciona con la disminución de los hidrocarburos en los sitios contaminados (Schlegel y Zaburosch 1997, Garrity 2001).
Se han reportado más de 22 géneros bacterianos capaces de metabolizar hidrocarburos aromáticos derivados del petróleo entre los que destacan Pseudomonas, Aeromonas, Synechocystis, Bacillus, Flavobacterium, Corynebacterium, Micrococcus, Rhodococcus, Achromobacter y Acinetobacter (Prakash e Irían 2011, El-Sheekh et al. 2012). Sin embargo, debido a la complejidad de la composición del petróleo se sabe que la biodegradación por parte de las bacterias depende de las proporciones que tenga cada una de las fracciones de hidrocarburos alifáticos, aromáticos y polares (Acuña et al. 2010). Un ejemplo de lo anterior es la investigación del genoma de la cepa PCC 6803 de Synechocystis sp. que reveló la existencia de genes de una enzima dioxigenasa. Dicha enzima cataliza la incorporación de dos átomos de oxígeno en un anillo aromático, produciendo dihidrodioles. Lo anterior sugiere que la enzima podría tener un papel en la degradación aerobia de compuestos como el dibenzotiofeno (DBT) y el fenantreno (Rullkötter y García 2002, Kocberber et al. 2011).
Por otra parte, para inhibir o controlar el proceso de corrosión en ductos petroleros se han diseñado los productos conocidos como inhibidores de corrosión (Kaiser et al. 1996, Sastri 1998, Hernández et al. 2014). Estos inhibidores de corrosión se definen como sustancias químicas que, adicionadas en pequeñas cantidades, provocan una disminución de la velocidad de corrosión de un material (Bradford 1993). Lamentablemente, muchos de estos compuestos son tóxicos y su descarga en aguas residuales provoca daño al ambiente (Branco 1984).
En los últimos años se ha reducido el uso de muchos compuestos químicos utilizados en las formulaciones de los recubrimientos, ya que han sido sujeto de regulaciones gubernamentales a nivel mundial. Lo anterior debido a la creciente preocupación sobre aspectos de seguridad, salud y protección ambiental y a la innovación tecnológica en el campo de los recubrimientos que ha originado nuevos sistemas disponibles que, en el mercado mexicano, cumplen con la normatividad ecológica (NRF-004-PEMEX-2011).
En la actualidad se considera el uso de compuestos orgánicos como inhibidores de corrosión, los cuales se caracterizan por ser moléculas cuya estructura contiene átomos de carbono, hidrógeno, nitrógeno, oxígeno o azufre (Gutiérrez et al. 2000). Sus características estructurales y energéticas, así como sus propiedades inhibitorias son adecuadas para disminuir la corrosión (McMurry 2004). Estas moléculas orgánicas generalmente se sintetizan sin considerar otras propiedades químicas, por ejemplo la isomería quiral, a la que no se le ha prestado mucha importancia. Sin embargo, considerando que los seres vivos presentan un metabolismo favorecido por este tipo de estructuras químicas como los L-aminoácidos, los D-azúcares, etc., en nuestra línea de trabajo se ha propuesto que esta propiedad podría resultar novedosa e interesante para el diseño de inhibidores de corrosión (Cadena-Franco 2010, Hernandez et al. 2014).
]]> La quiralidad le confiere selectividad a las moléculas químicas para generar una respuesta biológica deseada, pues el ambiente de los seres vivos incluido el humano y las bacterias, es quiral. Por lo tanto, el potencial de las moléculas para ser empleadas como inhibidores de corrosión biodegradables comparado con aquellos que se vuelven contaminantes, se incrementa en varios órdenes de magnitud. Aún no se ha determinado si la biodegradabilidad puede depender del tipo de isómero (R o S) empleado (Cadena-Franco 2010). Bajo las condiciones anteriores, se ha propuesto que las comunidades bacterianas pueden contribuir a eliminar o moléculas indeseables o desaparecer efectos adversos o negativos en el ambiente (Zipper et al. 1996).Aunque diversos microorganismos pueden metabolizar y biodegradar hidrocarburos derivados del petróleo, son las bacterias las que con mayor frecuencia se emplean. Las razones principales son que tienen rutas metabólicas más rápidas y diversas y que se adaptan fácilmente. Se han descrito que las bacterias presentan diversas vías metabólicas para diferentes contaminantes orgánicos y que además pueden ser manipuladas genéticamente para inducirles capacidades de biorremediación (Prakash e Irfan 2011, Vasdev 2011, El-Sheekh et al. 2012).
El objetivo de este trabajo fue evaluar la biodegradación bacteriana de dos compuestos quirales de tipo base de Schiff con características de inhibidores de la corrosión, sintetizados por química convencional y mecanosíntesis.
MATERIALES Y MÉTODOS
Aislamiento e identificación de los microorganismos
Para el aislamiento de los organismos se realizaron cultivos de agua residual en matraces Erlenmeyer con 100 mL de medio líquido para biodegradación (mlb), compuesto por MgSO4 - 0.0026 g/L, KCl - 0.25 g/L, FeSO4 - 0.002 g/L, NH4Cl - 3 g/L, K2HPO4 - 1 g/L y agua destilada (Felix-Soto et al. 1998), incubados a 30 °C con agitación a 200 rpm durante 24 h. Después se tomaron alicuotas de 10 μL para inocular cajas de petri, preparadas con medios de cultivo diferenciales (que son capaces de distinguir a dos o mas especies o géneros de microorganismos por sus características bioquímicas de crecimiento), que se incubaron a 30 °C por 24 h para obtener el crecimiento de varios tipos de colonias bacterianas (Acuña et al. 2010). Después de examinar la morfología colonial macroscópica y de evaluarla microscópicamente por tinción de Gram, se otuvo una identificación preliminar con pruebas bioquímicas convencionales. El análisis taxonómico final fue realizado con el sistema automatizado Treck Diagnostics System, Inc. (Aris®/Sensititre®).
Síntesis de los inhibidores de corrosión
Las sustancias empleadas para las reacciones fueron: 2-piridincarboxaldehído P62003, 99 %, CAS number 1121-60-4, C6H5NO, MW 107.11, (2.57mL; 26.89 mmol); (S)-(-)-α-metilbencilamina 77869 Fluka, ≥ 99.0 %, número CAS 2627-86-3, C6H5CH(CH3)NH2, MW 121.18, (2.0 mL; 15.71 mmol) y (R)-(+)-α-metilbencilamina 77879 Fluka,≥ 99.0 %, número CAS 3886-69-9, C6H5CH(CH3) NH2, MW 121.18, (2.0 mL; 15.71 mmol). Todas ellas de la marca Sigma-Aldrich. Los compuestos inhibidores (empleados y evaluados en los ensayos) fueron sintetizados siguiendo la metodología propuesta por la química convencional (MQ) y por mecanosíntesis (M) (Surynayana et al. 2001, Beyer y Clausen-Schaumann 2005, Cadena-Franco 2010) con una concentración final de 11.9 Molar (2.5 g/mL). Se identificaron de la siguiente manera: SiminaM = imina quiral de tipo S y RiminaM = imina quiral de tipo R obtenidas por mecanosíntesis. SiminaMQ = imina quiral tipo S y RiminaMQ = imina quiral tipo R sintetizadas por química convencional. (La nomenclatura oficial de los compuestos según la IUPAC es, 2-piridin-(S)-(-)-α-metilbencilimina y 2-piridin-(R)-(+)-α-metilbencilimina).
Detección de los inhibidores por espectrofotometría ultravioleta visible (UV-Vis)
]]> Para detectar la presencia de los inhibidores en los cultivos, primero se determinó el máximo de absorción característico de cada uno (SiminaM, RiminaM, SiminaMQ y RiminaMQ). Para lo cual se disolvió 25 μL (0.0625 g) de cada uno en 1 mL de etanol absoluto, obteniendo una concentración de 294.8 mM. Después se midió la densidad óptica, realizando un espectro de absorción en un rango de longitud de onda (λ) de 200 a 750 nm (Leahy y Colwell 1990, Rocha y Texeira 2004), a través de un espectrofotómetro de UV-visible automatizado marca Agilent modelo 8453. Este instrumento cuenta con arreglos de diodos para realizar y promediar tres lecturas simultáneas por cada nanómetro de los espectros, lo que permite obtener la respectiva desviación estándar por cada punto de la absorbancia vs. longitud de onda en cada curva o ensayo.Evaluación de la biodegradabilidad de los inhibidores en tubo
Se realizó un ensayo piloto por quintuplicado en tubos de ensayo estériles con tapa de rosca de 16 x 150 mm para cada cepa bacteriana, así como por par de conjuntos microbianos denominados: consorcio 11 (integrado con tres bacterias que mostraron un buen crecimiento previo: Alcaligenes faecalis, Citrobacter freundii y Pseudomonas pseudoalcaligenes) y consorcio 22 (con las cinco bacterias) con la finalidad de tener interacciones similares a las que los microorganismos realizan de manera natural. Todos los tubos se incubaron a 30 °C, con agitación constante a 200 rpm durante 72 h. El crecimiento bacteriano en cada cultivo se comprobó mediante la inoculación de microgotas en placa de medio sólido eosina azul de metileno (EMB).
Evaluación de la biodegradabilidad de los inhibidores en matraz
Los cultivos se realizaron por triplicado en matraces Erlenmeyer estériles de 250 mL con 100 mL de medio líquido para biodegradación (mlb), añadiendo a cada frasco 250 μL (0.625 g) de cada uno de los compuestos a una concentración de 11.9 M, diluidos en 9 mL de etanol absoluto, 5 mL de extracto de levadura líquida al 10 % y 4 mL de inóculo (bacteria seleccionada).
Para formar los consorcios se empleó 1 mL de cada bacteria (excepto para los matraces testigo). La concentración final para cada inhibidor fue de 327.6 mM. Los matraces se incubaron a 30 °C con agitación constante a 175 rpm durante 72 h. Con el propósito de verificar el crecimiento de las bacterias, durante las primeras 24 h de incubación se tomaron alícuotas para realizar curvas de crecimiento. Asimismo, se inocularon microgotas en cajas Petri con medio sólido para determinar las unidades formadoras de colonias (UFC).
Determinación del crecimiento bacteriano por medio de espectrofotometría
Se realizaron únicamente curvas de crecimiento para los cultivos de Citrobacter freundii, consorcio 11 y consorcio 22, pues fueron los que mejor crecimiento mostraron. Se tomaron alícuotas de 100 μL de cada cultivo y se diluyeron 1/1000 en agua durante cada hora desde el inicio de la incubación hasta las 12 h y una muestra adicional a las 24 h. Las lecturas se realizaron con el espectrofotómetro de UV-Vis a 600 nm. El mismo ensayo se realizó para los cultivos testigo, los cuales incluían mlb, inóculo bacteriano y extracto de levadura en proporciones similares al resto de los cultivos.
Determinación del crecimiento bacteriano por medio de UFC
El conteo de las UFC para cada cultivo en matraz se realizó por cuatriplicado poniendo 5 μL de microgotas en cajas Petri con medio EMB a una dilución de 1:1000 e incubando a 30 °C durante 24 h. Después se contaron las UFC con una fotografía digital en el microscopio estereoscópico para cada una de las áreas en las que se goteó, con ayuda del paquete SCAN® V6.
]]> Determinación del crecimiento bacteriano mediante su biomasaPasados tres días de incubación en matraz se centrifugó el contenido y se desechó cuidadosamente el sobrenadante para obtener el botón o precipitado de bacterias con el que se obtuvo el peso húmedo, después se dejaron secar en una estufa a 35 °C durante 24 h y se pesó nuevamente para registrar el peso seco.
Caracterización química de los inhibidores por espectroscopia de las transformadas de Fourier del espectro infrarojo (FTIR, por sus siglas en inglés)
Para realizar los espectros de FTIR, los materiales fueron secados para obtener sólidos. Posteriormente dichos materiales se pulverizaron y empacaron en pastillas con KBr. Las lecturas se realizaron en el rango de 370 a 4000 cm-1 con el cristal de ZnSe en modo de Reflectancia total horizontal atenuada. El paquete Spectrum v.3.02, incluido en el espectrofotómetro GX®Perkin-Elmer, se empleó para el análisis.
Los matraces en los que se formó anillo se dejaron a secar a 36 °C en estufa durante 24 h. Una vez secos, se desprendió el material con una espátula y etanol absoluto para colocarlo en cajas Petri, las cuales se dejaron a temperatura ambiente por un día para que se evaporara el etanol. El residuo se recolectó y fue analizado mediante FTIR.
RESULTADOS Y DISCUSIÓN
Síntesis de las iminas
En la figura 1A, se observa el espectro de absorción de los reactivos 2-piridincarboxaldehido, Ä-metilbencilamina y S-metübencilamina, los cuales fueron empleados para sintetizar los inhibidores. También se detectan los máximos y mínimos de absorción característicos de los compuestos SiminaM, RiminaM, SiminaMQ y RiminaMQ recién sintetizados, a 486 y 489 nm.

Identificación de bacterias biodegradadoras
Se aislaron cinco especies de bacterias Gram negativas en agua residual, a las cuales el sistema taxonómico automatizado clasificó considerando el microorganismo más probable por porcentaje de similitud siendo: Aeromonas caviae 98.15 %, Alcaligenes faecalis 98.55 %, Citrobacterfreundii 98.54 %, Pseudomonaspseudoalcaligenes 98.50 % y Psychrobacter phenylpyruvicus 96.36 %. Conocer el género y especie de nuevas bacterias que podrían tener un papel relevante en la biodegradación sería importante (Leahy y Collwell 1990, Kalwasinska et al 2011). En este aspecto el trabajo contribuye a la búsqueda de microorganismos potenciales que serían de utilidad, no sólo para la ciencia microbiológica sino para ser considerados en la biorremedación y atenuación del impacto ambiental que produce la contaminación.
Ensayo de biodegradación
En el cuadro I se muestran cuatro datos relacionados con la biodegradación: el crecimiento bacteriano en mlb, la formación de anillo, la formación de grumos y la disminución en la densidad óptica (DO) del medio con los inhibidores que fueron degradados. Se observa que en el consorcio 22 hay crecimiento con los cuatro compuestos con formación de anillo y grumos con la RiminaMQ. Un ejemplo similar es la bacteria Aeromonas caviae, la cual creció en los cuatro inhibidores y sólo formó grumos en SiminaMQ.
Asimismo, se muestran los valores máximos de absorción de los compuestos en densidad óptica para cada cultivo realizado en tubos. Además, se registran los testigos que permanecieron sin cambios durante la incubación, es decir que no fueron afectados por la temperatura y la agitación. En los cultivos con bacterias, los que tienen valores más bajos de DO o que han crecido más son Citrobacter freundii (0.2182) y el consorcio microbiano 11 (0.2709), lo que demuestra que con SiminaM se logró la mayor descomposición. En el caso de Pseudomonas pseu-doalcaligenes (0.6805), la biodegradación la efectúa sólo con RiminaMQ.
Respecto al ensayo en matraces (Cuadro I) se corrobora nuevamente que las bacterias con menores capacidades para biodegradar a los inhibidores son Pseudomonas pseudoalcaligenes, Psychrobacter phenylpyruvicus y Alcaligenes faecalis, pues crecieron eventualmente y donde lo hicieron no hubo una disminución significativa de los inhibidores. Por otra parte Citrobacter freundii nuevamente mostró la mayor capacidad para biodegradar a SiminaM, RiminaM y SiminaMQ, pues hay disminución de los máximos de absorción. También se puede ver que los consorcios (11 y 22) mostraron buenos resultados en el crecimiento y en la disminución de las absorbancias de los cuatro compuestos, aunque fueron superados por Citrobacter freundii.
Las bacterias con menor crecimiento en presencia de los inhibidores de corrosión fueron Pseudomonas pseudoalcaligenes, ya que sólo creció en un compuesto, y Psychrobacter phenylpyruvicus que creció en dos de los inhibidores. Estas bacteriasprobablemente son muy sensibles a este tipo de compuestos o la eficacia para metabolizarlos o emplearlos es pobre o nula.
En cuanto al porcentaje de biodegradación de los inhibidores, tanto en los ensayos de tubo como de matraz, quedaría en primer lugar la SiminaM por Citrobacter con 81.8 %, en segundo la SiminaMQ también por Citrobacter con 71.7 %, después la RiminaMQ por Pseudomonas con 52 % y en cuarto lugar la RiminaM por Citrobacter con 47.4 %.
Biodegradación y curvas del crecimiento bacteriano
]]> En las figuras 2A y 2B se muestran las curvas de crecimiento de Citrobacterfreundii y el consorcio 11 en presencia de los cuatro inhibidores de corrosión. Los valores de la densidad óptica a 600 nm muestran que el mayor crecimiento lo tuvieron los testigos que crecieron sin inhibidores. En cambio en los compuestos quirales disminuye, aunque es más inhibitorio en el caso de la RiminaM. Además, se observa que a las 24 h la curva de la SiminaM se aproxima a la del crecimiento de los testigos, por lo que es probable que el compuesto esté siendo metabolizado. Resultados similares se obtuvieron para el consorcio 22 (datos no mostrados).En el cuadro II están los resultados del conteo de UFC, que complementan las curvas de crecimiento. Se puede ver que los compuestos con quiralidad S como SiminaM y SiminaMQ, tuvieron un mayor número de colonias en los tres casos presentados (Citrobacterfreundii (350UFC), consorcio 11 (347UFC) y consorcio 22 (337UFC). Los datos sugieren nuevamente que la quiralidad de los inhibidores podría ser importante e independiente del método químico de síntesis. También se observa que el compuesto Si-minaM tuvo un mayor número de colonias en los tres casos presentados (Citrobacterfreundii, consorcio 11 y consorcio 22), seguido por SiminaMQ.
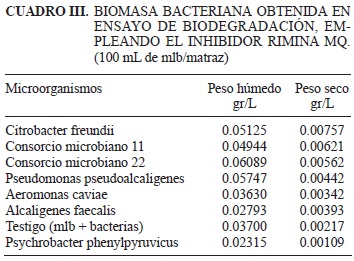
En el cuadro III se muestra la determinación de la biomasa bacteriana cuando crecieron únicamente en presencia del inhibidor RiminaMQ. Puede notarse que ambos valores del testigo (0.03700 y 0.00217) fueron inferiores al de Citrobacter freundii (0.05125 y 0.00757) y al del consorcio 22 (0.06089 y 0.00562) con el inhibidor RiminaMQ, lo que probablemente indica que el compuesto beneficia el crecimiento y proliferación de las bacterias porque éstas tienen la capacidad metabólica para emplearlos como posible fuente alterna de carbono y nitrógeno. En concordancia con los dos resultados anteriores, Citrobacter freundii muestra la mejor capacidad de biodegradación y adaptación a los inhibidores, seguida por los consorcios 11 y 22. Cabe mencionar que estos resultados se realizaron sin considerar la desviación estándar respectiva, debido a la cantidad limitada de inhibidores producidos pues la síntesis química se realizó a escala piloto y además también se emplearon en las pruebas de identificación.
Caracterización química de los reactivos y los inhibidores por FTIR
En la figura 3 se observa el espectro FTIR característico de los compuestos y los grupos funcionales que lo identifican. Para R-metilbencilamina y S-metilbencilamina se observa que tienen el mismo espectro cuya señal característica y distintiva para ambos es a 1572 cm, que distingue la unión amonio (C-NH2). El reactivo 2-piridincarboxaldehído tiene la señal distintiva del grupo aldehido a 1708 cm. Los inhibidores presentaron espectros similares, los cuatro isómeros mostraron la banda de vibración a 1646 cm-1 correspondiente al estiramiento C = N característico del grupo imino (Figs. 4A y B).
Caracterización química de los inhibidores biodegradados por FTIR
En las figuras 4A y B se presentan los espectros de FTIR que corresponden a SiminaM (A) y RiminaMQ (B), antes y después de ser biodegradados independientemente en los cultivos del consorcio 11. En estos se observan diferencias de transmitancia entre los compuestos biodegradados y los compuestos sintetizados. Sobre todo hay una reducción en la banda de vibración alrededor de 1646 cm de los inhibidores biodegradados, indicando que su concentración se redujo probablemente por la acción bacteriana.
Infrarojo (KBr, cm-1):
]]> Reactivos purosR y S-metilbencilamina KBr [2968.7, 1576, 1451.5, 1372.1, 1152.7, 1026.1, (764, 700, 591, 538.9)]. 1576 cm distintivo de la unión C-NH2 del grupo amino.
2-piridincarboxaldehido KBr [3055.4, 2822.7, 1700, 1585, 1438, 1214, 995.6, (833, 765.9, 663.9)]. 1700 cm señal distintiva del grupo aldehído.
Inhibidores: SiminaM, SiminaMQ, RiminaM y RiminaMQ KBr [2972.6, 2862.7, 1646, 1587, 1492.8, 1467.8, 1371, 1081.6, 908.7, (763, 699.7, 492.5)]. 1646 cm corresponde al estiramiento C = N característico del grupo imino.
Los cuatro espectros de los inhibidores biodegradados fueron obtenidos del precipitado de los cultivos del consorcio 11 y sus bandas características son las siguientes:
SiminaM KBr [3440.5, 2920, 2850, 1640, 1463, 1039.1, (691.3, 541.8)]
SiminaMQ KBr [3440.3, 2919.8, 2850.2, 2346.4, 1635.4, 1462.6, 1240.1, 1038.3, (694.5, 535.9, 394.5)]
RiminaM KBr [3419, 2929.9, 2851.1, 1642.1, 1540, 1452.8, 1404.2, 1238.7, 1057.2, (696, 540.8)]
RiminaMQ KBr [3439.8, 2924, 2853.3, 2344.8, 1639.1, 1538.4, 1462.3, 1378.1, 1239.3, 1056.9, (771.5, 695.9, 534)]
Los valores de las bandas similares o iguales que se repiten en las regiones 3000 a 2000, 1900 a 1000 y 900 a 370 cm-1 están marcadas en negritas; las bandas únicas están subrayadas; las bandas características de las iminas están en cursivas y las que se consideran como la huella dactilar de cada compuesto biodegradado están en paréntesis.
]]> Se puede concluir que los compuestos imínicos quirales de tipo S fueron mejor biodegradados por las bacterias aisladas que los compuestos de tipo R. Además, de los compuestos tipo S, el que se obtuvo por mecanosíntesis (SiminaM) es el que presenta las mejores características de biodegradabilidad, lo que permite decir que el método de síntesis también puede influir en la biodegradación de los inhibidores de corrosión de tipo iminas quirales.Finalmente, se concluye que mediante espectrofotometría UV-Vis y FTIR se demuestra que los compuestos de tipo S tuvieron mejores resultados de biodegradabilidad en contraste con los de tipo R, ya que las bacterias empleadas mostraron más habilidad para degradar a los primeros. Una explicación de lo anterior es que posiblemente en el metabolismo de los seres vivos, los enantiomeros S son los sustratos adecuados para la actividad enzimática quiral y suelen ser de un sólo tipo. Por ejemplo, los carbohidratos que conforman a los seres vivos sólo son de tipo D-(R-) o los aminoácidos que forman las proteínas son únicamente de tipo L (S-) (Stryer 2003).
Es probable que la vía de biodegradación de los inhibidores de corrosión incluya una enzima similar a la tolueno dioxigenasa que inicie hidroxilando dos veces el anillo benzil de las iminas. Esta enzima ya ha sido reportada para Citrobacter freundii (aromatic-ring-hydroxylating-dioxygenase -arhdo- GenBank:ADW84022.1), Alcaligenes faecalis (benzoate 1,2-dioxygenase NCBI WP_003800424), Aeromonas caviae (glyoxalase/bleomycin resistance protein/dioxygenase WP_010675147) y Pseudomonas pseudoalcaligenes (protocatechuate 3,4-dio-xygenase WP_003463171; Catechol 1,2-dioxyge-nase WP_003458236; Benzoate 1,2-dioxygenase WP_003454108; 2,3-dihydroxybiphenyl dioxyge-nase AAA25753). Posteriormente la predicción es que suceda el rompimiento del anillo bencénico generando tres productos al menos, como puede verse en el mapa catabólico, figura 5 (Gao et al. 2010)
Este análisis in silico (Hou et al. 2003, Gao et al. 2010) con la base de datos de la Universidad de Minesota, permite visualizar cómo las iminas continúan íntegras en las dos etapas que siguen y que hipotéticamente se predicen, pues siguen apareciendo las señales (1640, 1635, 1642.1, 1639.1 cm) en los espectros de infrarojo aunque a menor concentración. Estas fases que siguen son la de la doble hidroxilación y la del rompimiento del anillo piridínico mediante dioxigenasas (Fig. 5, compuestos 3 a 6, 5 a 7). El mapa metabólico predice el rompimiento de los dos anillos aromáticos quedando productos simples y no contaminantes.
En conclusión, el trabajo sugiere que las bacterias aisladas tienen el potencial enzimático para biodegradar a las iminas quirales.
AGRADECIMIENTOS
Este trabajo recibió fondos de la Secretaría de Educación Pública, así como del Programa para Mejoramiento del Profesorado (PROMEP-UAEH-CA-25 Investigación Biomédica) y del proyecto SEP-CONACyT Ciencia Básica No. 23889, denominado "Evaluación electroquímica de inhibidores de corrosión. Síntesis y biodegradabilidad".
REFERENCIAS
]]>Acuña A., Pucci G., Morales M.J. y Pucci O. (2010). Biodegradación de petróleo y sus derivados por la comunidad bacteriana en un suelo de la Patagonia, Argentina. Rev. Soc. Ven. Microbiol. 30, 29-36. [ Links ]
Beyer M.K. y Clausen-Schaumann H. (2005). Mechanochemistry: The activation of covalent bonds. Chem. Rev. 105, 2921-2948. [ Links ]
Bradford S.A. (1993). Corrosion control. Springer - Verlag. Nueva York, EUA, 235 pp. [ Links ]
Branco S.M. (1984). Limnología sanitaria, estudio de la polución de aguas continentales. Monografía científica. Omega. Barcelona, España, 119 pp. [ Links ]
Cadena-Franco J.H. (2010). Comparación Electroquímica de Compuestos Imínicos Quirales. Tesis de Licenciatura. Instituto de Ciencias Básicas e Ingeniería, Universidad Autónoma del Estado de Hidalgo, México, 47 pp. [ Links ]
]]>El-Sheekh M.M., Ghareib M.M. y Abou-El-Soud G.W. (2012). Biodegradation of phenolic and polycyclic aromatic compounds by some Algae and Cianobacteria. J. Bioremed. Biodegrad. 3, 1-9. [ Links ]
Félix-Soto J.N., Gutiérrez-Castrejón T., Lemos-Pastrana A., Ortiz-Jiménez M.A., Pescador-Elizondo N.L. y Varela-Fregoso L. (1998). Manual de laboratorio de ecología microbiana. Instituto Politécnico Nacional, México, 179 pp. [ Links ]
Gao J., Ellis L.B.M. y Wackett L.P. (2010). The University of Minnesota Biocatalysis/Biodegradation Database: improving public access. Nucleic Acids Research 38: D488-D491. [en línea] http://www.umbbd.ethz.ch/predict/. [ Links ]
Garrity M.G. (2001). Manual of systematic bacteriology. Springer - Verlag, Nueva York, EUA, 1256 pp. [ Links ]
Gutiérrez R., Vázquez R.A. y Bernés S. (2000). Reacción de cicloadición [4+2] Diels Alder del Fulereno C60 y la N, N'-bis[(S)-1-feniletil]-2,3-butanodiimina. Rev. Latinoamer. Quím. 28, 43-48. [ Links ]
]]>Hernández L., Vázquez R.A., Coreño O., Veloz M.A., Hernández L.E., Coreño J. y Martínez M. (2014). Mechanosynthesis of a-diimines with corrosion inhibitor properties. Adv. Mat. Res. 976, 64-69. [ Links ]
Hou B.K., Wackett L.P. y Ellis L.B.M. (2003). Microbial pathway prediction: A functional group approach. J. Chem. Inf. Comput. Sci. 43, 1051-1057. [ Links ]
Jones D.M., Head I.M., Gray N.D., Adams J.J., Rowan A.K., Aitken C.M., Bennett B., Huang H., Brown A., Bowler B.F. J., Oldenburg T., Erdmann M. y Larter S. R. (2008). Crude oil biodegradation via methanogenesis in subsurface petroleum reservoir. Nature 451, 176-181. [ Links ]
Kaiser J.P., Feng Y. y Bollag J.M. (1996). Microbial metabolism of pyridine, quinoline, acridine and their derivatives under aerobic and anaerobic conditions. Microbiol. Rev. 60, 483-498. [ Links ]
Kalwasinska A., Kesy J., Wilk I. y Donderski W. (2011). Neustonic versus epiphytic bacteria of eutrophic lake and their biodegradation ability on deltametrin. Biodegradation 22, 699-707. [ Links ]
]]>Kocberber N.K., Karacakaya P., Duygu E. y Donmez G. (2011). Biodegradation of phenol by Synechocystis sp. in media including triacontanol hormone. Water and Environ. J. 32, 87-92. [ Links ]
Leahy S.G. y Collwell R.R. (1990). Microbial degradation of hydrocarbons in the environment. Microbiol. Rev. 54, 305-315. [ Links ]
McMurry J. (2004). Química orgánica. International Thomson Editores S.A. México, D.F. 1172 pp. [ Links ]
PEMEX (2011). Norma Oficial Mexicana NRF-004-PE-MEX-2011. Protección con recubrimientos anticorrosivos a instalaciones superficiales de ductos. (Esta norma cancela y sustituye a la NRF-004-PEMEX-2003 del 24 de junio de 2003). Petróleos Mexicanos. Diario Oficial de la Federación. 21 de octubre de 2011. [ Links ]
Prakash B. e Irfan M. (2011). Pseudomonas aeruginosa is present in crude oil contaminated sites of Barmer region (India). J. Bioremed. Biodegrad. 2, 1-3. [ Links ]
]]>Rocha F.R. y Teixeira L.S. (2004). Estrategias para aumento de sensibilidad en espectrofotometría UV-Vis. Quim Nova. 27, 807-812. [ Links ]
Rullkótter J. y García-Pichel F. (2002). Microbial diversity of a heavily polluted microbial mat and its community changes following degradation of petroleum compounds. Appl. Environ. Microbiol. 68, 1674-1683. [ Links ]
Sastri V.S. (1998). Corrosion inhibitors: Principles and applications. Wiley,Chichester, Nueva York, EUA, 903 pp. [ Links ]
Surynayana C., Ivanov E. y Boldyrev V.V (2001). The science and technology of mechanical alloying. Mat. Sci. Eng. A 304-306, 151-158. [ Links ]
Schlegel H.G. y Zaburosch C. (1997). Microbiología general. Ediciones Omega S.A. Barcelona, España, 651 pp. [ Links ]
]]>Stryer L., Berg J.M. y Timockzo J.L. (2003) Bioquímica. 5ta. Ed. Editorial Reverté, Barcelona, España, 1096 pp. [ Links ]
Vasdev K. (2011). Decolorization of triphenylmethane dyes by six white-rot fungi isolated from nature. J. Bioremed. Biodegrad. 2, 1-5. [ Links ]
Zipper C., Nickel K., Angst W. y Kohler H.P. (1996). Complete microbial degradation of both enantiomers of the chiral herbicide mecoprop [(RS)-2-(chloro-2-methylphenoxy) propionic acid] in an enantioselective manner by Sphingomonas herbicidovorans sp. Appl. Environ. Microbiol. 12, 4318-4322. [ Links ]
]]>