
Tolerance of filamentous fungi to endosulfan, chlorpyrifos and chorotalonil in in vitro conditions
Katina Stamatiu-Sánchez1, Alejandro Alarcón2*, Ronald Ferrera-Cerrato2. Cristian Nava-Díaz3, Julio Sánchez-Escudero4, Jesús Samuel Cruz-Sánchez5 y María del Pilar Castillo6
1 Área de Entomología, Postgrado en Fitosanidad, Campus Montecillo, Colegio de Postgraduados, Carretera México-Texcoco Km. 36.5, Montecillo, Texcoco, Estado de México, México, C.P. 56230
2 Área de Microbiología, Postgrado de Edafología, Campus Montecillo, Colegio de Postgraduados, Carretera México-Texcoco Km. 36.5, Montecillo, Texcoco, Estado de México, México. C.P. 56230*Autor de correspondencia: aalarconcp@gmail.com
3 Área de Fitopatología, Postgrado en Fitosanidad. Campus Montecillo. Colegio de Postgraduados. Carretera México-Texcoco Km. 36.5, Montecillo, Texcoco, Estado de México, México, C.P. 56230
]]> 4 Área de Agroecología, Postgrado en Fitosanidad, Campus Montecillo, Colegio de Postgraduados, Carretera México-Texcoco Km. 36.5, Montecillo, Texcoco, Estado de México, México, C.P. 562305 Unidad de Servicios de Apoyo en Resolución Analítica (SARA), Universidad Veracruzana, Luis Castelazo S/N, Industrial Las Animas, Xalapa, Veracruz, México C.P. 91190
6 Swedish Institute of Agricultural and Environmental Engineering (JTI). Box 7033 | S-750 07 Uppsala, Suecia
(Recibido septiembre de 2013;
aceptado septiembre 2014)
RESUMEN
Los plaguicidas endosulfán (EN), clorpirifós (CRP) y clorotalonil (CTL) están catalogados como carcinógenos y persistentes en el ambiente, por lo que deben tomarse medidas eficientes de biorremediación para su degradación. Los hongos Phanerochaete chrysosporium (PC), Trametes versicolor (TV) y algunas especies de Trichoderma (TRI), Mucor, Fusarium y Penicillium pueden degradar plaguicidas. En la presente investigación se aislaron y purificaron siete cepas de hongos a partir de suelo agrícola, paja molida de trigo y trozos de paja de trigo. Las siete cepas fúngicas aisladas y tres cepas de referencia (PC, TV y TRl) se colocaron por triplicado, en cajas de Petri con un medio mínimo mineral contaminado con dosis crecientes de EN, CRP y CTL durante 18 días. Diariamente se midió el desarrollo micelial (DM) y se calculó el porcentaje de inhibición del desarrollo (PID). Los tres plaguicidas tuvieron un efecto adverso sobre el DM, en el que se observó una recuperación paulatina después de 72 h ante EN y CRP, mientras que CTL inhibió significativamente (P < 0.0001) el DM de la mayoría de las cepas durante los 18 días. En presencia de EN, las cepas K14S, PC, TV y TRI se recuperaron totalmente a los 18 días. Ante CRP, todas las cepas mostraron recuperación del DM desde el día 10. El fungicida (CTL) mostró los mayores PID, pero las cepas K8S, K14S, K11TP, PC y TV mostraron recuperación. Los aislamientos K12P, K8S, K14S, K11TP y las cepas de referencia PC, TV y TRI presentaron tolerancia a los plaguicidas en estudio por lo que pudieran ser consideradas para la biorremediación de plaguicidas.
Palabras clave: plaguicidas, insecticida organoclorado, insecticida organofosforado, fungicida policlorado, crecimiento fúngico, inhibición fúngica.
]]>ABSTRACT
Endosulfan (EN), chlorpyrifos (CRP) and chlorothalonil (CTL) are carcinogenic and toxic pesticides in the environment, by which bioremediation efficient actions must be directed for detoxifying contaminated systems. Fungi such as Phanerochaete chrysospo-rium (PC), Trametes versicolor (TV) and some species of Trichoderma (TRI), Mucor, Fusarium and Penicillium are able to degrade pesticides. Seven fungal strains were isolated from agricultural soil, wheat straw, and wheat straw pieces. The seven fungal strains as well as three referential fungi (PC, TV and TRI) were cultivated by triplicate in Petri dishes with minimal mineral medium contaminated with increased doses of EN, CRP or CTL for 18 days. The mycelial growth (MG) and the percentage of growth inhibition (PGI) were determined. The three pesticides negatively affected the MG, but the fungal recovery was observed after 72 h for EN and CRP. At 18 days, strains K14S, PC, TV and TRI showed total recovery when exposed to EN. In contrast, all fungal strains showed a recovery to CRP at the 10th day. The MG for most fungal strains was significantly inhibited (P < 0.0001) due to during CTL at 18 days. The fungicide CTL resulted in highest PGI, but strains K8S, K14S, K11TP, PC and TV were less affected. The fungal strains K12P, K8S, K14S, and K11TP showed acceptable tolerance to the three pesticides comparable to PC, TV and TRI. These four fungal strains are good candidates for being used for pesticide bioremediation.
Key words: pesticides, chlorinated insecticide, organophosphate insecticide, polychlorinated fungicide, fungal growth, fungal inhibition.
INTRODUCCIÓN
Las actividades agrícolas, el uso excesivo y las malas prácticas del manejo de plaguicidas durante la producción agrícola han llevado a la acumulación y a la contaminación de todos los ambientes por plaguicidas debido a su dispersión, lixiviación y volatilización (Linde 1994, Arias-Estévez et al. 2008), por lo que son un riesgo para la salud humana y otros organismos (Bohmont 2007). El endosulfán es un insecticida organoclorado del grupo de los ciclodienos catalogado como carcinógeno, es de amplio uso en el sector agrícola, su metabolito el endosulfán sulfato, es más tóxico y persistente que la molécula parental (Greene y Pohanish 2005, Jayashree y Vasudevan 2007). Por otro lado, el insecticida organofosforado clorpirifós es ampliamente usado para controlar plagas de importancia agrícola, humana y veterinaria, su persistencia es de hasta 120 días y está catalogado como carcinógeno y disruptor endócrino (Singh et al. 2006). Finalmente, el clorotalonil es un fungicida de contacto y amplio espectro utilizado en diversos cultivos, tiene una vida media de hasta 90 días y está catalogado como un compuesto carcinógeno (Greene y Pohanish 2005).
Para remediar los problemas de contaminación por plaguicidas en condiciones in situ, se han desarrollado técnicas de biorremediación mediante la selección y uso de microorganismos capaces de tolerar y degradar contaminantes. Los hongos degradadores de residuos ligninocelulósicos pueden degradar diversos contaminantes mediante la secreción de enzimas (Maloney 2001). Hongos ligninolíticos como Phanerochaete chrysosporium y Trametes versicolor, entre otros, son capaces de degradar hidrocarburos del petróleo y plaguicidas (Adam-Ali y Wainwrigth 1994, Kim et al. 2001, Jáuregui et al. 2003, Matsubara et al. 2006). Además, los hongos no ligninolíticos como Aspergillus, Fusarium, Mucor, Penicillium y Trichoderma son tolerantes y degradadores de plaguicidas e hidrocarburos (Mitra et al. 2001, Dan et al. 2006, Kim y Lee 2007, Sagar y Singh 2011, Argumedo-Delira et al. 2012).
El conocimiento de la capacidad de los microorganismos para degradar plaguicidas en campo ha permitido implementar sistemas de biorremediación in situ conocidos como biocamas (BD, por sus siglas en inglés). Estos sistemas están conformados por mezclas de residuos vegetales, turba o composta y suelo, y para su preparación se colocan a 60 cm de profundidad con el fin de minimizar la contaminación por plaguicidas en zonas agrícolas o industriales (Torstensson 2000, Castillo et al. 2008, Karanasios et al. 2010, Karanasios et al. 2012, Omirou et al. 2012, Urrutia et al. 2013). Para aumentar la capacidad y la velocidad de degradación de plaguicidas en las BD, se busca favorecer el desarrollo o la inoculación (bioaumentación) de hongos ligninolíticos. Sin embargo, el potencial de estos hongos puede ser inhibido por la rápida invasión y competencia de otros microorganismos presentes en los diferentes sustratos utilizados en las BD (Karanasios et al. 2012). Una alternativa es la adición de suelo o microorganismos capaces de degradar plaguicidas (Ónneby et al. 2010, Karanasios et al. 2012).
Este trabajo consistió en seleccionar hongos aislados de paja de trigo y de suelo agrícola con capacidad de tolerar endosulfán, clorpirifós y clorotalonil, como parte inicial de la búsqueda de hongos degradadores de plaguicidas para utilizarlos en procesos de biorremediación.
]]>MATERIALES Y MÉTODOS
Plaguicidas y cepas de referencia. Los plaguicidas utilizados correspondieron a formulaciones grado técnico. El endosulfán (98 % pureza) fue donado por Bayer Cropscience, México S.A. de C.V., el clorpirifós (98 % pureza) por Dow-AgroSciences de México S.A. de C.V. y el clorotalonil (98.8 % pureza) por Syngenta Agro S.A. de C.V. Las cepas de referencia Phanerochaete chrysosporium cepa CDBBh-298 (PC) y Trametes versicolor (TV) son hongos ligninolíticos donados por la Dra. Refugio Rodríguez del Centro de Investigación y de Estudios Avanzados del Instituto Politécnico Nacional. La cepa de Trichoderma koningii (Tri23) proviene del cepario microbiano del Área de Microbiología del Colegio de Postgraduados y aunque no es un hongo ligninolítico, es tolerante al petróleo crudo y a los hidrocarburos poliaromáticos (HPA) (Argumedo-Delira et al. 2012).
Aislamiento y selección de hongos filamentosos. Las siete cepas de hongos filamentosos consideradas en el presente trabajo fueron aisladas de suelo agrícola, paja molida de trigo y trozos de paja de trigo provenientes del municipio de Silao, en Guanajuato, México (Stamatiu-Sánchez 2013). El crecimiento fúngico fue reactivado con el método de extensión superficial (Ramírez-Gama et al. 1998) en un medio de papa dextrosa agar (PDA, Merck®). Las cepas fueron seleccionadas mediante ensayos preliminares (Stamatiu-Sánchez 2013) con base en su crecimiento en un medio de cultivo enriquecido con endosulfán < 1000 mg/kg, lo que sobrepasa los niveles de este plaguicida encontrados en suelo (Goncalves et al. 2006, ATSDR 2014). La identificación molecular se llevó a cabo en el Laboratorio de Identificación Fitopatológica del Colegio de Postgraduados. Los aislamientos fueron determinados como Fusarium sp. (cepa K2P), Fusarium sp. (cepa K12P), Fusarium oxysporum (cepa K1S), Penicillium janthinellum (cepa K8S), Mucor circinelloides (cepa K14S), Fusarium verticilloides (cepa K3TP) y Alternaria alternata (cepa K11TP).
Pruebas de tolerancia a endosulfán, clorpirifós y clorotalonil. Las dosis probadas para endosulfán fueron 1000, 2000 y 3000 mg/L, para clorpirifós 100, 250, 500, 1000 y 2000 mg/L y para clorotalonil 25, 50, 100 y 200 mg/L. Cada plaguicida fue diluido por separado con acetona grado reactivo (Fermont®) y se aplicaron de acuerdo con sus dosis, como única fuente de carbono sobre medio mínimo sólido (MMS) en cajas de Petri. La composición del MMS fue la siguiente (g/L): 0.5 (MD2SO4, 0.5 KH2PO4, 0.2 KCl, 0.2 MgSO4- 7H2O, 0.1 CaCl2 y 20 agar-agar. En cada ensayo con cada plaguicida se incluyó un testigo absoluto (TA) y un testigo con acetona (Ac), sin contaminante.
La contaminación del MMS se realizó en condiciones asépticas, distribuyendo 50 μL de la dilución del plaguicida correspondiente sobre la superficie de agar con ayuda de una espátula de Drigalski. Para cada cepa mencionada los plaguicidas se probaron con sus respectivas dosis por triplicado, incluyendo un testigo absoluto (TA) y un testigo con acetona (Ac). Las cajas de Petri para el testigo Ac fueron tratadas con 50 μL de acetona (3 μL/mL de medio de cultivo) sin plaguicida.
La siembra de las cepas se realizó colocando un sacabocados de la colonia fúngica con dos a seis días de edad en el centro de la caja contaminada. Cada 24 h se estimó el desarrollo del micelio (DM) al medir el diámetro (mm) de la colonia durante los primeros ocho días. Después, la medición se llevó a cabo cada 48 h hasta los 18 días. Las cajas de Petri se mantuvieron en incubadora (New Brunswick Scientific Inc. Edison) a 26 ± 1 °C durante todo el bioensayo.
El porcentaje de inhibición del desarrollo micelial (PID) a los tres, ocho y 18 días, se calculó mediante la siguiente fórmula:

Donde: DMTrat= Desarrollo micelial en el tratamiento con plaguicida, DMTA= Desarrollo micelial en el testigo absoluto.
]]> Análisis estadístico. Cada plaguicida fue analizado de manera individual, para lo cual el diseño experimental fue completamente al azar a través de un factorial 10 x 4 (diez cepas de hongos y cuatro dosis) para el endosulfán, 10 x 7 (diez cepas de hongos y siete dosis) para el clorpirifós y 10 x 6 (diez cepas de hongos y seis dosis) para el clorotalonil. Los datos obtenidos se sometieron a un análisis de varianza (ANOVA, por sus siglas en inglés) y a una prueba de comparación de medias (Tukey a = 0.05) mediante el programa Sistema de Análisis Estadístico (SAS 2002).
RESULTADOS
Tolerancia a endosulfán (EN). La figura 1 muestra el comportamiento del DM de las cepas. En ausencia del insecticida (TA y Ac) las cepas PC, TRI y K14S cubrieron la caja de Petri totalmente a los 4, 6 y 7 días, respectivamente. En presencia del insecticida el DM se vio afectado levemente, recuperándose por completo a los 6 (PC), 10 (TRI) y 16 (K14S) días. Las cepas TV y K8S cubrieron la caja de Petri en su totalidad a los 16 (TV) y 18 (K8S) días en los testigos. Sin embargo, ante EN a 1000, 2000 y 3000 mg/L, la cepa TV se recuperó totalmente a los 12 días. Por su parte, la cepa K8S no presentó una recuperación total, aunque no mostró diferencias significativas entre las tres dosis del contaminante y los testigos (Fig. 1).
Las cepas K2P, K12P y K11TP (Fig. 1), al igual que K1S y K3TP (datos no presentados) mostraron el crecimiento más lento y no hubo diferencias significativas entre los testigos TA y Ac. En contraste, la presencia de EN afectó significativamente (P < 0.0001) el DM en comparación con los testigos, con excepción de la cepa K3TP (datos no presentados). Lo anterior indica que el EN tuvo un efecto adverso en el desarrollo de estas cepas, sin embargo, hubo buena recuperación a los 18 días y no se obtuvieron diferencias significativas entre las dosis del insecticida (Fig. 1). La mayoría de las cepas mostraron una ligera inhibición en el DM con el solvente (Ac), aunque se recuperaron entre los 3 y 10 días (Fig. 1).
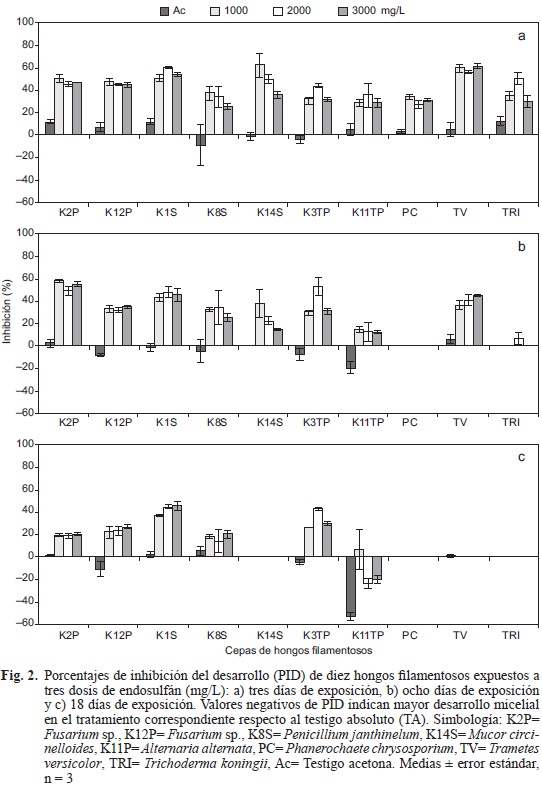
Con respecto a los porcentajes de inhibición de desarrollo (PID), por efecto del EN, todas las cepas fúngicas mostraron inhibición durante los primeros tres días. Las cepas PC, K11TP y K8S fueron las menos inhibidas por el insecticida en comparación con sus respectivos testigos. En contraste, las cepas con mayor inhibición fueron TV, K14S y K1S (Fig. 2 a). A los 8 días, los PID para las cepas PC y TRI fueron de cero por ciento en todos los tratamientos de EN, con excepción de TRI ante 2000 mg/L (Fig. 2b) cuyo PID fue de 6.8 %. En contraste, las cepas K12P, K1S, K8S, K3TP y K11TP tuvieron porcentajes de inhibición entre 15 y 55 %, mientras que la cepa K2P tuvo los PID más altos, con valores de hasta hasta 60 % (Fig. 2b). A los 18 días, las cepas TRI y K14S mostraron recuperación total al presentar cero por ciento de inhibición en todos los tratamientos, en tanto que las cepas K1S y K3TP presentaron inhibición mayor al 45 % (Fig. 2c). Los PID negativos que mostró TV y particularmente la cepa K11TP, indicaron mejor DM en los tratamientos con EN respecto al TA, con excepción de K11TP ante 1000 mg/L (Fig. 2c). Las cepas K12P, K8S, K3TP y K11TP presentaron mayor DM en el testigo acetona en comparación con el TA (Fig. 2a-c).
Tolerancia a clorpirifós (CRP). El DM de las cepas PC, TRI y K14S se inhibió inicialmente por la presencia de CRP. Sin embargo, se recuperaron en su totalidad a los 7, 10 y 12 días, respectivamente. En ausencia del plaguicida estas cepas alcanzaron el desarrollo máximo a los 4, 5 y 6 días, respectivamente (Fig. 3). La cepa TV mostró menor DM ante las cinco dosis de CRP en comparación con los testigos, pero tuvo una recuperación total a los 12 días (Fig. 3). Las cepas K11TP y K8S cubrieron la superficie de agar a los 10 (K11TP) y 14 (K8S) días. En ausencia del insecticida, ambas cepas mostraron disminución del DM en presencia de CRP. No obstante, se recuperaron totalmente a los 14 (K11TP) y 16 (K8S) días (Fig. 3). Por su parte, las cepas K2P y K12P (Fig. 3), al igual que K1S y K3TP (datos no mostrados), superaron el DM en comparación con sus testigos entre los días 3 y 8 cuando se expusieron ante las diferentes dosis de CRP, con excepción de K2P y K12P ante 2000 mg/L.
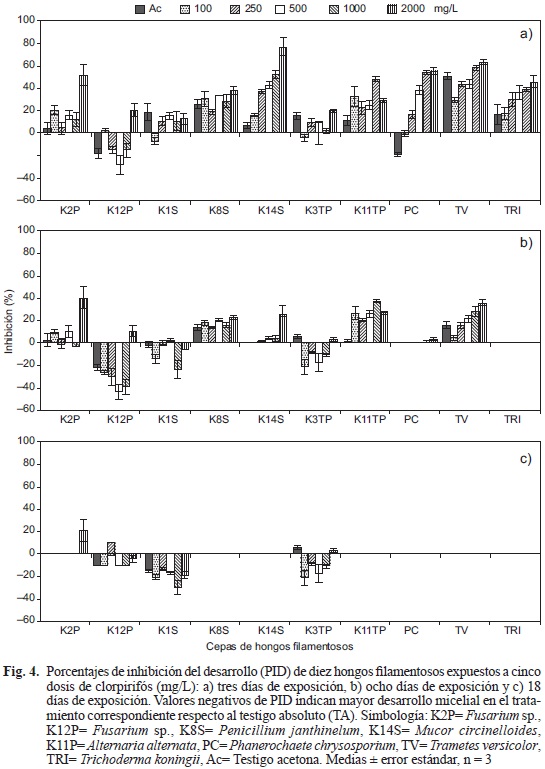
El CRP inhibió el desarrollo en todas las cepas en los primeros tres días, con excepción de la cepa K12P cuyos PID fueron negativos con Ac a 250, 500 y 1000 mg/L; la mayoría de las cepas mostraron ligera inhibición en el DM ante Ac (Fig. 4a). Las cepas PC, TRI, K14S y TV tuvieron los PID más altos con respecto a sus testigos y las cepas menos inhibidas fueron K1S, K3TP y K2P (Fig. 4a). A los ocho días la cepa TRI presentó cero por ciento de inhibición en todos los tratamientos, mientras que PC y K14S mostraron 3.2 y 26 % de inhibición ante CRP a 2000 mg/L, respectivamente (Fig. 4b). Las cepas TV, K11TP, K8S y K2P continuaron inhibidas hasta en un 40 % respecto a sus testigos. En contraste, las cepas K12P, K1S y K3TP mostraron valores de PID negativos, indicando mayor DM en los tratamientos con CRP respecto al TA (Fig. 4b). En el día 18, todas las cepas presentaron cero por ciento de inhibición por efecto del CRP, excepto la cepa K2P ante 2000 mg/L (Fig. 4c). Las cepas K12P, K1S y K3TP continuaron mostrando mayor desarrollo en los tratamientos respecto al testigo (Fig. 4c).
]]>
Tolerancia a clorotalonil (CTL). Las cepas K8S y PC se vieron afectadas por el fungicida. Sin embargo, mostraron recuperación a partir del día 10 (Fig. 5). En el día 18, en la concentración de 25 mg/L, la cepa PC alcanzó 83 mm de diámetro, mientras que la colonia de K8S alcanzó 79 mm y en ambos casos no hubo diferencias significativas entre esta dosis y los testigos (Fig. 5). El CTL afectó el DM de las cepas K14S, K11TP y TV pero se recuperaron a los 18 días, en este caso los diámetros de las colonias fluctuaron entre 53 y 83 mm. Además, el DM con las distintas dosis de CTL no fue significativamente diferente con respecto a TA y Ac (Fig. 5).
Las colonias de K2P, K12P (Fig. 5), K1S y K3TP (datos no presentados) sólo alcanzaron 40 mm de diámetro a los 18 días, pero el DM de estas cepas fue significativamente diferente (Tukey a = 0.05) respecto al TA y Ac (> 70 mm; Fig. 5). La cepa más afectada por el CTL fue TRI, cuyo DM fue menor a 8 mm en el quinto día y de apenas 32 mm a los 18 días, mientras que los testigos TA y Ac alcanzaron los 83 mm a los 4 y 5 días, respectivamente (Fig. 5).
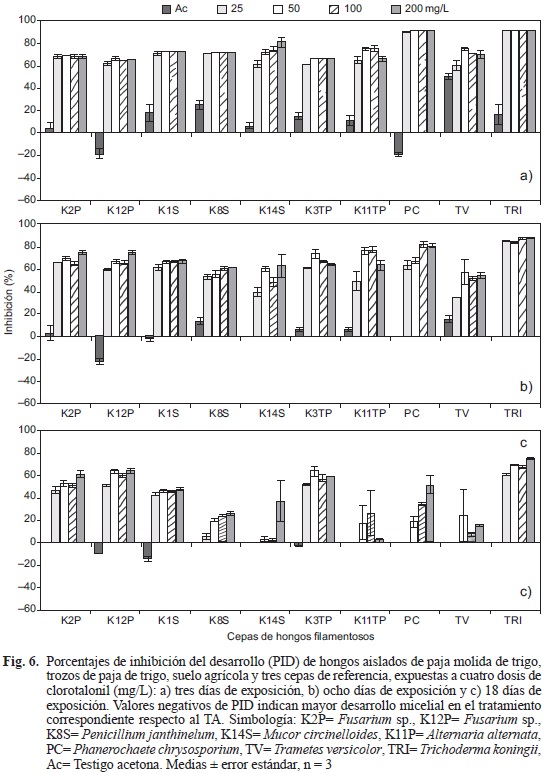
En cuanto a los PID, las cepas más afectadas por CTL a los tres días fueron TRI y PC (> 90 %), seguidas por la cepa K14S (81 %) mientras que para el resto de las cepas (K2P, K12P, K1S, K8S, K3TP, K11TP y TV) los valores de PID fueron de hasta 75.7 % (Fig. 6a). En el octavo día la cepa TRI presentó PID mayores a 85 %, siendo la cepa menos inhibida (58 %) en la dosis más alta de CTL, mientras que la cepa K14S mostró 39 % de inhibición ante 25 mg/L (Fig. 6b). Al día 18, la cepa TRI continuó siendo la cepa más afectada (PID > 60 %), en tanto que las cepas K2P, K12P, K1S y K3TP tuvieron valores de PID mayores a 42 % (Fig. 6c). Las cepas K8S, K14S, K11TP, PC y TV se recuperaron totalmente al mostrar cero por ciento de inhibición ante 25 mg/L, además las cepas K14S, K11TP y TV no presentaron diferencias significativas entre las dosis 50, 100 y 200 mg/L respecto al testigo Ac, lo que indica tolerancia al CTL. Las cepas se vieron afectadas con Ac al inicio, aunque en porcentajes bajos (Fig. 6a) con recuperación de la mayoría de las cepas desde los ocho días (Fig. 6b) y recuperación total de todas las cepas a los 18 días (Fig. 6c).
DISCUSIÓN
El disolvente Ac provocó inhibición en el DM en todas las cepas a los primeros tres días. Sin embargo, se recuperaron al final de los bioensayos (18 días) y en muchos casos el DM del testigo Ac superó al DM de sus correspondientes TA. El efecto tóxico que tuvo el disolvente en el presente trabajo (3 μL/mL de medio de cultivo) coincide con lo reportado por Vazquez-Nuñez et al. (2009) y Dutta et al. (2010). Estos autores, al adicionar acetona en un suelo, redujeron la actividad microbiana (medida en biomasa y emisión de CO2) durante los primeros siete días, en comparación con el testigo sin acetona y, transcurrido el periodo de inhibición, los microorganismos se recuperaron.
]]> El efecto tóxico de los solventes orgánicos como la acetona sobre los microorganismos en el suelo y el agua es conocido (Stratton 1989, Satsuma et al. 2001), pero este efecto es temporal y siempre hay una recuperación (Jenkinson y Powlson 1976). Algunos microorganismos pueden usar los solventes como fuente de carbono (Siller et al. 1996) e incluso la acetona puede facilitar la biodisponibilidad de nutrientes en el medio (Yeomans y Bremner 1989). La respuesta de los hongos ante la acetona fue medida por Field et al. (1992), quienes encontraron que altas concentraciones del solvente (100 y 200 mL/L) inhiben completamente el desarrollo de hongos como P. chrysosporium, Trametes sp. y Bjerkandera sp. Sin embargo, a concentraciones de 10 mL/L no hubo inhibición e incluso la cepa Bjerkandera sp. mostró mayor producción de CO2 con respecto al testigo, aunque esta cepa no utilizó a la acetona como fuente de carbono. Lo anterior coincide con lo observado en esta investigación ya que la cantidad aplicada de acetona al medio de cultivo equivale a 3 LL/mL de medio de cultivo, misma que no produjo efectos tóxicos permanentes en las cepas del bioensayo. Los hongos fueron inicialmente susceptibles al efecto tóxico de la acetona, pero después del periodo de adaptación (5 a 12 días) lograron tolerarla y usarla como fuente de carbono, superando el desarrollo del TA. Sin embargo, es necesario realizar estudios específicos del efecto y estímulo del solvente sobre los hongos.El EN disminuyó el DM en todas las cepas durante los primeros tres días con recuperación gradual. Este efecto inhibidor ha sido reportado por Mukherjee y Mittal (2005) al encontrar que Aspergillus terreus y Cladosporium oxysporum expuestos a EN incrementaron la disipación del insecticida a partir del tercer día. Hussain et al. (2007) encontraron poca degradación de EN durante los primeros tres días y observaron un notorio incremento en la degradación al sexto día de incubación con A. terreus, A. terricola y Chaetosartorius stromatoides. Bhalerao y Puranik (2007) indican que A. niger mostró inhibición de su crecimiento ante EN y después de la etapa de adaptación el hongo creció rápidamente, superando la biomasa obtenida en el testigo desde el segundo día de la contaminación. En la presente investigación, las cepas K14S, TRI, K8S, K11TP y K3TP presentaron mejor DM ante la dosis más alta de EN (3000 mg/L) en comparación con 1000 y 2000 mg/L entre los primeros tres y cuatro días (Fig. 1).
El insecticida CRP mostró un efecto adverso sobre el DM de todas las cepas a los tres días, pero con una recuperación total a los 18 días. La inhibición inicial de clorpirifós sobre el desarrollo fúngico, coincide con lo reportado por Fang et al. (2008) quienes encontraron que el CRP (100 mg/L) redujo la biomasa de Verticillium sp. durante los primeros cinco días y posteriormente se incrementó rápidamente. Un comportamiento similar fue descrito por Liu et al. (2002) con Trichoderma ante CRP (50 mg/L) durante siete días. De manera particular, las dos cepas de Fusarium (K2P y K12P) mostraron mayor DM en comparación con sus testigos entre los días 3 y 8 cuando se expusieron a las diferentes dosis de CRP (Fig. 3). Lo anterior denota su tolerancia y la posible estimulación del crecimiento por parte de este insecticida, misma que podría estar relacionada con su capacidad de degradación de plaguicidas organoclorados como el lindano (Guillén-Jiménez et al. 2012).
Al comparar los efectos inhibidores del EN y del CRP en el crecimiento de las cepas fúngicas, el del CRP fue mayor a los tres días (Fig. 4). Sin embargo, la mayoría de las cepas mostraron reducción en sus PID desde los 10 días, recuperándose totalmente a los 18 días. Mientras que ante EN, un número mayor de cepas continuaron inhibidas hasta los 18 días (Fig. 2). Este retraso en la recuperación del DM pudo deberse a que el EN (organoclorado) es químicamente más estable, acumulable y persistente (Ware 1994), con una presión de vapor baja (1.7 × 10-7 mm Hg a 20 °C; Green y Pohanish 2005), lo que lo hace una molécula de poca volatilidad. En contraste, la presión de vapor del CRP es media (1.87 × 10-5 mm Hg a 25 °C) y sus propiedades como organofosforado lo hacen menos persistente y menos tóxico (Ware 1994, Green y Po-hanish 2005). Con base en lo anterior, la residualidad y la complejidad de la estructura química del EN pudo provocar que la recuperación de los hongos ocurriera en mayor tiempo.
El CTL resultó más tóxico para los hongos al obtenerse altos PID (> 60 %) hasta los 18 días. De forma similar Singh et al. (2002) observaron que este fungicida (10 mg/kg) tuvo un fuerte efecto inhibidor sobre los microorganismos del suelo durante 90 días, en comparación con el CRP (10 mg/kg), cuyos efectos no fueron mayores a 30 días. La prolongada inhibición del desarrollo en la mayoría de las cepas (excepto las cepas K14S, K11TP, PC, TV) ante el CTL observada hasta los 18 días, se puede explicar por su acción fungicida, que afecta principalmente a las enzimas implicadas en la respiración y en la biosíntesis de proteínas (Tillman et al. 1973). Por lo anterior, es probable que las cepas fúngicas expuestas a CTL no hayan podido recuperarse durante el bioensayo (18 días) como lo hicieron ante el EN y el CRP. Sin embargo, varias cepas se recuperaron totalmente ante la concentración más baja de CTL (25 mg/L). Una respuesta similar es reportada por Guillén et al. (2009) quienes encontraron que los preservadores de madera con propiedades antifúngicas inhiben el desarrollo de tres cepas de hongos incluyendo a T. versicolor, el cual fue tolerante a dosis bajas, comportamiento similar al observado en esta investigación con el CTL (25 mg/L). Por su parte, el crecimiento de P. chrysosporium fue afectado por la aplicación de benomil ante dosis tan altas como 225 Lg/g (Adam-Ali y Wainwrigth 1994). Lo anterior explica la inhibición del crecimiento de este hongo a concentraciones altas de CTL, con lo que se resalta su susceptibilidad a la aplicación de fungicidas. En el presente estudio las cepas K8S, K14S, K11TP, PC y TV fueron tolerantes a la dosis más baja de CTL (25 mg/L).
Algunas cepas expuestas a CRP (K12P, K1S y K3TP) o a EN (K11TP) superaron el DM de sus respectivos testigos después de un periodo de inhibición (3 a 16 días). Dutta et al. (2010) encontraron un estímulo en la respiración basal y en la biomasa microbiana al aplicar CRP en comparación con el testigo. Das y Mukherjee (2000) y Eisenhauer et al. (2009) obtuvieron un incremento en la población de microorganismos en el suelo después de la aplicación de plaguicidas organofosforados y organoclorados. En cuanto a los hongos, Field et al. (1992) observaron que Bjerkandera sp. mostró mayor respiración en presencia de benzopireno, antraceno y antraquinona. Por su parte, Bhalerao y Puranik (2007) encontraron mayor biomasa fúngica de A. niger en presencia de EN, debido probablemente a su disponibilidad como fuente de carbono y sulfuro en el medio. Siddique et al. (2003) reportan que Fusarium ventricosum fue capaz de utilizar EN como única fuente de carbono. Es probable que en la presente investigación las cepas fúngicas que superaron el DM con respecto a sus testigos, además de tolerar, pudieron haber utilizado a los insecticidas (EN y CRP) como fuente de energía para su desarrollo, una vez superado el periodo de inhibición. Sin embargo, se requiere de mayor estudio al respecto.
Los hongos de referencia P. chrysosporium y T. versicolor mostraron tolerancia a las diferentes concentraciones de EN y CRP y ante CTL a 25 mg/L. Además, la cepa de referencia T. koningii también exhibió tolerancia a los insecticidas. La capacidad de estas especies fúngicas como degradadoras de endosulfán, pentaclorofenol, isoproturón y HPA ha sido demostrada en otras investigaciones (Dhawale et al. 1992, Rüttimann-Johnson y Lamar 1997, Kim et al. 2001, Wirén-Lehr et al. 2001). La cepa K12P (Fusarium sp.) presentó buena tolerancia al EN y excelente recuperación ante el CRP, sin embargo, se vio inhibida por el CTL. Las respuestas de este género fúngico a los plaguicidas han sido poco estudiadas, aunque se tienen reportes sobre su tolerancia, degradación y acumulación de compuestos tóxicos como trifluralina, atrazina, glifosato, lindano y HPA (Jeffery y Burguess 1990, Yu et al. 1998, Verdin et al. 2005, Sagar y Sing 2011).
La presente investigación reporta solamente la tolerancia de cinco especies de hongos filamentosos aislados de sustratos que potencialmente pueden ser utilizados en sistemas de biorremediación como lo son las biocamas. Se muestra evidencia de que estos hongos pueden tolerar concentraciones extremadamente altas de los tres plaguicidas. En el caso de las dos cepas Fusarium (K2P y K12P), la tolerancia observada ante el EN y el CRP puede relacionarse con la capacidad potencial de degradar plaguicidas organoclorados, como el lindano, a través de una carboxilación aeróbica descrita para F. verticillioides (Guillén-Jiménez et al. 2012). Mientras que para el caso del CRP, la cepa Fusarium WZ-I tiene enzimas que pueden contribuir en la degradación de este plaguicida (Xie et al. 2010). En el caso de la respuesta observada de Fusarium ante el CTL, se infiere que este género es altamente tolerante a este fungicida, ya que Fravel et al. (2010) describen efectos inhibidores del crecimiento miceliar a concentraciones de CTL de 10 mg/L. No obstante, la información sobre las respuestas fisiológicas o bioquímicas de los miembros de este género de hongos ante la presencia de plaguicidas requiere de un mayor estudio. Las cepas Mucor circinelloides (K14S) y Penicillium janthine-llum (K8S) mostraron excelente tolerancia al EN y el CRP y buena recuperación con CTL. Estos hongos tienen capacidad de tolerar y de degradar plaguicidas organoclorados como la atrazina, o bien creosota y HPA (Kaufman y Blake 1970, Atagana 2004, Silva-Jiménez y Zazueta-Sandoval 2005, Dan et al. 2006, Kim y Lee 2007, Kataoka et al. 2010). Sin embargo existe poca información sobre su tolerancia y degradación de EN, CRP y CTL. Con respecto al género Alternaria, la información es prácticamente nula, por lo que la presente investigación contribuye a la generación de información básica de este organismo en lo que respecta a su tolerancia a estos tres plaguicidas.
CONCLUSIONES
]]> Las cepas fúngicas evaluadas mostraron diferentes grados de tolerancia a EN, CRP y CTL. Estos plaguicidas causaron mayor inhibición del DM durante los primeros tres días, pero las cepas mostraron una recuperación gradual. El fungicida CTL provocó la mayor inhibición, en contraste, las cepas expuestas a CRP se recuperaron totalmente a los 18 días. Asimismo, a los 18 días la cepa TRI y Mucor circinelloides (cepa K14S) mostraron recuperación total ante EN en todas sus concentraciones. El crecimiento de Fusarium oxysporum (cepa K1S) y Fusarium verticilloides (cepa K3TP) fue inhibido en un 45 %. En el caso del CRP, todas las cepas presentaron cero por ciento de inhibición al día 18, excepto Fusarium sp. (K2P) a 2000 mg/L (Fig. 4c), mientras que las cepas Fusarium sp. (K12P), Fusarium oxysporum (K1S) y Fusarium verticilloides (K3TP) mostraron mayor desarrollo con respecto al TA. En presencia de CTL, la cepa TRI mostró PID mayores al 60 %, en tanto que en las cepas K2P, K12P, K1S y K3TP los valores de PID fueron mayores a 42 %. Las especies Penicillium janthinellum (K8S), Mucor circinelloides (K14S), Alternaria alternata (K11TP) y las cepas de referencia PC y TV, se recuperaron totalmente del CTL al mostrar cero por ciento de inhibición a los 25 mg/L. En resumen, las cepas K14S (Mucor circinelloides), K8S (Penicillium janthinellum), K11TP (Alternaria alternata) y K12P (Fusarium sp.), exhibieron una tolerancia hacia EN (1000, 2000 y 3000 mg/L), CRP (100, 250, 500, 100 y 2000 mg/L) y CTL (25 mg/L), por lo que tienen potencial para ser evaluadas sobre su capacidad de biodegradación de estos plaguicidas.
AGRADECIMIENTOS
Esta investigación fue financiada por el proyecto SEP-CONACyT 79456. Además, KSS agradece al CONACyT su apoyo durante su programa de doctorado.
REFERENCIAS
Adam-Ali T.A. y Wainwrigth M. (1994). Growth of Pha-nerochaete chrysosporium in soil and its ability to degrade the fungicide benomyl. Bioresource Technol. 49, 197-201. [ Links ]
Argumedo-Delira R., Alarcón A., Ferrera-Cerrato R., Almaraz J.J. y Peña-Cabriales J.J. (2012). Tolerance and growth of 11 Trichoderma strains to crude oil, naphthalene, phenanthrene and benzo[a]pyrene. J. Environ. Manage. 95, S291-S299. [ Links ]
]]>Arias-Estévez M., López-Periago E., Martínez-Carballo E., Simal-Gándara J., Mejuto J.C.y García-Río L. (2008). The mobility and degradation of pesticides in soils and the pollution of groundwater resources. Agric. Ecosyst. Environ. 123, 247-260. [ Links ]
Atagana H.I. (2004). Biodegradation of phenol, o-cresol, m-cresol and p-cresol by indigenous soil fungi in soil contaminated with creosote. World J. Microb. Biot. 20, 851- 85. [ Links ]
ATSDR (2014). ToxGuideTM for endosulfan. Agency for Toxic Substances and Disease Registry. Consultado en septiembre del 2014. [en línea]http://www.atsdr.cdc.gov/toxguides/toxguide-41.pdf. [ Links ]
Bhalerao T.S. y Puranik P.R. (2007). Biodegradation of organochlorine pesticide, endosulfan, by a fungal soil isolate, Aspergillus niger. Int. Biodeter. Biodegr. 59, 315-321. [ Links ]
Bohmont B.L. (2007). The standard pesticide users guide. Pearsons Prentice Hall. Upper Saddle River, Nueva Jersey, EUA. 245 pp. [ Links ]
]]>Castillo M.D.P., Torstensson L. y Stenstróm J. (2008). Biobeds for environmental protection from pesticide uses: a review. J. Agric. Food. Chem. 56, 6206-6219. [ Links ]
Dan S., Pei-jun L., Stagnitti F. y Xian-zhe X. (2006). Biodegradation of benzo[a]pyrene in soil by Mucor sp. SF06 and Bacillus sp. SB02 co-immobilized on vermiculite. J. Environ. Manage. 18, 1204-1209. [ Links ]
Das A.C. y Mukherjee D. (2000). Soil application of insecticides influences microorganisms and plant nutrients. Appl. Soil. Ecol. 14, 55-62. [ Links ]
Dhawale S.W., Dhawale S.S. y Dean-Ross D. (1992). Degradation of phenantrene by Phanerochaete chrysosporium occurs under ligninolytic as well nonligninolytic conditions. Appl. Environ. Microbiol. 58, 3000-3006. [ Links ]
Dutta M., Sardar D., Pal R. y Kole R. K. (2010). Effect of chlorpyrifos on microbial biomass and activities in tropical clay loam soil. Environ. Monit. Assess. 160, 385-391. [ Links ]
]]>Eisenhauer N., Klier M., Partsch S., Sabais C.W.A., Scherber C., Weisser W.W. y Scheu S. (2009). No interactive effects of pesticides and plant diversity on soil microbial biomass and respiration. Appl. Soil. Ecol. 42, 31-36. [ Links ]
Fang H., Xiang Y.Q., Hao Y.J., Chu X.Q., Pan X.D., Yu J.Q. y Yu Y.L. (2008). Fungal degradation of chlorpyrifos by Verticillium sp. DSP in pure cultures and its use in bioremediation of contaminated soil and pakchoi. Int. Biodeter. Biodegr. 61, 294- 303. [ Links ]
Field J.A., De Jong E., Feijoo C.G. y De Bont J.A.M. (1992). Biodegradation of polycyclic aromatic hydrocarbons by new isolates of white rot fungi. Appl. Environ. Microbiol. 58, 2219-2226. [ Links ]
Fravel D.R., Deahl K.L. y Stommel J.R. (2005). Compatibility of the biocontrol fungus Fusarium oxysporum strain CS-20 with selected fungicides. Biol. Control. 34, 165-169. [ Links ]
Goncalves C., Carvalho J.J., Azenha M.A. y Alpendurada M.F. (2006). Optimization of supercritical fluid extraction of pesticide residues in soil by means of central composite design and analysis by gas chromatographytandem mass spectrometry. J. Chromat. A 1110, 6-14. [ Links ]
]]>Guillén Y., Navias D. y Machuca A. (2009). Tolerance to wood preservatives by cooper- tolerant wood-rot fungi native to south-central Chile. Biodegradation 20, 135-142. [ Links ]
Guillén-Jiménez F.M, Cristiani-Urbina E., Cancino-Díaz J. C., Flores-Moreno J.L. y Barragán-Huerta B.E. (2012). Lindane biodegradation by the Fusarium verticillioides AT-100 strain, isolated from Agave tequilana leaves: Kinetic study and identification of metabolites. Internat. Biodet. Biodegrad. 74, 36-47. [ Links ]
Greene S.A. y Pohanish R. (2005). Sittig´s handbook of pesticides and agricultural chemicals. William Andrew Publishing. Nueva York, EUA. 1189 pp. [ Links ]
Hussain S., Arshad M., Saleem M. y Zahir Z. A. (2007). Screening of soil fungi for in vitro degradation of endosulfan. World J. Microb. Biot. 23, 939-945. [ Links ]
Jauregui J., Valderrama B., Albores A. y Vázquez-Duhalt R. (2003). Microsomal transformation of organophos-phorus pesticides by white rot fungi. Biodegradation 14, 397-406. [ Links ]
]]>Jayashree R. y Vasudevan N. (2007). Persistance and distribution of endosulfan under field condition. Environ. Monit. Assess. 131, 475-478. [ Links ]
Jeffery S. y Burguess L.W. (1990). Growth of Fusarium graminearum Schwabe group 1 on media amended with atrazine, chlorsulfuron or glyphosate in relation to temperature and osmotic potential. Soil. Biol. Biochem. 22, 665-670. [ Links ]
Jenkinson D.S. y Powlson D.S. (1976). The effects of biocidal treatments on metabolism in soil- V: a method for measuring soil biomass. Soil Biol. Biochem. 8, 209-213. [ Links ]
Karanasios E., Tsiropoulos N.G. y Karpouzas D. (2012). On-farm biopurification systems for the depuration of pesticide wastewaters: recent biotechnological advances and future perspectives. Biodegradation 23, 787-802. [ Links ]
Karanasios E., Tsiropoulos N.G., Karpouzas D.G. y Menkissoglu-Spiroudi U. (2010). Novel biomixtures based on local Mediterranean lignocellulosic materials: Evaluation for use in biobed systems. Chemosphere 80, 914-921. [ Links ]
]]>Kataoka R., Takagi K., Kamei I., Kiyota H. y Sato Y. (2010). Biodegradation of dieldrin by a soil fungus isolated from a soil with annual endosulfan applications. Environ. Sci. Techn. 44, 6343-6349. [ Links ]
Kaufman D.D. y Blake J. (1970). Degradation of atrazine by soil fungi. Soil Biol. Biochem. 2, 73-80. [ Links ]
Kim J.D. y Lee C.G. (2007). Microbial degradation of polycyclic aromatic hydrocarbons in soil by bacterium-fungus co-cultures. Biotechnol. Bioproc. E .12, 410-416. [ Links ]
Kim Y.K., Kim S.H. y Choi S.C. (2001). Kinetics of endo-sulfan degradation by Phanerochaete chrysosporium. Biotechnol. Lett. 23, 163-166. [ Links ]
Linde C.D. (1994). Physico-chemical properties and environmental fate of pesticides. Environmental Protection Agency, EPA, CA. 1-53. EH 94-03. [en línea] http://www.cdpr.ca.gov/docs/emon/pubs/ehapreps/eh9403.pdf 15/08/2012. [ Links ]
]]>Liu X., You M.S., Wei Y.Z. Cai Z.C. y Liao J.Y. (2002). Degradation effects of Trichoderma Y on chlorpyrifos and methamidofos. J. Fujian Agric. Forest. Univ. 31, 455-458. [ Links ]
Maloney A.E. (2001). Pesticide degradation. En: Fungi in Bioremediation (G. M. Gadd, Ed.) Cambridge, Reino Unido, pp. 188-223. [ Links ]
Matsubara M.J., Lynch M. y De Leij F.A.A.M. (2006). A simple screening procedure for selecting fungi with potential for use in the bioremediation of conataminated land. Enzyme Microb. Tech. 39, 1365-1372. [ Links ]
Mitra J., Mukherjee P.K., Kale S. P. y Murthy N. B. K. (2001). Bioremediation of DDT in soil by genetically improved strains of soil fungus Fusarium solani. Biodegradation 12, 235-245. [ Links ]
Mukherjee I. y Mittal A. (2005). Biorremediation of endosulfan using Aspergillus terreus and Cladosporium oxysporium. B. Environ. Contam. Toxicol. 75, 1034-1040. [ Links ]
]]>Omirou M., Dalias P., Costa C., Papastefanou C., Dados A., Ehaliotis C. y Karpouzas D.G. (2012). Exploring the potential of biobeds for the depuration of pesticide-contaminated wastewaters from the citrus production chain: Laboratory, column and field studies. Environ. Pollut. 166, 31-39. [ Links ]
Önneby K., Jonsson A. y Stenström J. (2010). A new concept for reduction of diffuse contamination by simultaneous application of pesticide and pesticide degrading microorganisms. Biodegradation 21, 21-29. [ Links ]
Ramírez-Gama R.M,. Luna-Millán B., Mejía-Chávez A., Velázquez-Madrazo O., Tzusuki-Reyes G., Vierna-García L., Hernández-Gómez L. y Müggenburg I. (1998). Manual de prácticas de microbiología general. Facultad de Química, Universidad Nacional Autónoma de México. México. 300 pp. [ Links ]
Rüttimann-Johnson C. y Lamar R.T. (1997). Binding on pentachlorophenol to humic substances in soil by the action of white rot fungi. Soil Biol. Biochem. 29, 1143-1148. [ Links ]
Sagar V. y Singh D.P. (2011). Biodegradation of lindane pesticide by non white-rot soil fungus Fusarium sp. World J. Microb. Biot. 27, 1747-1754. [ Links ]
]]>SAS (2002). Users's guide: Statics, Version 8.0. Statistical Analysis System Institute, Cary. Nueva York, EUA. [ Links ]
Satsuma K., Nakamura H., Sato K. y Kato Y. (2001). A negative effect of co-solvent on atrazine biodegradation in experimental river microcosms. Microbes Environ. 16, 185-189. [ Links ]
Siddique T., Okeke B.C., Arshhad M. y Frankenberger W.T. Jr. (2003). Enrichment and isolation of endosulfan-degrading microorganisms. J. Environ. Qual. 3, 47-54. [ Links ]
Siller H., Rainey F.A., Stackebrandt E. y Winter J. (1996). Isolation and characterization of a new gram-negative, acetone-degrading, nitrate-reducing bacterium from soil Paracoccus solventivorans sp. nov. Int. J. Syst. Bacteriol. 46, 1125-1130. [ Links ]
Silva-Jiménez H. y Zazueta-Sandoval R. (2005). Intracellular fate of hydrocarbons: possible existence of specific compartments for their biodegradation. App.l Biochem. Biotech. 2005, 121-124. [ Links ]
]]>Singh B. K., Walker A. y Wright D.J. (2002). Persistance of chlorpyrifos, fenamiphos, chlorothalonil and pendimethalin in soil and their effects on soil microbial characteristics. B. Environ. Contam. Tox. 69, 181-188. [ Links ]
Singh D.K., Walker A. y Wrigth D.J. (2006). Bioremedial potential of fenamiphos and chlorpyrifos degrading isolates: influence of different environmental conditions. Soil Biol. Biochem. 38, 2682-2693. [ Links ]
Stamatiu-Sánchez K. (2013). Tolerancia y biodegradación de plaguicidas con hongos filamentosos. Tesis doctoral. Área de Fitosanidad, Entomología y Acarología. Colegio de Postgraduados. Montecillo, Estado de México. México. 156 pp. [ Links ]
Stratton G.W. (1989). Effect of the solvent acetone on membrane integrity in the green alga Chlorella pyrenoidosa. Bull. Environ. Contam. Tox. 42, 754-760. [ Links ]
Tillman R.W., Malcolm K.S. y Long J.W. (1973). Mechanism of action and fate of the fungicide chlorothalonil (2,4,5,6-tetrachloroisophthalonitrile) in biological systems 1. Reactions with cells and subcellular components of Saccharomyces pastorianus. Pestic. Biochem. Phys. 3, 160-167. [ Links ]
]]>Torstensson L. (2000). Experiences of biobeds in practical use in Sweden. Pesticide Outlook 11, 206-211. [ Links ]
Urrutia C., Rubilar O., Tortella G. R. y Diez M.C. (2013). Degradation of pesticide mixture on modified matrix of a biopurification system with alternatives lignocellulosic wastes. Chemosphere 92, 1361-1366. [ Links ]
Vazquez-Nuñez E., Rodríguez V., García G.A., Luna-Guido M., Betancur-Galvis L.A., Marsh R. y Dendooven L. (2009). Using acetone as solvent to study removal of anthracene in soil inhibits microbial activity and alters nitrogen dynamics. Arch. Environ. Cont. Tox. 57, 239-246. [ Links ]
Verdin A., Loune's-Hadj S.A., Newsam R., Robinson G. y Durand R. (2005). Polycyclic aromatic hydrocarbons storage by Fusarium solani in intracellular lipid vesicles. Environ. Pollut. 13, 283-291. [ Links ]
Ware G.W. (1994). The pesticide book. Editorial Thomson publications Fresno, CA. 418 pp. [ Links ]
]]>Wiren-Lehr V., Castillo M.P., Scheunert S.I. y Torstensson L. (2001). Degradation of isoproturon in biobeds. Biol. Fert. Soils. 33, 535-540. [ Links ]
Xie H., Zhu L., Ma T., Wang J., Wang J., Su J. y Shao B. (2010). Immobilization of an enzyme from a Fusarium fungus WZ-I for chlorpyrifos degradation. J. Environ. Sci. 22, 1930-1935. [ Links ]
Yeomans J.C. y Bremner J.M. (1989). Effects of organic solvents on denitrification in soil. Biol. Fert. Soils. 7, 336-340. [ Links ]
Yu M., Templeton G.E. y Wolf D.C. (1988). Trifluralin concentration and the growth of Fusarium solani f. sp. cucurbitae in liquid medium and soil. Soil. Biol. Biochem. 20, 607-611. [ Links ]
]]>