
Degradación del AEDT y los complejos Cu(II)–AEDT y Cr(III)–AEDT mediante los procesos Fenton y Foto–Fenton asistido con radiación solar en soluciones acuosas
Fenton and photo–Fenton degradation of EDTA and the Cu(II)–EDTA and Cr(III)–EDTA complexes
Araceli DELFÍN PAZOS1, Carlos Antonio PINEDA ARELLANO1 y Susana SILVA MARTÍNEZ2,*
1 Posgrado en Ingeniería y Ciencias Aplicadas FCQI–CIICAp.
2 Centro de Investigación en Ingeniería y Ciencias Aplicadas (CIICAp), Universidad Autónoma del Estado de Morelos. Av. Universidad 1001. Col. Chamilpa, 62209. Cuernavaca, Morelos. * Correo electrónico: ssilva@uaem.mx
]]>Recibido septiembre 2007
Aceptado mayo 2009
RESUMEN
La degradación del ácido etilendiaminotetraacético (AEDT) y de los complejos organometálicos Cu(II)–AEDT y Cr(III)–AEDT se llevaron a cabo en un sistema por lotes, empleando los procesos Fenton y foto–Fenton asistidos con radiación solar. Se estudió el efecto del pH sobre la degradación de los complejos metal–AEDT y se evaluaron diferentes relaciones molares de [H2O2]:[AEDT]. Se observó que la presencia de hierro incrementa la degradación de los complejos. También se observó degradación del complejo Cu(II)–AEDT en la reacción Fenton asistido con luz solar y estando ausente el ión hierro a pH 3. La concentración inicial de los sustratos estudiados se abatió en más de 80 % con foto–Fenton.
Palabras clave: degradación de AEDT, complejos organometálicos, Fenton, foto–Fenton.
ABSTRACT
The degradation of ethylenediaminetetraacetic acid (EDTA) and the organometallic complexes Cu(II)–EDTA and Cr(III)–EDTA was carried out in a batch system by Fenton and photo–Fenton processes aided with solar radiation. The effects of pH (3–12) and molar ratios of [H2O2]:[EDTA] were studied on the degradation of the metal–EDTA complexes. It was observed that the presence of iron increased the degradation of these complexes. Also, the complex Cu(II)–EDTA was degraded by the Fenton type reaction with solar radiation in the absence of iron at pH 3. The initial concentration of the substrates decreased over 80 % by the photo–Fenton process.
]]> Key words: EDTA degradation, organometallic complexes, Fenton, photo–Fenton.
INTRODUCCIÓN
El ácido etilendiaminotetraacético (AEDT) es un agente quelante sintético de tiene numerosas aplicaciones debido a su capacidad para formar complejos solubles y estables con diversos metales pesados. El AEDT ha sido aplicado en la industria en general, en la farmacia y en la agricultura. El comportamiento y destino del AEDT y sus sales dentro del ambiente acuático han sido estudiados ampliamente (Sillanpää y Pirkanniemi 2001, Nowack 2002). Existe un consenso generalizado de que los complejos metal –AEDT son particularmente estables y persistentes en ambientes acuosos, con la excepción notable del complejo Fe(III)–AEDT que se fotodegrada rápidamente (Nowack et al. 1996, Satroutdinov et al. 2000, Sykora 2001, Nowack 2002), cuyos productos son biodegradables (Nowack 2002). El AEDT es un agente de difícil degradación biológica; se ha reportado que su remoción es insignificante en las plantas de tratamiento convencional (Alder et al. 1990, Kari y Giger 1996, Hinck et al. 1997), amenos que se incremente el pH del agua (Van–Ginkel et al. 1997) lo que provoca que una cantidad sustancial de AEDT se descargue en ríos y lagos. Adicionalmente, el AEDT tiene el potencial de movilizar iones metálicos de sedimentos y suelos debido a su capacidad de formar complejos muy estables, contaminando consecuentemente el agua superficial y subterránea.
Las especies químicas (iónicas o complejas) influyen en el comportamiento del AEDT y en general de los agentes complejantes presente en sistemas acuosos, lo que determina su destino final en el ambiente (Xue et al. 1975). Se ha demostrado que la degradación por medio de los procesos de adsorción (Nowack y Sigg 1996), fotoquímico (Lockhart y Blakeley 1975) y biológico (Hinck et al. 1997, Satroutdinov et al. 2000, Sillanpää y Pirkanniemi 2001, Satroutdinov et al. 2003) depende fuertemente del metal complejado con el AEDT. Incluso, teniendo en cuenta la predominancia de los metales alcalinotérreos y de transición, es de esperar que los agentes quelantes formen complejos en las aguas residuales (Sillanpää et al. 2001).
La degradación del AEDT se ha llevado a cabo por medio de la ozonización (Gilbert y Hoffmann 1990), UV/H2O2 (Sorensen y Frimmel 1995), fotocatálisis (Babay et al. 2001), ultrasonido (Frim et al. 2003, Chitra et al. 2004, Weavers et al. 2005), Fenton (Pirkanniemi et al. 2007) y en soluciones alcalinas (Ramo y Sillanpää 2001), con resultados variables. La degradación de complejos metal–AEDT también ha sido investigada mediante el uso de diversos métodos de tratamiento (Sillanpää y Pirkanniemi 2001, Nowack 2002, Bhattacharyya y Cheng 2006). Frim et al. (2003) reportaron que la degradación de los complejos Cu(II)–EDTA y Cr(III)–EDTA por medio de sonólisis obedece a una cinética de seudo primer orden, siendo el complejo con cromo el más lento en degradarse (20 %), en comparación con el de cobre (~77 %) y el AEDT (90 %) no complejado. Ku et al. (1998) reportaron que durante la descomposición de AEDT por medio del proceso UV/H2O2 se generan especies tales como nitrilo–tri–acetato (NTA), amoniaco y nitrato; inicialmente se lleva a cabo el rompimiento de los enlaces C–N de AEDT por los radicales OH• para formar EDDA, NTA e IDA. Los enlaces de estos compuestos son posteriormente transformados por los radicales OH• a glicina, amoniaco, ácido oxálico y ácido fórmico. Finalmente estas especies intermediarias se oxidan y se mineralizan en carbón y nitratos.
Los procesos Fenton y foto–Fenton ofrecen una alternativa económica y compatible con el ambiente debido a que generan especies oxidantes muy reactivas responsables de mineralizar contaminantes acuosos. La adición de sales de hierro como catalizador en presencia de peróxido de hidrógeno, en medio ácido, se conoce como Fenton (H2O2/Fe3+, Fe2+) que en combinación con luz UV/visible (foto–Fenton) acelera las reacciones Fenton, favoreciéndose así la degradación de contaminantes orgánicos acuosos. El proceso Fenton se lleva a cabo por medio de las ecuaciones siguientes:

En presencia de luz (ecuaciones [5] a [7]), la velocidad de formación de radicales OH• aumenta por medio de la fotoreacción de H2O2 (Chevaldonnet et al. 1986) y/o Fe(III), que produce OH• directamente o regenera Fe(II) para alimentar la reacción (5):

El objetivo de este trabajo fue estudiar la degradación del AEDT y los complejos formados de AEDT con los iones metálicos de Cu(II) y Cr(III) usando los reactivos Fenton y foto–Fenton.
MATERIALES Y MÉTODOS
Determinaciones analíticas. La determinación cuantitativa de AEDT se realizó en medio amortiguador básico (NH4+/NH3, pH 10) por el método volumétrico, empleando una solución estándar 10 mmol L–1 Zn2+ y negro de Eriocromo T como indicador (Vogel 1961). Este método determina no sólo AEDT, sino también todos los iones quelantes o especies intermedias provenientes de la degradación de AEDT, tales como ácido etilendiamino triacético (ED3A), ácido etilendiamino diacético (N,N–EDDA y N,N'–EDDA) y ácido etilendiamino monoacético (EDMA). El H2O2 se analizó siguiendo el método clásico del permanganato (Kolthoff y Belcher 1957). La demanda química de oxígeno (DQO) se determinó usando un espectrofotómetro, viales y procedimiento normalizado (Hach 1992). Se adicionó NaOH a las muestras antes del análisis de DQO para eliminar el efecto del H2O2 residual. Finalmente, la determinación cuantitativa de los complejos coloridos de Cu(II)–AEDT y Cr(III)–AEDT se llevó a cabo empleando la técnica de espectrofotometría, realizando una curva de calibración de absorbancia en función de la concentración del complejo respectivo.
Formación de los complejos metal–AEDT. El complejo Cr(III)–AEDT se preparó mezclando soluciones de AEDT y Cr(NO3)3•9H2O en concentraciones equimolares, manteniendo la solución acuosa en agitación y calentamiento (60–62 °C) por un periodo de 150 minutos (Szafran et al. 1991). El desarrollo del complejo se llevó a cabo a pH 3, 6, 8 y 12. El complejo Cu(II)–AEDT se preparó mezclando soluciones acuosas de AEDT y CuSO4•5H2O en concentraciones equimolares y en agitación durante 3 minutos (Hill y MacCarthy 1986). La formación del complejo se realizó a pH 3,6, 10 y 12. Las curvas de calibración se construyeron con valores de absorbancia medidos a 544 y 742 nm, obtenidos de los espectros de absorción de los complejos Cr(III)–AEDTy Cu(II)–AEDT, respectivamente. Se registró la absorbancia de las soluciones de los complejos durante 72 horas y se observó que éstos son muy estables. Tres meses después se midieron las absorbancias de las soluciones acuosas de metal–AEDT, corroborando la estabilidad de los mismos.
Sistema de lotes para la degradación de los compuestos del AEDT. Se empleó un volumen constante (50 mL) de cada solución acuosa (10 mmol L–1 AEDT, 1 mmol L–1 Cr(III)–AEDTy 5 mmol L–1 Cu(II)–AE–DT) por separado y se vertieron en varios reactores de vidrio cerrados (355 mL de capacidad) para realizar las pruebas de degradación Fenton (ausencia de luz) y foto–Fenton (exponiendo los reactores a la radiación solar). Las pruebas Fenton consistieron en la adición de 1.0 mM de sulfato ferroso (FeSO4x7H2O) y H2O2 en cantidad variable (y medio ácido) a los reactores que contenían los compuestos de AEDT; el proceso foto–Fenton se llevó a cabo en combinación con luz solar (UV/visible) para acelerar las reacciones Fenton. Posteriormente, se retiraron los reactores en función del tiempo de exposición con intervalos variables. Al inicio del experimento se retiraron cada minuto en los primeros 5 minutos de reacción y posteriormente cada 10 ó 20 minutos. El tiempo total de exposición solar de los reactores fue entre 60 y 220 minutos. Se evaluaron las concentraciones de AEDT, Cu(II)–AEDTy Cr(III)–AEDT remanentes a cada tiempo observado. Los experimentos se realizaron de febrero a junio dentro del intervalo que corresponde al periodo de mayor radiación solar incidente (11:00 a 16:00 horas), la cual varía durante el día y con cada estación del año. La intensidad promedio de la radiación incidente fue de 850 W/m2, que se midió con un piranómetro CS300 Campbell Scientific Inc. En cada proceso se retiraron tres reactores simultáneamente con el fin de contar con tres réplicas, expuestas al mismo tiempo y a las mismas condiciones de radiación solar, en cada tiempo observado. Un procedimiento similar se llevó a cabo durante la variación del pH de las soluciones metal–EDTA.
RESULTADOS Y DISCUSIÓN
Degradación de AEDT. Teóricamente, se requieren 25 moles de H2O2 para oxidar completamente 1 mol de AEDT, considerando que el átomo de nitrógeno se oxida completamente a nitratos. Ku et al. (1998) reportaron que durante la descomposición de AEDT por medio del proceso UV/H2O2 se generan especies tales como nitrilo–tri–acetato (NTA), amoniaco y nitrato. La degradación del AEDT se llevó a cabo empleando el proceso foto–Fenton asistido con radiación solar y las relaciones molares iniciales de [H2O2]: [AEDT] de 12.5:1, 25:1 y 37.5:1. En la figura 1 se observa que a medida que la relación molar [H2O2]: [AEDT] se incrementa, el tiempo de degradación del AEDT disminuye, logrando porcentajes de oxidación de 98 % a 30 y 40 minutos para las relaciones molares de 25:1 y 37.5:1, respectivamente, y de 88% para 12.5:1 en 45 minutos de reacción. Considerando estos resultados, se seleccionó la relación molar [H2O2]: [AEDT] de 25:1 para llevar a cabo la degradación del AEDT y los complejos metal–AEDT. La figura 2 compara los resultados de la oxidación de AEDT por medio de los procesos de fotólisis, Fenton y foto–Fenton, asistidos con radiación solar, empleando una relación molar inicial de [H2O2]: [AEDT] de 25:1. Se observa que la degradación del AEDT a pH 3 por medio de fotólisis (en ausencia de oxidante) prácticamente no se lleva cabo durante 120 minutos de reacción. En la figura 2 también se observa que el proceso Fenton degrada al AEDT en aproximadamente 30 % durante un tiempo de reacción de 120 minutos. Sin embargo, en el proceso foto–Fenton la degradación del AEDT se acelera debido a la acción de la luz sobre el reactivo Fenton, con lo que se obtiene una degradación de 99 % a los 40 minutos de reacción. Estos resultados indican que el AEDT puede ser casi completamente descompuesto en 40 minutos por medio del proceso foto–Fenton bajo la acción de la radiación solar. Por lo tanto, el uso de la radiación solar como fuente de luz proporciona un proceso económico y más atractivo con respecto al uso de lámparas UV. Estos resultados coinciden con los reportados por otros autores (Safarzadeh–Amiri et al. 1996, Ku et al. 1998, Ghiselli et al. 2004) que han observado que en ausencia de luz, el proceso Fenton no alcanza un porcentaje alto de degradación del AEDT por su naturaleza refractaria; para lograr la mineralización de este sustrato se requiere de la acción de la luz.
]]>

Degradación de los complejos Cu(II)–AEDT y Cr(III)–AEDT. Los iones metálicos de cobre y cromo forman complejos muy estables con el AEDT, cuyos valores promedio del logaritmo de las constantes condicionales de estabilidad son aproximadamente de 15 y 16 para el complejo Cr(III)–AEDT (entre pH 4–10) y Cu(II)–AEDT (entre pH 8–12), respectivamente (Ringbom 1979). La figura 3 muestra el perfil de degradación de estos complejos a pH 9 y 3 para Cu(II)–AEDT y a pH 6 y 3 para Cr(III)–AEDT, en función del tiempo de exposición a la radiación solar empleando H2O2 como oxidante en ausencia y presencia de Fe(II). Se observa, en ambas gráficas, que el proceso de fotólisis, en presencia de H2O2 como oxidante, no incrementa en forma apreciable la degradación de los complejos; el complejo de cobre se degrada ~15 % (pH 9) mientras que el de cromo lo hace 6 % (pH 6) después de 180 minutos de radiación. En contraste, la presencia de H2O2 y Fe(II) a pH 3 con irradiación solar, acelera la descomposición de los complejos, logrando la descomposición de ~ 80 % del complejo Cu(II)–AEDTy 100 % del complejo Cr(III)–AEDT en 40 y 120 minutos de reacción foto–Fenton, respectivamente, con la subsecuente inactivación de la reacción foto–Fenton en el complejo Cu(II)–AEDT después de 40 minutos de irradiación solar. Se ha reportado que cuando la concentración molar de las especies de cobre es menor que la del AEDT, la mayor parte del cobre se encuentra como Cu(II)–AEDT a pH 3 y las especies de Cu(II)–AEDT compiten favorablemente con H2O2 por la luz ultravioleta. Esto retarda la generación de radicales OH• provenientes de la fotólisis del H2O2 para descomponer el AEDT, originando que la eficiencia de la reacción foto–Fenton aumente (Ku et al. 1998). Lo anterior se confirma en esta investigación ya que inicialmente el cobre y el AEDT están como complejo Cu(II)–AEDT, y posteriormente, la concentración de las especies de cobre que se generan con la degradación del complejo es menor que la del AEDT complejado hasta 49 % de descomposición. Asimismo, Ku et al. (1998) encontraron que cuando la concentración molar de las especies de cobre es > a la del AEDT, la descomposición del segundo se acelera a pH 3 debido a la acción catalítica del cobre libre que descompone fotolíticamente el H2O2. De acuerdo con las observaciones de Ku et al. (1998), sería de esperar que después de 51 % de degradación del complejo, la descomposición de AEDT a pH 3 se acelerara debido a la formación de radicales OH• por la descomposición fotolítica de H2O2, catalizada por las especies de cobre libre. Esto se observa hasta llegar a 80 % de degradación a los 40 minutos de fotorreacción; posteriormente, la reacción se inactiva. Es posible que un exceso de especies de cobre como catalizador ([Cu(II)] ~4 mM) con respecto al AEDT ([Cu(II)–AEDT] ~1 mM) pueda reducir la capacidad oxidante de H2O2 (Sundstrom et al. 1996). Respecto a la descomposición de Cr(III)–AEDT a pH 3, no se observa reducción de la capacidad oxidante de H2O2 debido a que el complejo se degradó completamente en un tiempo de reacción foto–Fenton de 120 minutos. Este comportamiento confirma que Fe (II) aumenta la descomposición catalítica de H2O2 (Ku et al. 1998, Pignatello et al. 1999, Ghiselli et al. 2004), aun cuando los radicales OH• pueden ser generados en reacciones que ocurren en ambos procesos de oxidación. Adicionalmente, se ha reportado (Zhang y Bartlett 1999, Hsu et al. 2007) que Cr(III) se oxida a Cr(VI) por la acción de la luz en presencia de Fe(III) debido a los radicales OH• generados; las reacciones de la producción de OH• asociadas a la oxidación de Cr(III) se expresan por las reacciones (8) y (9), respectivamente.


Esta reacción está fuertemente controlada por el valor de pH, cuyo valor óptimo se encuentra entre 3.2 y 4.4 (Zhang y Bartlett 1999).

La figura 3 también muestra el perfil de degradación de Cu(II)–AEDT a pH 9 y Cr(III)–AEDT a pH 6 en presencia de Fe(II) y H2O2 con radiación solar. Es interesante observar que la sola presencia de Fe (II) en la solución, incrementa la degradación de los complejos. Obviamente, la degradación inicial de los complejos se lleva a cabo por los radicales OH• generados por la descomposición fotolítica de H2O2 catalizada por las especies de hierro, debido a que las especies de cobre y cromo no están libres inicialmente en solución; en consecuencia, no pueden catalizar la descomposición de H2O2 en ese estado. A medida que los complejos AEDT se descomponen, especies de cobre y cromo se incorporan a la solución e influencian su degradación. En el caso de Cu(II)–AEDT (pH 9), la influencia es parcialmente favorable, posiblemente por la formación de hidróxido de cobre y complejos hidroxilo que podrían inhibir la descomposición de H2O2 para generar OH• de manera efectiva. Como consecuencia, sólo se logra 60 % de degradación del complejo en los primeros tres minutos de fotorreacción solar, sin degradar aún más el complejo en un tiempo de reacción mayor.
Respecto a Cr(III)–AEDT (pH 6), la influencia de las especies de cromo es favorable. Se abate 77 % de la concentración inicial del complej o en 210 minutos de fotorreacción y se observa una disminución de su concentración en forma continua, así como un cambio en la pendiente del perfil de degradación. Esto indica la disminución en la velocidad de descomposición del complejo después de 140 minutos de irradiación solar. Es interesante observar que la reacción no se detiene a los pocos minutos de exposición solar como en el caso de Cu(II)–AEDT. Esto podría explicarse por el potencial de oxidación de Cr(III) que genera radicales OH•, de acuerdo con las ecuaciones (8) y (9).
Adicionalmente, se realizaron pruebas de degradación de los dos complejos en ausencia de Fe(II) con el fin de evaluar el efecto catalítico de Cu(II) y de Cr(III) sobre la descomposición de H2O2 para generar OH• empleando la relación molar [H2O2]: [AEDT] de 25:1 y la radiación solar (Fig. 4). Estas pruebas se llevaron a cabo a diferentes valores iniciales de pH: 3 y 9 para Cu(II)–AEDT, 3 y 6 para Cr(III)–AEDT. El pH 3 se seleccionó para comparar los resultados con los obtenidos en la reacción tipo foto–Fenton; los otros valores se seleccionaron debido a que la constante condicional de los complejos metálicos adquiere su valor más alto a ese pH. Esta figura muestra que el perfil de degradación de los complejos metálicos prácticamente permanece constante durante un periodo de fotorreacción de 60 minutos aproximadamente para todos los valores de pH; se exceptúa el pH 3, correspondiente al complejo Cr(III)–AEDT, donde el perfil de degradación permanece inalterable hasta 180 minutos de radiación solar en presencia de H2O2. Durante el periodo de fotorreacción, el complejo Cu(II)–AEDT se degrada lentamente, liberando especies de cobre que inician el efecto catalítico sobre el AEDT, lo que promueve su eventual degradación. Una vez pasado el periodo de fotorreacción, se observa una desintegración rápida del complejo de ~ 70 % después de 170 minutos de reacción a pH 3. La descomposición de este complejo se acelera debido a la acción catalítica del cobre libre que descompone fotolíticamente H2O2, generando los radicales OH• responsables de la degradación.

La acción catalítica del cobre es lenta a pH 9 y sólo degrada al complejo en ~13 %; esto se debe a la formación de hidróxido de cobre y complejos hidroxilo que podrían inhibir la descomposición de H2O2 para generar una concentración efectiva de OH•. Respecto al complejo Cr(III)–AEDT, después del periodo de fotorreacción, se logra una degradación de ~7 % a pH 6. La degradación limitada de este complejo puede deberse a que la velocidad de intercambio del ligante (AEDT) por el cromo es muy lenta, posible factor determinante de la rapidez de la degradación por el radical OH• (Morel y Hering 1993). Asimismo, se ha reportado que el complejo Cr(III)–AEDT es resistente a la degradación por medio de fotocatálisis (Madden et al. 1997). Weavers et al. (2005) obtuvieron también una limitada degradación de AEDT en presencia de Cr(III) en una relación AEDT: Cr(III) 1:1 mediante la aplicación de ultrasonido debido a que, además de la degradación del complejo que libera a Cr(III), éste último tiene el potencial de oxidarse a Cr(VI), que también puede transformarse en cromato (CrO42–).
Los resultados reportados en este trabajo muestran que la degradación del complejo no es tan efectiva como la degradación de AEDT en ausencia del metal. Por otro lado, Wang et al. (2008) observaron que la fotodegradación del oxalato es más efectiva en presencia de Fe(III) (mineralización ~96 %), en comparación con la combinación de Fe(III) y especies de cromo (Cr(III)/ Cr(VI)); reportaron mayor mineralización (~89 %) con Fe(III)–Cr(III) que con Fe(III)–Cr(VI) (~78 %) a pH 3. Estos investigadores atribuyen la disminución de la mineralización a que Cr(III) secuestra los radicales hidroxilo y gradualmente se oxida a Cr(IV), Cr(V) y Cr(VI); asimismo, la oxidación de Cr(III) acoplado con la fotólisis de Fe(OH)2+ altera el equilibrio redox de las especies de hierro (Hsu et al. 2007).
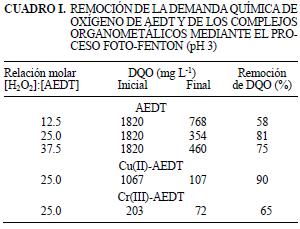
Demanda química de oxígeno. Se obtuvo mayor remoción de DQO durante la degradación foto–Fenton de AEDT para la relación molar de [H2O2]: [AEDT] de 25:1 (Cuadro I). Estos resultados son congruentes con la estequiometría teórica de la reacción de degradación de AEDT. La remoción de DQO después de 120 minutos de degradación de los complejos, usando la óptima relación molar [H2O2]: [AEDT] y foto–Fenton, fue 90 % para Cu(II)–AEDT y 65 % para Cr(III)–AEDT.
]]>
CONCLUSIONES
El empleo del proceso Fenton en la oxidación de AEDT y los complejos con cobre y cromo resultó muy eficiente cuando se combinó con la radiación solar. La degradación de los complejos depende del valor de pH de la solución acuosa. La presencia de hierro incrementa la eficiencia de degradación de Cu(II)–AEDT y Cr(III)–AEDT. También se observó que fue posible degradar el complejo Cu(II)–AEDT en la reacción tipo foto–Fenton en ausencia del ión hierro apH 3. Se obtuvieron remociones relativamente altas de DQO durante la degradación de AEDT y los complejos metálicos.
AGRADECIMIENTOS
Los autores agradecen el financiamiento a la Secretaría de Educación Pública a través del PROMEP (Programa de Mejoramiento al Profesorado).
REFERENCIAS
Alder A., Siegrist H., Gujer W. y Giger W. (1990). Behaviour of NTA and EDTA in biological wastewater treatment. Wat. Res. 24, 733–742. [ Links ]
Babay P.A., Emilio C.A., Ferreira R.E., Gautier E.A., Gettar R.T. y Litter M.I. (2001). Kinetics and mechanisms of EDTA photocatalytic degradation with TiO2 under different experimental conditions. Int. J. Photoenergy 3, 193–199. [ Links ]
Bhattacharyya D. y Cheng C.Y.R. (2006). Activated carbon adsorption of heavy metal chelates from single and multicomponent systems. Environ. Prog. 6, 110–118. [ Links ]
Chevaldonnet C., Cardy H. y Dargelos A. (1986). Ab initio CI calculations on the PE and VUV spectra of hydrogen peroxide. Chem. Phy. 102, 55–61. [ Links ]
Chitra S., Paramasivan K., Sinha P.K. y Lal K.B. (2004). Ultrasonic treatment of liquid waste containing EDTA. J. Clean. Prod. 12, 429–435. [ Links ]
Frim J.A., Rathman J.F. y Weavers L.K. (2003). Sono–chemical destruction of free and metal–binding ethylenediaminetetraacetic acid. Water Res. 37, 3155–3163. [ Links ]
Ghiselli G., Jardim W.F., Litter M.I. y Mansilla H.D. (2004). Destruction of EDTA using Fenton and photo Fenton–like reactions under UV–A irradiation. J. Pho–tochem. Photobiol. A: Chem. 167, 59–67. [ Links ]
Gilbert E. y Hoffmann G.S. (1990). Ozonation EDTA in aqueous solution, influence of pH value and metal ions. Water Res. 24, 39–44. [ Links ]
Hach Company (1997). Water analysis handbook. 3ª ed. Hach Co., Loveland, Colorado. 1309 pp. [ Links ]
Hill Z.D. y MacCarthy P. (1986). Novel approach to Job's method. J. Chem. Ed. 63, 162–167. [ Links ]
Hinck M.L., Ferguson J. y Puhakka J. (1997). Resistance of EDTA and DTPA to aerobic biodegradation. Water Sci. Technol. 35, 25–31. [ Links ]
Hsu C.L., Wang S.L. y Tzou Y.M. (2007). Photocatalytic reduction of Cr(VI) in the presence of NO3– and CI– electrolytes as influenced by Fe(III). Environ. Sci. Technol. 41, 7907–7914. [ Links ]
Kari F.G., y Giger W. (1996). Speciation and fate of ethylenediaminetetraacetate (EDTA) in municipal wastewater treatment. Water Res. 30, 122–134. [ Links ]
Kolthoff I.M. y Belcher R. (1957). Volumetric analysis. Tritation methods: oxidation reduction reactions. Vol. 3. Interscience Publisher, Nueva York. 714 pp. [ Links ]
Ku Y., Wang L.S. y Shen Y.S. (1998). Decomposition of EDTA in aqueous solution by UV/H2O2 process. J. Hazard. Mat. 60, 41–55. [ Links ]
Lockhart H.B. y Blakeley R.V. (1975). Aerobic photo–degradation of X(n) chelates of (Ethylenedinitrilo) tetraacetic acid (EDTA): implications for natural waters. Environ. Lett. 9, 19–31. [ Links ]
Madden T.H., Datye A.K., Fulton M., Prairie M.R., Majumdar S.A. y Stange B.M. (1997). Oxidation of metal–EDTA complexes by TiO2 photocataly sis. Environ. Sci. Technol. 31, 3475–3481. [ Links ]
Morel F. y Hering J. (1993). Principles and applications of aquatic chemistry. John Wiley and Sons, Nueva York. 584 pp. [ Links ]
Nowack B. (2002). Environmental chemistry of a Aminopolycarboxylate chelating agents. Environ. Sci. Technol. 36, 4009–4016. [ Links ]
Nowack B., Kari F.G., Hilger S.U. y Sigg L. (1996). Determination of dissolved and adsorbed EDTA species in water and sediments by HPLC. Anal. Chem. 68, 561–566. [ Links ]
Nowack B. y Sigg L. (1996). Adsorption of EDTA and metal–EDTA complexes onto goethite. J. Colloid Interface Sci. 177, 106–121. [ Links ]
Pignatello J.J., Liu D. y Huston P. (1999). Evidence for an aditional oxidant in the photoassisted Fenton reaction. Environ. Sci. Technol. 33, 1832–1839 [ Links ]
Pirkanniemi K., Metsärinne S. y Sillanpää M. (2007). Degradation of EDTA and novel complexing agents in pulp and paper mill process and wastewaters by Fenton's reagent. J Hazard Mater. 147, 556–561. [ Links ]
Ramo J. y Sillanpää M. (2001). Degradation of EDTA by hydrogen peroxide in alkaline conditions. J. Clean Prod. 9, 191–195. [ Links ]
Ringbom A. (1979). Formación de complejos en química analítica. Alhambra, Madrid. 458 pp. [ Links ]
Safarzadeh–Amiri A., Bolton J.R. y Cater S.R. (1996). The use of iron in advanced oxidation processes, J. Adv. Oxid. Technol. 1, 18–26. [ Links ]
Satroutdinov A.D., Dedyukhina E.G., Chistyakova T.I., Witschel M., Minkevich I.G., Eroshin V.K. y Egli T. (2000). Degradation of metal–EDTA complexes by resting cells of the bacterial strain DSM 9103. Environ. Sci. Technol. 34, 1715–1720. [ Links ]
Satroutdinov A.D., Dedyukhina E.G., Chistyakova T.I., Minkevich I.G., Eroshin V.K. y Egli T. (2003). Bacterial degradation of EDTA. Microbiology 72, 8–11. [ Links ]
Sillanpää M., Orama M., Rämö J. y Oikari A. (2001). The importante of ligand speciation in environmental research: a case study. Sci. Tot. Environ. 267, 23–31. [ Links ]
Sillanpää M. y Pirkanniemi K. (2001). Recent developments in chelate degradation. Environ. Technol. 22, 791–801. [ Links ]
Sorensen M. y Frimmel F.H. (1995). Photodegradation of EDTA and NTA in the UV/H2O2 process. Naturforsh Z. 50, 1845–53. [ Links ]
Sundstrom D.W., Allen J.S., Fenton S.S., Salimi F.E. y Walsh K.J. (1996). Treatment of chelated iron and copper wastes by chemical oxidation. J. Environ. Sci. Health A31, 1215–1235. [ Links ]
Sykora V. (2001). Biodegradability of ethylenediamine–based complexing agents. Water Res. 35, 2010–2016. [ Links ]
Szafran Z., Pike R.M. y Singh M.M. (1991). Microscale inorganic chemistry: a comprehensive laboratory experience. John Wiley and Sons, Nueva York. 271 pp. [ Links ]
Van–Ginkel C.G., Vandenbroucke K.L. y Stroo C.A. (1997). Biological removal of EDTA in conventional activated–sludge plants operated under alkaline conditions. Bioresource Technol. 59, 151–155. [ Links ]
Vogel A.I. (1961). A text–book of quantitative inorganic analysis. 3ª ed. Longman, Londres. 433 pp. [ Links ]
Wang Z., Ma W., Chen Ch. y Zhao J. (2008). Photochemical coupling reactions between Fe(III)/Fe(II), Cr(VI)/ Cr(III), and polycarboxylates: inhibitory effect of Cr species. Environ. Sci. Technol. 42, 7260–7266. [ Links ]
Weavers L.K., Yang P.G., Frim J.A., Yang L. y Rathman J.F. (2005). Ultrasonic destruction of surfactants: application to industrial wastewaters. Water Environ. Res. 77, 259–265. [ Links ]
Xue H., Sigg L. y Kary F.G. (1975). Speciation of EDTA in natural waters: exchange kinetics of Fe–EDTA in river water. Environ. Sci. Technol. 29, 59–68. [ Links ]
Zhang H. y Bartlett R.J. (1999). Light–induced oxidation of aqueous chromium(III) in the presence of iron(III). Environ. Sci. Technol. 33, 588–594. [ Links ] ]]>