
Biosorción de arsénico en materiales derivados de maracuyá
Arsenic biosorption in materials derived from maracuya
Anna ILINÁ, José L. MARTÍNEZ–HERNÁNDEZ, E. Patricia SEGURA–CENICEROS, Juan A. VILLARREAL–SÁNCHEZ y Karla M. GREGORIO–JÁUREGUI
Universidad Autónoma de Coahuila, Facultad de Ciencias Químicas, Departamento de Biotecnología, Blvd. V. Carranza e Ing. J. Cárdenas V. C.P. 25280, Saltillo, Coahuila, México, Fax: 844–415–95–34. Correo electrónico: ailina@mail.uadec.mx
]]> Recibido marzo 2008
RESUMEN
El arsénico ha sido clasificado como uno de los elementos químicos tóxicos y carcinogénicos, por lo tanto presenta un serio problema ambiental en varias regiones del país y del mundo. Se han descrito varios métodos para la remoción de arsénico pero estos tratamientos convencionales emplean materiales no renovables y los residuos formados no sonbiodegradables. En el presente trabajo se demostró que los materiales obtenidos a partir de la cascara y fibra de la cascara de maracuyá (residuos sólidos de la industria nacional de alimentos), de acuerdo a la técnica propuesta, pueden ser considerados como biosorbentes para los iones de arsenito y arsenato. Estos materiales permiten una remoción eficiente del arsénico de aguas provenientes de la región Lagunera, Coahuila, México, así como de las aguas artificiales que contienen As (III) o As (V), sin la necesidad de los tratamientos adicionales. Se demostró una mayor capacidad de biosorción del arsénico en los materiales enriquecidos con Fe (III) que en las matrices químicamente no modificadas. Se evaluaron también diferentes características del proceso de biosorción/desorción de este metaloide mediante estimación de la demanda química de oxígeno (DQO) del agua, prueba de lixiviación, así como las condiciones apropiadas para su aplicación (temperatura, pH, el efecto de la presencia de diferentes iones).
Palabras clave: residuo de maracuyá, arsenato, arsenito.
ABSTRACT
Arsenic has been classified as one of the toxic and carcinogenic chemical elements. One of the problems that the conventional treatments create is that non renewable materials are applied and the formed wastes are not biodegradable. In the present study it was demonstrated that the materials obtained from the maracuyá shell and fiber of the maracuya shell (solid residues of the national food industry), according to the proposal technique, can be considered as bioadsorbents for both arsenite and arsenate. These materials allow an efficient removal of arsenic from water samples coming of Lagunera region, Coahuila, México, as well as from the artificial water samples containing As (III) or As (V), without the necessity of additional treatments. The higher absorption capacity was detected for Fe (III)–loaded materials. Different characteristics of biosorption/desorption process of this metalloid were evaluated by means of chemical oxygen demand estimation, lixiviation tests, as well as the appropriate conditions for their use (temperature, pH, the effect of the presence of different ions) were defined.
Key words: maracuya waste, arsenate, arsenite.
]]>INTRODUCCIÓN
En la región Lagunera del estado de Coahuila, en varios países de América Latina, así como a nivel mundial, existe el problema de hidroarsenicismo crónico regional endémico (HACRE), que es una enfermedad producida por el consumo de aguas contaminadas con arsénico. Una enorme cantidad de personas consume en forma permanente agua con contenido elevado de arsénico lo que pone en riesgo su salud. El arsénico es acumulable en el organismo por exposición crónica y a ciertas concentraciones ocasiona afecciones severas. La Organización Mundial de la Salud (OMS) ha realizado investigaciones de la calidad del agua y ha llegado a la conclusión de que 1/10,000 habitantes tiene riesgo de adquirir cáncer de piel debido a la ingesta diaria de agua con concentraciones de 0.002 mg/L de arsénico (As). El arsénico, aun en concentraciones muy bajas (vestigios), puede causar a largo plazo enfermedades neoplásicas malignas, queratosis, atrofia cutánea, conjuntivitis, astenia o trastornos neurológicos y hematológicos (Ghimire et al. 2003).
A lo largo del tiempo, se han ensayado diferentes técnicas para reducir el arsénico del agua, entre ellas la destilación solar, la osmosis inversa y el paso del agua arsenical por mantos filtrantes de propiedades adsorbentes, tales como alúmina activada y óxido de hierro, entre otras (Sato et al. 2002, Yan et al. 2002). Estas y otras tecnologías tienen sus deficiencias (Driehaus et al. 1998, Haron 1999). Por ejemplo, la alcalinidad y el pH afectan la coagulación, el proceso de ablandamiento por cal produce grandes cantidades de lodo, los sulfatos afectan las membranas y los procesos de intercambio iónico, y el rendimiento por el sistema de alúmina activada se reduce al aumentar el pH y la concentración de flúor (Meng et al. 2002, Xu et al. 2002).
Las tecnologías propuestas funcionan más efectivamente tratando arsénico de la forma As (V). El As (III), por su parte, puede convertirse mediante preoxidación a As (V). Tanto el cloro como el permanganato de potasio han demostrado ser efectivos oxidantes del As (III), aunque la preoxidación con cloro puede crear concentraciones indeseables de subproductos de desinfección (Lee et al. 2003).
Además, los materiales y compuestos utilizados en procedimientos aplicados actualmente en la práctica provienen de fuentes no renovables y no son biodegradables lo que presenta un problema para su depósito (US EPA 2000). Los residuos con As son difíciles de manejar, ya que no es posible la "destrucción" del material. Los lodos residuales obtenidos en las plantas de tratamiento deben ser deshidratados, por ejemplo en lechos de secado. Luego se realiza la prueba estándar de lixiviado. Si la cumplen, pueden ser dispuestos en rellenos sanitarios. Los lodos con concentraciones de As mayores a 5 mg/L entran en la categoría de residuos peligrosos (Dambies et al. 2002). Si el residuo tiene concentraciones que se encuentran por encima de este valor, deberá ser llevado a tratamiento, en el que se convierta al As a una forma que pueda disponerse de manera segura.
El fenómeno de biosorción (Ghimire et al. 2003) ha demostrado actualmente ser una alternativa para el tratamiento de diferentes efluentes industriales con respecto a otros métodos fisicoquímicos (precipitación, intercambio iónico, separación por membranas, etc.). En el proceso de biosorción se utilizan materiales de origen biológico, tales como: algas, hongos, caparazón de artrópodos, bacterias, restos de vegetales etc., los cuales se encuentran en gran abundancia y son fácilmente transformables abiosorbentes. Los iones de metales pesados y metaloides se unen a los centros activos de biosorción del material biológico mediante la formación de complejos, quelatos, intercambio iónico, microprecipitación en la parte interna del material, etc.
El uso de los polisacáridos para la remoción de As fue reportado en trabajos previos en donde se utilizó quitosán (Elson et al. 1980, Dambies et al. 2002, Juang y Shao 2002). Los preparados de quitosán elaborados mediante adsorción de molibdato y coagulación, fueron probados para la remoción de arsénico en un intervalo de concentraciones de 5–20 mg/L, la mejor remoción se observó para As (V) a pH 2–3. La concentración residual fue de 0.5 mg/L en soluciones ácidas. El mecanismo de adsorción está relacionado con la capacidad de iones de molibdato para acomplejar As (V) en soluciones acidas. Para As (III) el mecanismo no fue identificado. El atrapamiento de As (V) no fue afectado por la presencia de otros iones, con excepción de fosfato a bajas concentraciones y silicatos a altas concentraciones.
En otro trabajo se utilizó la celulosa y residuo de naranja, los cuales fueron modificados químicamente mediante fosforilación (Ghimire et al. 2003) y cargados con hierro (III) para crear el ambiente quelante apropiado para remoción de As. Los geles de residuos de naranja tuvieron la capacidad de absorber iones de hierro en el orden de 1.21 mmol/g, comparado con los de celulosa de 0.96 mmol/g, lo que probablemente está relacionado con la presencia de pectina en la cáscara de naranja. La prueba de remoción de As fue efectuada en columna, en ambos casos el As (III) fue removido bajo condiciones alcalinas, observando que el gel de residuos de naranja mostró mayor capacidad en estas condiciones así como a pH neutro. Los arsenatos, al contrario, se removían a pH ácidos: 2–3 y 2–6 para gel de celulosa y de residuo de naranja, respectivamente.
Recientemente el mismo grupo de trabajo (Biswas et al. 2008) reportó que los geles obtenidos de residuos de naranja enriquecidos con iones Zr (IV) presentan una mayor capacidad de remoción de arsenato y arsenito, hasta 88 y 130 mg/g de material, respectivamente. La cinética de biosorción se describe con la ecuación de seudo segundo orden. El intervalo de pH apropiado para la remoción de As (V) fue de 2 a 6 y para As (III) de 9 a 10. La presencia de cloruro, carbonato y sulfato a 0.27 mM no alteraba el proceso de biosorción, mientras que la aplicación de NaOH a 1 M permitía elución de iones de arsénico sin remoción de Zr (IV) y la reutilización del gel en 6 ciclos consecutivos.
]]> Los procesos de adsorción selectiva de bajas concentraciones de As (III) y (V), los cuales no requieren ningún pre– y post tratamiento y no alteran la presencia de otros electrolitos, así como el pH, pueden ser efectuados por analogía con quitosán utilizando otros sorbentes resistentes al desgaste y fáciles de reutilizar, si se realiza la formación de complejos entre el polímero y los compuestos que contienen hierro (De–Marco et al. 2003). Se espera que cada partícula de sorbente híbrido tenga forma de un granulo con propiedades de intercambiador de cationes en el cual, mediante un tratamiento químico térmico serán dispersados los cationes de hierro. De ahí que la presencia en las materias primas de algunos componentes como la pectina, permite ese mismo efecto.El objetivo principal del presente trabajo, fue aprovechar los recursos naturales renovables de bajo costo, tales como la cáscara de maracuyá (residuos sólidos de la industria nacional de alimentos), para el desarrollo de una metodología que permita la obtención de materiales cuyo uso haga posible la remoción del arsénico de aguas contaminadas, así como establecer las condiciones adecuadas para su aplicación.
MATERIALES Y MÉTODOS
Obtención de los biosorbentes modificados (HQCMO, HQFMO, Fe–HQCMO, Fe–HQFMO)
Para la obtención de los materiales de interés, como materia prima se utilizó la cáscara de maracuyá (CM) congelada y parcialmente deshidratada, proporcionada por la fábrica de jugos de maracuyá de la ciudad de Puebla, México. La cáscara fue sometida a la extracción de pectina ligeramente unida para obtener la fibra de maracuyá (FM), rica en pectina intercruzada. La fibra de maracuyá (FM) fue obtenida del residuo del fruto crudo de acuerdo al método descrito por Segura–Ceniceros et al. (2003).
La materia prima (CM y FM) deshidratada se molió obteniendo un material con un 60 % de fracciones correspondientes al tamaño de partícula de 600 um. Se realizaron los siguientes tratamientos fisicoquímicos:
– Lavado: el lavado se efectuó en 6 ciclos repetidos con agua caliente y agitación continua a 150 rpm por 6 h cada ciclo para eliminar los compuestos solubles. La cantidad de materia prima sometida al lavado fue de 2 kg.
– Oxidación: se realizó hasta la decoloración de los pigmentos presentes en las materias primas con peróxido de hidrógeno al 30 %, obteniendo las muestras de CM oxidada (CMO) y FM oxidada (FMO).
]]> – Hidrólisis alcalina: la hidrólisis alcalina de los materiales (FMO y CMO) fue llevada a cabo a temperatura ambiente (25–27 °C) durante 24 h en reactores en lotes con agitación de 100 rpm utilizando 20 mL de NaOH 1 M por cada 100 g de material. Después de la hidrólisis, los materiales (HQFMO y HQCMO) fueron lavados con agua destilada hasta un pH neutro y una mezcla de etanol/acetona (1:1).– Enriquecimiento con iones de hierro: posteriormente, los materiales obtenidos se sometieron al proceso de biosorción de hierro (III) en un reactor en lotes durante 24 h, utilizando una concentración inicial de Fe (III) 0.03 M. La concentración de los preparados fue de 0.1 g/mL. Se obtuvieron los preparados Fe–HQCMO y Fe–HQFMO.
A nivel laboratorio, la modificación química se efectuó, empleando un reactor de 6 L con agitación mecánica y enchaquetado para el control de la temperatura mediante un flujo de agua caliente. El fondo de este tanque contenía dos salidas con filtro para el control del paso de agua: una para recuperación del agua residual, que puede tratarse por métodos biológicos, y otra para recuperación de solventes que pueden tratarse en un equipo de destilación. Esto permite realizar todos los tratamientos fisicoquímicos en forma continua, excepto la desecación al final del proceso, molienda en su inicio y tratamiento de los residuos líquidos.
Determinación analítica de arsénico
En todos los ensayos que involucran la determinación de arsénico, se aplicó el método de la Norma Oficial Mexicana NOM–AA–46–1981 (DOF 1982), que consiste en la determinación espectrofotométrica a 525 nm del complejo As–(dietilditiocarbamato), que se forma a partir de AsH3 (arsina), obtenida después de la reducción del arsénico en un medio que contiene Zn (0) apH ácido (Pérez–Moreno etal. 2002). La técnica aplicada permite la detección de arsénico desde 0.5 ppm. Finalmente, para las muestras de agua se calcula el coeficiente de biosorción (mg/g de material).
Cinética de la biosorción de As (III) y As (V) por CM y FM modificadas
Para cada una de las 4 muestras de los biosorbentes (HQCMO, HQFMO, Fe–HQCMO y Fe–HQF–MO), se prepararon una serie de reactores en lote que contenían 60 mL de la solución de arsenato de 19.82 ppm o arsenito de 20.52 ppm en agua destilada a pH 7 agregándole 0.06 g de material. La concentración final de biosorbente fue de 0.001 g/mL. Como testigo se utilizaron reactores sin la adición del biosorbente. Los ensayos se realizaron por duplicado. Los frascos se mantenían a temperatura de 25 °C. Inmediatamente después de añadir el biosorbente (para valoración del punto correspondiente a tiempo cero) y posteriormente cada 3 h, hasta cumplir un plazo de 24 h, se tomaban dos reactores correspondientes a cada ion para separar el agua del biosorbente mediante filtración con vacío. Posteriormente se realizó la detección de arsénico mediante la técnica descrita en el epígrafe anterior. Se obtuvieron las curvas cinéticas de la concentración de arsénico como una función del tiempo de reacción, se determinó la velocidad inicial de biosorción y el coeficiente de biosorción (q).
Efecto del pH sobre la biosorción de As (III) y As (V) por CM y FM modificadas
Considerando los resultados de los ensayos cinéticos se eligió el tiempo del tratamiento de 24 h, así como los dos materiales enriquecidos con Fe (III). Se prepararon las soluciones de arsenito y arsenato a pH 3, 5, 7, 9 en volúmenes de 60 mL por reactor. Los reactores se pusieron en agitación a 25 °C. En cada uno se añadieron 0.06 g de material. La reacción se detuvo por la filtración. En las soluciones se detectó la concentración de As y los volúmenes inicial y final. Se calculó el coeficiente de biosorción.
Efecto de la temperatura sobre la biosorción de As (III) y As (V) por CM y FM modificadas
]]> El ensayo se realizó de manera similar a la anteriormente descrita utilizando las soluciones de arsenato y arsenito a un pH 7. La incubación por 24 h se realizó a las temperaturas de 20, 25 y 45 °C. Se utilizaron los materiales enriquecidos con hierro: Fe–HQCMO y Fe–HQFMO.Efecto de iones interferentes sobre la biosorción de As (III) y As (V) por CM y FM modificadas
Para el ensayo se prepararon soluciones de arsenito y arsenato de 15 ppm adicionando diferentes concentraciones de cloruro de sodio, sulfato de sodio y fosfato de sodio a un pH de 7. Para el ion sulfato (SO4 2–) se utilizaron las concentraciones: 0, 200, 400 y 800 ppm; ion cloruro (Cl–): 0, 20, 70 y 140 ppm; ion fosfato (PO4 3–): 0, 50, 200 y 400 ppb. Se utilizaron 60 mL de cada solución por reactor con la concentración de material de 0.001 g/mL. El tratamiento se llevó a cabo a 25 °C por 24 h.
Biosorción de arsénico de aguas naturales y de As (III) y As (V) presente en aguas artificiales por CM y FM modificadas
La validación de la eficiencia en cuanto a la remoción de arsénico se realizó empleando soluciones con sales de arsénico y muestras de acuíferos contaminados de la región Lagunera, Coahuila, México. Las características de las muestras de agua natural (AN) aplicadas en el estudio se presentan en el cuadro I. Además de las aguas naturales en este ensayo se utilizaron soluciones estándares (aguas artificiales, AA) de arsenato y arsenito preparadas en agua destilada a un pH 7. La concentración de arsénico detectada según la técnica de la NOM–AA–46–1981 varió dentro de un intervalo de 16 a 18 ppm.

El procedimiento aplicado fue adicionar al agua los materiales de interés. Para las muestras de la región Lagunera (AN), la concentración fue de 0.001 g/mL (0.1 g de cada material en 100 mL) y el tiempo de tratamiento fue de 24 h. En el caso de las AA se utilizaron 0 (testigo), 0.1 y 0.5 g de materiales para 60 mL de agua con As (III) y As (V) y el tiempo de tratamiento fue de una semana. Los reactores en lote se mantuvieron a temperatura ambiente (20–27 °C).
La separación de los materiales se realizó por filtración. Los materiales utilizados a menor concentración en las pruebas con aguas artificiales de As (III) y As (V) se pesaron y se utilizaron posteriormente en la prueba de lixiviación. Las muestras de agua artificial se utilizaron en la determinación de la DQO y As.
DQO en agua antes y después del tratamiento
]]> Para estimar si la presencia de materiales en el agua no provoca la solubilización de compuestos o crecimiento de microorganismos, se evaluó la DQO. El ensayo se realizó con las muestras de agua que contenían los materiales en cuestión por un tiempo de 3 h y una semana de acuerdo a la norma NMX–AA–030–SCFI–2001 (SECOFI 2001).Desorción de As (III) y As (V) después del tratamiento con CM y FM (con y sin incineración), a diferentes valores de pH
Se realizaron los ensayos con las muestras de los biosorbentes que contenían As (III) y As (V). Se pesaron 0.07 g de cada muestra que se colocaron en un tubo con 27 mL de agua destilada a pH 2, 7, y 9. Los tubos se pusieron a incubación poruna semana a temperatura de 25 °C y 150 rpm. Después el material se recuperó por filtración y en el filtrado se realizó la medición de As. Además, se llevó a cabo un ensayo similar incinerando previamente el material (López–Santacruz 2007).
RESULTADOS Y DISCUSIÓN
Obtención de los biosorbentes modificados (HQCMO, HQFMO, Fe–HQCMO, Fe–HQFMO)
La tecnología propuesta para la producción de los materiales de interés comprendió los tratamientos fisicoquímicos descritos en la metodología. A una escala tecnológica mayor, se pueden considerar algunos procesos adicionales para la reutilización de los residuos generados como son: el tratamiento de los solventes mediante destilación y de las aguas residuales mediante procesos biológicos.
En general, el tratamiento de oxidación e hidrólisis conduce a la decoloración de las materias primas, pero después del tratamiento efectuado con Fe (III) el color de los materiales es todavía más intenso, lo que confirma la retención de iones Fe (III) en las muestras obtenidas.
En todos los tratamientos efectuados se aprecia la pérdida de materia prima. La mayor parte se pierde en el lavado, aproximadamente un 50 %, mediante el cual se eliminan los compuestos solubles en el agua.
En el caso de la fibra de maracuyá se obtiene una mayor cantidad del producto final al compararlo con la cascara de maracuyá. Esto se debe a que la fibra ya fue tratada y contiene una mayor cantidad de materia insoluble. Cabe mencionar, que la fibra de maracuyá se obtiene a partir de la cáscara mediante un tratamiento en el autoclave (calentamiento con vapor a sobrepresión) y lavado del material. Esta materia prima es el residuo que se genera después de la extracción de la pectina. Sin embargo, se debe considerar que la pérdida de materia prima no es sólo debido a la eliminación de compuestos insolubles, sino también puede estar relacionada con las imperfecciones de los procesos de separación (en este caso filtración).
]]> Los materiales obtenidos fueron almacenados a temperatura ambiente y utilizados en los ensayos posteriores. El tiempo de almacenamiento variaba de una semana hasta un año pero esto no se reflejó significativamente sobre las propiedades de biosorción y desorción del arsénico.Cinética de la biosorción de As (III) y As (V) por CM y FM modificadas
La cinética de la biosorción permite determinar el tiempo que necesita el proceso para alcanzar el equilibrio, así como la velocidad del mismo. La evaluación se realizó durante 24 h, considerando algunos reportes referentes a la biosorción de diferentes metales pesados y metaloides (Ghimire et al. 2003).
Utilizando los reactores sin el material, se demostró que a lo largo del ensayo la concentración inicial de As (III) de 20.52 y As (V) de 19.82 ppm se mantuvo constante. Estos valores de concentración se aplicaron para los cálculos del coeficiente de biosorción (q, mg de As/g de material), considerando el volumen de la mezcla de reacción (0.06 L) y la cantidad de la muestra del material de 0.06 g (Cuadro II).

Las cinéticas de biosorción de As (III) en los sistemas con los materiales de la cascara y fibra de maracuyá se presentan en las figuras 1 y 2. Las cinéticas de biosorción de As (V) en los materiales de cascara y fibra de maracuyá se presentan en las figuras 3 y 4.



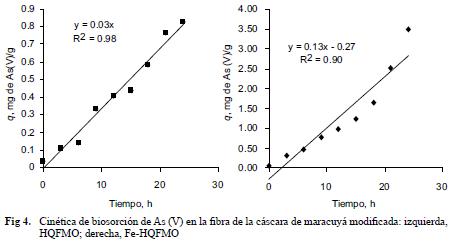
De los datos experimentales que se muestran en las figuras 1–4 se puede deducir que el proceso de biosorción se inicia inmediatamente después de poner en contacto los materiales con el agua ya que en el tiempo 0 (lo que se refiere a la inmediata separación del material) ya se detecta una fracción de As y después de 3 h de tratamiento la remoción es más evidente. Según los procedimientos establecidos en la cinética química, el valor de la velocidad inicial de remoción se calcula como la tangente de la recta trazada en la parte inicial de la curva cinética (Figs 1–4). Se puede apreciar (Cuadro II) que en todos los casos la velocidad inicial es considerablemente mayor (en 2–3 veces) en los ensayos realizados con los materiales enriquecidos con hierro.
También de las curvas cinéticas se deduce que en 24 h el proceso no alcanza a llegar al estado de equilibrio. Los valores correspondientes a la remoción de As son mayores a 24 h que a 21 h (Cuadro II y Figs. 1–4). En todos los casos estudiados, tanto paraAs (III) como para As (V), la mayor capacidad de remoción se observa con los materiales enriquecidos con hierro. Es necesario señalar que el proceso cinético de biosorción es muy complejo debido a que depende de varios factores tales como: transporte de los iones hacia la superficie y la parte interna de los granulos del material, distribución de la capa de solvatación y de los contraiones.
La comparación de la velocidad y la capacidad de remoción fue utilizada para seleccionar los materiales enriquecidos con hierro (Fe–HQCMO, Fe–HQFMO) como más eficientes y más aptos para la aplicación a mayor escala y para estudios posteriores, ya que con estos materiales se obtuvieron valores superiores de biosorción que con los materiales hidrolizados (HQCMO, HQFMO). La mayor capacidad de remoción de As (III) y As (V) se detectó con el material obtenido a partir de la fibra de maracuyá (Fe–HQFMO) enriquecida con hierro.
Efecto del pH sobre la biosorción de As (III) y As (V) por CM y FM modificadas
Se evaluó el efecto del pH sobre el proceso de biosorción de arsénico. En este ensayo se utilizaron sólo los materiales enriquecidos con hierro (Fe–HQCMO y Fe–HQFMO), seleccionados por sus propiedades de mayor biosorción. Los resultados obtenidos se presentan en el cuadro III.
]]> De los resultados experimentales de la biosorción de As (III) y As (V) por los materiales ensayados, se deduce que a un pH de 3 y 9, la capacidad de unión de los aniones del contaminante a los gránulos es baja. Este resultado se explica considerando que apH ácido en la solución hay una mayor cantidad de iones hidrónio H3O+ los cuales compiten con las formas acidificadas de arsenito y arsenato. A medida que aumenta el pH en la solución se cambia el contenido de las formas de los aniones del ión contaminante en cuestión (Fig. 5). El mayor porcentaje de remoción y capacidad de biosorción se detectó a pH 5, seguido por pH 7 (Cuadro III). Esto se debe por un lado a la disminución de la cantidad de iones H3O+ y por otro lado, al cambio en la concentración de las formas iónicas de arsenito y arsenato (Lee et al. 2003) que se caracteriza por las constantes de equilibrio correspondientes a cada uno de los compuestos (Fig. 5).
Por lo tanto, el pH óptimo para llevar a cabo el proceso de biosorción de As (III) y As (V) es de 5. A un pH inicial neutro del agua, el proceso se realiza con menor eficiencia sin embargo, alcanza los valores aceptables. Considerando que la aplicación del agua para el consumo a valores de pH ácidos no es conveniente o requiere de un tratamiento del agua adicional, en las siguientes etapas los ensayos fueron realizados a un pH de 7.
Efecto de la temperatura sobre la biosorción de As (III) y As (V) por CM y FM modificadas
Se evaluó el efecto de la temperatura sobre la retención de arsenato y arsenito. Los resultados arrojados en este ensayo se presentan en el cuadro IV. Para todos los biosorbentes y ambos tipos de aniones de arsénico se observó la misma tendencia: al aumentar la temperatura de 20 a 25 °C los coeficientes de retención se incrementaron, sin embargo, al aumentar la temperatura hasta 45 °C la capacidad de retención disminuyó.

Estos resultados demuestran que el proceso de biosorción depende fuertemente de la temperatura. Por un lado, esto está relacionado con que los procesos de biosorción son reversibles. Por otro lado, el incremento de la temperatura aumenta el movimiento cinético de los iones y cambia las estructuras de los sitios activos de los biosorbentes lo que conduce a una disminución de la biosorción (Hansen et al. 2006, López–Santacruz 2007).
Efecto de iones interferentes sobre la biosorción de As (III) y As (V) por CM y FM modificadas
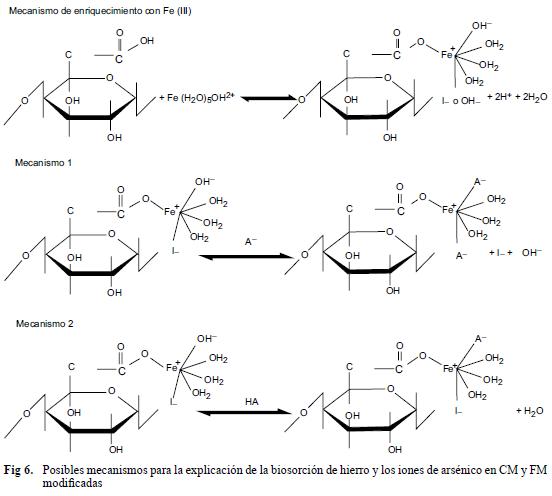
]]> El efecto de diferentes iones sobre la biosorción de arsenito y arsenato en los cuatro diferentes materiales se describe en el cuadro V. La observación interesante es que a bajas concentraciones de todos los iones, probados con todos los materiales, se detectó un incremento en el porcentaje y la capacidad aparente de biosorción al comparar con el control sin iones interferentes. Para los sulfatos esta concentración fue de 200 ppm, para los cloruros de 20 ppm y para los fosfatos de 50 ppb. El incremento de la concentración de los iones aplicados en el ensayo condujo a un decremento en los parámetros cuantificados, hasta niveles menores a los detectados en ausencia de los iones. La biosorción de arsenato fue más sensible al aumento de la concentración de sales que la detectada para arsenito.Este resultado puede ser explicado al considerar la posibilidad de la participación de aniones de sales en el proceso de intercambio de iones presentado en los mecanismos de la figura 6. Es posible que la presencia de aniones a bajas concentraciones desestabilice la capa aniónica formada alrededor de los iones de hierro (III), lo que simplifica el intercambio entre éstos y los aniones de arsenito y arsenato (Ghimire et al. 2003).
Biosorción de arsénico de aguas naturales y de As (III) y As (V) presente en aguas artificiales por CM y FM modificadas
En el presente ensayo se utilizaron soluciones de sales de arsénico III y V (agua artificial) y muestras de acuíferos (AN) contaminados de la región Lagunera, Coahuila, México. Los resultados de la biosorción de arsénico se presentan en los cuadros VI y VII. Considerando las características de las muestras de agua provenientes de la región Lagunera (Cuadro I) y los resultados de la aplicación de los biosorbentes, se demuestra que la presencia de los iones adicionales en las muestras de AN no afecta el proceso de remoción del arsénico que es mayor de 99 %, cuando la concentración de arsénico es menor a 5 ppm (Cuadro VI). Lo importante de estos resultados es que se demostró la posibilidad de utilizar los materiales en muestras de aguas reales que contienen arsénico en niveles 65 y 325 veces mayores de los permitidos por laNOM–AA–46–1981 (0.05 mg/L) y OMS(0.01mg/L).


Se demostró que la optimización del proceso de remoción está en relación con la concentración del contaminante y la concentración de los materiales aplicados (Cuadro VII). Aumentando la última se logra mayor porcentaje de remoción y lógicamente menor coeficiente de biosorción. La comparación del coeficiente de sorción detectado para los materiales probados justifica la modificación química de la matriz polimérica con los iones de Fe (III), ya que esto conduce a un incremento de la capacidad de adsorción de arsénico.
En varios trabajos se reporta (Zhang et al. 2003, Balaji et al. 2005, Hansen et al. 2006) que es difícil comparar directamente la capacidad de adsorción de diferentes sorbentes debido a la variedad de condiciones experimentales aplicadas. Aun así, los materiales enriquecidos con Fe (III) probados en el presente estudio tienen valores mayores en comparación con algunos otros sorbentes. Sin embargo, éstos muestran la desventaja en términos de este parámetro al compararse con los geles enriquecidos con Zr (IV) (Biswas et al. 2008). No obstante, el bajo costo de los residuos de maracuyá para la producción de los derivados en cuestión y de las sales de Fe (III), en comparación con otros iones así como su menor toxicidad, pueden ser considerados como puntos a favor de la aplicación de estos biosorbentes. Además, hay que tomar en cuenta que altas capacidades de adsorción conducen a la generación de residuos sólidos altamente tóxicos lo que presenta el problema de su almacenamiento (US EPA 2000). En el caso de los niveles bajos de arsénico, los residuos generados pueden ser desechados sin costosos tratamientos adicionales, comúnmente aplicados para los residuos tóxicos.
El mecanismo de biosorción del hierro y biosorción del arsénico en materiales enriquecidos con hierro se ilustra en la figura 6 (Ghimire et al. 2003). Para la biosorción del hierro se propone la reacción entre los grupos con carga negativa, por ejemplo, grupos carboxilo u otros presentes en el material oxidado. La biosorción del arsénico puede ser asociada con el intercambio iónico de los grupos carboxilo u otros iones que se encuentran en interacción con iones Fe (III). En los materiales no enriquecidos en lugar de iones de hierro pueden estar otros grupos con carga positiva que contienen los aniones a su alrededor. La interacción de los iones de arsénico puede comprender la simple sustitución del anión, al anión que contiene arsénico (mecanismo 1), en este caso se libera el grupo hidroxilo o el anión sustituido. El mecanismo 2 demuestra que también puede tener lugar la interacción entre grupos carboxilo y la forma ácida del anión de arsénico.
Se demostró nuevamente que los materiales enriquecidos con los iones de Fe (III) se caracterizan por mayores valores en la capacidad de biosorción. A diferencia de los ensayos cinéticos, el tiempo de tratamiento se incrementó, lo que permitió aumentar la capacidad de biosorción. Este resultado confirma las observaciones de la etapa anterior de que 24 h no es el tiempo en el que se llega a un estado de equilibrio. Sin embargo, una semana (el tiempo seleccionado para los propósitos de las etapas posteriores de la evaluación de la DQO es un periodo que desde el punto de vista operacional es demasiado largo para ser implementado en una tecnología viable, por lo tanto, el tiempo óptimo debe ser mayor de 24 h (para lograr la mayor capacidad de biosorción) pero menor de una semana.
DQO en agua antes y después del tratamiento
Utilizando las mismas muestras de agua artificial al inicio y al final del tratamiento, así como agua sin arsénico, se procedió a la evaluación de la DQO. Los valores de la DQO permiten la estimación de la cantidad de la materia orgánica oxidable. En una muestra de agua sometida al tratamiento, esta cantidad puede variarse si en el tratamiento efectuado hay liberación de algunos compuestos orgánicos o crecimiento de la flora microbiana. Considerando esto, para estimar si la presencia de materiales en el agua no provoca la solubilización de algunos compuestos o crecimiento de microorganismos se evaluó la DQO.
Los resultados obtenidos se presentan en la figura 7. En estas gráficas, las barras correspondientes al material hidrolizado sin hierro (HQXO) se marcan con los números 1 y 2. Las barras correspondientes al material con hierro (Fe–HQXO), se marcan con los números 3 y 4. En cada caso los números impares (1 y 3) describen los datos obtenidos con las muestras del agua en el inicio del tratamiento, aproximadamente de 3 h. Los números pares (2 y 4) corresponden a los resultados obtenidos después de una semana del tratamiento. En cada caso son cuatro barras que corresponden al peso diferente del material añadido en el tubo.

Desorción de As (III) y As (V) después del tratamiento con CM y FM (con y sin incineración), a diferentes valores de pH
Se realizaron los ensayos con los residuos sólidos formados en la prueba previa con aguas artificiales. Se utilizaron los materiales de ensayo con 0.0016 g/ mL. No fue posible detectar experimentalmente la concentración de arsénico en éstos, sólo estimarla tomando en cuenta el coeficiente de adsorción y la aplicación de 0.07 g de material en 27 mL (Cuadro VII). En la prueba de lixiviación se consideraron 3 valores de pH diferentes (2, 7 y 9) y el tiempo del tratamiento fue de una semana. Los resultados obtenidos se muestran en el cuadro VIII.

El efecto del pH sobre la liberación del As no fue muy pronunciado, es decir las diferencias detectadas entre los niveles del metaloide están dentro de la variación del método espectrofotométrico aplicado en la evaluación para la mayoría de los casos. Sólo se destaca la lixiviación ligeramente mayor a pH ácido en el caso de material HQCMO y menor lixiviación a pH 7 en el caso de Fe–HQFMO.
Se observó que los preparados enriquecidos con hierro (III) adsorben el arsénico más fuertemente ya que la lixiviación en estos casos fue menor. Los menores niveles de As liberado fueron detectados en los ensayos realizados con los preparados (Fe–HQCMO y Fe–HQFMO) enriquecidos con Fe (III) (Cuadro VIII). Esto se consideró como otro punto importante para la selección de los materiales, cuya composición comprende la presencia de los iones de Fe (III).
En otro ensayo, mediante la incineración a partir de los materiales con As, se obtuvieron los sólidos no volátiles que fueron sometidos a un proceso de solubilización en agua por un periodo de una semana.
Aplicando la técnica gravimétrica se evaluaron los porcentajes de los sólidos no volátiles (la parte inorgánica de los materiales). Los resultados se presentan en la figura 8. La mayor cantidad de los compuestos inorgánicos fue cuantificada en los preparados de la cáscara de maracuyá (Fig. 8).
En todos los ensayos realizados se observó que los materiales con arsénico tienen mayor porcentaje de compuestos no volátiles que los materiales no utilizados en el tratamiento del agua, además de que los materiales enriquecidos con hierro en la mayoría de los casos tienen mayor porcentaje de materia no volátil.
]]> Las muestras de las cenizas obtenidas a partir de los materiales con los iones de As III y V fueron aplicadas en el ensayo que permite estimar su solubilidad en agua a diferentes valores de pH. La concentración de arsénico total presente en las cenizas no se pudo cuantificar o estimar. Por esta razón, los resultados obtenidos (figura 9) se consideraron solo como tendencias de comportamiento de las sales arsenicales presentes en las cenizas en fase acuosa por un periodo de una semana. En el caso de los preparados enriquecidos con hierro (tercer y cuarto bloque de columnas) la solubilidad de As de las cenizas fue menor que en el caso de los preparados hidrolizados (primeros dos bloques de columnas). Otra tendencia observada es que los compuestos formados con As (V) mostraron menores niveles de concentración de As liberado que los compuestos formados con As (III).Los resultados obtenidos demuestran, en el caso de los materiales de la cáscara de maracuyá, que la mayor solubilidad se detecta a pH 7 que a pH 2 y 9 (Fig. 9, izquierda). En el caso de los materiales de fibra de la cascara de maracuyá, la solubilidad no difiere significativamente al cambiar el pH (Fig. 9, derecha).
CONCLUSIONES
Se ha demostrado que los materiales obtenidos a partir de la cascara de maracuyá y fibra de la cascara de maracuyá, de acuerdo a la técnica propuesta, pueden considerarse como biosorbentes para los iones de arsenito y arsenato. Estos materiales permiten una remoción eficiente del arsénico en aguas provenientes de la región Lagunera y al mismo tiempo de las aguas artificiales que contienen As (III) o As (V), sin la necesidad de tratamientos adicionales (por ejemplo, oxidación de As III) que comúnmente se aplican en las tecnologías convencionales para la remoción del As III. Los materiales diseñados tienen bajo costo de producción comparado con las resinas quelantes sintéticas. La cinética de la biosorción muestra que el proceso de fijación de los iones de arsenato As (V) y arsenito (III) en los centros activos del biosorbente, es relativamente lento, demora más de 24 h para alcanzar el equilibrio. Los materiales enriquecidos con hierro tuvieron mayor velocidad inicial y capacidad de biosorción del As.
Los materiales enriquecidos con hierro (a diferencia de los que fueron solo hidrolizados) en concentraciones bajas, por tiempo corto y por una semana no afectan mucho el contenido de la materia orgánica en el agua tratada.
El proceso de remoción de As se ajusta a un modelo de equilibrio de intercambio de ligandos. Los preparados enriquecidos con hierro (III) atrapan el arsénico más fuertemente ya que la lixiviación en estos casos fue menor. La desorción de los iones de arsénico confirma la hipótesis de que el proceso de biosorción es reversible.
Después de la incineración se obtienen muy bajos porcentajes de materia inorgánica no volátil. La lixiviación de arsénico de las cenizas obtenidas de los materiales con hierro es menor que en el caso del material incinerado de los derivados de cascara y fibra de maracuyá no enriquecidos con hierro.
El pH y temperatura adecuados para el proceso de biosorción del metaloide As (III) y As (V) en los materiales Fe–HQCMO, Fe–HQFMO, se encuentran en el intervalo de 5–7 y 25 °C, respectivamente. A bajas concentraciones de Cl–, SO42– y PO43– se incrementa la capacidad aparente de biosorción de As (III y V) por Fe–HQCMO, Fe–HQFMO al comparar con el testigo en ausencia de estos iones. La biosorción de arsenato es más sensible al aumento de la concentración de los aniones interferentes que la detectada con arsenito.
Los materiales biopoliméricos obtenidos de los residuos de la industria del jugo de maracuyá, después de su acondicionamiento, pueden ser utilizados para la remoción de las especies de arsénico en medios acuosos.
]]>AGRADECIMIENTOS
Se agradece al proyecto del CONACyT–Gobierno del Estado de Coahuila COAH–2003–CO2–41 por el apoyo recibido. De igual forma, agradecemos el apoyo técnico del M. en C. Federico Cerda Ramírez del Centro Investigación en Química Aplicada.
REFERENCIAS
Balaji T., Yokoyama T. y Matsunaga H. (2005). Adsorption and removal of As(V) and As(III) using Zr–loaded lysine diacetic acid chelating resin. Chemosphere 59, 1169–1174. [ Links ]
Biswas B.K., Inoue J.C., Inoue K., Ghimire K.N., Harada H., Ohto K. y Kawakita H. (2008). Adsorptive removal of As (V) and As (III) from water by a Zr (IV)–loaded orange waste gel. J. Hazard. Mater. 154, 1066–1074. [ Links ]
Dambies L., Vincent T. y Guibal E. (2002). Treatment of arsenic–containing solutions using chitosan derivatives: uptake mechanism and sorption performances. Water Res. 36, 3699–3710. [ Links ]
De–Marco M.J., Sen–Gupta A.K. y Greenleaf J.E. (2003). Arsenic renoval usinig a polymeric/inorganic hybrid sorbent. Water Res. 37, 164–176. [ Links ]
Driehaus W., Jekel M. y Hildebrandt U. (1998). Granular ferric hydroxide – a new adsorbent for the removal of arsenic from natural water. J. Water SRT – Aqua 47, 30–35. [ Links ]
DOF (1982) NOM–AA–46–1981. Protección del medio ambiente. Análisis de agua. Determinación de arsénico (Método espectrofotométrico). Diario Oficial de la Federación. 21–04–82, México. [ Links ]
Elson C.M., Davies D.H. y Hayes E.R. (1980). Removal of arsenic from contaminated drinking water by chitosan/ chitin mixture. Water Res. 14, 1307. [ Links ]
Ghimire K.N., Inoue K., Yamagchi H., Makino K. y Miyajima T. (2003). Adsortive separation of arsenate and arsenite anions from aqueous medium by using orange waste. Water Res. 37, 4945–4953. [ Links ]
Hansen H.K., Ribeiro A. y Mateus E. (2006). Biosorption of arsenic (V) with Lessonia nigrescens, Minerals Engineer. 19, 486–490. [ Links ]
Haron M.J., Wan–Yunus W.M., Yong N.L. y Tokunaga S. (1999). Sorption of arsenate and arsenite anions by iron (III)–poly (hydroxamic) acid. Chemosphere 39, 2459–2466. [ Links ]
Juang R.S. y Shao H.J. (2002). A simplified equilibrium model for sorption of heavy metal ions from aqueous solutions on chitosan. Water Res. 36, 2999–3008. [ Links ]
Lee Y., Um I.H. y Yoon J. (2003). Arsenic (III) oxidation by iron (VI) (ferrate) and subsequent removal of arsenic (V) by iron (III) coagulation. Environ. Sci. Technol. 37, 5750–5756. [ Links ]
López–Santacruz A.I. (2007). Evaluación de las características fisicoquímicas de los biosorbentes obtenidos a partir de derivados de algas marinas y cáscara de maracuyá aplicados a la remoción de arsénico del agua. Tesis de licenciatura. Facultad de Ciencias Químicas, Universidad Autónoma de Coahuila. Saltillo Coah. [ Links ]
Meng X., Korfiatis G.P., Bang S. y Bang K.W. (2002). Combined effects of anions on arsenic removal by iron hydroxides. Toxicol. Lett. 133, 103–111. [ Links ]
Pérez–Moreno F., Prieto–Garcia K, Barrado–Esteban E., Rojas–Hernández A. y Méndez–Marzo M.A. (2002). Optimización del método de determinación de arsénico en aguas potables por espectrofotometría UV–Vis con dimetil ditiocarbamato de plata. Rev. Soc. Quim. Méx. 46, 175–179. [ Links ]
Sato Y., Kang M., Kamei T. y Magara Y. (2002). Performance of nanofiltration for arsenic removal. Water Res. 36, 3371–3377. [ Links ]
Segura–Ceniceros E.P., Ilyina A., Contreras–Esquivel J.C., Rodríguez–Menchaca D., Flores–Espinoza J.C. y Montes–Rodríguez, O.E. (2003). Entrapment of enzymes in natural polymer extracted from residue of food industry: preparation methods, partial characterization and possible application. Vestn. Mosk. Univ., Ser. 2., Khimiya 44, 84–87. [ Links ]
SECOFI (2001) NMX–AA–030–SCFI–2001. Análisis de agua.Determinación de la demanda química de oxígeno en aguas naturales, residuales y residuales tratadas. Método de prueba (cancela a la NMX–AA 030–1981). Secretaría de Comercio y Fomento Industrial. http://www.semarnat.gob.mx/leyesnormas 15/10/2006 [ Links ]
US EPA 2000. Technologies and costs for removal of arsenic from drinking water. Prepared by International Consultants, Inc. and Malcolm Pirnie, Inc. under contract 68–C6–0039 for EPA OGWDW. [ Links ]
Xu Y.H., Nakajima T. y Ohki A. (2002). Adsorption and renoval of arsenic (V) from drinking water by aluminum–loaded Shirasu–zeolite. J. Hazard Mater. 92, 275–287. [ Links ]
Yan T., Hu J.Y., Ong S.L., Luo Q.F. y Ng W.J. (2002). Arsenic removal from household drinking water by adsorption. J. Environ. Sci. Health. Part A. 37, 1721–1736. [ Links ]
Zhang Y., Yang M. y Huang X. (2003). Arsenic (V) removal with a Ce (IV)–doped iron oxide adsorbent. Chemosphere 51, 945–952. [ Links ] ]]>