Relación estructura-propiedades de polímeros
Relationship between structure and properties of polymers
Juan Coreño-Alonso y María Teresa Méndez-Bautista*
* Área Académica de Ciencias de la Tierra y Materiales, Universidad Autónoma del Estado de Hidalgo. Correo electrónico: jcoreno@uaeh.edu.mx, tmendez@uaeh.edu.mx
]]>Fecha de recepción: 26 de octubre 2009.
Fecha de aceptación: 15 de abril 2010.
Resumen
En la actualidad se dispone de un número cada vez creciente de polímeros para satisfacer las diversas necesidades del ser humano. Estos materiales encuentran un amplio uso en la industria automotriz, en carcasas y mecanismos para electrodomésticos y dispositivos eléctricos, entre muchos otros. Esta gran variedad de usos se debe a que presentan propiedades químicas, mecánicas y térmicas excepcionales, sobre todo los polímeros de especialidad, que están estrechamente relacionadas, principalmente, con su composición química y estructura. El objetivo de este artículo es exponer los aspectos básicos sobre las relaciones existentes entre la composición química, la estructura y las principales propiedades de los polímeros, con mayor profundidad a la tratada en los libros de texto sobre materiales, para comprender mejor la estrecha dependencia entre las propiedades y la estructura de los polímeros. Este trabajo se presenta como complemento didáctico de apoyo para profesores o alumnos de asignaturas de polímeros y ciencia de materiales. La información presentada se ha recopilado de diversas fuentes: principalmente libros especializados, bibliografía de la que no se dispone de traducción en español, o libros que ya no se editan.
Abstract
This paper shows the main relationships that exist between the structural characteristics of polymers and their more common properties. These relations are explained, generally, by using commercial polymers as examples. Factors such as chemical composition, molecular weight, structural order, branching, crosslinking and intermolecular forces are related to cristallinity degree, flexibility of the polymer chains, glass temperature transition, melting point, and mechanical properties, mainly. These relationships are used to analyze two important mechanical behaviors of polymers: the variation of modulus of relaxation as a function of temperature and their responses when subjected to stress-strain tests, which is the basis of a widely used classification for polymers.
Keywords: cristallinity, thermal transitions, mechanical properties, polymer structure.
]]>Introducción
En la actualidad se dispone de un número cada vez creciente de polímeros para satisfacer las diversas necesidades del ser humano. De gran interés son los polímeros de ingeniería y de especialidad, pues se proyecta que su consumo aumente notablemente a un ritmo promedio de 8% anual hasta el 2020. (Conde, 2008). Estos materiales encuentran un amplio uso en la industria automotriz, en carcasas y mecanismos para electrodomésticos y dispositivos eléctricos, entre muchos otros. Esta gran variedad de usos se debe a que presentan propiedades químicas, mecánicas, ópticas y térmicas excepcionales, que están estrechamente relacionadas, principalmente, con su composición química y estructura. Esto es especialmente notorio en los polímeros de especialidad, que son aquéllos con propiedades sobresalientes diseñados, generalmente, para aplicaciones muy específicas. En general, la modificación de tales características en los polímeros puede mejorar en gran medida sus propiedades para obtener materiales con aplicaciones muy específicas. Un ejemplo común y muy ilustrativo es la vulcanización del caucho que en su estado natural es blando y pegajoso; sin embargo, al introducir azufre entre sus moléculas se forman enlaces entrecruzados que modifican notablemente sus propiedades originales. Ejemplos más sofisticados y recientes lo representan polímeros de especialidad como aquellos con memoria de forma (Behl, 2007), electroluminiscentes (Friend, 1999) y los denominados "auto-curables" (van der Zwaag, 2008) que encuentran aplicaciones en dispositivos médicos, ópticos y estructurales que requieren reparación espontánea, respectivamente.
El objetivo de este artículo es exponer los aspectos básicos sobre las relaciones existentes entre la composición química, la estructura y las principales propiedades de los polímeros, con mayor profundidad a la tratada en los libros de texto sobre materiales, para comprender mejor la estrecha dependencia entre las propiedades y la estructura de los polímeros. Este trabajo se presenta como complemento didáctico de apoyo para profesores o alumnos de asignaturas de polímeros y ciencia de materiales. La información presentada se ha recopilado de diversas fuentes: principalmente libros especializados, bibliografía de la que no se dispone de traducción en español, o libros que ya no se editan.
Efecto de las fuerzas intermoleculares
Existen tres diferentes tipos de enlaces químicos, también conocidos como enlaces primarios, los cuales se encuentran presentes en los sólidos: iónico, covalente y metálico. En esta clase de enlaces están involucrados necesariamente los electrones de valencia. Entre los materiales poliméricos, los enlaces covalentes son los predominantes.
A diferencia de los enlaces primarios, las fuerzas intermoleculares son fuerzas de atracción que mantienen unidas a las moléculas, sin que se transfieran o se compartan electrones de valencia (Callister, 2003, p. 21). También se les conoce como enlaces físicos o secundarios; resultan de la interacción de los dipolos de las moléculas involucradas y poseen energías entre 0.5 y 10 kcal mol–1, las cuales son muy inferiores a las energías de un enlace covalente típico (50-200+ kcal mol–1) (Maron, 1993, p. 737). Existen dos clases de fuerzas intermoleculares: las fuerzas de van der Waals y los puentes de hidrógeno.
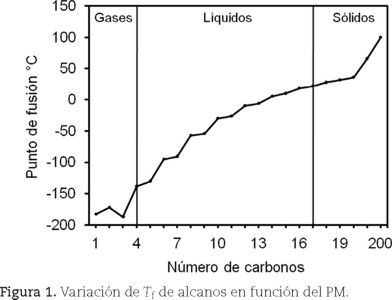
Los enlaces conocidos como fuerzas de Van der Waals son fuerzas de atracción que involucran interacciones: dipolo-dipolo, dipolo-dipolo inducido y fuerzas de dispersión. En la figura 1 se aprecia el efecto de las fuerzas de Van der Waals en las temperaturas de fusión (Tf) y estados físicos de alcanos lineales alifáticos. La Tf aumenta a medida que crece el número de carbonos en las moléculas y, como consecuencia, el número de enlaces de van der Waals. Los cuatro primeros hidrocarburos son gases, los 13 siguientes (C5-C17) son líquidos y los de 18 átomos de carbono o más, sólidos a temperatura ambiente. Es de esperar que al aumentar la longitud de la cadena hidrocarbonada los sólidos sean más consistentes porque, aunque estos enlaces son relativamente débiles, dan cohesión a las moléculas de polímeros cuando actúan en conjunto.
]]>
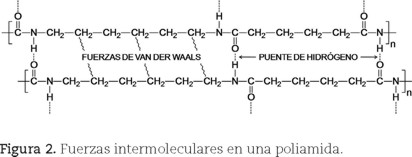
Los puentes de hidrógeno son un tipo especial de interacción dipolo-dipolo entre el átomo de hidrógeno de un enlace polar, como N–H, O–H ó F–H, y un átomo muy electronegativo como flúor (F), oxígeno (O) o nitrógeno (N). Estos enlaces son mucho más fuertes que los de van der Waals y, aunque son más débiles que los covalentes, al tomar en consideración un elevado número de ellos entre las cadenas poliméricas, resultan en mayores fuerzas de atracción en los polímeros que los presentan (figura 2).

Las fuerzas intermoleculares juegan un papel muy importante en propiedades de polímeros como la Tf, la temperatura de transición vítrea (Tg), la cristalinidad, y las propiedades mecánicas, como se explicará más adelante.
Efecto del grado de polimerizacion
El grado de polimerización (DP, por sus siglas en inglés) es una medida de la longitud de las cadenas poliméricas, ya que es el número promedio de unidades monoméricas por molécula de polímero y es, por tanto, directamente proporcional al peso molecular promedio en número,  . La longitud de las moléculas poliméricas tiene influencia notable en algunas de las propiedades de los polímeros, principalmente en las mecánicas (Sauer, 1977, pp. 396-399). Como puede apreciarse en la figura 3, a los polímeros se les puede asociar un DP, denominado crítico (DPc), a partir del cual presentan resistencia mecánica y que varía para las diferentes familias de polímeros. Por ejemplo, las poliamidas alcanzan este DPc alrededor de 40 (
. La longitud de las moléculas poliméricas tiene influencia notable en algunas de las propiedades de los polímeros, principalmente en las mecánicas (Sauer, 1977, pp. 396-399). Como puede apreciarse en la figura 3, a los polímeros se les puede asociar un DP, denominado crítico (DPc), a partir del cual presentan resistencia mecánica y que varía para las diferentes familias de polímeros. Por ejemplo, las poliamidas alcanzan este DPc alrededor de 40 ( ), las celulosas a 60 (
), las celulosas a 60 (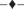 ) y algunos polímeros vinílicos hasta un DPc de 100 (
) y algunos polímeros vinílicos hasta un DPc de 100 ( ) (Mark, 1977, pp. 10-13).
) (Mark, 1977, pp. 10-13).
En este punto es interesante remitirse a la definición propuesta por la IUPAC para los polímeros como moléculas de peso molecular relativamente alto, donde el término relativamente alto se refiere al hecho de que al remover o agregar una o pocas moléculas de monómero sus propiedades no cambian apreciablemente.
Dentro de cierto intervalo de pesos moleculares de muchos termoplásticos, las magnitudes de módulo tensil, no parecen estar directamente influenciadas por la longitud de las cadenas; sin embargo, es de esperar que las propiedades de ruptura como la resistencia al impacto, la deformación y la resistencia últimas sí lo estén. A medida que aumenta el tamaño de las cadenas, lo hace el número de cadenas enlazantes entre los cristalitos, la flexibilidad y, por tanto, la tenacidad (Sauer, 1977, pp. 396-399). Matemáticamente la resistencia tensil, RT, está en función del  de acuerdo con la siguiente ecuación (Billmeyer, 1975, p. 235):
de acuerdo con la siguiente ecuación (Billmeyer, 1975, p. 235):
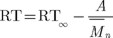
donde RT∞ es el esfuerzo tensil a un peso molecular infinito y A es una constante
Por otra parte, al aumentar el tamaño de las cadenas también se incrementan tanto la viscosidad del polímero en solución como la del polímero fundido. Esto último es de gran importancia en el procesamiento de los polímeros, pues la gran mayoría se procesan en estado fundido.
Relación estructura-cristalinidad-propiedades
En los polímeros con tendencia a la cristalinidad, sus cadenas o parte de ellas pueden agruparse de manera ordenada dando origen a regiones cristalinas, mientras que las secciones desordenadas forman regiones amorfas. Los polímeros que presentan ambos tipos de regiones, es decir que son parcialmente cristalinos, se denominan semicristalinos. Por otra parte, aquéllos cuyas moléculas están en total desorden se les denominan amorfos. Dentro de los primeros se encuentran las poliamidas, los poliésteres y los polietilenos, mientras que en los segundos están el hule natural, las resinas fenólicas y los copolímeros de estireno como el acrilonitrilo-butadieno- estireno (ABS).
Para explicar cómo se organizan las cadenas poliméricas en regiones cristalinas se han propuesto varios modelos (Odian, 1991, pp. 25-27). El modelo de micela de flecos considera que las cadenas o secciones de éstas se ordenan formando cristalitos dentro de una matriz amorfa. Una cadena puede formar parte de varios cristalitos y de varias regiones amorfas (figura 4a).
]]> Otro modelo, el de cadena plegada, explica la morfología de monocristales formados por la evaporación de soluciones de polímeros y propone que las cadenas de polímero cristalizan como placas formadas por laminitas, con una medida de 10,000 Å × 100 Å. En la figura 4b se representa una cadena de polietileno (PE) que se dobla a cierta distancia en varias ocasiones formando una cadena plegada.Las cadenas plegadas forman hileras que se acoplan una tras otra para formar una laminita y se conectan con otras laminitas por medio de las mismas cadenas provenientes de las regiones amorfas, como se muestra en la figura 4b.
La figura 5 muestra los dos principales modelos de laminitas. En la figura 5a las cadenas reingresan de forma inmediata y adyacente a la laminita, mientras que en la figura 5b las cadenas salen de la laminita y viajan cierta distancia sobre ella antes de reingresar a otra sección de la misma o en otra laminita. En estos modelos las zonas amorfas se forman por defectos en el proceso de plegamiento: plegamientos imperfectos, irregularidades en el empaquetamiento, impurezas ocluidas, cadenas enredadas o extremos de cadenas, entre otros.
Al enfriarse un polímero semicristalino fundido, cristaliza formando un conjunto de laminitas que crecen a partir de un centro radial, formando estructuras llamadas esferulitas que llegan a medir entre 5 y 10 micras, figura 6a (Hernández, 2010). Una representación esquemática se muestra en las figuras 6b y 6c. Las laminitas constituyen las regiones cristalinas y están unidas entre ellas por moléculas enlazantes que forman parte de las zonas amorfas (Geil, 1977, p. 228).
Existe otro tipo de morfología cristalina en los polímeros que consiste en cadenas extendidas y que se presenta: a) en polímeros naturales como la seda y el algodón, b) por la aplicación de esfuerzos como la que ocurre al estirar una liga de caucho (el caucho natural es amorfo, pero al estirarse más de 300% sus cadenas se alinean en arreglos que producen cristalinidad) (Sauer, 1977, p. 304) o, c) durante el enfriamiento en el procesamiento de fibras a partir de material fundido.
Las regiones cristalinas otorgan rigidez y resistencia, mientras que las amorfas dan flexibilidad y tenacidad a los polímeros (Sauer, 1977, p. 304). Por tanto, es de esperar que los defectos en el proceso de cristalización y las moléculas enlazantes aumenten la tenacidad de los polímeros. Por otra parte, la cristalinidad tiene un efecto marcado en ciertas propiedades: disminuye la solubilidad y la permeabilidad a los gases, pero aumenta la dispersión de la luz, especialmente si las regiones cristalinas son de tamaño significativo comparable con la longitud de onda de la luz, por lo que los plásticos cristalinos tienden a ser opacos.
Los factores que principalmente contribuyen a la cristalinidad de un polímero son la magnitud de las fuerzas secundarias y una estructura que permita un arreglo regular. Un efecto notable de las fuerzas intermoleculares en la formación de cristales, es el caso del Nylon 6,6 cuyas cadenas se encuentran fuertemente unidas entre sí a través de enlaces por puente de hidrógeno, además de fuerzas de Van der Waals (figura 2). Por otra parte, a pesar de que en el PE las fuerzas secundarias son débiles, su elevada regularidad estructural le permite un alto grado de cristalinidad, que se ve favorecido por la flexibilidad de las cadenas del PE y la ausencia de grupos voluminosos. Por el contrario, los tres principales efectos estructurales que limitan la cristalización son (Mark, 1977, pp. 14-22; Brydson, 1999, pp. 64-69):
a) Flexibilidad de la cadena y fuerzas intermoleculares.- Polímeros muy flexibles con fuerzas intermoleculares débiles no cristalizarán, como es el caso del polisiloxano (1), el cual es altamente flexible por la presencia de átomos de oxígeno en la cadena principal en cada unidad repetitiva. Sin embargo, si las fuerzas intermoleculares son altas, se favorece la cristalinidad, como en el caso del poliacetal (2).

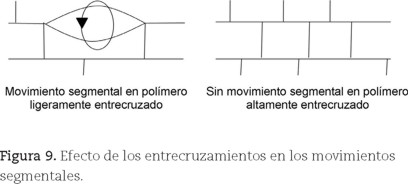
Las cadenas con estructuras cíclicas, que otorgan rigidez a los polímeros, como el poli (etilentereftalato), PET, no cristalizan fácilmente, aunque pueden hacerlo hasta cierto nivel debido al carácter polar de las moléculas, como se vio anteriormente. También se forman estructuras rígidas en polímeros entrecruzados (figuras 7c y 9). El entrecruzamiento se produce comúnmente cuando las cadenas se unen entre ellas por medio de enlaces covalentes, lo que impedirá el plegamiento de las cadenas y por tanto, la formación de cristales, como es el caso de los plásticos termoestables. También existen entrecruzamientos no covalentes, por tanto reversibles, como el debido a enlaces iónicos y el originado por puentes de hidrógeno (Brydson, 1999, p. 54).
]]> b) Estereorregularidad.- Si un H de cada unidad repetitiva del PE es sustituido por otro átomo o grupos de átomos, su regularidad puede perderse dependiendo de la colocación de estos grupos en la cadena. El orden relativo de dichos grupos a lo largo de la cadena se denomina tacticidad. Un ejemplo interesante de los diferentes tipos de tacticidad se presenta en el polipropileno (PP) donde un H del PE es sustituido por un grupo metilo en cada unidad monomérica.Cuando los grupos metilos están en un solo lado a lo largo de la cadena, el PP se llama isotáctico (3), si se encuentran alternadamente en ambos lados de la cadena se le llama PP sindiotáctico (4). Ambos presentan estructuras cristalinas. Si los grupos metilos están ubicados en ambos lados de la cadena principal sin ningún orden, el PP tiene dificultad para cristalizar. En este caso el PP se denomina atáctico (5), es amorfo y apenas se usa comercialmente. Otros polímeros ampliamente utilizados que, generalmente, son atácticos y amorfos incluyen al poliestireno (PS), el poli(metacrilato de metilo) (PMMA) y el poli(cloruro de vinilo) (PVC).
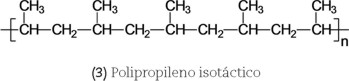

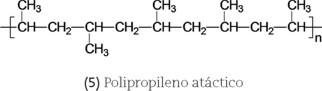
A diferencia del PE, el PP no tiene la capacidad de plegarse sobre sí mismo, puesto que el grupo metilo impide este arreglo. En este caso, las zonas cristalinas están formadas por cadenas que se acomodan formando rizos (arreglos helicoidales).
c) Ramificaciones y grupos voluminosos.- Cuando existen obstáculos para el plegamiento dentro de la estructura de las cadenas será más difícil que los polímeros cristalicen, lo cual puede ocurrir por la presencia de grupos voluminosos o de ramificaciones. En el primer caso se cuentan los polímeros como el PS o PMMA, donde grupos fenilo y metil metacrilato, respectivamente, sustituyen un H de cada unidad repetitiva del PE. Sin embargo, si el grupo sustituyente no es grande, como en el caso del F en el politetrafluoroetileno (PTFE, Teflón®), no hay interferencia para cristalizar.
El caso de las ramificaciones es bien conocido para el PE. El PE de alta densidad (PEAD) es un polímero lineal, (figura 7a) con una cristalinidad relativamente alta, debido a la facilidad que tienen las cadenas de plegarse unas con otras sin ningún impedimento. El PE de baja densidad (PEBD) es ramificado (figura 7b) y de menor cristalinidad, debido a que las ramificaciones en la cadena principal no facilitan la cristalización ni el acomodo compacto de las cadenas, por lo cual es menos denso que el PEAD. En la tabla 1 se comparan las propiedades de diferentes tipos de PE. Nótese cómo al aumentar la densidad (mayor cristalinidad) aumentan notablemente la resistencia tensil y el módulo (Sauer, 1977, p. 396).

Relación estructura-temperatura de transición vítrea
La temperatura de transición vítrea o Tg es un intervalo corto de temperaturas en el cual los materiales plásticos, al enfriarse, pasan de ser flexibles a rígidos. Esta transición está relacionada con la movilidad de segmentos de cadenas y con la disponibilidad de un cierto volumen (volumen libre) para que dicho segmento se mueva. Estos movimientos se pueden visualizar como rotaciones coordinadas en los extremos de los segmentos que abarcan aproximadamente entre 5 y 20 átomos, como se ve en la figura 8 (Odian, 1991, pp. 29-33)

La Tg se observa sólo en las regiones amorfas. Las cadenas que se encuentran dentro de un cristal no pueden ejecutar este movimiento debido a la fuerte interacción que hay entre ellas y a la falta de un volumen libre.
Los factores que determinan la Tg serán aquellos que afecten la facilidad de movimiento de los segmentos de las cadenas, siendo los más importantes la rigidez o flexibilidad de la cadena y la magnitud de las fuerzas intermoleculares. A continuación se describen los principales factores que afectan la Tg.
]]> a) La rigidez en la cadena.- Inhibe movimientos de segmentos de la misma y, por el contrario, su flexibilidad los favorece. Un ejemplo de grupos que otorgan rigidez a la cadena es el anillo aromático dentro de la cadena principal. En la tabla 2 se observa este efecto para el PET (6) y se compara con una cadena similar flexible (7). Como puede observarse, la diferencia entre sus valores de Tg es de casi 140ºC.b) Fuerzas intermoleculares.- La intensidad de las fuerzas intermoleculares entre los grupos laterales de las cadenas influirá en la facilidad de movimiento segmental, y por tanto, en su Tg. Polímeros como el PE y el PP presentan una baja Tg (ver tabla 3), debido en parte a las débiles atracciones entre sus cadenas, que dan como resultado una alta movilidad. Por el contrario, en el PVC o el poliacrilonitrilo (PAN) los grupos sustituyentes, cuyas fuerzas de atracción son más intensas, dificultan el movimiento segmental, causando un aumento en la Tg (Fried, 1995, pp. 157-158).
c) Separación entre las cadenas.- Mientras mayor sea la distancia entre cadenas, su Tg será más baja. Esto se atribuye al aumento del volumen libre entre las cadenas. En la tabla 4 se observa que a medida que se agregan grupos espaciadores (−CH2−) a R en los metacrilatos mostrados (9), aumenta la separación entre cadenas y disminuye la Tg (Fried, 1995, pp. 157-158).


d) Grupos voluminosos sustituyentes.- Los grupos voluminosos originarán una mayor dificultad para el movimiento a las cadenas en las que están unidos o impedirán el movimiento de moléculas vecinas, ocasionando que su Tg se eleve, como se puede observar al comparar el PS con el poli(α-vinil naftaleno) en la tabla 3.
e) Entrecruzamiento.- Al aumentar el grado de entrecruzamiento, aumenta el número de puntos de enlace entre las cadenas y disminuyen los segmentos que pueden moverse. La tabla 5 muestra el efecto notable de la adición de azufre, como agente entrecruzante, en la Tg del poliisopreno (Brydson, 1999, p. 64).

Relación estructura - Temperatura de fusión
La temperatura de fusión (Tf) de un polímero es la temperatura a la cual las regiones cristalinas de una muestra de polímero funden. En la Tf las fuerzas intermoleculares que mantienen el orden estructural de las cadenas son superadas. Como la Tf implica dar energía suficiente para que las cadenas se muevan en su totalidad, los factores que impiden estos movimientos serán, como en el caso de la Tg, la rigidez y las fuerzas intermoleculares, por lo que generalmente un polímero con una Tf alta también tendrá una Tg alta (Odian, 2004, pp. 29-33).
El efecto de las fuerzas intermoleculares en la Tf es más fácilmente observable para polímeros de una misma familia, y por tanto, con fuerzas secundarias similares. Un ejemplo puede notarse comparando poliamidas (10) cuyas cadenas se encuentran más cercanas unas de otras con polímeros similares pero con cadenas con mayor separación (tabla 6) (Putscher, 1982, pp. 342-346).


Puede observarse que la introducción de grupos espaciadores en R, causa desorden lateral forzando que las cadenas se aparten e interfieran en la cohesión intermolecular de los grupos polares existentes.
El efecto de las fuerzas intermoleculares se puede observar también para las dos series de poliamidas mostradas en la tabla 7: tereftalamidas alifáticas (11) y adipamidas (12) (Putscher, 1982, pp. 342-346).
]]>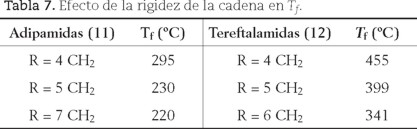


Como puede verse en ambos casos, a medida que aumenta la separación entre los grupos amino, debido a un mayor número de grupos espaciadores (−CH2−) en R, disminuye la proporción de grupos amido respecto al número total de átomos en la cadena, y por tanto la proporción de enlaces por puente de hidrógeno, lo que se refleja en una disminución de la Tf. Además, las adipamidas tienen una Tf entre 110ºC a 150ºC menor que las correspondientes tereftalamidas, lo cual muestra el efecto de la rigidez producida por el anillo fenileno en la estructura, como se vio anteriormente. Aunque existen algunas excepciones a estas observaciones, estas tendencias muestran el efecto de la estructura y las fuerzas intermoleculares en la Tf.
Variación del módulo con la temperatura y su relación con la estructura
El comportamiento mecánico de un polímero generalmente se ve influenciado por la temperatura. La figura 10, ejemplifica la variación del módulo de relajación para tres tipos de PS. Tal variación puede dividirse en 5 regiones, que se describen a continuación (Sauer,1977, pp. 373-374).
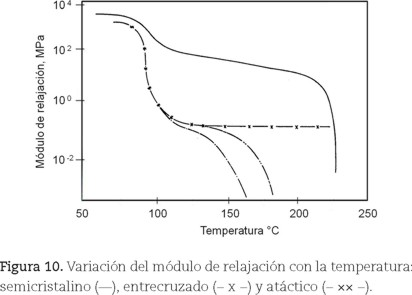
Al aumentar la temperatura se llega a la región de transición, que se ubica muy cerca de la Tg, donde se da la transición del estado rígido al flexible y el módulo cae notoriamente en un intervalo corto de temperatura. En esta región los polímeros semicristalinos son resistentes y tenaces. En ellos la magnitud de la caída del módulo dependerá de la fracción de zonas cristalinas, que dan rigidez y resistencia al polímero, mientras que la parte amorfa le permitirá deformación elástica.
Posteriormente, se ubica la región ahulada, en la que el módulo permanece casi constante con la temperatura. El material se deforma como el caucho. En esta región es posible una deformación extensiva con una rápida recuperación de regreso a la forma original cuando se elimina el esfuerzo puesto que las cadenas tienen movimientos segmentales muy rápidos. Una pequeña proporción de entrecruzamientos extiende esta región entre 100 y 200ºC.
Finalmente se presentan las regiones de flujo ahulado y flujo líquido donde el módulo vuelve a disminuir, notablemente en la última. El material experimenta una transformación gradual de sólido elástico blando a líquido viscoso. La movilidad de las cadenas se intensifica y los segmentos de éstas experimentan movimientos de vibración y de rotación completamente independientes unos de otros. En los polímeros semicristalinos, esta región comienza a temperaturas cercanas a la Tf.
Relación estructura-propiedades mecánicas
A partir de su comportamiento en ensayos esfuerzo-deformación, los polímeros se pueden clasificar en cuatro categorías principales, como se muestra en la figura 11 (Odian, 2001, pp. 33-37, y Sauer, 1977, pp. 304-307).

Los elastómeros tienen cadenas muy flexibles, lo cual los hace fácilmente deformables elásticamente y presentar elongaciones reversibles (<500-1000%) a esfuerzos relativamente bajos. Estas características se deben a que las fuerzas intermoleculares son muy bajas, así como las barreras de rotación, lo que permite que las cadenas, más que extendidas, adopten configuraciones enroscadas, por lo que pueden ser estiradas en altas proporciones fácilmente. Cuando existen entrecruzamientos químicos, físicos o enmarañamientos entre las cadenas debido a su alto peso molecular, los elastómeros tienden a regresar a sus dimensiones originales, al retirar el esfuerzo que origina la deformación. Ejemplos de estos materiales son los cauchos naturales o sintéticos.
]]> Los plásticos flexibles tienen bajo módulo (15000–350 000 N/cm2), baja resistencia tensil (1500–7000 N/cm2) y una elongación promedio entre 20-800%. En comparación con los elastómeros, las fuerzas intermoleculares y las barreras de rotación C-C son más altas lo que aumenta sus propiedades mecánicas, pero las cadenas conservan aún suficiente flexibilidad. Estos materiales pueden ser semicristalinos como el PE, Nylon y PP, o amorfos como el PC, el PS y el PMMA.El amplio intervalo de usos finales de los plásticos requiere una diversidad de combinaciones de propiedades que, en general, son intermedias entre las de las fibras y las de los elastómeros. Así, los plásticos típicos pueden tener energías cohesivas superiores a los elastómeros pero inferiores a las fibras. Cuando los plásticos flexibles se someten a un esfuerzo de tensión en su región elástica las laminitas se desplazan una con respecto a otra estirando las cadenas en las partes intermedias de la parte amorfa, pero cuando se deja de aplicar el esfuerzo éstas regresan a su lugar (figura 12).

Si se sigue aplicando esfuerzo se llega al punto de cedencia en donde las laminitas se rompen en secciones más pequeñas, venciendo algunas de las fuerzas intermoleculares, con la consecuente deformación permanente y la orientación de las cadenas en dirección del esfuerzo (Callister, 2003, p. 493).
Los plásticos rígidos tienen alto módulo (70 000–350 000 N/cm2), moderada resistencia tensil (3 000–8 500 N/cm2) y su elongación es muy pequeña (<0.5–3%). Son estructuras altamente entrecruzadas, por lo que son rígidas, de baja flexibilidad y frágiles si se usan en estado puro. Ejemplos son las resinas fenólicas, epóxicas y melamina-formaldehído.
Las fibras son polímeros con alta resistencia tensil (>35 000 N/cm2), alto módulo (>35 000 N/cm2) y sufren muy poca deformación (<10–50%). En estos materiales el eje de las cadenas de los polímeros tienden a alinearse a lo largo de la dirección de la fibra, por lo que sus propiedades mecánicas son mejores en esa dirección que en la perpendicular. Son altamente cristalinos y presentan fuerzas intermoleculares elevadas. Ejemplos comunes son el nylon, el PET, el PP y la celulosa.
Conclusiones
La estrecha relación que existe entre las propiedades y la estructura de los polímeros hace posible diseñar materiales poliméricos para aplicaciones con requerimientos de desempeño altamente específicos, pues su comportamiento en determinadas condiciones se puede anticipar, en gran medida, si se conoce su estructura. Por otra parte, la amplia cantidad de modificaciones posibles en la composición de los polímeros permite que éstos puedan abarcar una gama de propiedades químicas, mecánicas, ópticas y eléctricas y, por tanto, de usos en gran variedad de aplicaciones tecnológicas como sustitutos de otros materiales.
]]>Referencias
Behl, M., and Lendlein, A., Shape Memory Polymers. Materials Today, 10(4), 20–28, 2007. [ Links ]
Billmeyer, F. W., Ciencia de los polímeros, Barcelona, España: Reverté, 1975. [ Links ]
Brydson, J., Plastic Materials, Oxford, Great Britain: Butterworth-Heinemann, 1999. [ Links ]
Callister, W. D., Materials Science and Engineering. An Introduction, USA: John Wiley and Sons, 2003. [ Links ]
]]>Conde, N., A la altura de los súper-plásticos, Revista Ambiente Plástico, (28), 60–80, 2008. [ Links ]
Fried, J. R., Polymer Science and Technology, New Jersey, USA: Prentice-Hall PTR, 1995. [ Links ]
Friend, R. H., et al., Electroluminescence in conjugated polymers, Nature, (397), 121–128, 1999. [ Links ]
Putscher, R. E., "Polyamides", in: Encyclopedia of Chemical Technology. Vol 18. USA: John Wiley and Sons, 1982. [ Links ]
Geil, P. H., Polymer Morphology in Kaufman HS (editor), Introduction to polymer science and technology: An SPE textbook, (pp. 203-328), New York, USA: Wiley-Interscience Publication, 1977. [ Links ]
]]>Hernández S., R. A., Esterificación de la hidroxipropilcelulosa con derivados de bifenilo. Tesis: Benemérita Universidad Autónoma de Puebla, México, 2010. [ Links ]
IUPAC, Consultado por última vez en julio 20, 2009, en la URL http://goldbook.iupac.org/M03667.html
Mark, H. F., y Atlas, S., "Introduction to Polymer Science", in: Kaufman,H.S.(editor), Introduction to polymer science and technology: An SPE textbook (pp. 1-24), New York, USA: Wiley-Interscience Publication, 1977. [ Links ]
Maron, S. H. y Prutton, C. F., Fundamentos de Físico-química. México, DF, México: Limusa, S. A., 1993. [ Links ]
Odian, G., Principles of polymerization. USA: Wiley-Interscience, 2004. [ Links ]
Sauer, J. A., y Pae K. P., "Mechanical properties of high polymers", in: Kaufman H. S. (editor), Introduction to polymer science and technology: An SPE textbook, (pp. 302–423), New York, USA: Wiley-Interscience Publication, 1977. [ Links ]
van der Zwaag, S., Self-Healing Materials, Plastics Engineering, 64(4), 36-41, 2008. [ Links ]
]]>