Formas de expresar la composición química en el SI
Forms to express chemical composition in the frame of SI
Dora Marina Gutiérrez-Avella y Juan Antonio Guardado-Pérez1
1 Universidad Autónoma de Querétaro, Facultad de Química. Centro Universitario Cerro de las Campanas s/n. CP 76010. Correo electrónico: domagu@uaq.mx
]]>Recibido: 4 de marzo de 2009
Aceptado: 28 de mayo de 2009
Abstract
Due to wide range and complexity of materials and chemicals, several quantities are normally used to express the chemical composition of mixtures.Nevertheless,during years those quantities have been reviewed in the frame of the International System of Units (SI) by international organizations related to chemical sciences and a set of quantities with unified nomenclature and notation has been proposed to express chemical composition. Important concepts related to chemical measurements like uncertainty and traceability are discussed to aim correct use and understanding of quantities and units of composition. A brief description of SI units and writing rules are also included.
Keywords: International System (SI), chemical composition, uncertainty, traceability, writing rules in the SI.
Antecedentes
En virtud de la gran diversidad de materiales y sustancias químicas, desde los albores de la química se han venido proponiendo y utilizando diferentes magnitudes de composición química. Algunas de estas magnitudes de composición química están bien definidas en la actualidad y su uso está bien generalizado, pero otras necesitan ser revisadas dentro del marco del Sistema Internacional de Unidades (SI).
]]> El SI es el sistema de unidades más completo más robusto y es utilizado por convención en prácticamente todos los países del mundo. Incluso aquellos países donde aún se trabaja con el sistema inglés de unidades, van migrando paulatinamente hacia el SI. Puede decirse que el origen del SI se remonta a 1875 cuando se firmó el Tratado del Metro por la Convención del Metro y se adoptó el Sistema Métrico Decimal como sistema universal de unidades. En realidad el Sistema Métrico Decimal tuvo su origen en Francia varios años antes como resultado de los trabajos de científicos de alto renombre, entre ellos Lavoisier, considerado padre de la Química, quien afirmó,"... nada más grande ni más sublime ha salido de las manos del hombre que el Sistema Métrico Decimal" (Nava et al., 2001), sin embargo este último tomó el carácter de sistema internacional hasta que fue adoptado por la Convención del Metro en 1875. Ahora bien, por el auge científico y técnico a largo del siglo XX, el Sistema Métrico Decimal derivó en varios subsistemas de unidades como el CGS y el MKS pero fue reunificado, fortalecido y bautizado como Sistema Internacional de Unidades (SI) en 1960.La Convención del Metro, que es un tratado diplomático, opera por medio de la Conferencia General de Pesas y Medidas (CGPM) donde están representados todos los países miembros. A su vez, la CGPM creó y se soporta en el Comité Internacional de Pesas y Medidas (CIPM), organismo al más alto nivel científico que desarrolla y coordina los trabajos en metrología a nivel internacional. El CIPM ha establecido diferentes comités consultivos de apoyo para atender en lo particular cada área de la técnica o tipo de medición concerniente (BIPM, 2006). De entre éstos, mención especial merece el Comité Consultivo para la Cantidad de Sustancia (CCQM, por sus siglas en francés) que es la entidad encargada de coordinar y promover el trabajo relativo a las mediciones químicas y biológicas. Dentro del CCQM participan organizaciones internacionales tales como la IUPAC (Unión Internacional de Química Pura y Aplicada), la ISO (Organización Internacional de Normalización), la IAEA (Agencia Internacional de Energía Atómica) y los institutos nacionales de metrología de los países miembros. Así pues, las mediciones químicas son parte integrante y actuante del SI. Es justamente en el seno del CCQM que se ha visto la necesidad de acotar y homologar las magnitudes de composición al SI tanto es sus aspectos conceptuales como de notación y de lenguaje.
Objetivo
Dar a conocer y discutir las diferentes formas de expresar la composición química dentro del Sistema Internacional de Unidades junto con reglas de escritura y otros conceptos que deben tenerse en consideración con relación a las mediciones químicas. Esto con el fin de homologar y unificar el concepto, el lenguaje y la notación de la composición química.
El Sistema Internacional de Unidades
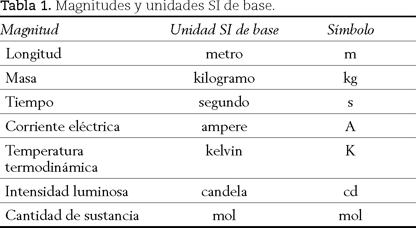
El SI está sustentado en siete magnitudes de base y para cada una de ellas se define una unidad, con nombre, símbolo y valor bien definidos, véase tabla 1. A partir de las unidades de base se obtiene un sinnúmero de unidades derivadas para expresar los valores de otras tantas magnitudes, por ejemplo, superficie, energía, resistencia eléctrica, véase tabla 2. Adicionalmente, el SI permite el uso de un conjunto de unidades aun cuando no pertenecen formalmente al SI, por ejemplo, el minuto, el litro, la tonelada. En principio, todas las magnitudes mecánicas, físicas, eléctricas y químicas pueden y debe rían expresarse por medio de las unidades definidas en el SI.

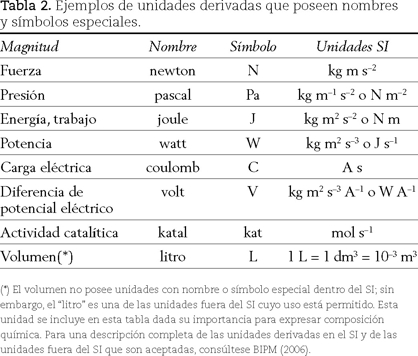
Aparte de un conjunto de unidades rigurosamente definidas, el SI incluye el uso prefijos para expresar múltiplos y submúltiplos de las unidades, por ejemplo, nano, mili, mega. Además, el SI describe las reglas de uso y de escritura de todas estas unidades (BIPM, 2006).
Magnitudes y unidades de composición química
Existe una gran diversidad de mediciones químicas relacionadas con las diferentes propiedades o parámetros de las sustancias o materiales, todas éstas se expresarían de una forma o de otra mediante las siete unidades de base del SI, por ejemplo, energías de enlace, distancias intersticiales, potenciales químicos. Sin embargo, el alcance de este artículo se limita a las magnitudes de composición química y a sus unidades en el SI. Aun así, la gran diversidad de sustancias, mezclas y compuestos químicos, hace que las magnitudes para expresar la composición química sean muy variadas.
La composición de una mezcla se expresa generalmente por medio de una magnitud intensiva ya que la composición es independiente del tamaño, dado éste en términos de cantidad de sustancia, masa o volumen de la muestra bajo estudio. Esta magnitud intensiva se obtiene del cociente de dos magnitudes extensivas, siendo el numerador, la magnitud de interés, y el denominador es una magnitud relacionada al tamaño de la muestra que se toma como base de cálculo. De esta forma, las magnitudes de composición se pueden expresar de diferentes maneras dependiendo de la combinación entre las magnitudes extensivas en juego y de la conveniencia de acuerdo a la aplicación a que están destinadas. En el seno del CCQM, se han tratado varias propuestas para unificar el uso de las unidades y magnitudes de composición química. La tabla 3 recopila las diferentes formas de expresar las magnitudes de composición química recomendadas en el CCQM (Cvitaš, 1996).

Ejemplo:
]]> La composición de una disolución de 10 mL/L (se hace la aclaración que aun cuando el litro no es una unidad SI, su uso está permitido) de etanol en agua, preparada a 20 ºC, puede expresarse de diferentes formas. Sabiendo que la densidad de esta disolución es de 0,9967 g cm-3, la del etanol puro es de 0,7893 g cm-3 y la del agua es de 0,9982 g cm-3, todas ellas a 20 ºC. Entonces 1 L de disolución tiene una masa de 996,7 g y contiene 10 mL de etanol, equivalentes a 7,893 g (o bien, 171,332 mmol); la diferencia, 988,807 g es la masa de agua, que es igual a 990,59 mL (o bien, 54,887 mol); con estos datos se calculan la magnitudes mostradas en la tabla 4.
Reglas de escritura en el SI
El valor de una magnitud se compone de un valor numérico y de las unidades asociadas a dicho valor, la escritura del valor de la magnitud y sus unidades sigue en lo general todas las reglas gramaticales aplicables ( BIPM, 2006). Algunas consideraciones especiales se señalan brevemente a continuación:
]]> Una descripción más amplia de las reglas de escritura del SI se encuentra en BIPM (2006) o Nava et al. (2001) o NOM008 (2002).i. El binomio, valor numérico y las unidades asociadas (o los símbolos de éstas), es indisociable y debe interpretarse como una entidad algebraica lógica, el valor numérico es el coeficiente o factor que multiplica al valor definido de una unidad (o conjunto de éstas). El valor numérico se separa de sus unidades por medio de un espacio.
Ejemplos: 2 metros o 2 m, 59 segundos o 59 s, 20 newton o 20 N.
ii. El SI permite el uso del "punto" o de la "coma" como separadores decimales, la decisión depende del símbolo decimal que se utiliza normalmente en cada contexto o país. Los países de habla inglesa usan tradicionalmente el punto, los países de habla hispana, francesa y alemana utilizan generalmente la coma. Nota: en este documento se utiliza la coma como separador decimal. Ejemplos: 298,15 kelvin o 298,15 K, 30,0009 metros o 30,0009 m. Opcionalmente, en números muy grandes, las cifras pueden agruparse en múltiplos de 1000 separadas por medio de un espacio, pero nunca utilizando ni puntos ni comas.
]]> Ejemplos: 100 000 3,141 592 654iii. Los símbolos de las unidades se escriben en caracteres romanos (rectos), esto aplica tanto a unidades SI de base como para las unidades derivadas. Los nombres o los símbolos de las unidades deben escribirse correctamente según se describen en el SI (BIPM, 2006 o ISO 31, 2000). Ejemplos: metro o metros (m), segundo o segundos (s), newton o newtons (N), pascales (Pa).
iv. Los símbolos de las unidades no son abreviaciones, por tanto, no se coloca punto en seguida del símbolo y no sufren modificación al plural.
Ejemplos de escritura incorrecta: kgs kg. Amps. mts.
v. Cuando una unidad derivada se expresa mediante el producto o cociente de una o varias unidades, los símbolos de las unidades se escriben separados por un punto a media altura o simplemente por un espacio.
Ejemplos: N·m, N m,W·s,W s.
Para evitar confusión o ambigüedad con el uso de puntos o espacios al expresar el producto de números o de nombres de unidades se permite el uso del símbolo "×".
Ejemplo: newton×metro o newton metro, pero es incorrecto escribir: newton·metro
vi. Cuando una unidad derivada se expresa mediante el cociente de una o varias unidades, los símbolos de las unidades en el denominador se escriben mediante potencias negativas o bien, separados de las unidades del numerador por una línea de división oblicua (/) o una línea de división horizontal (-) y si es el caso, agrupadas dentro de paréntesis para evitar cualquier ambigüedad.
Ejemplos: Pa/m2, Pa·m-2, Pa m-2, J/(mol·K), J mol-1 K-1
]]> vii. Los múltiplos y submúltiplos de las unidades se escriben utilizando los prefijos del SI. Para una descripción completa de los nombres y de los símbolos de los prefijos del SI, consulte la referencia al BIPM (2006) o ISO 31 (2000) o NOM008 (2002). Al igual que los símbolos de las unidades, los símbolos de los prefijos se escriben en caracteres romanos (rectos) y antecediendo al símbolo de la unidad sin espacio. La expresión formada de la asociación de un símbolo de un prefijo y de un símbolo de una unidad constituye un nuevo símbolo inseparable, es decir, el símbolo de un múltiplo o un submúltiplo de la unidad, y sigue por lo tanto todas las reglas de escritura que ya se han descrito.Ejemplos: cm, mm, cm-2, mg, µg, mg/cm3
La misma regla aplica a los nombres de las unidades asociados a prefijos, por ejemplo milímetros, microgramos o megapascales.
viii. No deben utilizarse prefijos compuestos o en combinación. NOTA: La unidad base de masa, el kilogramo (kg), lleva implícito un prefijo por lo que los múltiplos y submúltiplos de masa y sus prefijos se refieren al gramo.
ix. Un prefijo debe anteceder siempre al símbolo de la unidad a la que modifica. Un prefijo solo carece de sentido físico.
x. Debe evitarse el uso de unidades no reconocidas por el SI. Cuando se requiera expresar el valor de una magnitud en otro sistema de unidades se recomienda hacerlo acompañándolo de su valor equivalente en unidades SI.
xi. Las unidades de varias de las magnitudes de composición química se forman del cociente de la misma unidad. Se dice de estas magnitudes, que son sin dimensiones o bien, de dimensión "uno". Para este tipo de magnitudes, los valores pueden escribirse acompañados de sus unidades o bien sin dimensiones.
Ejemplo: xi = 0,001 mol/mol o simplemente, xi = 0,001.
Cuando se describen magnitudes sin dimensiones debe evitarse cualquier ambigüedad que pudiera dar lugar a interpretaciones indeseables.
xii. El SI permite el uso del litro como unidad de volumen, por lo que las magnitudes de concentración que involucran volumen pueden expresarse en litros (L/L, mol/L, etc.). El símbolo SI de la unidad "litro" puede ser "l (minúscula)" o "L (mayúscula)", pero se recomienda el uso del símbolo "L" para evitar confusión con el número "uno".
Uso de los términos %, ppm, ppb y ppt
Aun cuando el uso de términos tales como partes por millón (ppm), partes por billón (ppb) y partes por trillón (ppt) tienen cierto uso en el lenguaje de la composición química, estos términos no se han definido formalmente y no existe aún un consenso en cuanto a su uso (Quinn, Mills, 1998), incluso la norma ISO 310, Secc. 2.3.3 desaconseja su uso (ISO, 1992). Una de las principales dificultades que impiden unificar estos términos es que tienen significados totalmente distintos si se expresan en diferentes idiomas o países. Por ejemplo, la palabra "billón" en español representa al número 1012 mientras que un "billion" en inglés representa al número 109.
Los términos "ppb" y "ppt" pueden tener alguna utilidad para expresar el orden de magnitud de un valor cualitativo o semicuantitativo en un contexto definido, pero definitivamente su uso no es adecuado para expresar formalmente valores de composición química según el SI.
El símbolo % (por ciento) está reconocido y ampliamente consensado a nivel internacional, por lo que su uso para expresar magnitudes de composición química sin dimensiones es aceptado (BIPM, 2006). El símbolo % se utiliza únicamente para expresar valores de unidades sin dimensiones o de dimensión "uno" y es equivalente al factor 1/100. Ejemplo: xi = 0,10 % equivale a xi = (0,10 mol)/(100 mol) = 0,0010 mol/ mol o bien, xi = 0,0010 (sin dimensiones).
Sin embargo la expresión "porcentaje" o "por ciento" no debe utilizarse en combinación con el nombre de alguna magnitud, por ejemplo, no debe decirse por ciento de fracción masa, ni porcentaje de cantidad de sustancia.
Como se ha señalado en la sección precedente, en la regla de escritura xi con relación a las magnitudes sin unidades, cuando se utiliza el término % debe evitarse toda ambigüedad que pudiera conducir a interpretaciones indeseables.
Incertidumbre y trazabilidad en mediciones químicas
]]> Siempre que se hace la medición de una magnitud química o de cualquier tipo se debe procurar que la medición sea lo más confiable posible de acuerdo con los recursos tanto materiales y humanos con que cuenta el laboratorio, también es importante lograr que la confiabilidad de la medición sea apropiada al uso a que está destinada. Para lograr una medición confiable adecuada al uso previsto deben aplicarse algunos principios experimentales y estadísticos relativamente sencillos, éstos son: la validación del método de medición, el establecimiento de la trazabilidad y la estimación de la incertidumbre de medición, entre otros. Una discusión formal sobre estos temas esta fuera del alcance de este articulo, aquí se presta solamente una introducción general con la intención de llamar la atención sobre la importancia de estos temas al momento de realizar e interpretar los resultados de una medición y para orientar a los interesados hacia documentos especializados sobre cada tema.La incertidumbre es un parámetro estadístico que expresa la dispersión probables de los resultados de una medición y generalmente se expresa como un intervalo dentro del cual se espera que se encuentre una gran parte de los resultados. Así pues, la incertidumbre expresa cuantitativamente la falta de conocimiento o duda sobre el resultado de una medición o bien, su nivel de confiabilidad. Un valor estimado de la incertidumbre de una medición se calcula a partir de las incertidumbres de todas las variables y parámetros involucrados.
Algunas fuentes típicas de incertidumbre en mediciones analíticas son las siguientes:
— Incertidumbre de los instrumentos de medición: incertidumbre de balanzas y tolerancias del material volumétrico.
— Incertidumbre de los valores de referencia de patrones o materiales de referencia.
— La repetibilidad de las lecturas.
— La reproducibilidad de las mediciones por cambios en las condiciones de medición.
— Características propias de los instrumentos: resolución, estabilidad, etc.
— Variaciones en las mediciones debidas a cambios en las condiciones ambientales.
]]> — Incertidumbre de una curva de calibración.— Incertidumbre de los parámetros que intervienen en la medición: incertidumbre de las masas atómicas relativas reportadas por la IUPAC (Böhlke et al., 2003).
Ejemplo
Una de las mediciones más típicas en química es la titulación volumétrica acido base. La ecuación C2= C1V1/V2 muestra la relación entre la variable involucradas. Suponiendo que C1, la concentración de un titulante, es igual a 1,01 mol/L y tiene una incertidumbre de 0,01 mol/L, debida a su proceso de medición. Suponiendo que V1, el volumen de titulante gastado para neutralizar la alícuota de una muestra es igual a 9,8 mL con una incertidumbre de 0,1 mL debida a la resolución de la bureta y a las variaciones de volumen por las variaciones de temperatura. Suponiendo que V2, el volumen de la alícuota de muestra titulada es de 20,0 mL con una incertidumbre de 0,2 mL debida a la especificación del matraz volumétrico y a las variaciones de temperatura. Entonces la concentración de la muestra titulada será,
C2 = (1,01 mol/L)(9,8 mL)/(20 mL) = 0,49 mol/L
La incertidumbre de esta medición se calcula a partir de la ley de combinación de la incertidumbre como sigue:

En estas ecuaciones, u[Y], representa la incertidumbre de la variable Y.
Además, para asegurar el resultado deberían realizarse varias repeticiones de esta titulación y su desviación estándar sería una fuente más de incertidumbre que debería combinarse con las otras. En las referencias ISO GUM (1995) y Eurachem (2000), se presenta un tratamiento detallado sobre la expresión y la estimación de la incertidumbre de medición.
Por último, la trazabilidad metrológica, que representa la cualidad de que el resultado de una medición haya sido determinado a partir de los valores de patrones reconocidos de mayor jerarquía o exactitud, es otro de los aspectos que aseguran la confiabilidad y la exactitud de una medición. Por ejemplo, en la titulación que acaba de ser descrita, el resultado será confiable y exacto (trazable) si y sólo si los valores de cada magnitud usados en el cálculo de la concentración son a su vez trazables. Esto quiere decir que los volúmenes de titulante y de muestra fueron medidos utilizando material volumétrico calibrado apropiadamente y que la concentración del titulante ha sido determinada apropiadamente o bien, se trata de un material de referencia cuyo valor de concentración está certificado. Este tema es discutido en las referencias Eurachem (2003) y De Bièvre, et al. (2007).
]]>Conclusiones
Por la naturaleza tan variada y tan compleja de las diferentes sustancias y de los materiales, las formas de expresar la composición química pueden ser también muy variadas. Sin embargo, es deseable unificar las definiciones de composición entorno al Sistema Internacional de Unidades.
En este artículo se hace una descripción de la propuesta de unificación de las magnitudes de composición química que fue presentada ante el CCQM del CIPM.
También se describen las reglas y convenciones de uso y escritura para expresar valores y unidades según el Sistema Internacional de Unidades que son importantes considerar a fin de unificar el lenguaje de las magnitudes químicas.
Se hace una breve discusión acerca de otros conceptos fundamentales sobre las mediciones y la expresión de los resultados, tales como la incertidumbre y la trazabilidad. Se espera que esta breve descripción sea de utilidad para todas aquellas personas involucradas en llevar a cabo mediciones químicas o para interpretar sus resultados.
Referencias
Böhlke, J. K., Laeter, J. R., De Bièvre, P., Hidaka, H., Peiser, H. S., Rosman, K. J. R., Taylor, P. D. P., Atomic weights of the elements: Review 2000 (IUPAC Technical Report), Pure Appl. Chem., 75(6), 683-800, 2003. [ Links ]
]]>Bureau International des Poids et Mesures, BIPM. Le Système internationale d'unités. 8e édition, Francia 2006. Disponible en http://www.bipm.org [ Links ]
Cvitaš T., Quantities describing compositions of mixtures, Metrologia, 33, 35-39, 1996. [ Links ]
De Bièvre, P., Dybkaer, R., Fajgelj, A., Hibbert, D. B., Metrological Traceability of Measurement Results in Chemistry, Draft Report IUPAC 2007. Consultada por última vez en dicimebre 3, 2009, en la URL http://old.iupac.org/reports/provisional/abstract07/fajgelji_draft_20070918.pdf [ Links ]
Eurachem, Traceability in Chemical Measurement. A guide to achieving comparable results in chemical measurement, 2003. Disponible en http://www.eurachem.org [ Links ]
Eurachem, Quantifying Uncertainty in Analytical Measurements, 2000. Disponible en http://www.eurachem.org [ Links ]
International Organization for Standardization, International Standard ISO 31-0, Quantities and units – Part 0: General principles. ISO, Suiza, 1992. [ Links ]
International Organization for Standardization, ISO-GUM: Guide to the expression of uncertainty in measurement. ISO, Suiza, 1995. [ Links ]
]]>Nava, H., Pezet, F., Mendoza, J., Hernández, I. El Sistema Internacional de Unidades (SI). CENAM Publicación Técnica CNM-MMM-003, México, 2001. Disponible en http://www.cenam.mx [ Links ]
Norma Oficial Mexicana NOM-008-SCFI-2002, Sistema General de Unidades de Medida, DGN, México 2002. Disponible en http://www.economianoms.gob.mx [ Links ]
Quinn, T. J., Mills, I. M., The use and abuse of the terms percent, parts per million and parts in 10n, Metrologia, 35, 807-810, 1998. [ Links ]
]]>