
Análisis de las temperaturas, la eficiencia térmica y el trabajo neto en un ciclo dual
Temperatures, work and thermal efficiency analysis of the dual cycle
Manuel Malaver1
1 Universidad Marítima del Caribe, Avenida El Ejército, Catia La Mar, Estado Vargas, Venezuela.
]]>Recibido: 16 de abril de 2007;
Aceptado: 18 de octubre de 2007.
Abstract
The main objective of this article is show the influence of compression ratio, pressure ratio, cut-off relation, temperatures and efficiency in dual thermodynamic cycle. Results obtained show that work and efficiency of dual cycle is function of high temperature of cycle, compression ratio and cut-off relation.
Key words: compression ratio, pressure ratio, cut-off relation, dual cycle.
Introducción
La termodinámica estudia entre otras cosas, los procesos de transferencia de masa y energía y es un curso fundamental en las carreras de ciencias e ingeniería. Entre las aplicaciones de la termodinámica están la generación de potencia y la refrigeración. Su estudio se hace a través del análisis de ciclos termodinámicos como los de Carnot, Rankine, Otto, Diesel, Trinkel-Sabathé y los de combustión a presión o volumen constante.
]]> Los ciclos termodinámicos se pueden clasificar en ciclos cerrados y abiertos. En los ciclos cerrados la sustancia de trabajo se regresa a su estado inicial al final del ciclo y debe recircularse. En los ciclos abiertos la sustancia de trabajo se remueve al final de cada ciclo, en vez de recircularse. Los motores de automóviles llamados máquinas térmicas o de combustión interna, funcionan de tal manera que los gases de combustión se escapan y se reemplazan por una nueva mezcla de aire combustible al terminar cada ciclo (Cengel y Boles, 2003; Van Wylen et al, 2000; Wark y Richards, 2001).El análisis de los ciclos de los motores de combustión interna es complicado debido a la presencia de fenómenos como la fricción y la rapidez de los procesos de expansión-compresión que impiden establecer condiciones de equilibrio termodinámico Si se quiere hacer manejable el estudio de un ciclo es recomendable utilizar algunas simplificaciones. Cuando al ciclo real se le eliminan todos los problemas complejos internos se obtiene un ciclo constituido por pasos reversibles. Un ciclo con estas características recibe el nombre de ciclo ideal.
Planteamiento del problema
El objetivo del presente trabajo es analizar la influencia de factores como la relación de compresión, la relación de presiones, la relación de cierre de admisión y las temperaturas sobre la eficiencia y el trabajo neto en un ciclo dual de aire estándar para motores de encendido por compresión.
En el motor de encendido por compresión, el proceso de combustión se inicia por una elevación de la temperatura de la mezcla aire-combustible por encima de su temperatura de autoencendido debido a una compresión rápida, por lo que la mezcla se pone en ignición y ocurre la combustión tan rápidamente que el volumen permanece casi constante y la presión se eleva (Wark y Richards, 2001). Los productos de la combustión se expanden y la temperatura y la presión disminuye.
Debido a la complejidad de este ciclo de potencia, los ingenieros se ven en la necesidad de trabajar con modelos idealizados, por lo que se han de establecer las siguientes aproximaciones, llamadas suposiciones de aire estándar (Cengel y Boles, 2003):
1. La sustancia de trabajo es aire que circula de modo continuo en un circuito cerrado y se comporta como un gas ideal.
2. Todos los procesos que integran el ciclo son reversibles.
]]> 3. El proceso de combustión se reemplaza por un proceso de adición térmica desde una fuente externa.4. El proceso de escape se sustituye por un proceso de eliminación térmica que regresa la sustancia de trabajo a su estado inicial.
En los motores Otto y Diesel el proceso de combustión se simula como un proceso de adición de energía en forma de calor a volumen constante o a presión constante (Cengel y Boles, 2003; Van Wylen et al, 2000; Wark y Richards, 2001). Un enfoque más realista pero más complejo sería modelar el proceso de combustión, tanto en motores de gasolina y Diesel, como una combinación de dos procesos de transferencia de calor, uno a volumen constante y el otro a presión constante (Cengel y Boles, 2003). El ciclo ideal basado en este concepto recibe el nombre de ciclo dual y el diagrama P-V se representa en la figura 1. Se considera que el ciclo en estudio es un sistema cerrado y el aire está confinado en un dispositivo pistón-cilindro. Se toma como base una cantidad de sustancia igual a 1 kg de aire.

Con las suposiciones de aire estándar, el ciclo dual teórico (Wark y Richards, 2001) se compone de los siguientes procesos reversibles (figura 1):
1 → 2 Compresión adiabática
2 → χ Calentamiento isométrico
]]> χ → 3 Calentamiento isobárico3 → 4 Expansión adiabática
4 → 1 Enfriamiento isométrico
Desarrollo
Un factor muy importante en el análisis de los ciclos es la eficiencia térmica (Van Wylen et al., 2000; Cengel y Boles, 2003). De acuerdo con las aproximaciones realizadas, para un ciclo dual se tiene que:
Utilizando la convención de Wark y Richards (2001) que define el trabajo durante un proceso reversible como W = -∫PdV el trabajo total hecho por el ciclo está dado por:

donde W1→2 (ver figura 1) es 


por lo que 
Debe aclararse que sólo una parte de la energía suministrada en forma de calor se convierte en trabajo de salida y la fracción del calor suministrado que se convierte en trabajo es una medida del rendimiento de una máquina térmica y recibe el nombre de eficiencia térmica η (Cengel y Boles, 2003). La expresión para la eficiencia térmica estará dada por:

Qabs , es el calor absorbido en el ciclo.
Entonces 
reemplazando (4) y (6) en la expresión para la eficiencia (5) queda que

donde 
considerando que 

Metodología
Utilizando las suposiciones de aire estándar que permiten estudiar ciclos de potencia de gases, se analizó la influencia de la relación de compresión, relación de presiones, la relación de cierre de admisión y temperatura máxima y mínima en la eficiencia y el trabajo neto en un ciclo dual de aire estándar. Las relaciones de compresión variaron de 2 a 14 y los valores de temperatura máxima estaban comprendidos entre 2000 y 3000 K.
La temperatura al inicio del proceso de compresión en el ciclo dual era de 290 K. Se consideró que los capacidades caloríficas son constantes cuyos valores se determinan a temperatura ambiente, esto es a 300 K.
Análisis
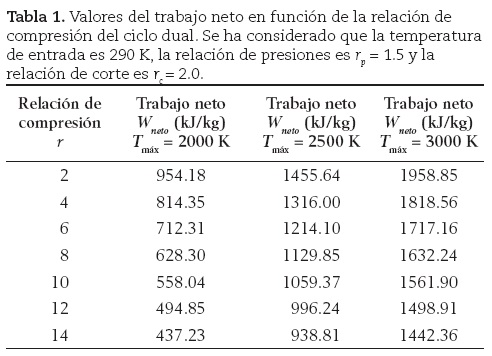
En la tabla 1 se muestra la variación del trabajo neto con la relación de compresión para una relación de relación de presiones de 1.5 y relación de cierre de admisión de 2. Se observa cómo disminuye el trabajo neto a medida que aumenta la relación de compresión. Es interesante mencionar el hecho de que, en general, los textos de termodinámica (Burghardt, 1984; Van Wylen et al., 2000; Cengel y Boles, 2003) no hacen referencia a este comportamiento. De hecho son pocos los textos de termodinámica que incluyen el ciclo dual cuando hacen el estudio de los ciclos de potencia de gases.
]]>
Considerando el procedimiento sugerido por Urrecheaga y Malaver (2003) en la determinación del trabajo neto para un ciclo de Otto, se puede entonces deducir una expresión para Wneto. De acuerdo con la ecuación (5):

Para el proceso 1-2 se tiene que 
y para el proceso 1-4 se cumple: 
lo que equivale a 
Sustituyendo la relación 
en la ecuación (15) se obtiene que:

Considerando que 

solo válida para un ciclo teórico dual. El trabajo neto para un ciclo dual de aire estándar puede entonces expresarse como:

El trabajo neto en un ciclo teórico dual es función de la relación de compresión r, la relación de presiones rp , la relación de cierre de admisión rc, las temperaturas mínima T1 y máxima T3 del ciclo, la temperatura Tx al final del calentamiento isocórico y del cociente g de capacidades calóricas.
Para la determinación de la variación del trabajo neto con la relación de compresión del motor se consideraron las siguientes condiciones iniciales:
Relación de cierre de admisió rc= 2.0
Relación de presiones rp = 1.5
Temperatura de entrada T1 = 290 K
]]> Cociente γ para el aire = 1.4
Se muestra a continuación un ejemplo de cálculo para el trabajo neto:
Sea r = 2 la relación de compresión inicial. De acuerdo con (13), la temperatura al final del proceso de compresión adiabática 1 → 2 será entonces T2 = 382.66 K. La temperatura al final del calentamiento isométrico es Tx = 573.99 K
Sustituyendo los valores de rc, rp, r, T1 y T3, Tx y γ en (20) se obtiene que Wneto = -954.18 kj/kg.
Para la determinación de la variación del rendimiento térmico en función de la relación de compresión, la relación de cierre de admisión y la relación de presiones se utilizó la ecuación (11).
En la figura 2 se observa que un aumento de la temperatura máxima ocasiona un incremento de los valores del trabajo neto para los mismos valores de la relación de compresión (tabla 1).
En la tabla 2 se muestra como varia la eficiencia térmica con la relación de compresión para distintos valores de la relación de cierre de admisión del motor. En la figura 3 se observa que para un valor dado de la relación de cierre de admisión la eficiencia térmica aumenta a medida que aumenta la relación de compresión, pero los valores obtenidos de las eficiencias se hacen cada vez menores para mayores valores de la relación rc. Del mismo modo, para un valor dado de la relación de compresión, la eficiencia térmica disminuye a medida que aumenta la relación de cierre de admisión del motor.

En la figura 4 se representa la variación de la eficiencia térmica con la relación de cierre de admisión para un valor determinado de la relación de compresión. Se observa que el rendimiento térmico decrece rápidamente al aumentar la relación de corte, para una relación de compresión dada (tabla 3). Para un valor de la relación de corte, el rendimiento térmico es mayor a medida que se incrementa la relación de compresión.
]]>

En la figura 5 se muestra como varia el rendimiento térmico con la relación de presiones del motor para líneas de relación de compresión constante. No se observa una variación apreciable de la eficiencia con la relación de presiones, en general, el rendimiento se mantiene constante para un amplio rango de valores de la relación de presiones. La eficiencia térmica tampoco presenta grandes variaciones para las distintas líneas de la relación de compresión.
Conclusiones
El motor de encendido de chispa y el de encendido por compresión no realizan la combustión de la mezcla aire-combustible ni a volumen constante ni a presión constante, por lo que parte del proceso de combustión es isométrico y el resto se realiza de una manera isobárica.
El estudio de las ecuaciones deducidas es capaz de predecir las condiciones de operación que permiten maximizar el trabajo neto e incrementar la eficiencia del ciclo estudiado. Para valores fijos de T1 y T3, el trabajo neto del ciclo dual disminuye con la relación de compresión del motor. Mientras mayor sea la temperatura al final del calentamiento isobárico, mayor será el trabajo neto del ciclo e estudiado.
Para una relación de compresión dada, el rendimiento térmico del ciclo decrece rápidamente al aumentar la relación de cierre de admisión del motor. Como es de esperarse, la eficiencia térmica se incrementa con la relación de compresión, para una relación de corte dada. Si el valor de la relación de compresión no varía, el rendimiento térmico se mantiene constante cuando se incrementa la relación de presiones del motor.
En un ciclo dual altos valores de la relación de compresión y de la temperatura máxima del ciclo incrementan el rendimiento térmico y el trabajo neto.
]]>Bibliografía
Burghardt, M.D., Ingeniería Termodinámica, 2a ed., Editorial Harla, México, 1984. [ Links ]
Cengel, Y. y Boles, M., Termodinámica, McGraw Hill, México, 2003. [ Links ]
Urrecheaga, K. y Malaver, M., Análisis de las temperaturas y de la eficiencia térmica en el ciclo de Otto, Educ. quím., 14(3) 138-141, 2003. [ Links ]
Van Wylen, G.J., R. E. Sonntag y C. Borgnakke, Fundamentos de Termodinámica, 2a ed., Limusa, México, 2000. [ Links ]
]]>Wark, K. y D. Richards, Termodinámica, 6a ed., McGraw Hill, México, 2001. [ Links ]
]]>