Producción a escala piloto de lacasa de Coriolopsis galilea
Production of laccase from Coriolopsis gallica at pilot plant scale
Rosa Román, Cristina Torres-Duarte, Marcela Ayala, Rafael Vázquez-Duhalt
Instituto de Biotecnología, Universidad Nacional Autónoma de México. Av. Universidad 2001, Col. Chamilpa, Cuernavaca, Morelos. 62250 México
]]>Autor para correspondencia:
R. Vázquez-Duhalt vazqduh@ibt.unam.mx
Recibido 20 de abril 2010;
Aceptado 28 de septiembre 2010.
Abstract
The production of laccase from the ligninolytic fungi Coriolopsis gallica was carried out at pilot plant scale in a 100 L bioreactor. A cheap fermentation medium was used containing 3% Bran Flakes in 60 mM phosphate buffer, pH 6.0 containing 0.8 mM copper sulfate. A total of 630 650 laccase units were obtained in 7-days cultures. After few purification steps, including centrifugation, ultracentrifugation, ammonium sulfate precipitation, and two ionic exchange chromatographies, a partially purified preparation was obtained with 79% of laccase showing a specific activity of 313 U/mg.
Key words: fungal laccases, enzyme production, white rot fungi.
]]>Resumen
Se realizó la producción de lacasa del hongo ligninolítico Coriolopsis gallica a escala piloto en un fermentador de 100 L. La fermentación se realizó en un medio muy económico consistente de 3% de bran flakes en un amortiguador de fosfatos de sodio 60 mM, pH 6.0, conteniendo 0.8 mM de sulfato de cobre. Se obtuvieron 630 650 unidades de actividad lacasa en 7 días de cultivo. Después de pocos pasos de purificación que consistieron en centrifugación, ultrafiltración, precipitación con sulfato de amonio y dos cromatografías de intercambio iónico, se obtuvo una preparación parcialmente pura con 79% de lacasa y una actividad específica de 313 U/mg.
Palabras Clave: lacasas fúngicas, producción de enzima, hongos de la pudrición blanca.
Introducción
Lacasas
La lacasa (EC 1.10.3.2, p-difenol:dioxígeno oxidorreductasa) es una enzima que cataliza la oxidación de sustratos utilizando al oxígeno molecular como aceptor de electrones. Esta enzima debe su nombre a que fue primeramente aislada del árbol de laca, Rhus vernicifera (Yoshida, 1883). La presencia de lacasa en otras plantas superiores es escasa. También se ha aislado de algunas bacterias, pero principalmente se encuentra en hongos (Valderrama et al., 2003).
La lacasa fúngica típica es una proteína de aproximadamente 60-70 kDa con un punto isoeléctrico ácido de alrededor de pH 4.0, y con un óptimo de actividad entre 50°C y 70°C (Baldrian, 2006). Es una glicoproteína cuya glicosilación es responsable de la estabilidad estructural de la enzima (Vite-Vallejo etal., 2009). También se ha encontrado que protege a la enzima de la proteólisis y la inactivación por radicales libres (Morozova et al., 2007).
La lacasa es una enzima comúnmente monomérica que normalmente contiene 4 átomos de cobre unidos a 3 sitios redox, clasificados de acuerdo a sus características espectroscópicas (Battistuzzi et al., 2005): El sitio tipo 1 (T1) es mononuclear y le confiere el color azul a la enzima en solución y se caracteriza por una banda de absorción a 600 nm (ε? 5000 M-1 cm-1) (Morozova et al., 2007). El sitio tipo 2 (T2) también es mononuclear y presenta una geometría metálica trigonal y propiedades de resonancia paramagnética nuclear comparables con los complejos tetragonales de Cu(II). Finalmente, el sitio tipo 3 (T3) es dinuclear y presenta un estado basal diamagnético que se origina por el acoplamiento antiferromagnético fuerte entre los dos iones Cu(II), conectados por un ión hidroxilo. En el sitio T1 el sustrato interactúa con la enzima y se lleva a cabo la sustracción de un electrón, mientras que en el sitio T2/T3 se lleva a cabo la reducción del oxígeno a agua.
]]> El potencial redox de la lacasa depende del organismo de origen, variando entre 0.5 y 0.8 V (Riva, 2006). Se ha propuesto que la identidad del ligando axial que coordina al cobre del sitio T1 afecta el potencial redox de la enzima (Morozova et al., 2007). Con base en la estructura cristalográfica de la lacasa de Trametes versicolor, Piontek et al. (2002) han sugerido que la longitud del enlace entre una de las histidinas que coordinan al cobre del sitio T1 modula el potencial redox.En la Figura 1 se muestra un esquema del ciclo catalítico de la lacasa, la cual actúa por un mecanismo tipo ping-pong que inicia cuando el cobre del sitio T1 oxida al sustrato, preferencialmente fenoles y anilinas, y se genera un radical libre (Petersen y Degn, 1978). El electrón extraído es transferido a través de un motivo tripéptido His-Cys-His, conservado en las lacasas. El electrón llega al sitio T2/T3 donde el oxígeno molecular es reducido a agua (Baldrian, 2006). El resultado global de este proceso es la reducción de una molécula de oxígeno a 2 moléculas de agua y la oxidación de 4 moléculas de sustrato para producir 4 radicales libres (Riva, 2006). Aunque la lacasa cataliza la oxidación de una gran variedad de compuestos, su catálisis está limitada por el bajo potencial redox de esta enzima, comparado con el de las peroxidasas (d'Acunzo et al., 2002).
Usos y potencial industrial de las lacasas
La baja especificidad de la lacasa es una característica que ha sido explotada en una gran variedad de procesos industriales. La función natural de la lacasa, la degradación de lignina, ha sido utilizada principalmente por la industria de la producción de papel. En 1997 Novo Nordisk patentó el sistema Lignozym® que utiliza un sistema lacasa-mediador para disminuir el contenido de lignina y aumentar la brillantez del papel (Call y Mücke, 1997). Este mismo sistema ha sido aplicado en la industria alimentaria para la clarificación de jugos, cervezas y vinos (Rodríguez-Couto y Toca-Herrera, 2006). La lacasa tiene un potencial importante en procesos de biorremediación debido a su eficiencia en la transformación de contaminantes como hidrocarburos poliaromáticos, plaguicidas, explosivos, disruptores endócrinos, bifenilos policlorados y colorantes sintéticos, entre otros (Pointing, 2001). Por su capacidad de transformar gran variedad de colorantes industriales, se ha sugerido su uso tanto para el saneamiento de efluentes de plantas industriales como para el tratamiento de fibras textiles (Rodríguez et al., 1999; Robinson y Nigam, 2008.). En 1996 Novozyme patentó un producto basado en la lacasa llamado DeniLite® y en la actualidad es utilizado ampliamente en la producción de mezclilla (Rodríguez-Couto y Toca-Herrera, 2006). La industria cosmética también ha aprovechado la capacidad de decoloración de esta enzima para sustituir al H2O2 en los tintes para el cabello (Yoshino et al., 2001), e incluso es utilizada en formulaciones para el aclarado de la piel (Rodríguez-Couto y Toca- Herrera, 2006). En la industria farmacéutica puede ser utilizada para la síntesis de antibióticos, como cefalosporinas, y nuevas variedades de penicilinas, así como para llevar a cabo reacciones de acoplamiento de compuestos fenólicos y para la producción de polímeros biológicamente activos (Witayakran y Ragauskas, 2009). Al generar un flujo de electrones durante la catálisis, la lacasa se ha utilizado para la fabricación de biosensores. Por ejemplo, para la detección de compuestos fenólicos en el vino (Fernandes y Rebelo, 2009), determinar la presencia de morfina y codeína, de algunos tipos de flavonoides, e incluso de algunos neurotransmisores (Rodríguez-Couto y Toca-Herrera, 2006). Esta misma característica se ha explotado para la producción de celdas de combustible como una fuente de energía limpia (Szot et al., 2009).
Una ventaja más de la lacasa es que sus aplicaciones pueden ampliarse a través del uso de mediadores, por lo que el diseño de nuevos compuestos que sean mediadores eficientes y no tóxicos es de suma importancia (Torres-Duarte et al., 2009). Por ejemplo, en la transformación de hidrocarburos aromáticos policíclicos la actividad mejoró significativamente en presencia de mediadores (Vandertol-Vanier et al., 2002; Pickard et al., 1999a). Por otro lado, las técnicas de inmovilización deben ser mejoradas con el fin de lograr que la enzima sea reusable y estable por largos tiempos y así facilitar su aplicación tanto en procesos a gran escala como en sistemas nanométricos.
Lacasa de Coriolopsis gallica
En cuanto a la producción de lacasa por el basidiomiceto Coriolopsis gallica, se encuentran pocas referencias en la literatura. Calvo y colaboradores (Calvo et al., 1998) reportaron la producción de lacasa por Coriolopsis gallica; la enzima resultó interesante por su capacidad de transformar diferentes colorantes industriales. La proteína se caracterizó bajo condiciones desnaturalizantes y se determinó un peso de 84.1 kDa. Se identificaron 4 isoenzimas con puntos isoeléctricos de 4.15, 4.20 y 4.27 (dos de ellas tienen el mismo p1). Su actividad máxima se obtuvo a pH 3, ya una temperatura de 70°C, con actividad estable a 28°C. Su vida media fue de 32 días a 37°C y 8 días a 60°C.
Por otro lado, la lacasa proveniente de la cepa de Coriolopsis gallica UAMH 8260 del herbario de la Universidad de Alberta en Canadá (University of Alberta Microfungus Collection and Herbarium) presentó una sola isoenzima con un p/de 3.4, un peso molecular de 66 kDa determinado por SDS-PAGE, y de 56.6 kDa determinado por MALDI-TOF, un contenido de carbohidratos de 21% (w/w, equivalentes de glucosa), y 3.3 átomos de cobre por molécula de lacasa (Vandertol-Vanier et al., 2002). Aunque el potencial redox de esta lacasa no se ha determinado, de acuerdo a la secuencia de aminoácidos reportada (PDB 2vds) , esta lacasa comparte los motivos conservados de las secuencias de las lacasas de alto potencial redox (Morozova et al., 2007). En la Figura 2 se muestra un diagrama del sitio catalítico de esta lacasa. Se puede observar que contiene el motivo His-Cys-His conservado a través del cual pasan los electrones extraídos por el cobre T1 hacia el sitio T2/T3. Además, esta lacasa contiene los 4 átomos de cobre coordinados por histidinas.
]]> Por lo anterior, queda de manifiesto la importancia de la lacasa en la nueva química "verde"; con el fin de desarrollar aplicaciones comerciales, su producción a gran escala es imperativa. En este trabajo presentamos la experiencia del Instituto de Biotecnología de la Universidad Nacional Autónoma de México en la producción a escala piloto de lacasa de Coriolopsis gallica.
Materiales y métodos
Cepa y reactivos
La cepa de Coriolopsis gallica UAMH 8260 fue obtenida de la de la Colección de Microhongos y herbario de la Universidad de Alberta. Para su mantenimiento, la cepa fue crecida a 28°C por 7 días en cajas Petri con medio de papa-dextrosa-agar (PDA). Posteriormente se conservó a 4°C.
La siringaldazina y la glucosa fueron obtenidas de Sigma-Aldrich. El extracto de levadura, el extracto de malta y el medio PDA fueron adquiridos de Difco. Las sales fueron compradas a J. T. Baker. Como sustrato orgánico para la fermentación piloto se usó Bran Flakes comerciales (Kellogg's, Queretaro) triturados en mortero.
Cultivos
Los preinóculos crecieron en matraces Erlenmeyer de 250 ml conteniendo 100 mL de medio GMY modificado como describe Mester et al. (1996). Este medio soporta excelente crecimiento pero relativamente bajos niveles de producción enzimática (Pickard et al. 1999b) y contiene por litro: 10 g de glucosa, 3.5 g extracto de malta, 2 g extracto de levadura, 2 g fosfato de potasio, 0.5 g sulfato de magnesio, 0.1 g bacto peptona, 1 mL de solución de minerales (0.5 mg sulfato de cobre, 0.16 mg sulfato de manganeso, 0.14 mg de sulfato de zinc, 0.29 mg de cloruro de cobalto en 1 litro). El medio se ajusta a un pH de 4.5. Los matraces fueron inoculados con 1cm2 de micelio de las cajas Petri previamente homogenizados con un homogenizador (Sorvall, Norwalk, Conn) por 10 segundos. Los matraces se colocaron en agitación orbital a 150 rpm a 29°C.
Los inóculos para el fermentador se prepararon en matraces Fernbach de 3 litros conteniendo 1 litro de medio GMY. Se usaron 4 matraces para inocular el fermentador de 100 litros.
]]>Fermentación Piloto
Se utilizó un fermentador enchaquetado de 40 cm de diámetro y 106 cm de altura. El fermentador está equipado con un motor de un caballo de fuerza, un impulsor de 19 cm de diámetro tipo Rushton y difusor de dona. El fermentador piloto, localizado en la planta piloto del Instituto de Biotecnología de la UNAM en Cuernavaca, fue preparado con 100 litros del medio Bran Flakes (Pickard et al., 1999b) que consiste en 3% de Bran Flakes en un amortiguador de 60 mM de fosfatos de sodio, pH 6.0 enriquecido con 0.8 mM de CuSO4 (Tinoco et al., 2010). Este medio ha sido reportado como inductor de producción de altas concentraciones de lacasa (Pickard et al 1999b; Tinoco et al., 2001). La fermentación se detuvo al séptimo día y se recuperó el caldo de cultivo para su posterior tratamiento.
Actividad enzimática
La actividad de la lacasa se evaluó a lo largo de la fermentación y en los diferentes pasos de purificación, utilizando como sustrato 50 hM de siringalazina (4-hidroxi-3,5-dimetoxibenzaldehidazina) en un amortiguador de acetatos 100 mM, pH 4.5 (Tinoco et al., 2001). La actividad fue monitoreada a una longitud de onda de 530 nm y estimada con un coeficiente de extinción de 64 000M-1 cm-1. Una unidad de actividad (U) fue definida como la cantidad de enzima que cataliza la transformación de 1 nmol de sustrato en un minuto. El contenido de proteína en las preparaciones de lacasa fue determinado con el método de Bradford (1976) usando el reactivo de Bio-Rad y la albúmina de suero bovino (BSA) como estándar.
Purificación de la enzima
El caldo de cultivo (100 litros) se centrifugó en una centrífuga tubular marca Sharples Modelo AS-16 a 15 000 RPM (13 200 g). Posteriormente, el sobrenadante se concentró por ultrafiltración en un equipo de fibra hueca de 20 litros marca Amicon Modelo DC 10 L. La primera filtración se realizó en un cartucho de fibra hueca (H5 MP-43) con un corte de 0.1 Hm. La segunda filtración y concentración se realizó con un cartucho (H10 P10-20) con un corte de 10 000 Da, obteniéndose un volumen de 3.8 litros.
La solución enzimática concentrada se sometió a un fraccionamiento por precipitación con sulfato de amonio. La primera precipitación se llevó a cabo con 50% de saturación a 4°C. El precipitado se desechó y el sobrenadante se llevó al 100% de saturación de sulfato de amonio. El precipitado de esta segunda fracción se redisolvió en 900 mL de amortiguador 60 mM de fosfato de sodio, pH 6.0. La solución enzimática se dividió en volúmenes de 100 mL y dializó en una membrana de 12 000 Da contra 4 L de un amortiguador 10 mM de fosfatos, pH 6.0, a 4°C. El solvente de diálisis se cambió dos veces.
]]> La solución se sometió a una cromatografía de intercambio aniónico débil sobre DEAE-celulosa (dietilaminoetilcelulosa) de Sigma-Aldrich Co, eluyendo con un gradiente de NaCl de 0 a 1 M en un amortiguador 10 mM de fosfatos pH 6.0. Las fracciones que presentaron actividad fueron colectadas y concentradas en una celda de ultrafiltración con una membrana de 10 000 Da de corte. Finalmente, la solución se sometió a una cromatografía de intercambio aniónico fuerte utilizando resina High Q (Bio-Rad laboratorios) y eluyendo con un gradiente de NaCl de 0 a 1 M en un amortiguador 10 mM de fosfatos pH 6.0.
Resultados y discusión
Las lacasas fúngicas son excretadas al medio por los hongos filamentosos (Bollag y Leonowicz, 1984). Las más altas producciones de lacasa son alcanzadas por los cultivos de hongos de pudrición blanca o ligninolíticos (Leonowicz et al., 1997), que son los microorganismos más eficientes para transformar la lignina en CO2 y agua. Por su importancia y potencial industrial, la producción de lacasas a gran escala es un desafío de actualidad. Las diferentes morfologías del crecimiento de los hongos filamentosos afectan la reología del caldo de fermentación, afectando por ende la productividad del biorreactor. Los efectos de la reología del caldo sobre la biomasa, momentum y transferencia de calor en un biorrecator han sido ampliamente estudiados (Charles, 1985; Moo-Young et al., 1987). La gran mayoría de los procesos de fermentación de hongos filamentosos en la industria son cultivos sumergidos.
Los fermentadores aireados más empleados en la industria son de tipo tanque agitado, representando el 93% (en valor del producto) de toda la producción biotecnológica (Li et al., 2009). En la configuración mayormente empleada en los reactores tipo tanque agitado mecánicamente la altura del líquido normalmente iguala el diámetro del tanque y la agitación se suministra por una turbina de disco de 6 hojas, tipo Rushton, con un diámetro de 1/3 el diámetro del tanque (dt). La distancia entre la turbina y la base del tanque por lo general es igual a un diámetro del impulsor. Estos fermentadores cuentan además con cuatro o más deflectores igualmente espaciados, con un ancho igual a dt/12, para prevenir la formación de vórtices. La dispersión del gas (aire u oxígeno) se realiza a través de un distribuidor de gas (sparger), situado debajo del impulsor, en el eje de la vasija. Este distribuidor en ocasiones se reduce a una simple tobera, aunque en otros casos se usan dispositivos más o menos complejos. El uso de la turbina tipo disco evita que se produzca la canalización del gas por el eje del impulsor y ayuda a lograr una correcta dispersión del gas en el líquido. Finalmente, los fermentadores están equipados con sondas para medir pH, oxígeno disuelto, espuma, temperatura y potencial redox.
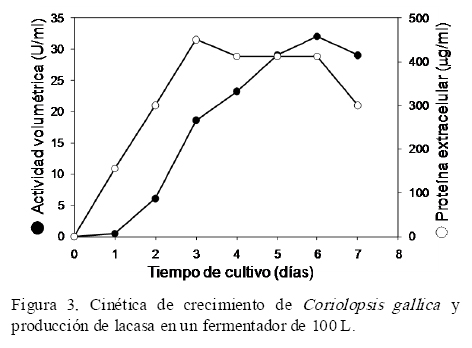
El medio económico y simple de 3% Bran Flakes (Pickard et al., 1999b) que demostró inducir la actividad lacasa, fue enriquecido con 0.8 mM de sulfato de cobre. La presencia de sulfato de cobre en el medio de cultivo demostró inducir significativamente la producción de lacasa en Pleurotus ostreatus (Tinoco et al., 2010). En la Figura 3 se muestra la cinética de crecimiento de Coriolopsis gallica UAMH 8260 medida en términos de la proteína extracelular, así como la cinética de producción de la lacasa. En el medio de Bran Flakes la proteína extracelular aumentó constantemente hasta el tercer día, alcanzando un valor de 450 mg/mL. Simultáneamente, la actividad lacasa aumentó de forma asociada al crecimiento, alcanzando un valor máximo de 32 U/mL al sexto día de cultivo (Figura 3).

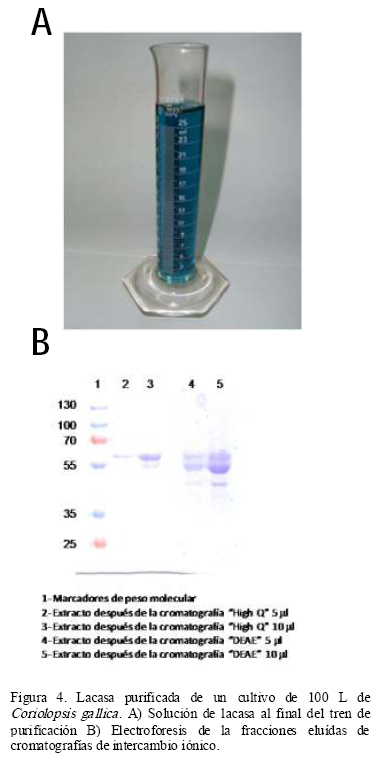
El proceso de purificación montado es sencillo, rápido y eficiente. En estas condiciones de cultivo la enzima se produce con buena pureza y solamente un fraccionamiento con sulfato de amonio y dos cromatografías de intercambio iónico fueron suficientes para purificar 3.23 veces a la enzima (Tabla 1). Excepto la ultrafiltración, las demás etapas de purificación tuvieron porcentajes de recuperación de al menos 70%, lo que se encuentra dentro de valores aceptables en procesos a escala comercial. En la ultrafiltración encontramos una pérdida de actividad del 55% principalmente por actividad asociada a partículas de gran tamaño (>100 000 Da). La pureza de la preparación al final del tren de purificación puede ser claramente observada por el intenso color azul de la solución debido al cobre del sitio T1 (Figura 4A) y verificada electroforéticamente (Figura 4B). Para esta preparación se determinó un grado de pureza de 79% por densitometría en un gel electroforético.
]]>
Datos sobre eficiencias en la purificación a nivel piloto en la literatura son inexistentes, sin embargo existen datos de purificaciones a nivel laboratorio que nos sirven de comparación. La purificación de la lacasa del hongo silvestre comestible Tricholoma mongolicum consistente en cromatografías de intercambio iónico DEAE-celulosa, CM-celulosa, Q-Sepharosa, y filtración en gel FPLC sobre Superdex 75, se obtuvieron rendimientos del 15% con actividades específicas de 1480 U/mg (Li et al., 2010). Por otro lado, con el uso de filtración, ultrafiltración y precipitación con acetona, la laccasa de Cerrena unicolor fue purificada con eficiencias del 73% (Bryjak y Rekuc, 2010). Garcia y col. (2007) purificaron la laccasa de Pycnoporus sanguineus usando dos etapas de cromatografía de interacción hidrofóbica en fenil-Sepharose obteniendo un rendimiento de solo 8.37%. La lacasa del hongo Pleurotus sajor-caju se purificó 10 veces por medio de una precipitación con sulfato de amonio y cromatografías DEAE-celulosa y Sephadex G-100 obteniéndose un rendimiento global del 53% (Murugesan et al., 2006). Finalmente, la lacasa extracellular de Panus tigrinus fue purificada por ultrafiltration, cromatografía de intercambio aniónico y filtración en gel hasta una preparación con 317 U/mg y un rendimiento del 66% (Quaratino et al., 2007).
De acuerdo con los datos en la Tabla 1, se produjeron 2 610 000 unidades de lacasa en siete días de cultivo. Considerando la actividad específica de la lacasa de C. gallica de 313 U/mg de proteína, se puede estimar que se produjeron aproximadamente 8 339 mg de lacasa por 100 L de cultivo de Coriolopsis gallica en 168 horas, lo que equivale a una productividad de 11.9 mg/L/día. La eficiencia global del tren de purificación fue del 24.16%, lo cual arroja un rendimiento para la enzima pura de 28.2 mg por litro de cultivo.
De acuerdo con la literatura, no existen ejemplos sobre la producción de lacasa a la escala que presenta este trabajo. Se ha observado que la producción de lacasa en biorreactores, que van hasta solo 20 L, puede variar entre 0.004 y 740 U/ml, de acuerdo a la especie y a las condiciones de cultivo (Rodríguez-Couto y Toca-Herrera, 2006). Los niveles más altos de producción de lacasa se han alcanzando en cultivos de Trametes pubescens, usando sales de cobre como inductor en cultivos de 20 L (Galhaup et al., 2002). Mientras que en cultivo en lote se obtuvieron 330 U/mL en 17 días de fermentación, el cultivo tipo lote alimentado con glucosa permitió incrementar la actividad de lacasa a 740 U/mL en 29 días, siempre y cuando se mantuviera un nivel bajo de glucosa para evitar la represión. Este nivel de producción equivale a una productividad de 24.13 mg/L/día.
La fuente de carbono utilizada en este trabajo no inhibe la producción de la lacasa, sino que la estimula de forma asociada al crecimiento, como se observa en la Figura 3. Algunas estrategias para mejorar el nivel de producción y por tanto la productividad consisten en el uso de inductores, tales como compuestos aromáticos o sales de cobre (Tinoco et al., 2010). Sin embargo, se ha observado que algunos de estos inductores pueden ser tóxicos y el efecto puede variar de manera importante entre especies, requiriéndose concentraciones altas en el medio de cultivo. Actualmente no existe en la literatura información sobre el efecto de inductores en la producción de lacasa de Coriolopsis gallica.
Una ventaja del cultivo con Coriolopsis gallica es que tiene un tiempo de fermentación corto, lo cual se traduce en una reducción tanto en los costos de operación como en el riesgo de contaminación. Por otro lado se ha comprobado que la lacasa de este hongo, en su forma purificada, presenta altas eficiencias catalíticas (kcat/KM) cuando se compara con lacasas de diversas cepas de Pleurotus ostreatus y Trametes versicolor (Tinoco et al., 2001).
Conclusiones
Los resultados de este trabajo muestran la factibilidad de producir y purificar una lacasa de interés industrial de forma rápida y eficiente. El medio de cultivo utilizado no contiene componentes tóxicos y la fermentación se lleva a cabo en una semana. El tren de purificación es simple y se obtiene un grado de pureza adecuado para las aplicaciones sugeridas de la enzima. Existe la posibilidad de mejorar el nivel de producción y por tanto la productividad a través de estrategias como el uso de inductores, aunque actualmente no existen investigaciones al respecto con Coriolopsis gallica.
]]> Agradecimientos
Se agradece al Biól. Mario Caro de la planta piloto del IBT por su apoyo técnico.
Literatura citada
Baldrian P., 2006. Fungal laccases: occurrence and properties. FEMS Microbiology Reviews 30:215-242. [ Links ]
Battistuzzi G., M. Bellei, A. Leonardi, R. Pierattelli, A. De Candia, A. Vila, M. Sola, 2005. Reduction thermodynamics of the T1 Cu site in plant and fungal laccases. Journal of Biological Inorganic Chemistry 10:867-873. [ Links ]
Bollag J.M., A. Leonowicz, 1984. Comparative studies of extracellular fungal laccases. Applied Environmental Microbiology 48:84954. [ Links ]
]]>Bradford M.M., 1976. A rapid and sensitive method for the quantitation of microgram quantities of protein utilizing the principle of protein-dye binding. Analytical Biochemistry 72:248-254. [ Links ]
Bryjak J., A. Rekuć, 2010. Effective purification of Cerrena unicolor laccase using microfiltration, ultrafiltration and acetone precipitation. Applied Biochemistry and Biotechnology 160:2219-2235. [ Links ]
Call H.P., I. Mücke, 1997. History, overview and applications of mediated lignolytic systems, especially laccase-mediator-systems (Lignozym®-process). Journal of Biotechnology 53: 163-202. [ Links ]
Calvo A.M., J.L. Copa-Patiño, O. Alonso, A.E. González, 1998. Studies of the production and characterization of laccase activity in the basidiomycete Coriolopsis gallica, an efficient decolorizer of alkaline effluents. Archives of Microbiology 171:31-36. [ Links ]
Charles M., 1985. Fermentation scale-up: problems and possibilities. Trends in Biotechnology 3:134-49. [ Links ]
]]>d'Acunzo F., C. Galli, B. Masci, 2002. Oxidation of phenols by laccase and laccase-mediator systems. European Journal of Biochemistry 269: 5330-5335. [ Links ]
Fernandes C.I.S., M.J.F. Rebelo, 2009. Polyphenolic biosensors. Application in red wines. Portugaliae Electrochimica Acta 27: 457-462. [ Links ]
Galhaup C., H. Wagner, B. Hinterstoisser, D. Haltrich, 2002. Increased production of laccase by the wood-degrading basidiomycete Trametes pubescens. Enzyme and Microbial Technology 30: 529536. [ Links ]
Garcia T.A., M.F. Santiago, C.J. Ulhoa, 2007. Studies on the Pycnoporus sanguineus CCT-4518 laccase purified by hydrophobic interaction chromatography. Applied Microbiology and Biotechnology 75:311-318. [ Links ]
Leonowicz A., L. Gianfreda, J. Rogalski, M. Jaszek, J. Luterek, M. Wojtas-Wasilewska, E. Malarczyk, A. Dawidowicz, M. Fink-Boots, G. Ginalska, N.-S. Cho, 1997. Purification of extracellular Cerrena unicolor laccase by means of affinity chromatography. Journal Korea Tappi 29:7-17. [ Links ]
]]>Li M., G. Zhang, H. Wang, T. Ng, 2010. Purification and characterization of a laccase from the edible wild mushroom Tricholoma mongolicum. Journal Microbiology and Biotechnology 20:1069-1076. [ Links ]
Li Q., L.M. Harvey, B. McNeil, 2009. Oxidative stress in industrial fungi. Critical Reviews in Biotechnology 29:199-213. [ Links ]
Mester, T., M. Pena, J.A. Field, 1996. Nutrient regulation of extracellular peroxidases in the white rot fungus Bjerkandera sp. Strain BOS55. Applied Microbiology and Biotechnology 44: 778-784. [ Links ]
Morozova O.V., G.P. Shumakovich, M.A. Gorbacheva, S.V. Shleev, A.I. Yaropolov, 2007. "Blue" laccases. Biochemistry 72: 1136-1150. [ Links ]
Moo-Young M., B. Halard, D.G. Allen, R. Burrell, Y. Kawase, 1987. Oxygen transfer to mycelial fermentation broths in an air-lift fermenter. Biotechnology and Bioengineering 30:746-53. [ Links ]
]]>Murugesan K., M. Arulmani, I.H. Nam, Y.M. Kim, Y.S. Chang, P.T. Kalaichelvan, 2006. Purification and characterization of laccase produced by a white rot fungus Pleurotus sajor-caju under submerged culture condition and its potential in decolorization of azo dyes. Applied Microbiology and Biotechnology 72: 939-946. [ Links ]
Pickard M.A., R. Roman, R. Tinoco, R. Vazquez-Duhalt, 1999a. Polycyclic aromatic hydrocarbon metabolism by white rot fungi and oxidation by Coriolopsis gallica UAMH 8260 laccase. Applied and Environmental Microbiology 65: 3805-3809. [ Links ]
Pickard, M.A., H.Vandertol, R. Roman, R. Vazquez-Duhalt, 1999b. High production of ligninolytic enzymes from white rot fungi in cereal bran liquid medium. Canadian Journal of Microbiology 45:627631. [ Links ]
Piontek K., M. Antorini, T. Choinowski, 2002. Crystal structure of a laccase from the fungus Trametes versicolor at 1.90-A resolution containing a full complement of coppers. Journal of Biological Chemistry 277: 37663-37669. [ Links ]
Pointing S.B., 2001. Feasibility of bioremediation by white-rot fungi. Applied Microbiology and Biotechnology 57: 20-33. [ Links ]
]]>Protein Data Bank: http://www.rcsb.org/pdb/explore.do?structureId=2VDS. Última fecha de acceso: Noviembre 20, 2008. [ Links ]
Quaratino D., F. Federici, M. Petruccioli, M. Fenice, A. D'Annibale, 2007. Production, purification and partial characterisation of a novel laccase from the white-rot fungus Panus tigrinus CBS 577.79. Antonie Van Leeuwenhoek 91:57-69. [ Links ]
Riva S., 2006. Laccases: blue enzymes for green chemistry. Trends in Biotechnology 24: 219-226. [ Links ]
Robinson T., S.P. Nigam, 2008. Remediation of textile dye waste water using a white-rot fungus Bjerkandera adusta through solid-state fermentation (SSF). Applied Biochemistry and Biotechnology 151:618-628. [ Links ]
Rodríguez E., M.A. Pickard, R. Vazquez-Duhalt, 1999. Industrial dye decolorization by laccases from ligninolytic fungi. Current Microbiology 38: 27-32. [ Links ]
]]>Rodríguez-Couto S., J.L. Toca-Herrera, 2006. Industrial and biotechnological applications of laccases: a review. Biotechnology Advances 24: 500-513. [ Links ]
Szot K., W. Nogala, J. Niedziolka-Jönsson, M. Jönsson-Niedziolka, F. Marken, J. Rogalski, C.N. Kirchner, G. Wittstock, M. Opallo, 2009. Hydrophilic carbon nanoparticle-laccase thin film electrode for mediator less dioxygen reduction: SECM activity mapping and application in zinc-dioxygen battery. Electrochimica Acta 54: 4620-4625. [ Links ]
Tinoco R., M.A. Pickard, R. Vazquez-Duhalt, 2001. Kinetic differences of purified laccases from six Pleurotus ostreatus strains. Letters of Applied Microbiology 32:331-335. [ Links ]
Tinoco R., A. Acevedo, E. Galindo, L. Serrano-Carreón, 2010. Increasing Pleurotus ostreatus laccase production by culture medium optimization and copper/lignin synergistic induction. Journal of the Industrial Microbiology and Biotechnology (en prensa) (DOI 10.1007/s10295-010-0797-3). [ Links ]
Torres-Duarte C., R. Roman, R. Tinoco, R. Vazquez-Duhalt, 2009. Halogenated pesticide transformation by a laccase-mediator system. Chemosphere 77: 687-692. [ Links ]
]]>Valderrama B., P. Oliver, A. Medrano-Soto, R. Vazquez-Duhalt, 2003. Evolutionary and structural diversity of fungal laccases. Antonie van Leeuwenhoek 84: 289-299. [ Links ]
Vandertol-Vanier H.A., R. Vazquez-Duhalt, R. Tinoco, M.A. Pickard, 2002. Enhanced activity by poly(ethylene glycol) modification of Coriolopsis gallica laccase. Journal of Industrial Microbiology and Biotechnology 29: 214-220. [ Links ]
Vite-Vallejo O., L.A. Palomares, E. Dantán-González, H.G. Ayala-Castro, C. Martínez-Anaya, B. Valderrama, J. Folch-Mallol, 2009. The role of N-glycosylation on the enzymatic activity of a Pycnoporus sanguineus laccase. Enzyme and Microbial Technology 45: 233239. [ Links ]
Witayakran S., A.J. Ragauskas, 2009. Synthetic applications of laccase in green chemistry. Advances in Synthetic Catalysis 351: 11871209. [ Links ]
Yoshida H., 1883. Chemistry of lacquer (Urishi) part 1. Journal of the Chemical Society 43:472-486. [ Links ]
]]>Yoshino T., A. Kimura, Y. Asai, 2001. Hair dye compositions. European Patent No. Ep1142563. [ Links ]
]]>