La mitosis y su regulación
Mitosis and its regulation
Alfredo de Jesús Rodríguez-Gómez,1 Sara Frias-Vázquez1,2
1 Laboratorio de Citogenética, Departamento de Investigación en Genética Humana, Instituto Nacional de Pediatría.
]]> 2 Departamento de Medicina Genómica y Toxicología Ambiental, Instituto de Investigaciones Biomédicas, UNAM.
Correspondencia
Dra. Sara Frias
Laboratorio de Citogenética
Instituto Nacional de Pediatría
Insurgentes Sur 3700-C, 6° piso
04530 México DF Teléfono y
fax: +52 55 10845533, 10840900, extensión 1436
sarafrias@biomedicas.unam.mx
Recibido: abril, 2013
Aceptado: septiembre, 2013
RESUMEN
La división celular por mitosis es decisiva para el desarrollo de los organismos y su reproducción; aunado a ello, es necesario que cada nueva célula sea genéticamente idéntica de la que proviene. En los eucariontes esto se logra gracias a mecanismos complejos que aseguran la integridad del material genómico y su segregación apropiada durante la mitosis. La visión tradicional de la mitosis la ha dividido en diferentes etapas que lograron caracterizarse gracias a los estudios morfológicos en células en división; los avances en biología molecular han llevado más allá esta caracterización, de manera que ahora se conoce toda una gama de participantes moleculares. En este artículo se abordarán el proceso de la mitosis celular y molecular y una breve síntesis de los actores moleculares que regulan este proceso.
Palabras clave: división celular, mitosis, ciclo celular.
ABSTRACT
Cell division by mitosis is essential for the development of organisms and their reproduction; it is also necessary that each new cell is genetically identical to that from which it comes. In eukaryotes this is achieved by the presence of complex mechanisms that ensure the integrity of genomic material and their proper segregation during mitosis. The traditional view of mitosis has been divided into different stages that were characterized by morphological studies in dividing cells; advances in molecular biology have led beyond this characterization, so that we now know a range of participant molecules. This article will discuss the process of mitosis, both at the cellular and molecular level and a brief summary of the molecular players that regulate this process.
]]> Key words: Division celular, Mitosis, Ciclo celular.
En los organismos pluricelulares, como el humano, que inician su vida con una célula huevo o cigoto, la división celular mitótica es decisiva para el desarrollo y mantenimiento de los diversos tejidos, órganos y sistemas que lo forman. Las nuevas células originadas por la mitosis son genéticamente idénticas a la célula madre; esto se logra gracias a mecanismos complejos de regulación que aseguran la integridad del material genómico y su segregación apropiada. La serie de eventos que conducen a la división de una célula se conoce como ciclo celular y está constituído por dos fases principales: la interfase y la division celular, que puede ser mitosis o meiosis. La mitosis es el proceso nuclear por el cual los cromosomas replicados se segregan en dos núcleos hijos, generalmente va acompañada de la citocinesis, que es la división del citoplasma y separación física de las dos células hijas.
El proceso mitótico fue descrito primeramente por Flemming, en 1882; su duración es generalmente de menos de una hora, tiempo en el que la célula es capaz de separar su información genética en dos grupos idénticos, que junto con el resto de sus componentes subcelulares serán heredados a las células hijas. Durante la mitosis, la célula se ocupa en una actividad principal, que es la segregación cromosómica y prácticamente detiene el metabolismo, la transcripción y la traducción.1
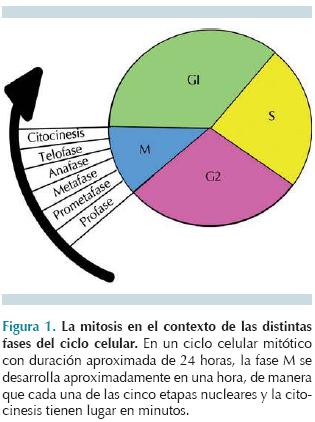
Antes del proceso de mitosis, durante la fase S del ciclo celular, los cromosomas se replican, de manera que en el momento de iniciar la división celular en humanos, cada uno de los 46 cromosomas replicados tendrá dos cromátidas unidas por el centrómero, cada una de ellas representa un cromosoma funcional. Cada cromátida hermana de un cromosoma segrega una célula hija, al igual que las otras 45, y juntas integrarán el "grupo" diploide de 46 cromosomas de la nueva célula. La mitosis se caracteriza por dos eventos importantes que pueden visualizarse bajo el microscopio de luz: la condensación y la segregación cromosómica. El movimiento cromosómico está mediado por una estructura compuesta primordialmente por microtúbulos: el huso mitótico, que se encarga de alinear a los cromosomas replicados y condensados en el centro de la célula, para así posicionar a las cromátidas hermanas con el cinetocoro de una, apuntando hacia un polo y el de la otra apuntando al polo opuesto; en ese momento se escinde la proteína que mantenía unidos los centrómeros y a las cromátidas hermanas. Aquí el huso mitótico mediante sus microtúbulos cinetocóricos jala las cromátidas hacia polos opuestos. El último paso es la reinstalación de un núcleo interfásico y la división del citoplasma para formar dos células hijas idénticas. Todos estos eventos se realizan en cinco etapas nucleares: profase, prometafase, metafase, anafase, telofase y finalmente se realiza la citocinesis que es la división del citoplasma.2 (Figura 1)

ETAPAS DE LA MITOSIS
Profase
]]> La transición de interfase a mitosis es la profase. En esta etapa ocurren los siguientes eventos: la cromatina se condensa para formar cromosomas, se forma el huso mitótico y desaparece la envoltura nuclear.1) Condensación cromosómica
La primera manifestación visible de la división celular es la compactación progresiva de la cromatina nuclear (Figura 2a), para dar lugar a hebras cromosómicas; en este punto los cromosomas se definen como hebras dobles porque ya están replicados; este empaquetamiento es indispensable para que los cromosomas no sufran alteraciones generadas por el estrés mecánico a que son sometidos debido a los movimientos del huso mitótico durante la segregación cromosómica.2
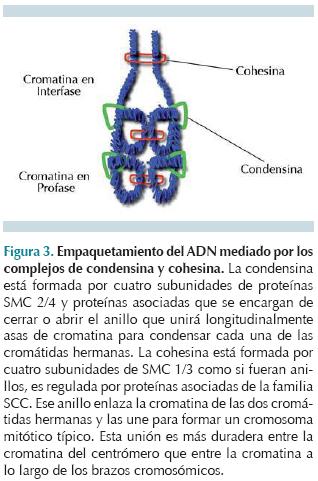
La cromatina que está en fibras de 30 nm en interfase comienza a condensarse por la intervención de un complejo proteico de condensina y de topoisomerasa II, que superenrollan la fibra de 30 nm formando asas de ADN superenrollado a lo largo de cada cromátida. Para mantener unidas a las cromátidas hermanas del cromosoma replicado y condensado, interviene otro complejo proteico llamado cohesina, que mantiene unidas a las dos cromátidas desde que terminaron su replicación en fase S hasta la anafase mitótica. La condensina y la cohesina son estructuras similares que pueden formar anillos que retienen segmentos distantes de cromatina unidos (Figura 3). La cohesina se encuentra a lo largo de los brazos cromosómicos, manteniendo unidas longitudinalmente a las cromátidas hermanas y dando la apariencia de una sola hebra al cromosoma mitótico temprano. También se encuentra uniendo fuertemente a las cromátidas por el centrómero; la cohesina localizada a lo largo de los brazos se separa de la cromatina en profase y la del centrómero se retiene hasta anafase.3
La cromatina extendida del núcleo en interfase permite el ingreso de la maquinaria transcripcional; pero durante la mitosis, cuando la cromatina tiene la mayor condensación del ciclo celular, la transcripción se inhibe. Debido a esto, el nucleolo -estructura formada primordialmente por productos de la transcripción del ADN ribosomal y proteínas, desaparece y, en consecuencia, también la traducción se detiene.
2) Formación del huso mitótico
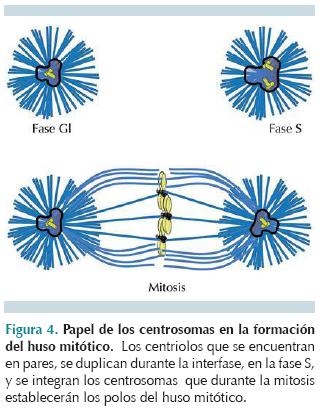
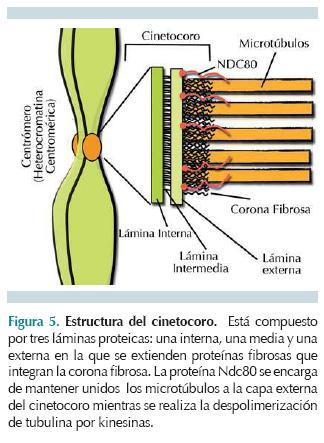
Los microtúbulos del citoesqueleto de interfase se desensamblan debido a modificación de proteínas asociadas con microtúbulos o MAPs; los microtúbulos se reorganizan para contribuir a la formación del huso mitótico. Esta nueva organización de los microtúbulos se inicia por la escisión de una estructura duplicada en fase S del ciclo celular llamada centrosoma; cada uno de los dos centrosomas consta de dos centriolos posicionados en ángulo recto uno del otro, rodeados por una matriz proteica. Durante la profase, el primer paso para formar el huso mitótico es la aparición o nucleación de microtúbulos alrededor de los centrosomas que forman una especie de estrella, integrando así los ásteres, cuyos microtúbulos tienen un extremo menos (-) asociado al centrosoma y un extremo más (+) al cual se adicionan dímeros de tubulina a mayor velocidad. Cada áster migra a posiciones opuestas dentro de la célula, estableciendo así los polos celulares a partir de donde se formará un huso mitótico bipolar (Figura 4). Los microtúbulos de los ásteres continúan creciendo por sus extremos + hasta que algunos de ellos, los llamados microtúbulos cinetocóricos, encuentran el cinetocoro de una de las dos cromátidas hermanas de un cromosoma, en donde quedan anclados a proteínas del cinetocoro, específicamente de la corona fibrosa con ayuda de otras proteínas, como Ndc80, CENP-E-kinesina y dineína (Figura 5). Los microtúbulos del polo opuesto harán contacto con la otra cromátida hermana del mismo cromosoma. Los microtúbulos que no encontraron un cinetocoro se llaman microtúbulos interpolares, continúan creciendo por su extremo + hasta que se encuentran y se superponen con los extremos + de los microtúbulos del polo contrario quedando así un huso mitótico funcional, con tres tipos de microtúbulos: los microtúbulos astrales, los microtúbulos cinetocóricos y los microtúbulos interpolares (Figura 6).4
]]>
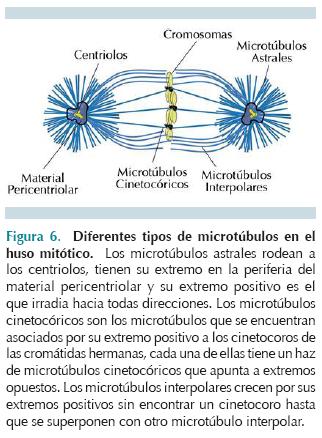
Existen dos tipos de mitosis: las dependientes y las independientes de centrosomas; en las segundas la nucleación de los microtúbulos se origina en los cinetocoros y es muy probable que aun en las células con centrosomas funcionales haya también nucleación de microtúbulos desde el cinetocoro de las cromátidas.5
3) Desaparición de la envoltura nuclear y fragmentación del aparato de Golgi
Para que los microtúbulos cinetocóricos interactúen con los cromosomas, la envoltura nuclear debe desaparecer; esto se realiza por fragmentación debido a la interacción del complejo ciclina B-Cdk1 con elementos de cada uno de los tres componentes de la envoltura: a) las membranas nucleares, b) los poros nucleares y c) la lámina nuclear.6 Es probable que los fragmentos resultantes en forma de vesículas se dispersen a través de la célula mitótica o, bien, que se integren a fragmentos de retículo endoplásmico. De manera similar, el aparato de Golgi se desintegra en pequeñas vesículas cuyo destino es similar al de la envoltura nuclear. En cualquiera de los dos casos, las vesículas independientes o bien asociadas al retículo endoplásmico, se segregarán a las células hijas y volverán a integrar sus estructuras originales dentro de ellas. El retículo endoplásmico podría no fragmentarse hasta vesículas y, simplemente, segregarse en fragmentos de éste hacia las dos células hijas. Otros componentes membranosos, como las mitocondrias, lisosomas y peroxisomas no se disgregan y, simplemente, se segregan de manera generalmente simétrica a las células hijas.7
Prometafase
Esta segunda fase se caracteriza por un movimiento activo que dirige a los cromosomas al ecuador celular. El inicio de la prometafase se reconoce por la interacción del huso mitótico con los cromosomas duplicados debido a la disolución de la envoltura nuclear, después de esto se inician los movimientos cromosómicos.8
]]> Los extremos + de los microtúbulos de los ásteres se mueven mediante polimerización hacia el centro de la célula buscando cromosomas en un movimiento que se piensa que es al azar y cuando hacen contacto con un cinetocoro se estabilizan; eventualmente, el cinetocoro de la otra cromátida, hermana del mismo cromosoma, se une también a un grupo de microtúbulos que provienen del polo opuesto. Se ha propuesto también que los cinetocoros no atrapados pueden iniciar, por sí mismos, una nucleación de microtúbulos. De una u otra manera los cromosomas llegan a tener sus dos cinetocoros conectados cada uno a microtúbulos que provienen de polos opuestos; en ese momento los microtúbulos jalan y empujan al cromosoma mediante polimerización-despolimerización de tubulina con la ayuda de proteínas motor tipo cinesinas y dineínas. Debido a que los dos polos atraen al mismo cromosoma a través de sus dos cinetocoros —que permanecen unidos por medio de la cohesina— se inicia un estado en el que se empiezan a equilibrar las fuerzas de tracción de cada polo, polimerizando más activamente el extremo + de los microtúbulos asociados al cinetocoro que se encuentra más cercano a su polo y acortando los microtúbulos asociados al polo más lejano (Figura 7). El acortamiento o elongación de los microtúbulos obedece a las diferencias en las fuerzas de tensión en los cinetocoros. Con estos movimientos se alcanza la congregación, que es la reunión de todos los cromosomas en el ecuador celular, posicionados ahí por el equilibrio de las fuerzas de tracción de los polos opuestos del huso. La congregación cromosómica marca el fin de la prometafase y el inicio de la metafase.4,8
Metafase
La condensación cromosómica iniciada en la profase continúa, por lo que los cromosomas metafásicos se observan con una cromatina perfectamente empaquetada que le permite al material genético mantener su integridad durante el estrés mecánico de los movimientos de anafase.2 En esta etapa es en la que generalmente se realizan los estudios cromosómicos, debido a que su morfología es muy clara.
Los cromosomas, movidos por el huso mitótico, se colocan en el centro, entre los dos ásteres y forman la llamada placa metafásica (Figura 2b) en la que los cromosomas se posicionan de tal manera que los cinetocoros de cada cromátida hermana están orientados hacia los polos opuestos.2 Mantener a los cromosomas en el ecuador celular implica un equilibrio entre las fuerzas de los microtúbulos que tienden a mover a los cinetocoros hacia los polos opuestos, de manera que posicionarlos en el centro implica una gran cantidad de energía. La energía de los movimientos cromosómicos proviene de la polimerización-despolimerización de los microtúbulos en los que se utiliza la conversión de GTP a GDP y de las proteínas motoras en las que se utiliza la conversión de ATP a ADP.4
En cada cinetocoro se pueden anclar entre 20-30 microtúbulos que ejercen fuerza de tracción hacia el polo del que provienen, por lo que la placa metafásica se mantiene por el equilibrio entre las fuerzas opuestas de los polos sobre los cromosomas, que mantienen juntas a sus cromátidas hermanas por la cohesina centromérica, de manera que cuando esta proteína se retira del centrómero, la metafase termina y se inicia la anafase con la migración de las cromátidas hermanas a polos opuestos.9,10
Anafase
Una vez que todos los cromosomas se encuentran en el ecuador formando la placa metafásica, los centrómeros, que mantenían unidas a las cromátidas hermanas, se escinden permitiendo que cada cromátida migre hacia el polo que estaba encarando, iniciándose así la anafase, que se divide en anafase A y anafase B. Los movimientos de la anafase A corren a cargo, principalmente, de los microtúbulos cinetocóricos que se acortan por despolimerización en ambos extremos de tubulina, con intervención de cinesinas (familia 13); esto permite jalar hacia los polos celulares a los cromosomas sencillos —a los que llamamos cromátidas hermanas cuando se encuentran unidas por el centrómero—, dividiendo el genoma replicado en dos grupos cromosómicos diploides, con 46 cromosomas sencillos cada uno. En la anafase B intervienen los microtúbulos interpolares que se encargan de alejar los dos grupos cromosómicos mediante un incremento en la longitud del huso mitótico (Figura 2c).2
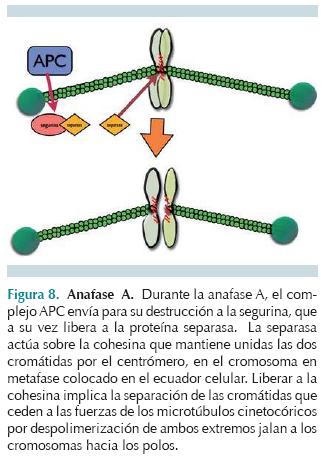
La anafase A se inicia cuando el complejo promotor de anafase (APC) unido a CDC20 induce la escisión del centrómero, dejando libres a las cromátidas hermanas para que cada una migre hacia polos opuestos. El mecanismo de acción de APC-CDC20 es ubiquitinizar una proteína llamada segurina,11,12 que la envía a destrucción por el proteasoma y con la destrucción de la segurina queda libre una proteína llamada separasa, que es una proteasa, que actúa sobre la cohesina, el complejo que mantiene unidas a las cromátidas hermanas. En el momento en que la cohesina se retira del centrómero existe un cambio de tensión sobre los cinetocoros, lo que activa una despolimerización de tubulina en ambos extremos + y - de los microtúbulos cinetocóricos; al acortarse, jalan a los cromosomas unidos a ellos hacia los centrosomas ubicados en los polos celulares (Figura 8).11,12,13 Durante la anafase B, los dos grupos de cromosomas ya colocados en los polos son alejados uno de otro por la intervención de los microtúbulos polares, que despolimerizan dímeros de tubulina en sus extremos - y polimerizan activamente en sus extremos + dirigidos al centro celular; estos microtubulos crecen tanto que los extremos se cruzan y continúan desarrollándose en direcciones opuestas. Gracias a la intervención de proteínas motoras asociadas con microtúbulos, los segmentos superpuestos de los microtúbulos polares comienzan un proceso de deslizamiento "en reversa" hacia los polos, que hace que el huso mitótico en total se haga muy largo y separe de esta manera a los dos grupos de cromosomas, que habían arribado a los polos en anafase A.2,12
]]>
Telofase
En la telofase, los microtúbulos cinetocóricos desaparecen y los cromosomas quedan libres en ambos extremos celulares. En ese momento, los cromosomas comienzan a descondensarse y la envoltura nuclear se reintegra. Durante la telofase tardía los cromosomas empiezan a transcribir y se restablece el nucleolo, marcando el término de la mitosis.2 (Figura 2d)
Citocinesis
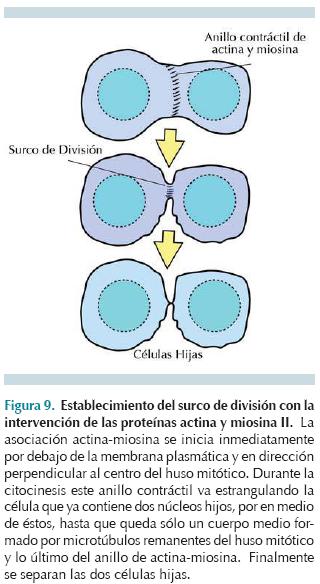
Es la última etapa de la división celular; en ella el citoplasma se divide para dar lugar a dos células hijas completamente independientes. Sin embargo, la citocinesis empieza desde la anafase, cuando se forma, inmediatamente por debajo de la membrana plasmática a nivel del ecuador celular, un cinturón de proteínas filamentosas, principalmente actina y miosina que se contraen y dan lugar a un surco de división. Éste se va haciendo progresivamente más profundo, hasta que la cintura que se forma llega a tocar los microtúbulos que aún quedan remanentes del huso mitótico; todo este conjunto de proteínas se conoce como cuerpo medio. Finalmente, la célula se estrangula y da lugar a dos células hijas (Figura 9).14
REGULACIÓN MOLECULAR DE LA MITOSIS
]]> El ciclo celular se regula gracias a un patrón de ciclinas y cinasas dependientes de ciclinas (CDKs)Para su estudio, el ciclo celular puede dividirse en dos etapas: la interfase, integrada por las fases G1, S y G2, y la fase M, durante la que sobrevienen la segregación cromosómica y la citocinesis. Para que una célula avance a lo largo de las fases del ciclo celular y, finalmente, pueda segregar su material genético, se requiere una regulación muy fina, que se caracteriza por la actividad de las CDKs (cinasas dependientes de ciclina), que actúan como cinasas de otras proteínas reguladoras del ciclo celular, y marcan de este modo la progresión de una fase del ciclo a otra. Estas cinasas alcanzan su forma activa en un complejo heterodimérico con una ciclina reguladora (Figura 10a). La expresión de las ciclinas es un factor limitante para la activación de las CDKs. En general, los niveles de ciclinas están determinados por control transcripcional y su proteólisis a través del sistema de ubicuitina-proteosoma.15,16 La expresión de la ciclina D1 es necesaria durante la fase G1 para estimular la entrada de las células al ciclo celular y sus concentraciones permanecen altas mientras haya agentes mitogénicos. La ciclina E se requiere en fase G1 después de la intervención de la ciclina D1 y alcanza su máxima expresión en la transición G1/S, lo que la vuelve necesaria para la entrada a la fase de síntesis. La ciclina A se requiere para el inicio de S y la transición de G2/M, mientras que la ciclina B regula la entrada y salida de mitosis (Figura 10b).15,16
El punto de control de G2 regula la entrada a mitosis
Después de la síntesis del ADN, y para reducir la acumulación de errores genéticos, las células monitorean que el ADN haya sido replicado correctamente, si detecta algún error, el ciclo celular se detiene, y si no detecta errores, la célula progresará hacia mitosis. Este punto de control se denomina G2 (o G2/M). Cuando en el ADN existe daño se activan las cinasas ATM (mutado en ataxia telangiectasia) y ATR (relacionado con ATM y Rad3). La primera detecta rompimientos de cadena doble en el ADN; mientras que la segunda, detecta rompimientos de cadena sencilla.17 Las cinasas ATM/ATR propagan la señal de alerta, apoyadas por las proteínas mediadoras del punto de control, que incluyen a MDC1 (mediador 1 del punto de revisión de daño al ADN; también conocido como NFBD1), 53BP1 (proteína 1 de unión a p53) y BRCA (proteína del cáncer de mama). Además, se requiere de las cinasas transductoras CHK1 y CHK2. 18-21 ATM/ATR fosforilan a la histona H2AX (γ-H2AX) y esto marca la región de la cromatina que flanquea cada rompimiento, a su vez la γ-H2AX permite el agrupamiento de las proteínas reparadoras en el sitio del daño. Los mediadores 53BP1, MDC1 y BRCA funcionan como un puente molecular entre la histona γ-H2AX y las proteínas del complejo reparador MRN (MRE11, RAD50, NBS1). El complejo MRN, ya en el sitio del daño, lleva a cabo la reparación del rompimiento de doble cadena de la hebra del ADN mediante recombinación homóloga.17,18Las células evitan que se llegue a la mitosis con daño cromosómico, de manera que mientras se efectúa la reparación del ADN, el punto de control de G2 bloquea la actividad del factor promotor de la mitosis (MPF), compuesto por la ciclina B y la CDK1. La actividad del MPF puede ser inhibida por la señalización a través de ATM/ATR, mediante dos actividades principales:
1. Las cinasas de la familia de p38 pueden inhibir a las fosfatasas CDC25; estas últimas activan al complejo MPF en el límite de las fases G2/M, por lo que al ser inhibidas no se entra a mitosis. 2. Las cinasas CHK1/CHK2 pueden activar a WEE1, que es un regulador negativo del complejo MPF, o bien activar secuencialmente a p53 y a GADD45, un secuestrador de ciclina B. De este modo, se evita que la ciclina B entre al núcleo y no se forma el complejo MPF.15,22
2.3. La transición G2/M (entrada a mitosis)
La progresión de la fase G2 hacia M se debe a la activación del complejo MPF, cuya actividad se mantiene de la profase hasta la metafase. El complejo MPF fosforila aproximadamente 70 sustratos mitóticos que actúan en la separación de los centrosomas, la fosforilación y activación de enzimas reguladoras de la condensación de la cromatina, fosforilación de la histona H1, ruptura de la envoltura nuclear y reorganización del citoesqueleto de microtúbulos y de actina para realizar la mitosis. 23,24 La actividad del complejo MPF se regula a dos niveles; el primero es transcripcional por la proteína p53, que mantiene la transcripción y, por lo tanto, la presencia de CDK1 estable durante todo el ciclo celular y la de ciclina B desde finales de la fase S. El segundo nivel de regulación de la actividad de MPF es por modificaciones postraduccionales, específicamente por fosforilación inhibitoria y activadora; en la fase G2 se realizan fosforilaciones inhibitorias sobre la CDK1 por las cinasas MYT y WEE1 y, posteriormente, la fosfatasa CDC25 libera la inhibición a CDK1;15,25 esto, junto con una fosforilación activadora sobre la misma CDK1, realizada por CAK (cinasa activadora de CDK, un heterodímero de ciclina H y CDK7), conduce a la célula a entrar a mitosis.
La actividad promotora de mitosis de CDK1 puede inhibirla directamente el gen supresor de tumor p21 (Cip1/Waf1). En relación con la ciclina B, se requiere una fosforilación para cambiar su localización subcelular de citoplasma a núcleo en las etapas tempranas de la mitosis. La salida de metafase se caracteriza por la caída crítica de las concentraciones de complejo MPF debido a su destrucción.15, 22
Cuando la célula ha pasado el punto de control de la fase G2, sus cromosomas duplicados inician el proceso de condensación, gracias a los complejos de condensina I y II, que funcionan empaquetando la cromatina del estado interfásico a cromosoma mitótico, para que pueda ser segregada apropiadamente entre las células hijas. 26-29 En el complejo condensina I se encuentran las proteínas SMC (Structural maintenance of chromosome) con actividad de ATPasa, como SMC2/CAP-E y SMC4/CAP-C, y proteínas no SMC, como CAP-G y CAP-H.30,31 El complejo condensina II consiste de las subunidades SMC2 y SMC4 y las proteínas hCAP-D3, hCAP- G2 y hCAP-H2. 32,33 Al parecer, el complejo I funciona en prometafase y el complejo II en profase temprana.31 Durante el empaquetamiento, las cromátidas hermanas permanecen unidas gracias a las cohesinas, que se cargan en los cromosomas en la fases G1 tardía/S temprana y se mantienen hasta que se alcanza la biorientación de las cromátidas en metafase.29 El proceso de condensación de los cromosomas y la entrada a mitosis pueden revertirse en presencia de estrés o condiciones no óptimas para la división celular, gracias a la activación de las proteínas del punto de control de antefase.29,32-38 Las proteínas involucradas en ese proceso comienzan apenas a ser descritas, pero CHFR (Checkpoint with FHA and RING domains) y la cinasa p38 ya se consideran parte esencial del proceso. CHFR es una ligasa de ubicuitinas que se acumula en respuesta a microtúbulos dañados y tiene entre sus blancos a proteínas importantes para la progresión mitótica, como Aurora A y PLK1, que son marcadas para su destrucción por medio del sistema ubicuitina-proteosoma; de este modo, se retrasa la progresión mitótica.35,36 Por otra parte, la cinasa p38, que se activa en caso de daño por radiación ultravioleta o alteración de la estructura de la cromatina evita la entrada a mitosis. Se ha especulado que el blanco inhibitorio del punto de control de la antefase es el complejo de condensina II. 29,34,37
]]> 2.4. El punto de control de metafaseEntre los puntos de control especializados en detener la progresión mitótica, el más estudiado y, quizá el principal, es el conocido como SAC (Spindle Assembly Checkpoint) o punto de control mitótico. El SAC se activa en cada ciclo celular inmediatamente después de la entrada a mitosis y funciona retrasando la entrada a anafase hasta que todos los cromosomas están correctamente anclados en la placa metafásica, biorientados y con tensión adecuada.38
Cuando el alineamiento de los cromosomas satisface al SAC se procede a la segregación de los cromosomas. Este proceso se inicia cuando el cofactor proteico CDC20 se une y activa al complejo promotor de la anafase/ciclosoma (APC/C), que tiene función de ligasa de ubicuitinas. Cuando el APC/C se activa, transfiere tres ubicuitinas a la ciclina B1 y a la proteína segurina, marcándolas de este modo para su degradación vía proteosoma 26S. La segurina es importante porque se encarga de mantener secuestrada a la proteasa separasa; cuando ésta es liberada, gracias a la degradación de la segurina, tiene lugar la degradación de la cohesina que mantiene unidas a la cromátidas hermanas. La degradación de la cohesina permite la segregación cromosómica, mientras que la degradación de la ciclina B1 tiene como resultado la inactivación de la CDK1; gracias a esto se consigue salir de mitosis. 38,39 Cuando el alineamiento de los cromosomas no satisface al SAC, la señal proveniente de cinetocoros no anclados induce el reclutamiento de proteínas del punto de control, como MAD2 (deficiente en la detención mitótica), BUB3 (gemación no inhibida por benzimidazol) y BUBR1 (relacionado con BUB). Esta señal conduce a la formación de dos complejos independientes, uno compuesto por BUB3/BUBR1 y el otro por C-MAD2/CDC20. La unión de estos dos complejos dará lugar al MCC (complejo mitótico de control), en el que ya ha quedado secuestrado CDC20, inhibiendo así la activación del complejo APC/C. De este modo, la segurina no será marcada para su degradación, la separasa no se liberará y los cromosomas no segregarán hasta que los requerimientos del SAC se satisfagan.39-41 A pesar del alto grado de especialización del SAC, éste no es capaz de reconocer las uniones erróneas entre el cinetocoro y los microtúbulos, conocidas como uniones merotélicas; sin embargo, estas últimas pueden repararse gracias a la actividad del complejo CPC (Chromosome Passenger Complex). El complejo CPC está formado por las proteínas SUR (survivina), BOR (borealina), INCENP (proteina centromérica) y AurB (aurora cinasa B) y hasta ahora es el mejor candidato para ser el complejo sensor de tensión de las uniones al cinetocoro. La actividad de AurB es primordial porque detecta y desestabiliza las uniones erróneas entre los microtúbulos y los cinetocoros, tales como uniones sintélicas y merotélicas, de este modo genera cinetocoros no anclados que son detectados por el SAC y se conduce a la detención de la mitosis. Al llegar a anafase, la AurB se desplaza de la región centromérica. Durante la prometafase, CDC20 y todas las proteínas del SAC se concentran en los cinetocoros, gracias al reclutamiento efectuado por las cinasas BUB1, MPS1 y AurB, pero se activan ante las señales de cinetocoros no anclados.38,40-42 Para el silenciamiento del SAC se han propuesto varios mecanismos. El primero consiste en retirar, por medio de la dineína, a las proteínas del SAC en los microtúbulos correctamente anclados; el segundo es el de silenciamiento, que ocurre cuando la proteína CENP-E se une a los microtúbulos e inhibe la actividad cinasa de BUBR1; el tercer proceso de silenciamiento es el mediado por la unión inhibitoria de p31-COMET a MAD2-CDC20 e, incluso, la degradación de los componentes del SAC por el sistema de ubicuitina-proteosoma mediada por el complejo APC/C.43,44-46
La progresión a través de mitosis no sólo está regulada por los puntos de control sino que también está íntimamente relacionada con la actividad del APC/C, que en la mitosis tardía se asocia con CDH1 y permanece activa a través de la fase G1 siguiente. APC/C-CDC20 degrada a la ciclina B y a la cohesina cuando todos los cromosomas han hecho contacto con el huso bipolar y se mueven a través de la placa metafásica, lo que conduce a la separación de las cromátidas hermanas. Por su parte, el complejo APC/CDH1 marca para degradación a las cinasas tipo polo 1 (PLK1), aurora A, survivina, NEK2, CDC20 y SKP2 durante la anafase y durante la fase G1 siguiente. Los niveles de CDH1 permanecen relativamente constantes durante todo el ciclo celular y su actividad es regulada sobre todo a través de las fosforilaciones dependientes del ciclo celular. La fosforilación de CDH1 por las CDKs durante S, G2 y M temprana inhibe su unión a APC/C, mientras que su desfosforilación en la fase M tardía permite su unión a APC/C y la activación del complejo15(Figura 8).
2.5. Regulación de la citocinesis
La citocinesis no debe ocurrir sino hasta que la separación de los cromosomas se ha completado. En general, se considera que la ejecución apropiada de la citocinesis recae en la organización estructural celular y no en moléculas difusibles; sin embargo, estudios recientes han encontrado que las deficiencias en la cinasa CHK1 pueden tener como consecuencia errores en la segregación cromosómica, regresión de la citocinesis y binucleación. Asimismo, esta deficiencia correlaciona con una localización errónea de las proteínas AurB y CHK1, que se acumulan en el surco de segmentación para facilitar la producción de dos células hijas. Esto pone de manifiesto que las proteínas que regulan los puntos de control del ciclo celular también pueden tener funciones importantes durante la segregación cromosómica y la citocinesis.47
2.6. Modificaciones covalentes de las histonas durante la mitosis
Las histonas son un grupo de proteínas conservadas que tienen un papel crítico en el empaquetamiento del ADN de las células eucariontes. Hay cuatro tipos de histonas nucleosomales, H2A, H2B, H3 y H4, y la histona H1, de unión al ADN espaciador. Las histonas poseen funciones regulatorias que se llevan a cabo gracias a las modificaciones covalentes de los residuos de aminoácidos de sus colas.48 Se han descrito muchos tipos de modificaciones en las histonas, que incluyen fosforilación, acetilación, metilación, ubicuitinación y sumoilación. Las diferentes combinaciones de modificaciones histónicas se han propuesto como un código que identifica diferentes estados funcionales de la cromatina; estos códigos poseen un papel relevante en la regulación epigenética de la expresión de los genes. Estas modificaciones también son relevantes para el proceso mitótico.48,49 La fosforilación de H3S10 (serina 10 de la histona 3) y H3S28 (serina 28 de la istona 3) se requiere para la condensación de los cromosomas y su segregación. La metilación de H3K9 (lisina 9 de la histona 3) promueve la formación de heterocromatina e inhibe la fosforilación de H3S10 y, viceversa, lo que indica una interacción entre estas dos modificaciones. La fosforilación de H3S10 evita la unión de la proteína HP1 (proteína formadora de heterocromatina) que se disocia de la cromatina durante la mitosis; cuando ocurre la desfosforilación de H3S10 la proteína HP1 puede unirse a cromatina. 49,50,51 Al parecer, la ubicuitinación de la histona H2A inhibe la actividad de la aurora A en etapas que no sean la mitosis, mientras que su desubicuitinación se requiere para que la H3S10 se fosforile y ocurra la segregación cromosómica. Durante la división celular, la acetilación y la metilación de histonas son eventos antagónicos, con disminución de la acetilación e incremento de la metilación durante el proceso.52
REFERENCIAS
]]>1. Salaün P, Rannou Y, Prigent C. Cdk1, PLKs, Auroras, and NEKs: the mitotic bodyguards. Adv Exp Med Biol 2008; 617: 41-56. [ Links ]
2. Walczak CE, Cai S y Khodjakov A. Mechanisms of chromosome behaviour during mitosis. Nat Rev Mol Cell Biol 2010; 11: 91-102. [ Links ]
3. Hirano T. At the heart of the chromosome: SMC proteins in action. Nat Rev Mol Cell Biol 2006; 7: 311-322. [ Links ]
4. Sharp DJ, Rogers GC, Scholey JM. Microtubule motors in mitosis. Nature 2000; 407: 41-47. [ Links ]
5. Oegema K, Hyman AA. Cell division (January19, 2006). WormBook, ed. The C. elegans Research Community, WormBook, doi/10.1895/ wormbook.1.72.1, http://www.wormbook.org. [ Links ]
]]>6. Güttinger S, Laurell E, Kutay U. Orchestrating nuclear envelope disassembly and reassembly during mitosis. Nat Rev Mol Cell Biol 2009; 10: 178-191. [ Links ]
7. Pecot MY, Malhotra V. Golgi membranes remain segregated from the endoplasmic reticulum during mitosis in mammalian cells. Cell 2004; 116:99-107. [ Links ]
8. Wittmann T, Hyman A, Desai A. The spindle: a dynamic assembly of microtubules and Motors. Nat Cell Biol 2001; 3:28-34. [ Links ]
9. Lampert F, Westermann S. A blueprint for kinetochores — new insights into the molecular mechanics of cell division Nat Rev Mol Cell Biol 2011; 12:407-412. [ Links ]
10. Akiyoshi B, Sarangapani KK, Powers AF, Nelson CR, Reichow SL, Arellano-Santoyo H, Gonen T, et al . Tension directly stabilizes reconstituted kinetochore-microtubule attachments Nature 2010; 468: 576-581. [ Links ]
]]>11. Acquaviva C, Pines J. The anaphase- promoting complex/cyclosome: APC/C. 2006. Journal of Cell Science 2006; 119: 2401-4. [ Links ]
12. Sullivan M, Morgan DO. Finishing mitosis, one step at a time. Nat Rev Mol Cell Biol 2007; 8: 894-903. [ Links ]
13. Pines J. Mitosis: a matter of getting rid of the right protein at the right time. Trends Cell Biol 2006; 16: 55-63. [ Links ]
14. Norden C, Mendoza M, Dobbelaere J. The NoCut Pathway Links Completion of Cytokinesis to Spindle Midzone Function to Prevent Chromosome Breakage. 2006 Cell 125: 85-98. [ Links ]
15. van den Heuvel, S. Cell-cycle regulation (September 21, 2005), WormBook, ed. The C. elegans Research Community, WormBook, doi/10.1895/wormbook.1.28.1, http://www.wormbook.org. [ Links ]
]]>16. Malumbres M, Barbacid M. Cell cycle, CDKs and cancer: a changing paradigm. Nat Rev Cancer 2009; 9: 153- 166. [ Links ]
17. Branzei D, Foiani M. Regulation of DNA repair throughout the cell cycle Nat Rev Mol Cell Biol 2008; 3: 297- 308. [ Links ]
18. Reinhardt HC, Yaffe MB. Kinases that control the cell cycle in response to DNA damage: Chk1, Chk2, and MK2. Curr Opin Cell Biol 2009; 21:245-255. [ Links ]
19. Kitagawa R, Bakkenist CJ, McKinnon PJ, Kastan MB. Phosphorylation of SMC1 is a critical downstream event in the ATM-NBS1-BRCA1 pathway. Genes Dev 2004; 18: 1423-38. [ Links ]
20. Shibata A, Barton A, Noon AT, Dahm K, Deckbar D, Goodarzi AA, Löbrich M, Jeggo PA. Role of ATM and the Damage Response Mediator Proteins 53BP1 and MDC1 in the Maintenance of G2/M Checkpoint Arrest. Mol Cell Biol 2010; 30: 3371-83. [ Links ]
]]>21. Stucki M, Jackson SP. MDC1/NFBD1: a key regulator of the DNA damage response in higher eukaryotes. DNA Repair (Amst) 2004; 3: 953-7. [ Links ]
22. Kastan MN, Bartek J. Cell-cycle checkpoints and cancer. Nature 2004; 432:316-23. [ Links ]
23. Nigg EA. Mitotic kinases as regulators of cell división and its checkpoints. Nat Rev Mol Cell Biol 2001; 2:21-32. [ Links ]
24. Löbrich M, Jeggo P. The impact of a negligent G2/M checkpoint on genomic instability and cancer induction Nat Rev Cancer 2007; 7: 861- 869. [ Links ]
25. Malumbres M, Barbacid M. Mammalian cyclin-dependent kinases. Trends Biochem. Sci., 2005; 30, 630-41. [ Links ]
]]>26. Belmont AS. Mitotic chromosome structure and condensation. Curr Opin Cell Biol 2006; 18:632-8. [ Links ]
27. Hirano T. Condensins: organizing and segregating the genome. Curr Biol 2005; 15:265-75. [ Links ]
28. Hirota T, Gerlich D, Koch B, Ellenberg J, Peters JM. Distinct functions of condensin I and II in mitotic chromosome assembly. J Cell Sci 2004;117:6435-45. [ Links ]
29. Chin FC, Yeong MF. Safeguarding entry into Mitosis: the Antephase Checkpoint. Mol Cell Biol 2010; 30: 22-32. [ Links ]
30. Hagstrom KA, Meyer BJ. Condensin and cohesin: more than chromosome compactor and glue. Nat Rev Genet 2003; 4:520-34. [ Links ]
]]>31. Hirano T. At the heart of the chromosome: SMC proteins in action Nat Rev Mol Cell Biol 2006; 7: 311- 322. [ Links ]
32. Ono T, Fang Y, Spector DL, Hirano T. Spatial and temporal regulation of condensins I and II in mitotic chromosome assembly in human cells. Mol Biol Cell 2004;15:3296-308. [ Links ]
33. Yeong FM, Hombauer H, Wendt KS, Mudrak I, Mechtler K, Loregger T, Marchler-Bauer A, Tanaka K, Peters JM, Ogris E. Identification of a subunit of a novel Kleisin-beta/SMC complex as a potential substrate of protein phosphatase 2A. Curr Biol 2003; 13: 2058-64. [ Links ]
34. Mikhailov A, Shinohara M, Rieder CL. The p38-mediated stress-activated checkpoint. A rapid response system for delaying progression through antephase and entry into mitosis. Cell Cycle 2005; 4:57-62. [ Links ]
35. Kang D, Chen J, Wong J, Fang G. The checkpoint protein CHFR is a ligase that ubiquitinates PLK1 and inhibits CDC2 at the G2 to M transition. J Cell Biol 2002;156:249-259. [ Links ]
]]>36. Kim JS, Park YY, Park SY, Cho H, Kang D, Cho H. The Auto-ubiquitylation of Chfr at G2 Phase Is Required for Accumulation of Plk1 and Mitotic Entry in Mammalian Cells. J Biol Chem 2011. [ Links ]
37. Mikhailov A, Shinohara M, Rieder CL. Topoisomerase II and histone deacetylase inhibitors delay the G2/M transition by triggering the p38 MAPK checkpoint pathway. J Cell Biol 2004;166:517-26. [ Links ]
38. Musacchio A, Salmon ED. The spindle-assembly checkpoint in space and time. Nat Rev Mol Cell Biol 2007; 8: 379-93. [ Links ]
39. Pines J, Rieder CL. Re-staging mitosis: a contemporary view of mitotic progression. Nat Cell Biol 2001; 3:3-6. [ Links ]
40. Pérez de Castro I, de Cárcer G, Malumbres M. A census of mitotic cancer genes: new insights into tumor cell biology and cancer therapy. Carcinogenesis 2007; 28:899-912. [ Links ]
]]>41. Ditchfield C, Johnson VL, Tighe A, Ellston R, Haworths C, Johnson T, Mortlock A, Keen A, Keen N, Taylor SS. Aurora B couples chromosome alignment with anaphase by targeting BubR1, Mad2, and Cenp-E to kinetochores. J Cell Biol 2003; 161:267-80. [ Links ]
42. Kops GJ, Weaver BA, Cleveland DW. On the road to cancer: aneuploidy and the mitotic checkpoint. Nat Rev Cancer 2005; 5:773-85. [ Links ]
43. Howell BJ, McEwen BF, Canman JC, Hoffman DB, Farrar EM, RIeder CL, Salmon ED. Cytoplasmic dynein/dynactin drives kinetochore protein transport to the spindle poles and has a role in mitotic spindle checkpoint inactivation. J Cell Biol 2001; 155: 1159-72. [ Links ]
44. Mao Y, Desai A, Cleveland DW. Microtubule capture by CENP-E silences BubR1-dependent mitotic checkpoint signaling. J Cell Biol 2005; 170:873-80. [ Links ]
45. Xia G, Luo X, Habu T, Rizo J, Matsumoto T, Yu H. Conformation-specific binding of p31(comet) antagonizes the function of Mad2 in the spindle checkpoint. EMBO J 2004; 23: 3133-43. [ Links ]
]]>46. Palframan WJ, Meehl JB, Jaspersen SL, Winey M, Murray AW. Anaphase inactivation of the spindle checkpoint. Science 2006; 313: 680-684. [ Links ]
47. Peddibhotla S, Rosen J. Checking and executing cell division to prevent genomic instability. Cell Cycle 2009 8:15, 2339-42. [ Links ]
48. Luger K, Richmond TJ. The histone tails of the nucleosome. Curr Opin Genet Dev 1998; 8:140-6. [ Links ]
49. Xu D, Bai J, Duan Q, Costa M, Dai W. Covalent modifications of histones during mitosis and meiosis. Cell Cycle 2009; 8:3688-94. [ Links ]
50. Eissenberg JC, Elgin SC. The HP1 protein family: getting a grip on chromatin. Curr Opin Genet Dev 2000; 10:204-10. [ Links ]
]]>51. Fischle W, Tseng BS, Dormann HL, Ueberheide BM, Garcia BA, Shabanowitz J, Hunt DF, Funabiki H, Allis CD. Regulation of HP1- chromatin binding by histone H3 methylation and phosphorylation. Nature 2005; 438:1116-22. [ Links ]
52. Joo HY, Zhai L, Yang C, Shuyi Nie, Erdjument-Bromage H, Tempst P, Chang C, Wang H. Regulation of cell cycle progression and gene expression by H2A deubiquitination. Nature 2007; 449:1068-72. [ Links ]
Nota
Este artículo debe citarse como
Rodríguez-Gómez AJ, Frias-Vázquez S. La mitosis y su regulación. Acta Pediat Mex 2014;35:55-68.