Los flavonoides y el Sistema Nervioso Central
Flavonoids and Central Nervous System
Rosa Estrada-Reyes,1 Denisse Ubaldo-Suárez,1 Ana Gabriela Araujo-Escalona1
1 Laboratorio de Fitofarmacología, Dirección de Neurociencias, Instituto Nacional de Psiquiatría Ramón de la Fuente Muñiz.
]]>Correspondencia:
MS. Rosa Estrada-Reyes. Laboratorio de Fitofarmacología, Dirección de Neurociencias,
Instituto Nacional de Psiquiatría Ramón de la Fuente Muñiz.
Calz. México-Xochimilco 101 . San Lorenzo Huipulco, Tlalpan,
14370 México, DF. Tel: (52) (55) 41 60-5080.
Fax: (52) (55) 5655-9980. E-mail: restrada@imp.edu.mx
SUMMARY
The aim of the present study was to show the most relevant aspects of the flavonoids such as their origin, sources, chemical structures, and metabolism in the body human. We offer a brief review about their antiallergic, anti-cancer, anti-inflammatory, and analgesic properties. This review shows their effects on CNS and evidences their pharmacologic potential in the therapeutics of the mental disorders.
]]> Flavonoids may have existed in nature for over 1 billion years and thus have interacted with evolving organisms. These compounds are molecules of low molecular mass, abundant in all berries and citric fruits, chocolate, nuts, red wine, and several medicinal plants. Flavonoids interact with several enzymes responsible for the transport of xenobiotics to the brain, which are considering modifiers of the biological response. Perhaps the most studied have been their anti-oxidant properties, which have met reflected in his capacity to protect to the cells of the oxidative stress, implicated several pathologies associated with aging, such as Alzheimer's and Parkinson's diseases.In the last 30 years, a intensive research about the effects of the flavonoids on CNS has been carried out; in this regard, flavonoids have showed effective effects as anxiolytic, antidepressants, and anticonvulsive drugs, and although their actions in the CNS occur through a variety of interactions with different receptors and signaling pathways, it has been demonstrated that these effects are mediated principally by GABA, in particular GABAA receptors, which these has led them to being postulates as a new benzodiazepines family, but without the side effects of these.
Key words: Flavonoids, CNS, GABAergic receptors, anxiety, depression, oxidative stress.
RESUMEN
El propósito de esta revisión fue describir los aspectos más relevantes de los flavonoides como su origen, sus fuentes y metabolismo, sus propiedades farmacológicas como antialérgicos, anticancerosos, anti-inflamatorios, analgésicos. También revisamos sus efectos sobre el SNC poniendo en evidencia su potencial farmacológico en la terapéutica de los trastornos mentales.
Los flavonoides son sustancias de bajo peso molecular que han estado presentes en la naturaleza durante millones de años. El hombre los consume en la dieta ya que están presentes de forma abundante en los vegetales, las frutas rojas como las fresas, zarzamoras, frutas cítricas, el chocolate, las nueces, el vino tinto y en varias plantas medicinales. Estos compuestos poseen una amplia gama de actividades farmacológicas entre las que destacan sus propiedades anti-oxidantes, las cuales les confieren capacidad de proteger a las células del estrés oxidativo relacionado con patologías asociadas al envejecimiento, como las enfermedades de Alzheimer y Parkinson.
En los últimos 30 años se ha realizado una intensa investigación sobre sus acciones en el SNC, entre las que sobresalen sus propiedades como ansiolíticos, sedantes, antidepresivos y anticonvulsivos. Se ha demostrado que estos efectos son mediados principalmente por los receptores GABA, en particular los receptores GABAA, por lo que los flavonoides han sido reconocidos como una nueva familia de benzodiazepinas, con la ventaja de no presentar los efectos colaterales que éstas producen.
Palabras clave: Flavonoides, SNC, receptors GABAérgicos, ansiedad, depresión, estrés oxidativo.
]]> ¿QUÉ SON LOS FLAVONOIDES?
Los flavonoides son sustancias de bajo peso molecular producidas por casi todas las plantas vasculares. Esta gran familia de compuestos ha estado presente en la naturaleza durante más de mil millones de años, de manera que han actuado recíprocamente con el desarrollo de muchos organismos. Los flavonoides cumplen un importante papel en la naturaleza que ha perdurado en las plantas vasculares a lo largo de la evolución. Esta asociación entre las plantas productoras de flavonoides y las diversas especies animales y otros organismos, puede explicar la gama extraordinaria de actividades bioquímicas y farmacológicas que estos productos ejercen en el hombre y otros mamíferos, como resultado de la coexistencia o coevolución de ambos reinos.
En las plantas, algunos flavonoides confieren resistencia contra la fotooxidación de la luz ultravioleta del sol, intervienen en el transporte de hormonas y algunos funcionan como defensa ante los depredadores. Desde el siglo pasado es bien conocida la relación que existe entre la presencia de flavonoides en las plantas y su resistencia a las infecciones fúngicas y virales. Otra de sus importantes funciones en muchas plantas es la atracción de los insectos polinizadores por medio del color o del olor que les confieren a éstas o a sus flores asegurando así su reproducción y conservación.1,2
El hombre los consume cotidianamente en la dieta ya que están presentes de forma abundante en los vegetales, las frutas rojas como las moras, fresas, zarzamoras (Vaccinium ssp.); frutas cítricas (Citrus ssp.), el chocolate (Theobroma cacao), las nueces, las bebidas derivadas de la uva (Vitis vinifera) como el vino tinto, los tés verde y negro (Camelia sinensis), así como en otros alimentos. También están presentes en plantas medicinales aromáticas pertenecientes a la familia Lamiaceae.
METABOLISMO DE LOS FLAVONOIDES
Se calcula que la ingesta diaria de flavonoides contenidos en la dieta es de uno a dos gramos por día, dependiendo principalmente de los hábitos dietéticos. En México no existe información acerca de las cantidades que se consumen.3
La mayor parte de los flavonoides (a excepción de las catequinas) está presente en las plantas y alimentos en forma de β-glicósidos. Aunque la más frecuente de las unidades de glicosidación es la glucosa también están presentes la glucoramnosa, la galactosa, la arabinosa y la ramnosa. Una vez que son ingeridos y antes de entrar a la circulación general, estos glicósidos pueden sufrir deglicosilación (hidrólisis) de la siguiente forma: debido a que la unión β de estos azucares resiste la hidrólisis de las enzimas pancreáticas, este proceso se lleva a cabo predominantemente en el lumen intestinal por la acción de dos enzimas: 1. la lactasa phloridzina hidrolasa (LPH), que se encuentra en la membrana de los enterocitos (cuando los flavonoides son hidrolizados por esta enzima atraviesan por difusión pasiva la membrana intestinal) y 2. la enzima β-glucocidasa citosólica no específica (CBG), que es capaz de hidrolizar una amplia gama de glicósidos incluyendo glucósidos, galactósidos, xilósidos, arabinósidos y fructósidos.4-6 Esta enzima está localizada intracelularmente en los enterocitos, por lo que se requiere del transporte activo de los glicósidos por medio del transportador de azúcar SGLT-1 dependiente de sodio.4
Por otra parte, los glicósidos que no son sustratos para la LPH o para el SGLT-1 son transportados hacia el colon donde son hidrolizados por las bacterias ahí presentes.7
Los flavonoides una vez hidrolizados (agliconas) se conjugan por metilación, sulfatación o glucuronidación principalmente y debido a que tienen una capacidad de conjugación alta su concentración en el plasma es por lo general baja.8 Estudios realizados con ratas mostraron la presencia de metabolitos conjugados en la sangre portal, lo cual apoya que la conjugación se inicia en los enterocitos antes que en el hígado.9,10
]]> Aunque numerosos estudios han descrito los efectos de diversos flavonoides en el SNC, es escasa la información de cómo permean la barrera hematoencefálica (BHE). Investigaciones recientes in vitro e in vivo indican que tanto los flavonoides hidrolizados (agliconas) como sus productos de conjugación son capaces de atravesar la BHE.11 Algunas investigaciones indican que flavonoides glicosidados como el 3-β-rutinósido de cianidina y el glucósido de pelargonina, así como las flavanonas (agliconas) hesperetina, naringenina y sus productos de conjugación atraviesan la BHE.12-14 Por lo que, al parecer, la capacidad de los flavonoides de permear la BHE no sólo depende de su lipofilicidad sino también de su capacidad de conjugación; metabolitos que son conjugados por metilación en el intestino delgado y en el hígado, al ser más lipofílicos, pueden permear la BHE con mayor facilidad que sus agliconas de origen. Por la misma razón se pensaría que los metabolitos más polares, por ejemplo los resultantes de conjugación por glucuronidación o los glicosilados, no podrían permear la BHE; existen investigaciones que sugieren que in vivo esta clase de glicósidos la atraviesan cuando se unen a transportadores específicos dependientes de ATP como la glicoproteína P (P-gp) expresada en la BHE. La P-gp pertenece al grupo de transportadores ABC (ATP-binding-casette) y están encargados de transportar compuestos estructuralmente diferentes así como sus derivados conjugados, además de regular la salida ("efflux") de estos compuestos de una manera activa y dependiente de ATP.14,15 Estudios recientes muestran que algunos flavonoides no sólo son transportados por la P-gp sino que interactúan con ésta moderando su actividad, por lo que los flavonoides han sido descritos como "modificadores de la respuesta biológica" por su capacidad de modular la reacción del cuerpo ante xenobióticos.9,16,17
CLASIFICACIÓN DE LOS FLAVONOIDES
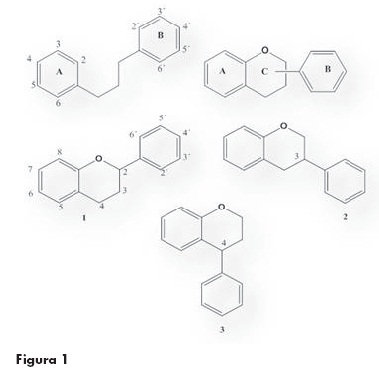
De forma coloquial se tiende a generalizar cuando se habla de "los flavonoides" y sus beneficios en la salud, sin embargo esta familia se caracteriza por su diversidad estructural de tal manera que se han identificado más de 6000 de estos metabolitos secundarios cuyas propiedades biológicas dependen en gran medida de su estructura particular, es decir del tipo de sustituyentes, grupos funcionales, grado de oxidación, formas diméricas, polimóricas, formas glicosidadas o libres, entre otras. El término flavonoide es generalmente utilizado para describir una amplia gama de productos naturales con un sistema C6-C3-C6 (anillos A, C y B) o más específicamente con una funcionalidad fenilbenzopirano, benzo-γ-pirona o cromano, consistente en un anillo fenólico y un anillo pirano y son clasificados de acuerdo a sus sustitución (figura 1).

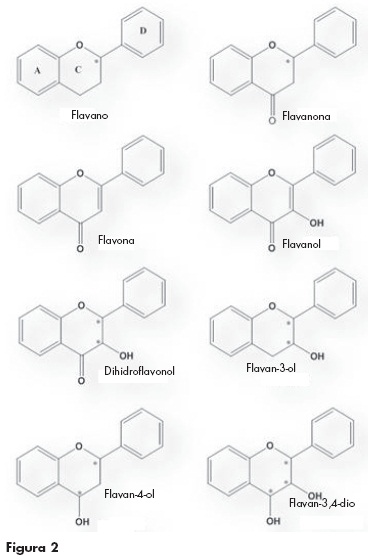
Los flavonoides se dividen inicialmente en tres clases, dependiendo del sitio de unión del anillo B con el benzopirano (A): los flavonoides 1 (2-fenilbenzopiranos), isoflavonoides 2 (3-benzopiranos) y los neoflavonoides 3 (4-benzopiranos). Los flavonoides 1 (2-fenilpiranos), a su vez, dependiendo del grado de oxidación y saturación presente en el heterociclo se dividen en los siguientes grupos: Los isoflavonoides (3-benzopiranos 2) son una clase distintiva de flavonoides, estos compuestos poseen un esqueleto, 3-fenilcromano que es derivado biogenéticamente de una migración 1,2-aril del precursor 2-fenilcromano. A pesar de su limitada distribución en el reino vegetal, los isoflavonoides son notablemente diversos en cuanto a sus variaciones estructurales, no sólo en el número y complejidad de los sustituyentes sobre el sistema básico, también en los diferentes niveles de oxidación y en la presencia de un heterociclo adicional (figura 2). Es así que los isoflavonoides se dividen en los siguientes grupos:
a) Los neoflavonoides (4-benzopiranos 3) que están estructural y biogenéticamente relacionados con los flavonoides, y b) los isoflavonoides, conformados por las 4-aril-coumarinas (4-aril-2fi-1-benzopiran-2-onas), las 3,4-dihi-dro-4-arilcoumarinas y el neoflavano.
EFECTOS FARMACOLÓGICOS DE LOS FLAVONOIDES
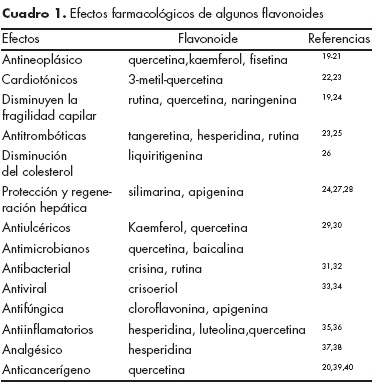
Esta variedad estructural está relacionada con las diversas actividades biológicas que poseen los flavonoides, de entre las cuales destaca, tal vez por ser una de las más estudiadas, sus propiedades antiinflamatorias. Desde 1948 se describieron las propiedades antiinflamatorias de la hesperidina, la naringenina y la nobiletina, presentes en la fracción soluble en agua de casi todas las especies de Citrus; a partir de entonces son muchos los estudios in vivo e in vitro que describen las propiedades antiinflamatorias de los flavonoides y sus mecanismos.18
Además de sus propiedades antiinflamatorias se ha descrito una variedad de efectos producidos por estos metabolitos. En el cuadro 1 se describen los más documentados, sin mencionar sus efectos sobre el SNC, los cuales se abordarán a continuación.
EFECTOS DE LOS FLAVONOIDES SOBRE EL SISTEMA NERVIOSO CENTRAL
Históricamente las acciones biológicas de los flavonoides se han atribuido a sus propiedades antioxidantes; debidas principalmente al potencial quelante que les confiere su estructura química, de tal manera que la actividad antioxidante puede deberse a sus capacidades reductoras per se o por influenciar el estado de oxidación/reducción (redox) intracelular. Este potencial antioxidante ha sido asociado con la reducción del riesgo de ciertas enfermedades crónicas, la prevención de algunas enfermedades cardiovasculares y de algunas clases de cáncer. Sin embargo, también se ha especulado que su clásica actividad antioxidante donadora de hidrógenos no puede explicar la bioactividad de los flavonoides en los sistemas vivos.
El estado de redox de la célula es el equilibrio entre los niveles fijos de especies reactivas de oxigeno (ERO) y especies reactivas de nitrógeno (ERN) con los sistemas celulares antioxidantes. Un indicador clave en este balance es la relación entre el sistema enzimático glutatión reducido (GSH) y el glutatión oxidado (GSSG), o mejor dicho el potencial redox de GSH. La reserva celular de GSH/GSSG es un sistema dinámico que lleva a cabo reacciones de oxidación y reducción con ERO y ERN, en sistemas antioxidantes y grupos tioles de algunas proteínas. Al parecer las células se hacen más oxidadas durante la progresión del ciclo de vida a partir del estado de proliferación (-230 a 260mV) hacia el ciclo de arresto y diferenciación (-200mV), hasta la apoptosis de la célula (-150mV). Considerando en conjunto estos datos el estrés oxidativo/nitrosativo es el cambio del estado de redox de una célula hacia la oxidación que causa daño a las funciones celulares y a las biomoléculas esenciales.
]]> Es en este contexto en el que los efectos antioxidantes de algunos flavonoides pueden ser importantes para ayudar a recuperar la homeostasis de óxido-reducción en las patologías degenerativas y los trastornos asociados al envejecimiento, como la enfermedad de Alzheimer, la demencia senil y las fallas en los procesos cognitivos como la memoria y el aprendizaje, que se caracterizan por presentar un alto estrés oxidativo celular. De estas investigaciones destacan las realizadas por Matsuzaki et al. (2006),41 quienes han descrito la participación de la nobiletina en los mecanismos relacionados con la memoria y el aprendizaje. En este estudio demostraron que la nobiletina posee un mecanismo único de acción neurotrófica, es decir favorece el desarrollo, crecimiento y funcionamiento neuronal, revirtió la pérdida de memoria inducida por la proteína β-amiloide y mejoró la memoria olfativa de ratas bulbectomizadas. Esto se logró gracias a que interactúa selectivamente con dos proteínas cinasas: la proteína cinasa activada por mitógeno (MAPK) (la cual está asociada al crecimiento celular) y por la proteína fijadora del elemento de reconocimiento del AMPc (CREB) (una proteína de transcripción génica) cuya activación favorece el crecimiento de nuevas conexiones sinápticas proporcionando un estado estable de la memoria a largo plazo.42 En 2007 este mismo equipo de investigación mostró que la nobiletina interactúa con el sistema glutamatérgico, en particular con los receptores AMPA, para ejercer sus efectos sobre la memoria.43,44Curiosamente la historia del descubrimiento de los efectos de los flavonoides sobre el Sistema Nervioso Central está ligada al descubrimiento de los receptores del ácido gama amino butírico (GABA), que condujo a la caracterización de dichos receptores y a una incesante búsqueda de las sustancias cerebrales endógenas que se unen a este receptor. Como parte de esta búsqueda se investigó también la presencia de moléculas afines a los receptores a GABA en alimentos de origen animal y vegetal, así como en plantas utilizadas en la etnomedicina de todo el mundo.45
Por otro lado, a partir de los años 1960 los fármacos ansiolíticos más utilizados en la práctica clínica han sido los de la familia de las benzodiacepinas (BDZ), utilizados también para el tratamiento de la epilepsia, el insomnio, ciertos estados depresivos, algunos estados afectivos, etcétera. Las benzodiazepinas ejercen su acción por su interacción con los receptores GABAérgicos tipo A. Estos receptores son proteínas transmembranales con un ensamble hetero-oligomérico ya que están constituidas por varias subunidades, que conforman un canal iónico permeable al ion cloruro (Cl-) y cuyo ligando es el ácido gama amino butírico (GABA). Cuando el GABA se une al receptor el canal iónico se abre permitiendo el flujo del ion cloruro el cual produce la hiperpolarización de la membrana de la neurona receptora y la inhibición de la transmisión de los impulsos nerviosos, produciendo efectos tranquilizantes, sedantes o ansiolíticos.
Estos efectos son atribuidos a la interacción selectiva de las subunidades que conforman al receptor con distintos ligandos que pueden hacer más eficiente la transmisión GABAérgica. En el SNC de los vertebrados se han identificado diferentes subunidades de los receptores GABAA como α1-α6, β1-β3 (más β4 en el cerebro del pollo), γ1-γ3 (más γ4 en el cerebro del pollo),δ, ε, ,Π p1-p3.46,47
Además de los receptores GABAA, el GABA activa a otros dos tipos de receptores: el GABAB que es conocido por estar acoplado a canales de Ca2+ o K+, los cuales activan sistemas de segundos mensajeros en la célula vía proteínas G; y los receptores GABAc, un subgrupo de los receptores GABAA en el cual predomina la subunidad p y están directamente asociados con los canales de cloruro.
El receptor GABA tiene un sitio de unión a las BDZ que está localizado en la interfase de la subunidad ( y la subunidad y, en los receptores GABAA. Las BDZ actúan aumentando la corriente de cloruro inducida por GABA. La presencia de las subunidades (α1 y γ2 es un requisito indispensable para que la unión funcional de BDZ sea completa y la modulación de la corriente de cloruro sea óptima. La diversidad de ligandos GABA/BDZ, la cual resulta de la existencia de las subunidades, ha sido implicada en las múltiples propiedades farmacológicas producidas por ligandos con escasa selectividad subtipo como el diazepam. Más aún, la heterogeneidad regional del complejo GABA/BDZ se ha sugerido como otra razón para la multiplicidad de propiedades farmacológicas de los ligandos a BDZ.
En 1983, el grupo argentino de Medina, Paladini y colaboradores realizaron investigaciones buscando los principios activos de plantas con propiedades sedantes. Realizaron estudios de unión a receptores a BDZ con la esperanza de encontrar principios activos con estructuras similares a las benzodiazepinas. Como resultado de este estudio aislaron y demostraron por primera vez que la flavona crisina y la apigenina aisladas de la pasiflora (Passiflora coerulea), de la manzanilla (matricaria rucutita) y el núcleo flavona en sí mismo, poseen propiedades ansiolíticas en modelos de conducta en ratones. En modelos in vitro estos metabolitos secundarios mostraron alta y mediana afinidad por el sitio de unión a BDZ. Estas flavonas presentaron además escasa actividad sedante y miorrelajante, lo cual representó la primera ventaja de estos metabolitos sobre las BDZ y mostró su potencial como fármacos para uso humano. Siguiendo la investigación de estos importantes hallazgos, Paladini y colaboradores hicieron modificaciones químicas de las flavonas ansiolíticas naturales y obtuvieron derivados con mejores propiedades, de los cuales la 6,3'-dinitroflavona mostró una afinidad por los receptores cerebrales específicos, comparable a la de las BDZ, pero con una actividad 10 veces superior. También realizaron un estudio análogo al descrito, con las valerianas, plantas de uso milenario en la medicina tradicional por sus propiedades tranquilizantes e inductoras del sueño. Esta investigación permitió descubrir en sus extractos la presencia del flavonoide 6-metilapigenina, que resultó ser un ligando para el receptor GABAA con propiedades ansiolíticas pero no sedantes ni hipnóticas, y de los rutinósidos de flavanona hesperidina y linarina, que no tuvieron afinidad por el receptor GABAA ni presentaron efectos ansiolíticos. En cambio, ambos rutinósidos resultaron potentes sedantes e hipnóticos (figura 3).45,48,49
La asombrosa variedad de interacciones que presentan diversos flavonoides con el receptor tipo A del GABA, condujo a realizar estudios para determinar la interacción selectiva de una variedad de flavonoides naturales y derivados sintéticos con las diferentes isoformas del receptor GABAA. Tal es el caso de la 2'-metoxy-6-metilflavona y la trans-(2S,3R)-3-acetoxi-4'-metoxiflavanona. Ambas flavanonas incrementaron las corrientes iónicas del canal gracias a su interacción con las subunidades (α2β2/3 y (α2β1γ2L (expresados en ovocitos de Xenopus leavis); mismas subunidades que producen los efectos ansiolíticos y sedantes del diazepam, el loreclezole y la etamida, explicando así los efectos ansiolíticos a dosis bajas y sedantes a dosis altas que posee la 2'-metoxy-6-metilflavona en ratones, mientras que la trans-(2S,3R)-3-acetoxi-4'-metoxiflavanona solamente presentó efectos ansiolíticos debido a su selectividad por la subunidad (2 de los receptores GABAA.
]]> Se ha descrito que la administración oral de la flavona wogonina, aislada de Scutellaria baicalensis, una planta utilizada en la medicina tradicional de China, tiene efectos ansiolíticos y previene las convulsiones inducidas por pentilentetrazol y electrochoques en ratones, sin producir efectos sedantes o miorrelajantes. Además se demostró su interacción con el receptor GABAA cuando sus efectos fueron bloqueados mediante su coadministración con el antagonista GABAérgico flumazenil.La amentoflavona es una flavona dimérica cuya actividad ansiolítica ha sido extensamente explorada, ésta fue inicialmente identificada como un ligando de alta afinidad al sitio de BDZs de los receptores GABAérgicos. En estudios subsecuentes se demostró que la amentoflavona posee una actividad bifásica actuando como antagonista a concentraciones nanomolares y, a concentraciones altas (μmolares), como modulador alostérico negativo de GABA en el sitio α1β2γ2L; insensible al flumazenil. Una extensa batería de ensayos in vivo realizados con radio ligandos han mostrado que la amentoflavona inhibe significativamente la unión de serotonina, dopamina, δ-opioides, mientras que no tiene efecto sobre la unión de GABA al sitio de unión del receptor GABAA.50
Un ejemplo interesante de esto es que la 6-hidroxiflavanona presentó efectos ansiolíticos al ser evaluada en modelos de conducta en ratones. Esta flavanona no presentó los efectos indeseables que producen las BDZs como la sedación, el deterioro cognitivo, la miorrelajación y la falta de coordinación motriz. En estudios recientes realizados con receptores GABA expresados en células HEK 293T, se demostró que la 6-hidroxiflavonona es un modulador alostérico parcial positivo, selectivo al sitio de unión a BDZssensible al flumazenil, con afinidad significativa por las subunidades α2 y α3.
Otro ejemplo de interacción con el sistema GABAérgico es la flavona hespidulina que posee efectos ansiolíticos y anticonvulsivos en roedores. En estudios realizados con receptores recombinantes expresados en ovocitos de Xenopus leavis, la hespidulina mostró una actividad bifásica: a concentraciones bajas (0.8-5µM) mostró un efecto modulador positivo en las subunidades receptores α1,2,3,5, 6β2γ2S, por medio del incremento del flujo de corriente en estas subunidades, mientras que a concentraciones mayores (>30mM)mostró un efecto contrario sobre estas mismas subunidades. Además la actividad de hespidulina fue parcialmente bloqueada por el flumazenil y fue inactiva sobre los receptores α1β2. La acción bifásica y el hecho de que la hespidulina mostró afinidad por los receptores GABAérgicos que contenían la subunidad (6, indicaron que ésta interactúa con más de un sitio de unión en estos receptores.
Los ejemplos antes mencionados hacen evidente que las acciones de los flavonoides sobre los receptores GABAérgicos son más complejas que una simple acción sobre el sitio de acoplamiento de las BDZs de estos receptores.
En el cuadro 2 se mencionan los efectos más documentados de los flavonoides sobre el SNC.

MODELO FARMACÓFORO DE LOS FLAVONOIDES (INTERACCIÓN FLAVONOIDE-RECEPTOR GABAA)
]]> Después de los hallazgos de Paladini et al. en los años 1980, quienes observaron una similitud estructural, de afinidad y de respuesta farmacológica entre las BDZs y los flavonoides, se han publicado más de 6000 artículos científicos de estudios in vitro, in vivo y ex vivo, para caracterizar los efectos farmacológicos de los flavonoides naturales y los sintéticos, así como estudios teóricos computacionales ab initio y semiempíricos para establecer un modelo de las interacciones ligando-receptor (flavonoide- receptor GABAA) con el fin de correlacionar las características estructurales y fisicoquímicas de estos compuestos con su afinidad por los diferentes sitios del receptor y sus consecuentes respuestas conductuales y farmacológicas. De estos estudios destacan la creación de un modelo farmacóforo que describe los requerimientos mínimos necesarios que deben poseer las flavonas para una unión específica y eficiente con el sitio flavona (FS) (que es el mismo que para las BDZs) del receptor GABA. Como se representa en la figura 4, en este modelo el grupo carbonilo de las flavonas interactúa sólo con el sitio bifuncional H2/ A3 y el anillo B se coloca cerca de la región lipofílica L2. El anillo A en las flavonas se superpone al anillo 5-fenil del diazepam; no hay interacciones entre las flavonas y el sitio de H1 y no hay posibilidad de interacciones con A2. También en ésta se representan áreas del receptor de características fisicoquímicas particulares, que son localizadas en un arreglo espacial definido. H1 y A2 son donadores de enlaces de hidrógeno y sitios aceptores, respectivamente, mientras que H2/ A3 es un sitio bifuncional donador y aceptor de hidrógeno. L1, L2 y L3 es un pocket lipofílico y S1, S2 y S3 son regiones de interacciones estéricas negativas. Los efectos de los sustituyentes en el núcleo flavona en las posiciones 6 y/o 3' muestran que la unión de alta afinidad es relevante y cuantitativa. Este modelo farmacóforo ha servido como base para la síntesis y diseño de una gran variedad de análogos de flavonoides con el propósito de diseñar nuevos fármacos con mejores y más selectivos efectos, y sin los efectos colaterales que aún presentan las BDZs.69-74 Como resultado de estas intensas investigaciones los flavonoides han sido postulados como "una nueva familia de ligandos con sitios de afinidad específicos en los receptores GABA."
Finalmente podríamos preguntarnos ¿por qué existen sitios de interacción específicos para los flavonoides en el complejo receptor de neurotransmisión de inhibición más importante en nuestro cerebro? ¿Es esto una estrategia evolutiva de la especie humana?
Por otro lado, en 2008 Machado et al. describieron las propiedades tipo antidepresivos de la rutina, un rutinósido de flavanona, en modelos de conducta en ratones y mediante experimentos de co-administración con inhibidores de serotonina y noradrenalina determinaron que los efectos antidepresivos de la rutina fueron debidos a un incremento de la disponibilidad tanto de serotonina como de noradrenalina en la zona sináptica.75 Después de este estudio se han publicados los efectos antidepresivos de una gran variedad de flavonoides, mostrando así que también interactúan con otros sistemas de neurotransmisión.
LA INGESTA DESMEDIDA DE FLAVONOIDES PUEDE REPRESENTAR RIESGOS A LA SALUD
Se han tomado como referencia las poblaciones con bajo riesgo como las mediterráneas y los vegetarianos, con un consumo promedio de flavonoides como la quercetina de 68mg, y de 20 a 240mg, respectivamente. El uso de suplementos, particularmente las formulaciones antioxidantes y mezclas herbales que son comúnmente recomendadas en términos de gramos más que de miligramos, puede ser potencialmente tóxico. Por ejemplo, en los suplementos comerciales de quercetina la dosis recomendada está en un intervalo de entre 500 y 1000mg diarios, lo cual es de 10 a 20 veces más que el consumo obtenido en una dieta vegetariana típica. En México la venta de suplementos que contienen flavonoides no está regulada y, en general, en estos productos no se especifica la cantidad ni el tipo de flavonoides que contienen. Un significativo número de estudios proveen evidencia de que algunos flavonoides presentan un papel dual en la mutagénesis y en la carcinogénesis, es decir pueden actuar como antimutagénicos o como promutágenos; como antioxidantes y como pro-oxidantes, lo cual depende en gran medida de los niveles de consumo así como de las condiciones fisiológicas del cuerpo. La exposición a niveles altos de flavonoides, ya sea por medio de la dieta o por consumo de suplementos, puede potencialmente saturar al sistema, propiciando una sobreproducción de especies ERO y produciendo posteriormente daño al DNA y a sus procesos de replicación. Estos efectos pueden ser mayores durante el desarrollo fetal donde el crecimiento celular es rápido, lo cual puede incrementar la sensibilidad a la exposición a diversos flavonoides.76-78
A pesar de la inmensa cantidad de información que se ha generado sobre las diversas interacciones de los flavonoides y los seres humanos, es realmente pobre el conocimiento acerca de la toxicidad producida por el exceso en su consumo, mientras que sus atributos benéficos son sobrevalorados.
Sin embargo, la presencia de éstos como parte de una dieta equilibrada puede a mejorar la salud.
]]>CONCLUSIONES
Los flavonoides son componentes importantes de la dieta del ser humano y han estado en contacto con éste a lo largo de la evolución. Interactúan de manera directa y/o indirecta con los sistemas esenciales de neurotransmisión cerebral, modulan la actividad de diversas enzimas en las cascadas de señalización de procesos tan importantes como el de la memoria y el aprendizaje, promoviendo un mejor funcionamiento neuronal, por lo que es importante entender cómo influyen en la función cerebral.
El conocer sus características estructurales necesarias para sus efectos sobre los receptores GABAA es un desafío clave para el desarrollo de agentes específicos "para los receptores subtipo GABAA con el fin de lograr la producción de nuevos fármacos más selectivos y con menos efectos colaterales, útiles en la terapéutica de las disfunciones cerebrales y los trastornos mentales.
También resulta atractivo realizar la síntesis de nuevos flavonoides no sólo para producir agentes terapéuticos sino también para el desarrollo de moléculas que puedan ser usadas para investigar el papel de los diferentes sitios de modulación en los receptores GABAA.
Finalmente, debemos reiterar que los flavonoides forman o deben formar parte de nuestra dieta diaria; es un hecho que su consumo mejora la salud, por lo que más allá de considerarlos sólo como fármacos para aliviar condiciones patológicas, podemos promover su consumo para prevenir enfermedades.
Si de verdad somos lo que bebemos y comemos, los flavonoides deben considerarse un alimento para el pensamiento ágil y la vida sana.
REFERENCIAS
1. Tomás-Barberán FA, Wollenweber E. Flavonoid aglycones from the leaf surfaces of some Labiatae species. Plant Syst Evol 1990;173(3-4):109-118. [ Links ]
2. Harborne JB (editores). The flavonoids, advances in research since 1986. Londres: Chapman & Hall; 1994. [ Links ]
3. Manuchair E. Pharmacodynamic basis of herbal medicine. USA: CRC Press; 2001. [ Links ]
4. Németh K, Plumb GW, Berrin JG, Juge N et al. Deglycosylation by small intestinal epithelial cell beta-glucosidases is a critical step in the absorption and metabolism of dietary flavonoid glycosides in humans. Eur J Nutr 2003;42:29-42. [ Links ]
5. Day AJ, Canada FJ, Diaz JC, Kroon PA et al. Dietary flavonoid and isoflavone glycosides are hydrolyzed by the lactase site of lactase phlorizin hydrolase. FEBS Lett. 2000;468:166-170. [ Links ]
6. Berrin JG, McLauchlan WR, Needs P, Williamson G et al. Functional expression of human liver cytosolic beta-glucosidase in Pichia pastoris. Insights into its role in the metabolism of dietary glucosides. Eur J Biochem 2002;269:249-258. [ Links ]
7. Hollman PC. H. Absorption, bioavailability, and metabolism of flavonoids. Arch Physiol Biochem 2004;42:74-83. [ Links ]
8. Manach C, Scalbert A, Morand C, Remesy C et al. Polyphenols: food sources and bioavailability. Am J Clin Nutr 2004;79:727-747. [ Links ]
9. Spencer JPE, Chowrimootoo G, Choudhury R, Debnam ES et al. The small intestine can both absorb and glucuronidate luminal flavonoids. FEBS Lett 1999;458:224-230. [ Links ]
10. Crespy V, Morand C, Besson C, Manach C et al. Comparison of the intestinal absorption of quercetin, phloretin and their glucosides in rats. J Nutr 2001;131:2109-2114. [ Links ]
11. De Boer AG, Gaillard PJ. Drug targeting to the brain. Annu Rev Pharmacol Toxicol 2007;47:323-355. [ Links ]
12. Rang H, Dale M, Ritter J, Moore P. Pharmacology. Sexta edición. Edinburgh, UK: ed. Churchill Livingstone; 2007. [ Links ]
13. Wieland HA, Luddens H, Seeburg PH. A single histidine in Gaba-A receptors is essential for benzodiazepine agonist binding. J Biol Chem1992;267:1426-1429. [ Links ]
14. Bruton R, Qume M. [3H]-GABA binding to GABA-A and GABA-B sites on rat brain crude synaptic membranes. Methods Mol Biol 1999;106:27-35. [ Links ]
15. Jäger AK, Saaby L. Flavonoids and the CNS. Molecules 2011;16:1471-1485. [ Links ]
16. Álvarez de Felipe AI, Pulido Duarte MM. Transportadores de tipo ABC: consecuencias de su interacción con flavonoides. BLACPMA 2008;7(6):296-311. [ Links ]
17. Versantvoort CH, Schuurhuis GJ, Pinedo HM, Bekman CA et al. Genistein modulates the decreased drug accumulation in non-p-glycoprotein mediated multidrug resistant tumor cells-. Br J Cancer 1993;68:939-946. [ Links ]
18. Ferraro HK, Namgoong SY, Kim HP. Biological actions of flavonoids. Arc Pharmacol Res 1993;16:18-27. [ Links ]
19. Paul P, Ritra J, Ritva S, Mackku H. Dietary flavonoids and risk of lung cancer and other malignant neoplasms. Am J Epidemiol 1997;146:223-230. [ Links ]
20. Felicia VS, Najla GPC, Madeleine M, Keneeth KC. Inhibition of Human Breast cancer cell proliferation and delay of mammary tumorigenisis by flavonoids and citrus juices. Nutr Cancer 1996;26:167-181. [ Links ]
21. Fritz B, Tobias S, Albrecht K, Chaelotte B et al. Selected novel flavones inhibit the DNA binding or the DNA relegation step of eukaryotic topoisomerase-I. J Biol Chem 1996;271:2262-2270. [ Links ]
22. Huesken BCP, Dejong J, Beekman B, Onderwater RCA. Flavonoids as cardio protective agents. Cancer Chemother Pharmacol 1995;37:55-62. [ Links ]
23. Izzo AA, Dicarlo G, Mascolo N, Capasso F et al. Antiulcer effect of flavonoids. Role of endogenous PAF. Phytoterapy Res 1991;8:179-181. [ Links ]
24. Raj KJ, Shalini K. Flavonoids. A review of biological activities. Indian Drugs 1999;36:668-678. [ Links ]
25. Nishino C, Enoki N, Tawata S, Mori A et al. Tea flavonoids and microbial disease: A review. Agric Biol Chem 1987;51:139-145. [ Links ]
26. Arai Y, Watanabe S, Kimira M. Dietary intake of flavonols, flavones and isoflavones by Japanesee women and the inverse correlation between quercetin, liquiritigenin intake and plasma LDL cholesterol concentration. J Nutr 2000;130:2243-2250. [ Links ]
27. Ruikc. Advances in pharmacological studies of silymarin. Mem Inst Oswaldo Cruz 1991;86:79-85. [ Links ]
28. Pradhan SC, Girish C. Hepatoprotective herbal drug, silymarin from experimental pharmacology to clinical medicine. Indian J Med Res 2006;124(5):491-504. [ Links ]
29. De Lira Mota KS, Nunes Dias GE, Ferreira Pinto ME, Ferreira ÂL et al. Flavonoids with gastroprotective activity. Molecules 2009;14:979-1012. [ Links ]
30. Suzuki Y, Ishihara M, Segami T, Ito M. Anti-ulcer effects of antioxidants, quercetin, alphatocopherol, nifedipine and tetracycline in rats. Jpn J Pharmacol 1998;78(4):435-441. [ Links ]
31. Pharm TK, Vinh PT, Nong HD, Nguyen DK. Flavonoids as antimicrobial agents. Tap chi Duouc Hoc 1993;6:14-21. [ Links ]
32. Nishino C, Enoki N, Tawata S, Mori A et al. Tea flavonoids and microbial disease: A review. Agric Biol Chem 1987;51:139-145. [ Links ]
33. Kujumgier A, Tsvetkova J, Serkedjieva Y, Bankova V et al. Antibacterial, antifungal and antiviral activity of propolis of different geographic origin. J Ethno Pharmacol 1999;64:235-240. [ Links ]
34. Sato M, Fujiwara S, Tsuchiya H, Fujii T et al. Role of flavonoids in microbial diseases. J Ethnopharmacol 1996;54:171-178. [ Links ]
35. Ghazal SA, Abuzarqua M, Mahansneh AM. Effect of plant flavonoids on immune and inflammatory cell function. Phytother Res 1992;6:265-271. [ Links ]
36. Sanabria GA, Ospina SA, Ceronn JA, Raman MJ. Quercetin and related bioflavonoids: A review. Rev Colomb Cienc Quim Farm 1991;19:44-51. [ Links ]
37. Galati EM, Monforte MT, Kirjavainen S, Forestieri AM et al. Biological effects of hesperidin, a citrus flavonoid. (Note I): antiinflammatory and analgesic activity. Farmacol 1994;40(11):709-712. [ Links ]
38. Loscalzo LM, Wasowski C, Paladini AC et al. Marder. Opioid receptors are involved in the sedative and antinociceptive effects of hesperidin as well as in its potentiation with benzodiazepines. Eur J Pharmacol. 2000;580(3):306-313. [ Links ]
39. K Raj Narayana M, Sripal Reddy MR, Chaluvadi DR. Krishna. Bio-flavonoids classification, pharmacological, biochemical effects and therapeutic potential. Indian J Pharmacol 2001;33:2-16. [ Links ]
40. Paul P, Ritra J, Ritva S, Mackku H et al. Dietary flavonoids and risk of lung cancer and other malignant neoplasms. Am J Epidemiol 1997;146:223-230. [ Links ]
41. Matsuzaki K, Yamakuni T, Hashimoto M, Haque A et al. Nobiletin restoring β-amyloid-impaired CREB phosphorylation rescues memory deterioration in Alzheimer's disease model rats. Neurosci Lett 2006;400(3):230-234. [ Links ]
42. Nagase H, Omae N, Omori A, Nakagawasai O et al. Nobiletin and its related flavonoids with CRE-dependent transcription-stimulating and neuritegenic activities. Biochem. Biophys Res Commun 2005;4(337):1330-1336. [ Links ]
43. Matsuzaki K, Miyazaki K, Sakai S, Yawo H et al. Nobiletin, a citrus flavonoid with neurotrophic action, augments protein kinasa A-mediated phosphorylation of the AMPA receptor subunit, GluR1, and the postsynaptic receptor response to glutamate in murine hippocampus. Eur J Pharm 2008;578:194-200. [ Links ]
44. Nakajima A, Yamakuni T, Haraguchi M, Omae N et al. Nobiletin, a citrus flavonoid that improves memory impairment, rescues bulbectomy-induced cholinergic neurodegeneration in mice. J Pharmacol Sci 2007;105:122-126. [ Links ]
45. Wolfman C, Viola H, Marder M, Wasowski C et al. Anxioselective properties of 6,3'-dinitroflavone, a high-affinity benzodiazepine receptor ligand. Eur J Pharm 1996;318:23-30. [ Links ]
46. Olsen WR, Siergart W. International Union of Pharmacology. LXX. Subtypes of y-Aminobutyric acidA receptors: Classification, pharmacology and function. Update. Pharmcol Rev 2008;60(3):243-260. [ Links ]
47. Goutman JD, Waxemberg MD, Doñate-Oliver F, Pomata PE et al. Flavonoid modulation of ionic currents mediated by GABAA and receptors GABAC receptors. Eur J Pharmacol 2003;461:79-87. [ Links ]
48. Marder M, Viola H, Wasowski C, Fernandez S et al. 6-Methylapigenin and hesperidin: new valeriana flavonoids with activity on the CNS. Pharmacol Biochem Behav 2003;75:537-545. [ Links ]
49. Martínez MC, Fernandez SP, Loscalzo LL, Wasowski C et al. Hesperidin, a flavonoid glycoside with sedative effect, decreases brain Perk1/2 levels in mice. Pharmacol Biochem Behav 2009;92:291-296. [ Links ]
50. Hanrahan RJ, Chebib M, Johnston ARG. Flavonoid modulation of GABAa receptors. Brit J Pharmacol 2011;163:234-245. [ Links ]
51. Hui KM, Huen MS, Wang HY, Zheng H et al. Anxiolytic effect of wogonin, a benzodiazepine receptor ligand isolated from Scutellaria bai-calensis Georgi. Biochem Pharm 2002;64:1415-1424. [ Links ]
52. Coleta M, Graca Campos M, Cotrim MD, de Lima TCM et al. Assessment of luteolin (3', 4',5, 7-tetrahydroxyflavone)neuropharmacological activity. Behav Brain Research 2008;189:75-82. [ Links ]
53. Ognibene E, Bovicelli P, Adriani W, Saso L et al. Behavioral effects of 6-bromoflavanone and 5-methoxy-6, 8-dibromoflavanone as anxiolytic compounds. Prog Neuropsychopharmacol Biol Psych 2008;32:128-134. [ Links ]
54. Nassiri-Asl M, Shariati-Rad S, Zamansoltani F. Anticonvulsive effects of intracerebroventricular administration of rutin in rats. Prog Neuropsychopharmacol Biol Psych 2008;32:989-993. [ Links ]
55. Rasilingam D, Duraisamy S, Subramanian R. Anticonvulsant activity of bioflavonoid gossypin. J Bangladesh Pharmacol Soc 2009;4:51-54. [ Links ]
56. Martínez MC, Fernandez SP, Loscalzo LM, Wasowski C et al. Hesperidin, a flavonoid glycoside with sedative effect, decreases brain pERK1/2 levels in mice. Pharmacol Biochem Behav 2009;92:291-296. [ Links ]
57. Wang LE, Cui XY, Cui SY, Cao JX et al. Potentiating effect of spinosin, a C-glycoside flavonoid of Semen Ziziphi spinosae, on pentobarbital-induced sleep may be related to postsynaptic 5-HT1A receptors. Phytomedicine 2010;17:404-409. [ Links ]
58. Meotti FC, Posser T, Missau FC, Pizzolatti MG et al. Involvement of p38MAPK on the antinociceptive action of myricitrin in mice. Biochem Pharmacol 2007;74(6):924-931. [ Links ]
59. Kawabata K, Kawai Y, Tera J. Suppressive effect of quercetin on acute stress-induced hypothalamic-pituitary-adrenal axis response in Wistar rats. J Nutr Biochem 2010;21:374-380. [ Links ]
60. Li-Tao Y, Jian-Mei L, Yu-Cheng L, Ying P et al. Antidepressant-like behavioral andneurochemical effects of the citrus-associated chemical apigenin. Life Sci 2008;82:741-751. [ Links ]
61. Nagase H, Yamakuni T, Matsuzaki K, Maruyama Y. Mechanism of neurotrophic action of nobiletin in PC12D cells. Biochemistry 2005;44:13683-13691. [ Links ]
62. Lee H, Kim YO, Kim H, Kim SY. Flavonoid wogonin from medicinal herb is neuroprotective by inhibiting inflammatory activation of microglia. FASEB J 2003;17:1943-1944. [ Links ]
63. Li R, Huang YG, Fang D, Le WD. (-)-Epigallocatechin gallate inhibits lipopolysaccharide-induced microglial activation and protects against inflammation-mediated dopaminergic neuronal injury. J Neurosc Res 2004;78:723-731. [ Links ]
64. Sharma V, Mishra M, Ghosh S, Tewari R et al. Modulation of interleu-kin-1β mediated inflammatory response in human astrocytes by flavonoids: Implications in neuroprotection. Brain Res Bull 2007;73: 55-63. [ Links ]
65. Muthiah NS, Viswanathan S, Thirugnanasambantham P, Reddy MK et al. Antiinflammatory activity of flavone and its mono-methoxy derivatives. A structure activity study. Indian J Pharmacol Sci 1993;55:180-183. [ Links ]
66. Lou H, Fan P, Pérez RG, Lou H. Neuroprotective effects of linarin through activation of the PI3/Akt pathway in amiloid-β- induced neuronal cell death. Bior Med Chem 2011;19:4021-4027. [ Links ]
67. Schroeter H, Boyd C, Spencer JPE, Williams RJ et al. MAPK signaling in neurodegeneration: influences of flavonoids and of nitric oxide. Neurobiol Aging 2002;23:861-880. [ Links ]
68. Richetti SK, Blank M, Capiotti KM, Piato AL et al. Quercetin and rutin prevent scopolamine-induced memory impairment in zebrafish. Behav Brain Res 2011;217:10-15. [ Links ]
69. Huang Q, Xiaohui H, Chourong. Pharmacophore/receptor models for GABAa/BZ subtypes (a1 b3 g2 a5 g2 a6 b3 g2) Via a comprehensive ligand-maping approach. J Med Chem 2000;43:71-95. [ Links ]
70. Kahberg P. Refinement and evolution of a pharmacophore model for flavone derivates binding to the benzodiazepine site of the GABAa receptor. J Med Chem 2002;45:4188-4201. [ Links ]
71. Paladini A, Marder M, Medina J. 6-Bromo flavone. A high affinity ligands for the chemical benzodiazepine receptor is a member of family of active flavonoids. Biochem Biophys Res Commun 1996;223:384-389. [ Links ]
72. Paladini A, Marder M, Medina J. Detection of benzodiazepine receptor ligands in small libraries of flavone derivates sinthetyzed by solution phase combinatorial chemistry. Biochem Biophys Res Commun 1998;249:481-485. [ Links ]
73. Paladini A, Marder M, Medina J, Viola H et al. Flavonoids and the Central Nervous System: from forgotten factors to potent anxiolytic compounds. J Pharm 1999;51:519-526. [ Links ]
74. Huang X, Liu T, Gu J, Xiaomin L et al. 3D QSAR Model of flavonoids binding at benzodiazepine site in GABAA Receptors. J Med Chem 2001;44:1883-1891. [ Links ]
75. Machado D, Bettio L, Cunha M, Santos A et al. Antidepressant-like effect of rutin isolated from the ethanolic extract from Schinus molle L. in mice: Evidence for the involvement of the serotonergic and noradrenergic systems. Eur J Pharmacol 2008;587:163-168. [ Links ]
76. Williams RJ, Spencer JPE, Rice-Evans C. Flavonoids: Antioxidants or signaling molecules? Free Rad Biol Med 2004;36(7):838-849. [ Links ]
77. Pérez-Trueba G. Los flavonoides antioxidantes o prooxidantes. Rev Cub Invest Biomed 2003;22(1)1-10. [ Links ]
78. Spencer JPE. Flavonoids and brain health: multiple effects underpinned by common mechanism. Genes Nutr 2009;4:243-250. [ Links ]
]]>