>. Un conocimiento más profundo de los patrones epigenéticos podría contribuir a identificar factores de riesgo para estos trastornos.]]>
La epigenética y los estudios en gemelos en el campo de la psiquiatría
Epigenetics and twin studies in psychiatric domains
Adriana Estrella González Ramírez1 *, Alejandro Díaz Martínez2, Adriana Díaz–Anzaldúa1
1 Departamento de Genética, Instituto Nacional de Psiquiatría Ramón de la Fuente.
2 Departamento de Psicología Médica, Psiquiatría y Salud Mental, Facultad de Medicina, UNAM.
]]>*Correspondencia:
Adriana Díaz–Anzaldúa.
Departamento de Genética.
Instituto Nacional de Psiquiatría Ramón de la Fuente.
Calz. México–Xochimilco 101,
San Lorenzo Huipulco,Tlalpan,
14370, México, D.F.
Fax: 52 (55) 5513–3722.
E–mail: adiaza2@imp.edu.mx
Recibido: 9 de octubre de 2007.
Aceptado: 5 de diciembre de 2007.
Abstract
The sequence of the human genome integrates the keystone of our life. Part of it is transcribed to RNA, which in turn provides the information required by our cells to produce proteins. Discoveries in the genetics field have been essential to medicine and have been used to develop strategies to modify, prevent and propose new therapeutic approaches for human diseases.
In the 19th Century, Gregor Johann Mendel developed a theoretical model which was able to predict in an accurate way hereditary mechanisms; indeed, his laws still explain the basis of human inheritance. Almost ninety years later, James Watson and Francis Crick announced their double–helix model of the DNA molecule. Then, positional cloning and the polymerase chain reaction (PCR) were introduced; more recently, almost 99% of the sequence of our genome was made public.
The current period of time is known as the post–genomic era, due to the fact that researchers are not only obtaining the complete sequences of thousands of genomes, but are also searching for clues that may help understand the mechanisms that affect gene activation and deactivation, in which epigenetic factors are also involved.
In medical domains, twins constitute a suitable group to study inherited disorders. Dizygotic or fraternal twins are produced by different egg and sperm cells, and even when these two fertilization events occur simultaneously, dizygotic twins share approximately the same percentage of genetic material than any pair of siblings, that is, around 50%. Some authors have suggested that the tendency for spontaneous dizygotic twinning could be attributed to a double ovulation which is genetically determined in an autosomal dominant manner.
Monozygotic, as opposed to dizygotic twins, are produced by a single zygote whose cells are dissociated and originate two independent organisms; approximately a third of monozygotic twins are separated before the 5th day after fertilization, and the rest between the 5th and the 15th day. Most monozygotic twins are very similar; nevertheless, some few exceptions prove that in fact they actually do not have to be identical.
]]> Relatives of a person with a mental disorder tend to share traits associated with this disease, especially if the patient and the relative are monozygotic twins. However, important differences may be detected even between each pair of identical twins.Parameters such as concordance and heritability have shown that a monozygotic twin can develop an inherited disorder while his or her co–twin will always be disease–free. In addition to differences in susceptibility to inherited diseases, this kind of twins can display dissimilarities in somatic cell mutations (more overtly noticeable when ageing), their set of antibodies and T cell receptors, their number of mitochondrial DNA molecules, and chromosome X inactivation patterns in women, all of which are the main subject of many ongoing studies. A recent report shows that from 160 monozygotic twin pairs who were 3 to 74 years old, epigenetic patterns were identical early in life, but differences were more obvious at older ages, especially if twins were raised apart or if they had different medical history. Medical conditions, but also environmental factors such as pregnancy tobacco exposure, physical activity, and diet could contribute to differences in epigenetic patterns. It has been shown that epigenetic modifications (or epi–mutations) are more frequent than the ones that modify DNA sequence, so they are part of the fundamental causes of biological diversity, and they show how environment can modulate gene expression and contribute to our phenotype.
Even when twin studies are sometimes considered purely genetic, they also give information about the influence of environmental factors. However, it is important to consider with caution the results from this type of studies. Heritability estimates are not unchangeable facts. They depend on the sample being analyzed, the genes involved in the specific sample, the characteristics of the environmental factors which members of this group were exposed to, and the precise moment the study was done.
Epigenetics refers to changes that do not alter the DNA sequence but affect gene function due to chemical modifications which mainly occur in DNA cytosines and in chromatin–related histones. Epigenetic processes are covalent modifications which include the addition of functional groups (methyl, acetyl, phosphate, etc.) or proteins (ubiquitin, SUMO, etc.) to the DNA molecule or to associated proteins. These modifications contribute to the activation or inhibition of transcription, which leads to changes in messenger ARN expression that can ultimately influence the onset of disease.
Pseudogenes are still being excluded while new genes are being confirmed in our genome sequence, but the current estimates indicate that each one of our nucleated cells contains almost 22000 genes (excluding mitochondrial DNA) which encode for polypeptides and more than 4,000 whose final product is RNA.
Gene expression is partially controlled by DNA coiling around globular proteins called histones, which constitute a structure known as chromatin, a DNA–protein complex that represents the packaging of 3.25 billion base pairs of our genetic information. Physical and chemical chromatin modifications can also affect gene expression by changing DNA–protein interactions; in general terms, genes are inhibited when chromatin is packed and they are active when it is free. These dynamic states are controlled by epigenetic reversible modifications on DNA methylation or by changes in histones. It has been shown that subtle epigenetic differences between any two human beings are associated with dissimilar final chromatin remodeling, as well as expression/repression of genes.
In order to explain how DNA methylation controls transcription, two mechanisms have been proposed. First, the presence of a methyl group on specific sites could simply prevent transcription factors from binding the DNA. Second, some proteins contain a specific domain that recognizes and binds methylated DNA, and works as a transcription repressor.
Regarding histone modifications, acetyl group addition occurs on the amino acid lysine; there are reports that indicate that almost 14% of lysines are susceptible to acetylation. On the other hand, methyl groups bind arginines and lysines. Different combinations of covalent modifications lead to what is known as the histone code. This review gathers information about the possible involvement of epigenetics in some mental disorders and attempts to explain how it can account for differences observed between <<identical>> twins. Some examples of a plausible link between epigenetic modifications and mental disorders are discussed.
Regarding bipolar disorder, valproate efficacy has been linked to its inhibitory activity, suggesting that an epigenetic modification (that represses transcription of a gene) may play a role in the onset of some of the symptoms of the disease. Perhaps one of the most studied aspects regarding schizophrenia is the hypermethylation of Reelin (RELN) and GAD67 genes in the prefrontal cortex, due to the over–expression of DNMT1 (DNA methyl–trasferase 1) in GABAergic cortical interneurons. Reelin is an important protein during prenatal development of the Central Nervous System and it is relevant for the expression of cortical pyramidal neurons in the adult brain; it regulates the migration of neurons during brain development and it is essential for the correct organization and plasticity of the cerebral cortex. GAD67 is one of two molecular forms of GABA synthetizing enzymes, being GABA the main inhibitory neurotransmitter in humans.
Hypermethylation of these genes leads to transcription repression either by interference of transcription promoters by methyl groups or by MBD protein binding. The final outcome is a low production of Reelin and GAD67, a typical feature found in brains of shchizophrenic patients.
]]> Epigenetic analyses of autism are sometimes with Rett and Angelman's syndromes. The latter are pathological conditions that share clinical features with autism, such as development retardation, language impairments and stereotypic behaviors. Rett syndrome is caused by mutations at the MECP2 gene, and Angelman's syndrome by a maternal deficiency on chromosome 15 q11–q13 region, impaired methylation of DNA or maternal mutation of the ubiquitin–protein ligase E3A (UBE3A). However, there have also been reports of patients with Angelman's syndrome or autism who have mutations at MECP2.In conclusion, the onset of mental disorders is influenced both by environmental and genetic factors. Concordance and heritability estimates are just two of the many ways of analyzing differences between monozygotic twins. Part of the reported disparity between monozygotic twins could be caused by epigenetic factors. Epigenetic modifications could partially explain the etiology of mental disorders.
Key words: Twins, epigenetics, heritability, concordance, mental disorders.
Resumen
La secuencia de ADN genómico que caracteriza a nuestra especie constituye la piedra fundamental de la vida humana; parte de ella se refleja en la secuencia del ARN y a través de éste se dicta la información necesaria para que nuestras células produzcan proteínas.
La genética contribuye de manera importante a los avances en el campo médico. Los descubrimientos genéticos han permitido desarrollar estrategias para modificar, prevenir y proponer nuevas terapias para diversas enfermedades.
En el siglo XIX, Gregor Johann Mendel desarrolló un modelo teórico capaz de predecir la naturaleza y propiedades de los mecanismos de la herencia, que sigue siendo indispensable para explicar la base de la herencia humana. Otro suceso determinante en la historia de la Medicina se dio a conocer casi nueve décadas después cuando James Watson y Francis Crick describieron su modelo estructural para el ADN. Posteriormente se introdujeron la clonación posicional y la reacción en cadena de la polimerasa; más recientemente se publicó cerca del 99% de la secuencia del genoma humano. El período actual se conoce como la era post–genómica, ya que además de descifrar genomas completos, los investigadores pretenden, entre otras cosas, esclarecer los mecanismos que influyen en la activación e inactivación de los genes, lo cual en parte involucra un nivel epigenético.
En las ciencias médicas los gemelos constituyen un grupo idóneo para abordar el estudio de las enfermedades hereditarias. En este tipo de padecimientos suelen observarse similitudes entre parientes, en especial si se trata de gemelos monocigóticos. Sin embargo, aun en este tipo de hermanos se detectan diferencias importantes. Parámetros como los grados de concordancia y porcentajes de heredabilidad han puesto de manifiesto que un gemelo monocigótico puede presentar trastornos hereditarios que su co–gemelo nunca tendrá.
La epigenética es el estudio de los cambios en la función de los genes que no afectan la secuencia del ADN, por modificaciones que tienen lugar principalmente en las citosinas de éste y en las histonas de la cromatina. Se ha determinado que las modificaciones epigenéticas son mucho más frecuentes que aquellas que modifican la secuencia del ADN, por lo que constituyen uno de los fundamentos de la diversidad biológica, muestran la manera en que el ambiente puede modular la expresión genética y contribuyen así a nuestro fenotipo. Esta revisión reúne datos sobre la posible relevancia de la epigenética en el estudio de los trastornos mentales y como posible explicación parcial de las diferencias observadas entre gemelos <<idénticos>>. Un conocimiento más profundo de los patrones epigenéticos podría contribuir a identificar factores de riesgo para estos trastornos.
]]> Palabras clave: Gemelos, epigenética, heredabilidad, concordancia, trastornos mentales.
INTRODUCCIÓN
Uno de los principales objetivos de la genética es descifrar el orden exacto en que las cuatro letras del alfabeto del ADN se suceden en los cromosomas humanos, tanto en ausencia como en presencia de patología heredable. La combinación de adeninas (A), citocinas (C), guaninas (G) y timinas (T) característica de nuestra especie, constituye la piedra fundamental de nuestra vida y está íntimamente relacionada con la secuencia del ARN mensajero, emisario que transmite la información necesaria para que la célula produzca proteínas. La gran cantidad de investigaciones sobre los ácidos nucleicos y las proteínas, que día con día se lleva a cabo en diversas disciplinas médicas, ejemplifica la manera en que la genética ha modificado el punto de vista de la humanidad acerca de sí misma y acerca de su relación con el resto del planeta. Los conocimientos obtenidos a partir de la genética han permitido desarrollar estrategias para modificar, prevenir y proponer nuevas terapias para las enfermedades humanas.1
Hace 143 años, Gregor Johann Mendel, fraile de la Orden de San Agustín, propuso las leyes que permiten entender la base de la herencia humana, basándose en análisis matemáticos y casi una década de minuciosa observación de variantes puras e híbridas del chícharo.2 El merecidamente considerado padre de la genética desarrolló un modelo teórico que predecía con total exactitud la naturaleza y propiedades de los mecanismos de la herencia.
La genética ha sido parte integral de la medicina moderna desde que en 1953 James Watson y Francis Crick, influenciados por estudios previos, describieron su modelo estructural de doble hélice para el Ácido Desoxirribo–nucleico (ADN).3 A mediados de la década de 1980, dos avances en la genética fueron considerados entre los más determinantes en la historia de la medicina: la <<clonación posicional>>, que permite identificar genes relacionados con enfermedades, aun sin conocer su función, sólo por su posición cromosómica, y el descubrimiento del método de reacción en cadena de la polimerasa (PCR), que facilitó el análisis del ADN en distintas disciplinas.4 Asimismo, la publicación en 2003 de cerca del 99% de la secuencia de nuestro genoma constituye otro gran avance. El periodo científico actual se conoce como <<la era post–genómica>>. Dicho término se refiere al hecho de que los científicos han llegado más allá del puro desciframiento de más de miles de genomas completos de virus y de especies de todos los reinos. En el momento actual, se ha incrementado además el interés por esclarecer las razones por las que una misma información genómica puede ser regulada para producir distintos tipos celulares en un mismo individuo o distintas características aun en individuos genéticamente idénticos. Aunado a la secuencia nucleotídica unidimensional del ADN, se ha demostrado que hay un nivel epigenético que afecta la morfología y la función celulares, es decir, su fenotipo, al influir en la activación e inactivación de genes.5 Este nivel epigenético puede variar incluso entre gemelos <<idénticos>>.
En nuestra especie, los gemelos representan una forma singular de las relaciones fraternas. No sólo comparten familia y ambiente social durante por lo menos la primera etapa de sus vidas, sino que también tienen altos niveles de proximidad en cuanto a número de años que pasan juntos antes de abandonar el hogar familiar y hay mayor frecuencia de contacto después de ello.6 Los gemelos dicigóticos (DC) o mellizos se originan a partir de distintos óvulos y espermatozoides y aunque estos dos eventos de fecundación son simultáneos, los mellizos comparten el mismo porcentaje de material hereditario que cualquier par de hermanos de distintas gestaciones, es decir aproximadamente 50%. Algunos reportes indican que la tendencia a tener gemelos DC de manera espontánea podría atribuirse a una ovulación doble genéticamente determinada,7 tendencia que podría transmitirse de manera autosómica dominante.8 Los gemelos monocigóticos (MC), en cambio, se forman a partir de un solo cigoto cuyas células se disocian dando origen a dos organismos independientes;9 aproximadamente un tercio de las parejas gemelares MC se separan antes del día cinco de la gestación y el resto entre el día cinco y el quince. La mayoría de los gemelos MC son notoriamente parecidos, pero algunas excepciones muestran que no tienen que ser idénticos. Se ha observado que pueden diferir en mutaciones en células somáticas, sobre todo a largo plazo,10 en su conjunto de anticuerpos y receptores de células T, en el número de moléculas de ADN mitocondrial, en el esquema de inactivación del cromosoma X en las mujeres11 e incluso en el grado de susceptibilidad a enfermedades, lo cual en nuestros días es objeto de numerosos estudios.
Parte de estas diferencias podrían relacionarse con cambios epigenéticos, ya que tanto en animales clonados como en gemelos humanos MC se han encontrado discrepancias epigenéticas que se asocian con diferencias en ciertos rasgos.12 En un estudio reciente se compararon las diferencias epigenéticas del genoma de 160 pares de gemelos monocigóticos de tres a 74 años de edad; los perfiles epigenéticos eran idénticos entre hermanos a temprana edad, pero a medida que ésta avanzaba aumentaban las diferencias epigenéticas.9 Estas diferencias son aún más notorias cuando los gemelos crecen en ambientes separados o cuando tienen antecedentes médicos distintos, lo que sugiere que los factores ambientales como la exposición al tabaco durante el embarazo, la actividad física, la dieta y las afecciones médicas podrían contribuir a la diferenciación de los perfiles epigenéticos. De esta manera, los gemelos MC representan un modelo excelente para estudiar la contribución epigenética a la susceptibilidad de ciertas enfermedades como las psiquiátricas, las tumorales o las metabólicas.13 Se ha determinado que las modificaciones epigenéticas (o epimutaciones) son mucho más frecuentes que las mutaciones que modifican la secuencia del ADN y de esta forma constituyen uno de los fundamentos de la diversidad biológica, muestran la manera en que el ambiente puede modular la expresión de nuestro patrimonio hereditario y contribuir así a nuestro fenotipo.
En esta revisión exponemos aspectos teóricos sobre la epigenética y resumimos algunos de los reportes de los últimos seis años sobre la relación de la epigenética con los trastornos mentales, para facilitar la noción de que todos los seres humanos somos distintos, incluso los llamados idénticos.
]]> EPIGENÉTICA
La epigenética estudia las variaciones hereditarias que ocurren sin que cambie la secuencia del ADN,3 es decir, sin que se altere la lectura de las bases nitrogenadas A, C, G y T. Los procesos epigenéticos son modificaciones covalentes por adición de grupos funcionales (metilos, acetilos, fosfatos, etc.) o proteínas (ubiquitina, modificador relacionado a la ubiquitina <<SUMO>>, etc.) al ADN o a algunas de sus proteínas asociadas. Estas modificaciones contribuyen a activar o inhibir los procesos de transcripción, afectando así el grado de expresión del ARN mensajero, lo cual puede influir en el desarrollo de patología.14
Sin olvidar que el análisis fino de la secuencia de nuestro genoma permite aun excluir pseudogenes y agregar genes confirmados, se estima que en cada una de nuestras células nucleadas hay cerca de 22000 genes (excluyendo el ADN de las mitocondrias) que codifican para polipéptidos y más de 4000 que codifican únicamente para ARN. La expresión de los genes se controla en parte por el enrollamiento del ADN alrededor de grupos de proteínas globulares llamadas histonas,3 lo cual a su vez conforma una estructura compacta conocida como cromatina,14 un complejo ADN–proteína que representa el empaquetamiento de aproximadamente tres mil doscientos cincuenta millones de pares de bases de material genético.15 Los cambios físicos y químicos de la estructura de la cromatina también influyen en la expresión de los genes al alterar las interacciones ADN–proteína; los genes se inactivan cuando la cromatina está condensada y se activan cuando está libre. Estos estados dinámicos se controlan por medio de modificaciones epigenéticas reversibles en la metilación del ADN o en los cambios en las histonas3 con sus correspondientes enzimas y grupos de proteínas reguladoras.15 Entre cualquier par de personas las diferencias sutiles en el número, sitio y combinación de modificaciones epigenéticas determinan en cada una el remodelamiento final de la cromatina y por ende la expresión/represión de los genes.14
METILACIÓN DEL ADN
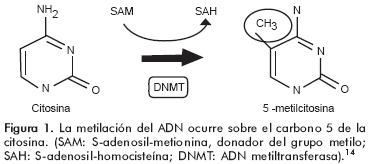
La metilación del ADN generalmente consiste en la adición de un grupo metilo en la posición C5 de las citosinas que se encuentran enlazadas con guaninas (CpG) en una de las cadenas de la molécula de ADN, resultando en lo que se conoce como 5–metil–citosina (5mC), o en la posición N6 de adeninas, resultando en 6mA. La donación de los átomos de carbono para la metilación se obtiene por medio de la dieta y posteriormente, a través de la vía del folato. Además están involucrados otros micronutrientes importantes como la vitamina B12, la vitamina B6 y la colina. Todos estos elementos son requeridos directa o indirectamente para la conversión de homocisteína a metionina, que es el precursor inmediato de S–adenosil metionina (SAM), el principal donador de metilos para el ADN. Después de donar el grupo metilo, SAM se convierte en S–adenosilhomocisteína (SAH), la cual pierde la adenosina y llega a ser nuevamente homocisteína (figura 1). La presencia de polimorfismos genéticos que afectan la función de las moléculas de transporte y de enzimas necesarias en el ciclo de folato/homocisteína predisponen a una inestabilidad genómica, por recombinación alterada o segregación anormal. Sin embargo, los efectos de estas variantes dependen del estado nutricional de cada individuo. Por ejemplo, los polimorfismos que disminuyen la disponibilidad de folato/homocisteína antes o durante el embarazo asociados a una baja ingesta de los nutrientes necesarios, podrían contribuir a anormalidades en el feto como falla en el cierre del tubo neural, paladar hendido y a trastornos como el síndrome de Down y la trisomía 18.16 Agentes ambientales tales como los metales y los hidrocarburos aromáticos, encontrados en emisiones de combustible fósil, aguas contaminadas y humo de cigarro, influyen en el contenido de grupos metilo que pueden unirse al ADN, desestabilizando el genoma o el metabolismo celular. La metilación es una modificación post–sintética, es decir, se lleva a cabo después de que se han incorporado los nucleótidos en la nueva cadena de ADN.3

En nuestro genoma, la metilación es común en regiones cortas que se conocen como islotes CpG, presentes especialmente en los promotores, secuencias que preceden a los genes y que propician la transcripción del ADN a ARN, o en el primer exón de más de 60% de los genes.5 Los genomas de los espermatozoides y los ovocitos, como el de las células somáticas diferenciadas, presentan un grado relativamente importante de metilación. Después de la fecundación y la formación del cigoto, durante el desarrollo previo a la implantación, se presentan cambios drásticos en los niveles de metilación. Así, el desarrollo embrionario comienza con una oleada que suprime casi todas las marcas epigenéticas que estaban presentes en los genomas de los gametos, exceptuando las de la <<impronta>> parental, que se conservan. En el genoma paterno (proporcionado por el espermatozoide), esta oleada de desmetilación es un proceso activo que elimina del genoma casi todas las metilaciones a pocas horas de la fecundación,17 mientras que en el genoma materno (proveniente del ovocito) el proceso es pasivo y se produce durante las divisiones de los blastómeros. Después de la implantación, el genoma de los tejidos embrionarios se metila durante los procesos de diferenciación celular que definen las características de los nuevos tejidos, con perfiles de metilación específicos, mientras que el ADN de la placenta y otros anexos embrionarios permanece hipometilado. Tales modificaciones se heredan de células madres a células hijas.10 Como resultado, cada tipo celular tiene su propio esquema epigenético que debe cuidarse para mantener la función de los genes. Si este patrón es afectado (cuadro 1), los resultados pueden ser la aparición de trastornos congénitos o la predisposición para adquirir determinados estados patológicos como cáncer y trastornos neurodegenerativos.3 En general, a mayor metilación en los islotes CpG presentes en las regiones reguladoras de un gen, más baja es la tasa de transcripción de éste.
]]>
Las enzimas involucradas en este proceso epigenético son las ADN metiltransferasas (DNMTs, por sus siglas en inglés) y se clasifican como DNMTs de novo, que adicionan grupos metilo a moléculas de ADN que no poseen ninguno de estos grupos, y DNMTs de mantenimiento, que tienen gran afinidad por moléculas semimetiladas, es decir, cuando sólo una cadena se encuentra modificada.5
De igual forma se presentan desmetilasas que retiran los grupos metilo durante el desarrollo celular; estas enzimas incluyen, por un lado, glicosilasas cuya actividad asemeja la reparación del ADN por excisión de bases donde se eliminan las citosinas metiladas. Por otra parte, puede ocurrir desmetilación del ADN por intervención de la proteína MBD2, de la que se ha reportado actividad tanto represora como desmetilante; sin embargo, el mecanismo de acción de esta última no ha sido completamente esclarecido.5
Se han propuesto dos mecanismos para explicar cómo la metilación del ADN controla la transcripción. El primero de ellos se basa en la presencia de grupos metilo en sitios específicos, lo que simplemente no permite la unión de los factores de transcripción por impedimento estérico.5 El otro mecanismo se relaciona con una familia de proteínas que poseen un dominio de reconocimiento y unión al ADN metilado y que fungen como represoras de la transcripción.14 En los mamíferos, esta familia comprende cinco proteínas, MBD 1 a 4 y MeCP2; todas comparten el dominio de unión a los sitios 5mC, excepto la MBD3 que tiene dos sustituciones de aminoácidos. La MBD4 es la única que no está involucrada en la regulación transcripcional sino en la reducción del riesgo mutacional en genomas con altos niveles de mutilación.5 La MeCP2 fue la primera de estas proteínas en ser clonada, cuenta con 486 aminoácidos y dos dominios: el izquierdo, de unión al grupo metilo, y el derecho, de represión transcripcional de aproximadamente 100 aminoácidos, localizado a la mitad de la proteína.5,15 Esta se expresa más abundantemente en el cerebro que en otros órganos, preferentemente en el núcleo de las neuronas, aunque en el caso de las postsinápticas también en el citoplasma. En el núcleo, la MeCP2 forma un complejo correpresor junto con las histona–deacetilasas y las proteínas remodeladoras de la cromatina.15 Se le ha asociado también con una actividad metiladora de histonas, específicamente de la H3 en la lisina 9, lo que significa nuevamente una señal represora de la transcripción. Así mismo, participa indirectamente en la supresión del proceso de transcripción, favoreciendo una estructura más densa de la cromatina, lo que impide la unión de los factores que activan este proceso. Las mutaciones en el gen para MeCP2 están relacionadas con fenotipos clínicos tales como retraso mental asociado al cromosoma X, síndrome de Angelman y autismo.5
Es relativamente reciente la propuesta de que las variaciones en la metilación de CpG pueden explicar parte de la etiología de los trastornos mentales. Algunos de los descubrimientos que sugieren este vínculo son los siguientes:
1). Múltiples mutaciones en el gen que codifica para la proteína MeCP2 están involucrados en síndromes relacionados con el neurodesarrollo, como el de Rett. 2). Se han encontrado en estudios postmortem deficiencias en la expresión del gen MECP2 en cerebros de personas que padecieron autismo.3 3). La regulación de los genes RELN y GAD67 (reelina y GAD67 respectivamente), relevantes en trastornos psiquiátricos, está influenciada por cambios en la metilación del promotor y por modificaciones en las histonas. 4). Se ha encontrado que la expresión de DNMT1 está significativamente incrementada en interneuronas GABAérgicas en cerebros de pacientes con esquizofrenia y trastorno bipolar.15,18
MODIFICACIONES DE LAS HISTONAS Y EL <<CÓDIGO DE LAS HISTONAS>>
Como se mencionó anteriormente, las histonas son las proteínas alrededor de las cuales el ADN se enrolla para su empaquetamiento. Las modificaciones epigenéticas que se llevan a cabo en ellas incluyen modificaciones covalentes por acetilación, metilación, fosforilación y adición de grupos ADP–ribosilos o moléculas pequeñas como ubiquitina o SUMO.5,19
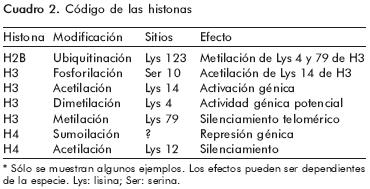
La adición de grupos acetilo ocurre sobre el aminoácido lisina: se ha detectado que aproximadamente 14% de las lisinas son susceptibles de acetilación.14 Los grupos metilo se unen en argininas y lisinas. Las distintas combinaciones de modificaciones covalentes son las que dan lugar a lo que se conoce como el <<Código de las histonas>> (cuadro 2).15
]]>
CONTRIBUCIÓN DE LOS ESTUDIOS EN GEMELOS AL ÁREA PSIQUIÁTRICA
La genética psiquiátrica es una disciplina cuyas estrategias no sólo están enfocadas a estudiar los factores hereditarios que predisponen a padecer trastornos mentales, sino también a comprender las interacciones genético–ambientales tomando como núcleo de estudio a la población, a la familia y en algunas ocasiones a los gemelos. Desde hace más de 20 años, numerosos estudios realizados con pares de gemelos MC y DC han mostrado que, para la mayoría de los trastornos mentales, una persona puede no presentar una enfermedad mientras que su gemelo idéntico o fraterno la padece.20
La búsqueda de explicaciones para estas diferencias ha sido el propósito central de muchas investigaciones; actualmente se cuenta con útiles herramientas como la genética molecular cuyo objetivo es identificar el o los cambios en la función de los genes, y la epidemiología psiquiátrica, que cuantifica el grado en el cual las diferencias individuales en el desarrollo de las enfermedades resultan de factores genéticos.21
Dos conceptos cobran importancia en los estudios genéticos con grupos de gemelos: la vulnerabilidad y la heredabilidad. El primero se refiere a la predisposición causada por un grupo de factores de riesgo genético y ambiental, cuya interacción determina si algún trastorno mental se presenta o no en un individuo. La heredabilidad es la proporción de varianza en la vulnerabilidad para el desarrollo de un trastorno que es debida a la influencia de los genes. Un valor de heredabilidad de cero (0%) indica que la vulnerabilidad se debe a factores ambientales; un valor de 1 (100%) indica que el desarrollo de un trastorno se puede explicar completamente por acción de los genes.
Los gemelos representan un grupo de estudio experimental natural muy útil sobre todo cuando se trata de un trastorno propiciado por variaciones en la función de los genes. Si los gemelos MC comparten 100% de la secuencia genética y los gemelos DC comparten 50%, entonces se espera que entre gemelos MC exista una mayor concordancia para un trastorno que entre los DC. Esto es justamente lo que se ha encontrado en las investigaciones que se han llevado a cabo.
Aunque los estudios en gemelos suelen catalogarse como <<genéticos>>, también nos dicen mucho acerca de las influencias de factores ambientales. No obstante, es importante considerar con cierta cautela los resultados de éstos, ya que las estimaciones de heredabilidad no representan hechos inmutables. El cálculo de heredabilidad en un trastorno depende de la muestra que se estudie, los genes involucrados en esa muestra y la naturaleza de los factores ambientales a los que los miembros de la muestra están expuestos en el momento determinado de la investigación.
El éxito de un estudio en gemelos comienza desde la correcta determinación de la cigocidad entre un hermano y otro, es decir, definir si éstos son MC o DC. Si la cigocidad es determinada erróneamente, los resultados carecerán de significado. Además, las inferencias que se hagan de resultados obtenidos en gemelos pueden ser inapropiadas para la población de no gemelos si los factores biológicos o psicosociales asociados específicamente con los gemelos son parte importante en el desarrollo del trastorno mental; por ejemplo, los gemelos presentan pesos más bajos al nacer y las madres sufren más frecuentemente complicaciones durante el embarazo. Por lo tanto, ya que hay diferencias sistemáticas entre los gemelos y los no gemelos, las estimaciones de heredabilidad en los primeros podrían no ser generalizables a los segundos.
]]> Sin embargo, la mayoría de los genetistas psiquiátricos consideran que los grupos de gemelos, junto con las personas dadas en adopción, pueden ser la mejor fuente de información para obtener evidencia de la importancia de los factores genéticos en los trastornos psiquiátricos.20El cuadro 3 es una recopilación de datos de investigaciones realizadas en diferentes tiempos y por diferentes autores para algunos trastornos mentales, y muestra los grados de concordancia y/o los porcentajes de heredabilidad calculados en grupos de gemelos monocigóticos y dicigóticos.
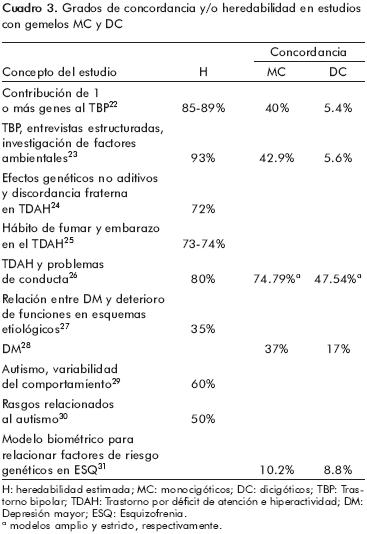
Como puede observarse, las heredabilidades estimadas para estos trastornos indican la importante influencia de los genes. Así mismo, los grados de concordancia entre gemelos MC son más altos que entre los DC, lo que refrenda lo anteriormente mencionado.
LA EPIGENÉTICA Y LAS EPIMUTACIONES EN LOS TRASTORNOS MENTALES
En esta sección presentamos tres ejemplos de trastornos mentales en los que se explican las formas en las que modificaciones epigenéticas podrían participan en su fisiopatología.
Trastorno bipolar. Se sabe que uno de los fármacos estabilizadores del ánimo, el valproato, es un inhibidor de la enzima HDAC, y que las histonas desacetiladas, en conjunto con el ADN no metilado, conllevan a la expresión de los genes. Se ha relacionado la eficacia del fármaco en el tratamiento del TBP con la actividad inhibitoria que ejerce, sugiriendo por tanto que una modificación epigenética (que reprime la transcripción de un gen) juega un papel importante en la manifestación de algunos síntomas del trastorno.12
Esquizofrenia. Quizá el ejemplo más estudiado en la esquizofrenia es la hipermetilación en los genes RELN y GAD67 en la corteza prefrontal, debida a la sobreexpresión de la DNMT1 en las interneuronas corticales GABAérgicas.
]]> RELN codifica para la reelina, que es una proteína importante en el desarrollo prenatal del Sistema Nervioso Central y en la modulación de la expresión de las neuronas piramidales corticales en el cerebro adulto.18 Regula la migración de las neuronas durante el desarrollo del encéfalo, resultando esencial para la correcta organización y plasticidad de la corteza cerebral.32 GAD67 es una de las dos formas moleculares de las enzimas sintetizadoras de GABA, el principal neurotransmisor inhibitorio en humanos.La hipermetilación de estos genes favorece la represión de la transcripción, ya sea por interferencia de los grupos metilo a los promotores de la transcripción o por unión de alguna proteína MBD. El resultado es la baja producción de reelina y de GAD67, característica típica que se ha encontrado en cerebros de pacientes con esquizofrenia.18
Autismo. La epigenética se refleja en este trastorno genético complejo junto con el síndrome de Rett (RTT) y el síndrome de Angelman (AS); estos dos últimos estados patológicos comparten características clínicas con el autismo, como retraso en el desarrollo, problemas de lenguaje y comportamientos estereotípicos. El RTT es causado por mutaciones en el gen MECP2 y el AS por deficiencia materna del cromosoma 15q11–q13, defectos en la metilación del ADN o mutación materna de la ligasa de ubiquitina–proteína E3A (UBE3A). Sin embargo, se han encontrado pacientes con AS y autismo que presentan mutaciones en MECP2; incluso para estos mismos trastornos se han demostrado defectos en la expresión de MeCP2 mediante el método de inmunofluorescencia cuantitativa en muestras de cerebro. La proteina MeCP2 es esencial para el desarrollo postnatal del cerebro en los mamíferos, de ahí que al disminuir su actividad baja el nivel de represión en la transcripción de ciertos genes y se conduce al desarrollo de RTT, AS o autismo.33
La participación de la epigenética en trastornos mentales se ejemplifica con los casos anteriormente citados, sin embargo es importante considerar un aspecto más. Durante la división mitótica, los cambios epigenéticos se transmiten de célula a célula (proceso conocido como sistema hereditario epigenético),34 pero en la gametogénesis estas modificaciones desaparecen aparentemente. Dicho lo anterior, se entiende el desarrollo de un trastorno psiquiátrico como el resultado, entre otros factores, de una serie de eventos epigenéticos desfavorables que se determinan cuando hay un error en la línea germinal durante la reprogramación epigenética. Estos errores se conocen como epimutaciones e incrementan el riesgo para padecer una enfermedad, pero no necesariamente la definen como inevitable. Pueden no causar ninguna manifestación clínica durante mucho tiempo, provocar cambios menores en el desarrollo cerebral y estar sujetas a variaciones posteriores probablemente durante la embriogénesis, la niñez o la adolescencia; incluso en la etapa de envejecimiento pueden volver a su estado normal y aparentar una disminución en la psicopatología o una recuperación parcial.35
CONCLUSIÓN
Cada trastorno mental tiene su propio esquema tanto etiológico como en cuanto a sus y características. La manifestación de alguno de ellos en una persona obedece a diversos factores ambientales y hereditarios.
Los grados de concordancia y los porcentajes de heredabilidad son sólo dos de los muchos indicios en la amplia gama de explicaciones ante las diferencias entre individuos <<idénticos>>.
Nos hemos valido de la epigenética, de las muchas combinaciones de los estados metilados y/o acetilados en la molécula del ADN, de las epimutaciones y de los estudios en gemelos para presentarla como una explicación probable de parte de las diferencias en la susceptibilidad a los trastornos mentales, de la misma manera en que lo hizo Esteller y su equipo en el 200536 al referirse al código epigenómico como el código físico y químico que proporciona las respuestas a las interrogantes en lo que a enfermedades en gemelos se refiere. Todo esto sin dejar de lado, por supuesto, la influencia ambiental de la que también existen numerosos estudios que sustentan su participación,25,37 sin embargo, quizá no esté fuera de lugar considerar que en algunos casos lo hacen en menor medida. En la actualidad, con el proyecto del Epigenoma Humano se pretende catalogar e interpretar por medio de una colaboración internacional los patrones de metilación a lo largo de todo el genoma, es decir, comprendiendo todos los genes humanos, en los principales tejidos. El futuro conocimiento de los patrones epigenéticos podría contribuir a identificar factores de riesgo para los trastornos mentales.38
]]> REFERENCIAS
1. Semsarian C, Seidman CE. Molecular medicine in the 21st Century. Intern Med J 2001; 31(1):53–59. [ Links ]
2. Hackett S, Feldheim K, Alvey M. Genes and genius: The inheritance of gregor mendel. DNA Cell Biol 2006; 25(12):655–658. [ Links ]
3. Rodenhiser D, Mann M. Epigenetics and human disease: Translating basic biology into clinical applications. CMAJ 2006; 174(3):341–348. [ Links ]
4. Stratakis C. Applications of genomic medicine in endocrinology and post–genomic endocrine research. Hormones (Athens Greece) 2005; 4(1):38–44. [ Links ]
5. Brero, A, Leonhardt H, Cardoso M. Replication and translation of epigenetic information. Curr Top Microbiol Immunol 2006; 301:21–44. [ Links ]
6. Tomassini C, Juel K, Holm N, Skytthe A, Christensen K. Risk of suicide in twins: 51 year follow up study. BMJ 2003; 327(7411):373–374. [ Links ]
7. Gilbert SF. Developmental biology. Sunderland: Sinauer Associates, Inc., 2000. [ Links ]
8. Derom C, Jawaheer D, Chen W, McBride K, Xiao X et al. Genome–wide linkage scan for spontaneous Dz Twinning Eur J Hum Gen 2006; 14(1):117–122. [ Links ]
9. Fraga M, Ballestar E, Paz M, Ropero S, Setien F et al. Epigenetic differences arise during the lifetime of monozygotic twins. Proc Natl Acad Sci USA 2005; 102(30):10604–10609. [ Links ]
10. Kato T, Iwayama Y, Kakiuchi C, Iwamoto K, Yamada K et al. Gene expression and association analyses of lim (Pdlim5) in bipolar disorder and schizophrenia. Mol Psychiatry 2005; 10(11):1045–1055. [ Links ]
11. Strachan T, Read AP. Human molecular genetics 2. London: Taylor & Francis, 1999. [ Links ]
12. Kato T, Iwamoto K, Kakiuchi C, Kuratomi G, Okazaki Y. Genetic or epigenetic difference causing discordance between monozygotic twins as a clue to molecular basis of mental disorders. Molecular Psychiatry 2005; 10(7):622–630. [ Links ]
13. Wong AH, Gottesman II, Petronis A. Phenotypic differences in genetically identical organisms. The epignetic perspective. H Mol Genet 2005; 14, número especial 1:R11–R18. [ Links ]
14. Neissa J, Guerrero C. Del código genético Al código epigenético: nuevas estrategias terapéuticas. Rev Fac Med Univ Nac Colomb 2004; 52(4):395–401. [ Links ]
15. Sharma R, Grayson D, Guidotti A, Costa E. Chromatin, DNA methylation and neuron gene regulation—the purpose of the package. J Psychiatry Neurosci 2005; 30(4):257–263. [ Links ]
16. Santos–Rebouças, C, Pimentel M. Implication of anormal epigenetic patterns for human diseases. Eur J Hum Gen 2007; 15:10–17. [ Links ]
17. Mayer W, Niveleau A, Walter J, Fundele R, Haaf T. Demethylation of the zygotic paternal genome. Nature 2000; 403(6769):501–502. [ Links ]
18. Dong E, Agis–Balboa R, Simonini M, Grayson D, Costa E et al. Reelin and glutamic acid decarboxylase67 promoter remodeling in an epigenetic methionine–induced mouse model of schizophrenia. Proc Natl Acad Sci U S A 2005; 102(35):12578–12583. [ Links ]
19. Jenuwein T, Allis C. Translating the histone code. Science 2001; 293(5532):1074–1080. [ Links ]
20. Faraone S, Tsuang M, Tsuang D. Genetics of mental disorders. New York: The Guilford Press, 1999. [ Links ]
21. Kendler K, Eaves L. Psychiatric genetics. Washington: American Psychiatric Publishing, Inc., 2005. [ Links ]
22. McGuffin P, Rijsdijk F, Andrew M, Sham P, Katz R et al. The heritability of bipolar affective disorder and the genetic relationship to unipolar depression. Arch Gen Psychiatry 2003; 60(497):502. [ Links ]
23. Kieseppä T, Partonen T, Haukka J, Kaprio J, Lönnqvist J. High concordance of bipolar I disorder in a nationwide sample of twins. Am J Psychiatry 2004; 161(10):1814–1821. [ Links ]
24. Martin N, Scourfield J, McGuffin P. Observer effects and heritability of childhood attention–deficit hyperactivity disorder symptoms. Br J Psychiatry 2002; 180:260–265. [ Links ]
25. Thapar A, Fowler T, Rice F, Scourfield J, Van Den Bree M et al. Maternal smoking during pregnancy and attention deficit hyperactivity disorder symptoms in offspring. Am J Psychiatry 2003; 160(11):1985–1989. [ Links ]
26. Thapar A, Harrington R, McGuffin P. Examining the comorbidity of adhd–related behaviours and conduct problems using a twin study design. Br J Psychiatry 2001; 179:224–229. [ Links ]
27. Foley D, Neale M, Gardner C, Pickles A, Prescott C et al. Major depression and associated impairment: Same or different genetic and environmental risk factors? Am J Psychiatry 2003; 160(12):2128–2133. [ Links ]
28. Scherrer J, Xian H, Bucholz K, Eisen S, Lyons M et al. A twin study of depression symptoms, hypertension, and heart disease in middle–aged men. Psychosom Med 2003; 65(4):548–557. [ Links ]
29. Spiker D, Lotspeich L, Dimiceli S, Myers R, Risch N. Behavioral phenotypic variation in autism multiplex families: Evidence for a continuous severity gradient. Am J Med Genet 2002; 114(2):129–136. [ Links ]
30. Sung Y, Dawson G, Munson J, Estes A, Schellenberg G et al. Genetic investigation of quantitative traits related to autism: use of multivariate polygenic models with ascertainment adjustment. Am J Hum Genet 2005; 76(1):68–81. [ Links ]
31. Cardno A, Rijsdijk F, Sham P, Murray R, McGuffin P. A twin study of genetic relationships between psychotic symptoms. Am J Psychiatry 2002; 159(4):539–545. [ Links ]
32. Botella L, Burgaya F, Gavín M, Garcéa–Ayllón S, Gómez–Tortosa E et al. Reelin expression and glycosylation patterns are altered in Alzheimer's disease. Proc Natl Acad Sci U S A 2006; 103:(14): 5573–5578. [ Links ]
33. Samaco R, Hogart A, Lasalle J. Epigenetic overlap in autism–spectrum neurodevelopmental disorders: Mecp2 deficiency causes reduced expression of Ube3a and Gabrb3. Hum Mol Genet 2005; 14(4):483–492. [ Links ]
34. Maynard, S. Models of a dual inheritance system. J Theor Biol 1990; 143:41–53. [ Links ]
35. Petronis A. The origin of schizophrenia: Genetic thesis, epigenetic antithesis, and resolving synthesis. Biol Psychiatry 2004; 55(10):965–970. [ Links ]
36. Qiu J. Epigenetics: Unfinished symphony. Nature 2006; 441(7090):143–145. [ Links ]
37. Hakkarainen R, Johansson C, Kieseppa T, Partonen T, Koskenvuo M et al. Seasonal changes, sleep length and circadian preference among twins with bipolar disorder. BMC Psychiatry 2003; 3(6):1–7. [ Links ]
38. Pérez–Rincón H. Genealogías, herencias, historias. Archivos Psiquiatría 2004; 67(4):261–278. [ Links ] ]]>