
Identificación y Control Químico de los Agentes Causales de la Mancha Foliar y la Cenicilla del Tomatillo (Physalis ixocarpa Brot.) en el Norte de Sinaloa, México
Identification and chemical control of the causal agents of leaf spot and powdery mildew of husk tomato (Physalis ixocarpa Brot.) in northern Sinaloa, Mexico
Rubén Félix-Gastélum1, Jeován Alberto Ávila-Díaz2, Beatriz Odette Valenzuela-Cota3, José Ángel Trigueros-Salmerón1 y Rosa María Longoria-Espinoza4
1 Universidad de Occidente, Unidad Los Mochis, Depto. de Biología, Blvd. Macario Gaxiola y Carretera Internacional s/n, Los Mochis, Sinaloa, México CP 81223. Correspondencia: rfelix@mochis.udo.mx.
2 Lázaro Cárdenas del Río s/n, Ejido Bachomobampo No. 1, Ahorne, Sinaloa CP 81372.
]]> 3 Agridiagnósticos, Allende No. 5 11 Nte., Los Mochis, Sinaloa CP 81200.4 Universidad de Occidente, Unidad Guasave, Depto. de Ciencias Biológicas, Av. Universidad s/n, Guasave, Sinaloa, México.
Recibido: Mayo 31, 2006
Aceptado: Agosto 24, 2006
Resumen
En ciclos agrícolas recientes, la mancha foliar y la cenicilla han cobrado importancia económica en el cultivo de tomatillo en el norte de Sinaloa, México. El presente estudio tuvo como objetivos: a) identificar los agentes causales de dichas enfermedades, b) determinar la sensibilidad de los agentes causales a tres fungicidas in vitro y c) determinar la efectividad biológica de cinco fungicidas en el control de estas enfermedades en condiciones de campo. Las características morfológicas del hongo asociado a la mancha foliar del tomatillo corresponden al hongo Cercospora sp., el cual resultó patogénico al cultivo en inoculaciones artificiales en condiciones de invernadero. Por otro lado, las características morfométricas de las estructuras de origen asexual e imágenes al microscopio electrónico de barrido de los conidios permitieron determinar que el hongo causante de la cenicilla del tomatillo es Podosphaera (Sphaeroiheca) xanthii. Los fungicidas azoxystrobin, trifloxystrobin y tebuconazole inhibieron en un 100% la germinación de los conidios de Cercospora sp. in vitro a las dosis de 0.02,0.1 y 30.0 ppm, respectivamente; mientras que el crecimiento micelial se inhibió en forma marcada con los mismos fungicidas a las dosis 1.5, 0.1 y 5.0 ppm, respectivamente. Tres aplicaciones preventivas en intervalos semanales de tebuconazole (Folicur® 0.6 L/ha), trifloxystrobin (Flint® 250 g/ ha), clorotalonil (Bravo® 720 2.5 L/ha) y benomilo + mancozeb (Benlate® + Mancozeb® 500 g/ha + 2.0 kg/ha) ejercieron un excelente control contra la mancha foliar y la cenicilla. Los resultados del presente estudio permitirán un control eficiente de estas enfermedades en mención en el norte de Sinaloa, y otras áreas productoras de tomatillo en el país.
Palabras clave: Enfermedades fungosas, Podosphaera xanthii, Cercospora sp., fungicidas, características morfométricas.
]]> Abstract
In recent growing seasons, leaf spot and powdery mildew have become economically important diseases in husk tomato in northern Sinaloa, Mexico. The objectives of this study were to: a) identify the causal agents of these two diseases, b) determine the sensitivity of the causal agents to three fungicides in vitro, and c) determine the biological efficacy of five fungicides to control these diseases under field conditions. The morphology of asexual structures of the fungus associated with leaf spot of husk tomato coincide with those reported for the genus Cercospora; which was pathogenic to husk tomato under artificial inoculation in the greenhouse. The morphometric characteristics of sexual structures and images of conidia under the scanning electron microscope indicated that the causal agent of powdery mildew of husk tomato was Podosphaera (Sphaerotheca) xanthii. In vitro, azoxystrobin, trifloxystrobin. and tcbuconazole inhibited 100% conidial germination of Cescospora at the rates at 0.02, 0.1. and 30.0 ppm. respectively. The same fungicides at the rates of 1.5, 0.1, and 5.0 ppm markedly inhibited mycclial growth. Three spray applications at weekly intervals of tebuconazole (Folicur® 0.6 L/ha), trifloxystrobin (Flint® 250 g/ha), chlorothalonil (Bravo® 720 2.5 L/ha) and benomyl + mancozcb (Benlate® + Mancozeb® 500 g/ha + 2.0 kg/ha) provided an excellent control of leaf spot and powdery mildew. The results of this study will allow growers to control both diseases efficiently in northern Sinaloa and in other husk tomato growing regions of Mexico.
Keywords: Fungal diseases, Podosphaera xanthii, Cercospora sp., fungicides, morphometric characteristics.
El tomatillo (Physalis ixocarpa Brot.) es uno de los principales cultivos en Sinaloa, México, en el ciclo agrícola otoño-invierno de 2003-2004. ocupó una superficie de 16.256 ha. de las cuales el 79% se sembró en el norte del estado (CAADES. 2004). La producción y calidad de este cultivo se ven afectados por enfermedades de origen fungoso y viral. La etiología de algunas enfermedades virales ha sido determinada en algunas zonas productoras de la República Mexicana; al respecto. De la Torre-Almaráz et al. (2003). consignaron en los estados de México. Morelos y Puebla al virus del jaspeado del tabaco (TEV), virus mosaico del pepino (CMV), virus marchitez manchada del tomate (TSWV). virus mancha necrótica del impaciente (INSV). virus mancha anular del tabaco (TRSV) y virus mosaico del tabaco (TMV); en tanto que Smith et al. (2002) reportan en los cultivos de tomatillo en California, EUA, el virus del mosaico del pepino (CMV). el virus del mosaico de la alfalfa(AMV), el virus Y de la papa(PVY)y el virus del mosaico del tabaco (TMV). Así mismo. Peña-Lomelí (2001) reporta en el estado de México a Oidium spp. y Entyloma australe Speg como agentes causales de la cenicilla y el carbón del tomatillo, respectivamente; el autor indica que estas enfermedades son importantes, pues reducen el ciclo vegetativo, lo cual limita la producción. En ciclos agrícolas recientes, el tomatillo se ha visto afectado por enfermedades foliares que originan pérdidas en la producción y calidad del fruto en el norte de Sinaloa. Observaciones preliminares indican que dichas enfermedades podrían ser ocasionadas por hongos, pero no existe investigación científica que lo sustente. El desconocimiento de la etiología de las enfermedades foliares y del fruto en tomatillo, ha propiciado que se realicen aplicaciones ineficaces de fungicidas para su control. Por tal motivo, en el presente estudio se plantearon los siguientes objetivos: a) identificar los agentes causales de la mancha foliar y del fruto y la cenicilla del tomatillo en el norte de Sinaloa y b) determinar la efectividad biológica in vitro y en campo de algunos fungicidas para su control.
MATERIALES Y MÉTODOS
Experimentos de laboratorio. Identificación del agente causal de mancha foliar y del fruto del tomatillo. Seis muestras de tomatillo con síntomas de origen fungoso, que consistieron en lesiones de color café oscuro, con círculos concéntricos en hojas y cáliz de los frutos, se colectaron en un número igual de lotes comerciales de tomatillo en el norte de Sinaloa (Valles del Fuerte y del Carrizo) y se colocaron en bolsas de polietileno para trasladarse al laboratorio. A partir de las lesiones se efectuaron preparaciones de conidióforos y conidios, mediante una cinta adhesiva transparente misma que fue presionada sobre la lesión y luego colocada sobre un portaobjetos al que previamente se le depositó una gota de agua destilada. Para la identificación a nivel género del hongo asociado en forma consistente al tejido sintomático, se utilizaron las claves taxonómicas de Barnett y Munter (1972) y la descripción del género Cercospora por otros autores (García et al., 1996; Mya-Thaung, 1984). Aislamiento y pruebas de patogenicidad con el hongo asociado a la mancha foliar y del fruto del tomatillo. El aislamiento del hongo asociado al tejido sintomático se llevó a cubo mediante el frotamiento suave de los conidios presentes en lesiones en hojas y cáliz de fruto, con una porción de medio de cultivo agar-agua (AA) bajo el microscopio estereoscópico (Fisher Scientific. modelo SPT-ITH), lo que permitió transferir dichas estructuras a cajas de Petri con el mismo medio de cultivo e incubarlas por 12 h a temperatura de laboratorio (25 ± 2°C). Doce horas después de la siembra, se transfirieron puntas de hifas a papa-dextrosa-agar (PDA) donde se desarrollaron colonias del hongo. Para determinar su patogenicidad. el hongo se transfirió a PDA y doce días después de la siembra se cortaron fragmentos de 0.5 cm de diámetro del margen de las colonias, de seis aislamientos procedentes del cultivo de un número igual de lotes comerciales del norte de Sinaloa. Cuatro fragmentos de micelio se utilizaron por cada aislamiento los cuales se colocaron en el envés de un número igual de hojas del tercio medio de una planta de tomatillo var. Orizaba, en la etapa de floración. Las plantas se cubrieron con bolsas de polietileno para generar humedad relativa de 100%, donde la temperatura promedio fue de 25 ± 2°C durante las primeras 72 h de incubación; en los siete días subsiguientes, las plantas inoculadas se incubaron en las condiciones de humedad anteriormente mencionadas solamente durante la noche, mientras que durante el día se incubaron a temperatura y humedad ambiente. Diez días después de la inoculación se reaisló el hongo de las lesiones similares a aquéllas que se observaron en campo. Identificación del agente causal de la cenicilla en tomatillo. Seis muestras con síntomas de origen fungosos que consistieron en lesiones blanquecinas y aspecto polvoso en el haz de hojas, tallo y cáliz de los frutos de tomatillo se colectaron en un número igual de lotes comerciales de dicho cultivo en el norte de Sinaloa durante el ciclo agrícola 2003-2004 y se colocaron en bolsas de polietileno para trasladarse al laboratorio, se conservaron en un refrigeradora 5-7°C para su análisis, el cual se practicó en un período menor a 48 h después de su colecta. A partir de las lesiones en tallo, hojas y cáliz de frutos, se efectuaron preparaciones de conidióforos y conidios mediante una cinta adhesiva transparente, misma que fue presionada sobre la lesión y luego colocada sobre un portaobjetos, al que previamente se le depositó una gota de agua destilada. Se midió el diámetro del micelio, longitud del conidióforo, longitud y diámetro de la célula basal del mismo, así como la longitud y diámetro de los conidios desprendidos del conidióforo. El diámetro del micelio se dieterminó en la segunda o tercera célula a partir de la base del conidióforo. De acuerdo a Boesewinkcl (1980), se consideró como conidióforo, al segmento comprendido desde el septo de la célula basal hasta el último septo de la célula no hinchada del mismo. La longitud de la célula basal del conidióforo se midió desde la primera septa basal hasta la primera septa del conidióforo y el diámetro de la misma se determinó en su parte media. Para detectar la presencia de cuerpos de fíbrosina en el interior de los conidios, se tomaron muestras de ellos a partir de hojas, frutos y tallos infectados, mediante una cinta adhesiva transparente y se colocaron directamente en una gota de hidróxido de potasio al 3% sobre un portaobjeto (Kable et al., 1963). Con el fin de determinar las características del tubo germinativo, los conidios se desprendieron del tejido infectado mediante un pincel ce cerdas suaves y se esparcieron sobre un portaobjetos, el cual se incubó durante 96 h a 100% de humedad relativa a temperaturas de 23 ± 2°C; después se determinó la forma y el diámetro del tubo germinativo en su parte media. En cada muestra se midieron 50 especímenes representativos de cada estructura somática o reproductivas, obteniéndose el promedio y la desviación estándar de cada variable. Fotografías de conidios del hongo de la cenicilla al microscopio electrónico de barrido. Fragmentos de hojas de tomatillo con síntomas característicos de cenicilla se fijaron por 48 h en FaA (35% agua destilada, 10% formaIdeh¡do, 5% ácido acética, 50% alcohol etílico al 96%) Las muestras se lavaron con ac.ua corriente por 10 min y posteriormente se deshidrataron en una serie de etanoles graduales (Ruzin, 1999). Seguidamente se desecaron a punto crítico con CO, en un desecador (BAL-TEC CPD030); después se montaron en portamuestras de aluminio sobre cinta conductiva de carbón y se cubrieron con una fina capa de orcen una ionizadora (Dentón Vacuum Desk II). Finalmente las observaciones y toma de placas fotográficas se hicieron en microscopio electrónico de barrido (JEOL JSM-5310 LV) (Bozzola y Russcll. 1999). Efectividad. biológica de azoxystrobin, trifloxystrobin y tebuconazole en la inhibición de la germinación de conidios in vitro de Cercospora sp. Los conid ios de Cercospora sp. se colectaron de lesiones en hojas de planta de tomatillo, previamente inoculadas e incubadas.cn cámara húmeda durante 10 días a 26 ± 2°C. Los conidios se desprendieron mediante el frotamiento suave de las lesiones con un disco de AA de 0.5 cm de diámetro, el cual se desfizó sobre placas de Petri con medio AA + azoxystrobin, trifloxystrobin o tebuconazole a las dosis de 0.0,0.02,0.1,1.5, 2.0.3.0,4.0,5.0,6.0,7.0,10.0,20.0 ó 30.0 ppm. Los tratamientos se distribuyeron en un arreglo completamente al azar con cuatro repeticiones. Cada repetición consistió en una caja de Petri con 250 ± 20 conidios; las siembras se incubaron a 25 ± 2°C durante 12 h, para después determinar el porcentaje de germinación en 100 conidios bajo el microscopio compuesto (Carl Zeizz, Serie 470801 -9097). Se consideraron como conidios germ¡nados cuando longitud del tuto germinativo superó al diámetro mayor de cada conidio. Les datos se sometieron a análisis de varianza y separación de medias utilizando el procedimiento de Tukey (Little y Hills. 1973) previa transformación a la forma Arc sen-1 √x + 0.05. Efectividad biológica de azoxystrobin, trifloxystrobin o tebuconazole en la inhibición del desarrollo micelial in vitro de tres aislamientos de Cercospora sn. Se obtuvieron discos de PDA de 0.5 cm de diámetro con crecimiento activo del hongo a partir de colonias de 12 días de edad y se transfirieron a medio de cultivo PDA conteniendo0.0,0.02, l.S.2.0,3.0,4.0,5.0,6.0,7.0.10.0ó20j0 ppm de azoxystrobin. trifloxystrobin o tebuconazole. Para ello, el medio se esterilizó a 15 Ib durante 15 min, una vez enfriado a temperatura cercana a los 45°C, se adicionó cada uno de les fungicidas por separado y se dispensó en cajas de Petri. Posteriormente, los aislamientos se incubaron a 25 ± 2°C. Cuando el crecimiento micclial en el medio sin fungicida cubrió 50% del medio de cultivo en las placas de Petri, se determinó el diámetro de las colonias. Los tratamientos se distribuyeron en un arreglo completamente al azar con tres repeticiones (tres cajas de Petri por tratamiento). Los datos de la variable diámetro de colonias se sometieron a análisis de varianza, previa transformación a la forma vx+1, para finalmente realizar la separación de medias de acuerdo al procedimiento de Tukey (Little and Hill.1973).
Efectividad biológica de cinco fungicidas en el control de h mancha foliar y del fruto, y cenicilla del tomatillo en campo. Los experimentos de campo para determinar la efectividad biológica de cinco fungicidas [Tebuconazole (Folicur®) 0.6 L/ ha; Trifloxystrobin (Flint®) 250 g/ha; Clorotalonil (Bravo® 720) 2.5 L/ha; Bcnomilo + Mancozcb (Benlate®+Mancozcb®) 500 g/ha + 2.0 kg/ha; Propiconazol (Tilt®) 0.5 L/ha: Testigo sin aplicación], en el control de enfermedades foliares en tomatillo, se estableció en un lote experimental del Ejido Benito Juárez, Ahorne. Sinaloa. Se utilizó un diseño experimental de bloques completos al azar con cinco tratamientos y un testigo sin aplicación con cuatro repeticiones. Las unidades experimentales consistieron de tres surcos de tomatillo var. San Juanito con una separación de 1.6 m por 7.0 m de longitud. Con el objetivode exponer al cultivo al mayor número posible de enfermedades fungosas, el experimento se estableció en una etapa intermedia de siembra, en la segunda semana de octubre. El enfoque de los tratamientos fue preventivo y se iniciaron a los 40 días después del trasplante y continuando a intervalos de siete días, hasta realizar un total de tres de ellas durante el período experimental. Las aplicaciones se realizaron con una aspersora motorizada Arimitsu con un aguilón de cuatro boquillas de cono hucco No. 6X Conc Jet, previamente calibrada, donde el gasto de agua varió de 360 a 477 L/ha. Las evaluaciones de eficacia se realizaron a los siete días despjés de cada aplicación, tomando 20 hojas al azar del tercio inferior en 20 plantas del surco central de cada unidad experimental. Para la evaluación de efectividad biológica de los tratamientos se recurrió a los siguientes índices de daño: 0 = hoja sana, 1 = hoja con 1 -10% de área foliar afectada (AFA), 2 - hoja con 11 -20% de AFA. 3 = hoja con 21 -40% deAFA, 4 = hoja con 41 -60% de AFA y 5 = hoja con 60% o más de AFA. I.os datos ya categorizados se sustituyeron en la fórmula de Townsend y Heuberger (1943). que indica: % de infección = (Σni vi/ NV) x 100: donde ni representa el número de hojas en cada categoría; vi valor numérico de cada categoría; N, número total de hojas en la muestra y V valor de la categoría más alta. Los porcentajes de infección en hojas, expresados en AFA, que se obtuvieron mediante la sustitución de datos en la fórmula antes descrita, se transformaron a la forma Arc sen-1 √x+0.05 para finalmente someterlos a análisis de varianza y comparaciones de medias utilizando la prueba de Tukey (p - 0.05) (Little y Hills. 1973).
]]>RESULTADOS
Características de las estructuras de origen asexual del hongo, asociado a la mancha foliar y del fruto del tomatillo y pruebas de patogenicidad. El hongo asociado en forma consistente a la mancha foliar de tomatillo, no presentó micelio externo ni estroma; los conidióforos fueron simples, oscuros, agrupados en fascículo, rectos, lisos, cilindricos con cicatrices conspicuas de color pardo-oscuro ubicadas en los ápices. Los conidios se localizaron de forma individual, hialinos, filiformes, lisos con cicatriz conspicua (engrosada) en la base truncada, ápice obtuso, 2-10 septos (Figs. 1A y B) y presentaron tubos germinativos en ambos extremos en los inicios de proceso de germinación, aunque posteriormente también se originaron en el resto de las células de los conidios. Las características morfológicas de las estructuras de origen asexual del hongo correspondieron al género Cercospora (Barnett y Hunter, 1972; García et al., 1996; Mya-Thaung, 1984). Las pruebas de patogenicidad con seis aislamientos de Cercospora sp., permitieron la inducción de síntomas similares a los observados en campo en hojas de tomatillo a los diez días después de la inoculación. Observaciones al microscopio, permitieron constatar la presencia del hongo que se inoculó originalmente en las plantas sanas; además de que el organismo se rcaisló en AA de tejido sintomático y se lograron colonias en PDA idénticas a aquéllas que se utilizaron para la inoculación. Morfometría de las estructuras asexuales del hongo asociado a la cenicilla del tomatillo. En todas las muestras la fase asexual correspondió al género Oidium (Barnett and Hunter, 1972; Yarwood. 1973). En el Cuadro 1 se indican las dimensiones de las estructuras de origen asexual del hongo en seis colectas del mismo en el norte de Sinaloa. El micelio superficial y hialino tuvo un diámetro promedio de 7.4-8.0 pm. Los conidióforos, simples y rectos estuvieron constituidos de 2-4 células predominando aquéllos con un número de tres. Los conidióforos presentaron los márgenes crenados y cadenas de 2-7 conidios (Fig. 2). La longitud promedio del conidióforo fue de 99.8-122.2 µm; su célula basal fue recta, cilindrica, sin hinchamiento, con una longitud de 62-79 µm y un diámetro en la parte media de 12.5-13.0 µm. Los conidios fueron predominantemente ovoides, pero ocasionalmente en forma en barril; midieron de 4 1.0-43.3 pm de largo y de 20.9-22.8 ìm de diámetro; la presencia de cuerpos de fíbrosina en el interior de éstos fue consistente, aunque de forma y tamaño variable (Fig. 3A). El tubo germinativo, corto, con un diámetro en su parte media de 7.4- 7.6 pm se originó generalmente a partir de la parte media del conidio y en ocasiones se orientó paralelo al eje longitudinal de éste o se bifurcó (Fig. 3B). Estas características, además del estudio morfométrico de las estructuras asexuales coinciden con las indicadas para el anamorfo de Podosphaera (sect. Sphaerotheca) xanthii (Castagne) U. Brawn y N. Shishkoff. Microscopía Electrónica de barrido de conidios del hongo asociado a la cenicilla del tomatillo. La superficie de la pared de los conidios es lisa (Fig. 4A). aunque con ligeras ondulaciones; la superficie de la parte terminal de los mismos, la cual representa la ubicación del septo que separa a los conidios cuando forman cadenas, mostraron anillos concéntricos tenues (Fig. 4B), y los conidios deshidratados presentaron un arrugamiento que originó líneas sinuosas longitudinales y en algunas ocasiones transversales.



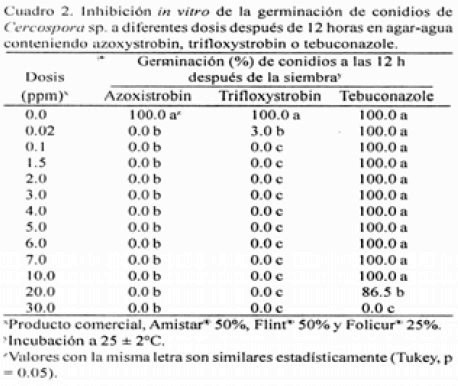
Efectividad biológica de azoxystrobin, trifloxystrobin y tebuconazole, en la inhibición de la germinación in vitro de conidios de Cercospora sp. El 100% de los conidios de Cercospora sp. germinaron a las 12 h después de la siembra en PDA sin fungicida. En contraste, no ocurrió germinación cuando se sembraron en el mismo medio de cultivo conteniendo Azoxystrobin a las dosis de 0.02, 0.1. 1.5, 2.0, 3.0.4.0. 5.0,6.0, 7.0. 10.0,20.0 y 30 ppm. La inhibición de la genni nación de los conidios en PDA con Trifloxystrobin a las mismas dosis resultó similar, pues sólo el 3% germinó en la dosis de 0.02 ppm y no ocurrió germinación en el resto de las dosis, detectándose diferencias significativas (p = 0.05) entre los tratamientos y el testigo sin aplicación. En contraste, el porcentaje de germinación de los conidios en medio de cultivo más tebuconazole fue del 100% en la dosis de 0.02 a 10 ppm. al igual que en el testigo sin fungicida, mientras que en la dosis de 20 ppm fue de 86.5% y no ocurrió germinación a la dosis de 30 ppm. con diferencias significativas (p = 0.05) entre los tratamientos y el testigo sin fungicida (Cuadro 2).
]]>
Efectividad biológica de azoxystrobin, trifloxystrobin y tebuconazole en la inhibición del desarrollo micclial in vitro de Cercospora sp. Azoxystrobin no ejerció un marcado efecto inhibitorio en el desarrollo micelial en los tres aislamientos de Cercospora sp. a la dosis de 0.02 ppm. pero dicho efecto fue evidente a partir de la dosis de 1.5 ppm y se incrementó gradualmente en forma paralela al aumento de las dosis hasta llegar a 7.0. 10.0 y 20.0 ppm donde el crecimiento micelial varió de 1.0 a 1.1 cm de diámetro, sin diferencias significativas (p = 0.05) entre estos tratamientos (Cuadro 3). A diferencia del fungicida azoxystrobin. trifloxystrobin ejerció un efecto fungistático marcado contra los tres aislamientos de Cercospora sp. a partir de la dosis de 0.02 ppm: el análisis estadístico mostró diferencias significativas (p = 0.05) entre el diámetro de las colonias miceliales de los tres aislamientos del patógeno y el diámetro de aquéllas que se desarrollaron en medio de cultivo sin el fungicida; a su vez, el diámetro del crecimiento micelial de los aislamientos en las dosis de 0.1 a 20 ppm, varió de 0.6 a 0.8 cm sin diferencia significativas entre las dosis, pero si se presentaron con respecto al diámetro de las colonias testigo y aquéllas que se desarrollaron en la dosis de 0.02 ppm (Cuadro 4). Con respecto al fungicida tebuconazole, el diámetro de las colonias miceliales de Cercospora sp. a la dosis de 0.02 ppm y en medio de cultivo sin fungicida, no mostró diferencias significativas (p = 0.05); el efecto inhibitorio sobre el hongo fue mas evidente a partir de las dosis de 0.1 ppm, particularmente en el aislamiento Carrizo 1. La inhibición del desarrollo micclial aumentó en forma paralela con el incremento de las dosis del producto hasta llegar a 6.0 ppm, donde el diámetro del crecimiento micclial varió de 1.7 a 1.8 cm en los tres aislamientos del hongo; a su vez. el diámetro de las colonias de los tres aislamientos no fue significativamente diferente (p = 0.05) en las dosis de 6.0,7.0, 10.0 y 20.0 ppm, donde en la última dosis el crecimiento micelial varió de 1.3 a 1.4 cm de diámetro (Cuadro 5). Se demostró el efecto fungistático de los tres fungicidas, pues al transferir los aislamientos a PDA sin las moléculas, éstos reactivaron su crecimiento.



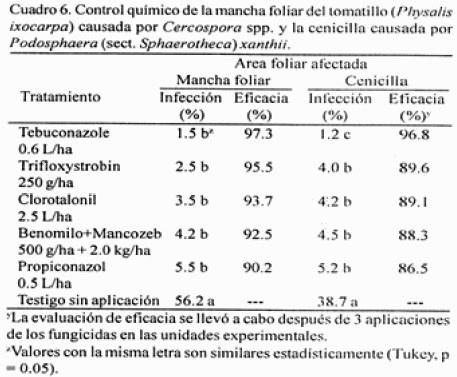
Efectividad biológica de cinco fungicidas en el control de la mancha foliar y del fruto, y la cenicilla del tomatillo en campo. En la evaluación final de eficacia cuando el cultivo se encontraba en la etapa de cosecha, el AFA por la mancha foliar causada por Cercospora sp. en las parcelas aplicadas con tebuconazole, trifloxystrobin, clorotalonil, benomilo + mancozeb y propiconazol, varió de 1.5 a 5.5% sin diferencias significativas (p = 0.05) entre tratamientos, pero si se observaron con respecto al testigo sin aplicación, las cuales presentaron una AFA de 56.2%. La eficacia Abbot (1925) varió de 90.2 a 97.3%, donde sobresalió tebuconazole con la mayor eficacia en el control de la mancha foliar del tomatillo causada Cercospora sp. (Cuadro 6). En esta misma evaluación de eficacia, el AFA por cenicilla causada por P. xanthii en las unidades experimentales que se aplicaron con tebuconazole fue de 1.2% y hubo diferencias significativas (p = 0.05) con respecto al daño en las parcelas que se aplicaron con trifloxystrobin, benomilo + mancozeb, propiconazol y clorotalonil, donde el AFA varió de 4.0 a 5.2%; a su vez, estos tratamientos fueron significativamente diferentes al testigo sin aplicación donde la infección final de cenicilla fue de 38.7%. La eficacia Abbot de los fungicidas en el control de la cenicilla varió de 86.5 a 96.8%.
]]>
DISCUSIÓN
Las estructuras del hongo asociado en forma consistente a la mancha foliar y del fruto del tomatillo, corresponden al genero Cercospora (Barnett and Hunter, 1972; García et al., 1996; Mya-Thaung, 1984). Las pruebas de patogenicidad utilizando fragmentos de micelio, demostraron que Cercospora sp. es el agente etiológicode la enfermedad en tomatillo, pues causó síntomas similares a los observados en campo. Este hallazgo es relevante, pues la incidencia de esta enfermedad se ha incrementado en ciclos agrícolas recientes, lo que afecta el rendimiento y calidad de la producción; adicionalmente, los técnicos de campo asumían que la enfermedad era causada por el hongo Alternaría spp. lo que conducía a la utilización de fungicidas inapropiados para su control. Con respecto a la cenicilla del tomatillo, la fase asexual correspondió al genero Oidium (Barnett and Hunter, 1972; Yarwood. 1973) y al subgénero Fibroidium (Cook et al., 1997). Las dimensiones, el tipo y la forma de los conidióforos y de los conidios, la presencia de cuerpos de fibrosina en los conidios, asi como la formación de tubos germinativos cortos, robustos y raras veces bifurcados (Boesewinkel, 1980; Hammett, 1977; Hyeon-Dong and Yong-Joon, 1993; Reifschneider et al., 1985; Vanhaarveld. 1984; Zaracovitis. 1965; Zitter et al., 1996), permitieron identificar al hongo asociado a la cenicilla del tomatillo como el an amorfo de Podosphaera (sect. Sphaerotheca) xanthii (Castagne) U. Braun y N. Shishkoff. anteriormente conocida como Sphaerotheca fuliginea (Schclechtend:Fr.) Pollacci y S. fusca (Fr.) S. Blumer. La identidad de la especie también se sustenta mediante fotografías al microscopio electrónico de barrido, lo que permitió observar la pared lisa (Hammett, 1977), aunque con ligeras ondulaciones de los conidios; además, la parte terminal de los mismos presentó anillos concéntricos tenues (Cook et al., 1997) confirmándose así la identidad del hongo. En ausencia de la fase sexual del patógeno, los márgenes erenados de los conodióforos y la presencia de cuerpos de fibrosina en los conidios, complementan la identificación de P. xanthii en su fase asexual, pues representan una característica taxonómica estable en la identificación del liongo en aquellos hospedantes donde no se presenta su fase sexual, como ocurre en tomatillo. Sin embargo, es importante señalar que la presencia de dichas inclusiones está influenciada por las condiciones ambientales (Zitter et al., 1996). además de que éstas desaparecen en conidios germinados y es difícil o imposible encontrarlos en especímenes conservados en herbarios (Boescwinkel, 1980). En la presente investigación se observó que los primeros sintonías de cenicilla. se observaron primeramente en el follaje del tercio inferior de las plantas, tal como ocurre en cucurbitáceas, donde los períodos con alta humedad relativa son más prolongados. Al respecto, estudios realizados en Nueva Zelanda (Cheah et al., 1996). indican que los conidios de P. xanthii germinan entre 15 y 30°C con una temperatura óptima de 25°C y humedad relativa = 95%. Estas condiciones climáticas se presentan de noviembre a marzo en el norte de Sinaloa. donde ocurren epidemias de cenicilla en tomatillo. En otros países se consignó a P. xanthii como el agente causal de la cenicilla en especies de las familias Cruciferae. Malvaceae. Leguminosae y Solanaceae (Boesewinkel. 1980); de ellos, el frijol (Phaseolus vulgaris L.), el tomate y la berenjena (Solanum melongena L.) son cultivos de importancia económica en Sinaloa y dentro de éstos resalta el tomatillo como cultivo de importancia económica en la región. Con base en lo anterior se abren nuevas líneas de investigación: dentro de ellas el determinar si P. xanthii de tomatillo ataca a cucurbitáceas y viceversa, pues este conocimiento es de importancia para el manejo de la enfermedad. En México, P. xanthii se a consignado en calabaza (Cucurbita pepo L.) en Aguascalicntes (Moreno-Rico y Romero-Coba, 1992) y melón (Cucumis meto L.) en La Comarca Lagunera (Hernández y Cano. 1990) y varias cucurbitáceas cultivadas en el norte de Sinaloa (Félix-Gastélum et al., 2005). Es importante señalar que este es el primer estudio donde se determinó la asociación consistente de P. xanthii en tomatillo, y aún cuando no se realizaron pruebas de patogenicidad se infiere que este parásito obligado es el agente causal de la enfermedad. Con relación a los estudios de efectividad in vitro, los fungicidas azoxystrobin, trifloxystrobin y tebuconazole ejercieron, particularmente los dos primeros, un excelente efecto inhibitorio en la genninación de los conidios de Cercospora sp. agente causal de la mancha foliar del tomatillo, lo que indica que si estos productos se utilizan en forma preventiva en campo ejercerán un control aceptable contra la enfermedad. De igual fonua. los fungicidas azoxystrobin y trifloxystrobin ejercieron un marcado efecto inhibitorio en el desarrollo micelial del mismo patógeno a las concentraciones de 2.0 a 20.0 ppm, en cambio tebuconazole ejerció un efecto inhibitorio evidente a partir de la dosis de 20.0 ppm, lo que indica que estos productos pueden ejercer un efecto curativo contra la enfermedad. Los experimentos en campo indicaron que los fungicidas tebuconazole, trifloxystrobin, la mezcla benomilo + mancozeb y clorotalonil, ejercieron un excelente control contra la mancha foliar del tomatillo, lo cual confirmó los resultados de las pruebas in vitro de los dos primeros fungicidas. En estudios futuros será importante definir el número adecuado de aplicaciones y la etapa fenológica ideal del tomatillo para el inicio de dichas aplicaciones, para controlar la enfermedad de una manera eficiente. Se observó además, que los mismos fungicidas ejercen un excelente control contra la cenicilla del tomatillo causada por P. xanthii, Estos resultados indican que los productores pueden recurrir a dichos fungicidas para el manejo de ambas enfermedades en lotes comerciales. Es importante señalar que en algunas áreas productoras de cucurbitáceas, se ha reportado resistencia en P. xanthii a los fungicidas, tales como benomilo (McGrath et al ., 1996; Shroeder y Provvidenti, 1969), triadimefon (McGrath, 1991) y azoxystrobin (McGrath, 2001 ), por lo anterior se justifica la conducción de estudios orientados hacia la determinación de sensibilidad del hongo a estos fungicidas, ya que con frecuencia se utilizan para el control del patógeno en Sinaloa y otras áreas productoras de tomatillo. Con respecto a la variación genética de P. xanthii, actualmente se conocen siete razas fisiológicas del mismo a nivel mundial (Jahn et al., 2002), situación que se desconoce en el norte de Sinaloa. Considerando la importancia del tomatillo como cultivo hortícola, se justifica la identificación de razas fisiológicas del patógeno, ya que el entender la variación genética contribuirá en el proceso de mejoramiento genético, orientado a la obtención de cultivares resistentes a la enfermedad.
CONCLUSIONES
El hongo asociado en forma consistente a la mancha foliar del tomatillo se identificó como Cercospora sp., y se determinó su patogenicidad en el cultivo. Las características morfométricas de las estructuras de origen asexual e imágenes al microscopio electrónico de barrido de los conidios, permitieron identificar al hongo P. xanthii como agente causal de la cenicilla del tomatillo. Los fungicidas azoxystrobin, trifloxystrobin y tebuconazole a las dosis de 0.02. 0.1 y 30.0 ppm. respectivamente, ejercen un marcado efecto inhibitorio de la germinación in vitro en los conidios de Cercospora sp.; en tanto que los mismos fungicidas mostraron el mismo efecto en la inhibición del desarrollo micelial del patógeno a partir de las dosis 1.5,0.1 y 5.0 ppm, respectivamente. Los fungicidas tebuconazole (Folicur® 0.6 L/ha), trifloxystrobin (Flint® 250 gr/ha), clorotalonil (Bravo® 720 2.5 L/ha) y benomilo + mancozcb (Benlate® + Mancozeb® 500 g/ha + 2.0 kg/lia), ejercieron un excelente control contra la mancha foliar y la cenicil la del tomatillo en campo.
]]> LITERATURA CITADA
Abbott. W.S. 1925. A method of computing the effectiveness of an insecticide. Journal of Economic Entomology 18:265-267. [ Links ]
Barnett, H.L., and Hunter, B.B. 1972. Illustrated Genera of Imperfect Fungi. Third Edition. Burgess Publishing Company. Minneapolis. MN, USA. 241 p. [ Links ]
Boesevvinkel. H.J. 1980. The morphology of the imperfect states of powdery mildews (Erysiphaccae). The Botanical Review 46:167-224. [ Links ]
Bozzola. J.J., and Russell, L.D. 1999. Electron Microscopy. Principles and Techniques for Biologists. Jones and Bartlett Publishers. London, UK. 670 p. [ Links ]
CAADES. 2004. Comparativo del avance de siembras de hortalizas en las temporadas 2002-2003 y 2003-2004. Documento interno del Departamento de Estudios Económicos, de la Confederación de Asociaciones Agrícolas del Estado del Sinaloa. Culiacán, México, s/p. [ Links ]
Cheah, L., Page, B.B.C., and Cox, J.K. 1996. Epidemiology of powdery mildew (Sphaerothcca fuliginea) of squash, pp. 147-151. Proceedings of the 49th New Zealand Plant Protection Conference. The Horticulture and Food Research Institute of New Zealand. Palmerston North, New Zealand. 313 p. [ Links ]
Cook, R.T.A., Inman, A.J., and Billings, C. 1997. Identification and classification of powdery mildew anamorphs using light and scanning electron microscopy and host range data. Mycological Research 101:975-1002. [ Links ]
De la Torre-Almaráz, R., Salazar-Segura, M. y Valverde R.A. 2003. Etiología del moteado amarillo del tomate de cáscara (Physatis ixocarpa Brot.) en México. Agrociencia 37:277-289. [ Links ]
Félix-Gastélum, R., Apodaca-Sánchez, M.A., MartÃnez-Valenzuela, M.C. y Espinosa-MatÃas. S. 2005. Podosphaera ( sect. Sphaerotheca) xanthii (Castagne) U. Brawn y N. Shishkoffen el Norte de Sinaloa, México. Revista Mexicana de Fitopatología 23:162-168. [ Links ]
García. C.E., Pons, N. y Benítez de Rojas, C. 1996. Cercospora y hongos similares sobre especies de Ipomea. Fitopatología Venezolana 9:22-36. [ Links ]
Hammett. K.R.W. 1977. Taxonomy of Erysiphaceae in New Zealand. New Zealand Journal of Botany 15:687-711. [ Links ]
Hernández, H.V. y Cano, R.P. 1990. Sphaerotheca fuliginea agente causal de la cenicilla del melón y sus razas fisiológicas en La Comarca Lagunera. Memorias del XVII Congreso Nacional de la Sociedad Mexicana de Fitopatología. Culiacán, Sinaloa. México. Resumen p. 7. [ Links ]
Hyeon-Dong, S.. and Yong-Joon. L. 1993. Morphology of edge lines of chained immature conidia on conidiophorcs in powdery mildew fungi and their taxonomic significance. Mycotaxon 46:445-451. [ Links ]
Janh M., Munger, H.M., and McCreight, J.D. 2002. Breeding cucurbit crops for powdery mildew resistance, pp. 239-248. In: R.R. Bélanger, W.R. Bushnell. A.J. Dik. and T.L.W. Carver (eds.). The Powdery Mildews a Comprehensive Treatise. The American Phytopathological Society Press. St. Paul. Minnesota. USA. 292 p. [ Links ]
Kable. P.F.. Ballantyne, B.. and Barbara. J. 1963. Observations on the cucurbits powdery mildew in the Ithaca district. Plant Disease Reporter 47:842. [ Links ]
Little, T.M., and Hills. FJ. 1973. Agricultural Experimentation Design and Analysis. John Wiley and Sons. New York. USA. 350 p. [ Links ]
McGrath. M.T. 1991. Reduced effectiveness of triadimefon for controlling cucurbit power mildew associated with fungicide resistance in Sphaerothcca filliginca (Abstr.) Phytopathology 81:1191. [ Links ]
McGrath. M.T. 2001. Fungicide resistance in cucurbit powdery mildew: Experiences and challenges. Plant Disease 85:236-345. [ Links ]
McGrath. M.T., Staniszewka. H., Shishkoff, N., and Casella. G. 1996. Fungicide sensitivily of Sphaerotheca fulginea populations in the United States. Plant Disease 80:697-703. [ Links ]
Moreno-Rico, O. y Romero-Coba, S. 1992. Formación de clcistotecios en calabaza variedad Castilla (Cuercubita moschata Dene.) por Sphaerotheca fulginea (Schlecht. ex Fries) Poll, en Jesús Maria, Aguascalicntes. Memorias del XIX Congreso Nacional de la Sociedad Mexicana de Fitopatología. Saltillo. Coahuila, México. Resumen p. 85. [ Links ]
Mya-Thaung, M. 1984. Some fungi of Cercospora complex from Bunna. Mycotaxon 19:425-452. [ Links ]
Peña-Lomelí, A. 2001. Situación actual y perspectivas de la producción y mejoramiento genético de tomate tie cáscara (Physalis ixocarpa Brot.) en México. En: J. Hernández-Dávila y A. Robledo-Torres (Compiladores). Memorias del Primer Simposio Nacional sobre Técnicas Modernas en Producción de Tomate, Papa y otras Solanáceas. Saltillo. Coahuila, México. 111 p. [ Links ]
Reifschneider, F.J.B., Boiteux, L.S., and Occheiena, E.M. 1985. Powdery mildew of melon (Cucumis melo) caused by Sphaerotheca fulginea in Brazil. Plant Disease 69:1069-1070. [ Links ]
Ruzin, S.E. 1999. Plant Microtechnique and Microscopy. Oxford University Press. New York. USA. 322 p. [ Links ]
Schroeder, W.T., and Provvidenti, R. 1969. Resistance to benomyl in powdery mildew of cucurbits. Plane Disease Reporter 53:271-275 [ Links ]
Smith, R., Jiménez, M. y Cantwell, M. 2002. Producción de tomatillo en California. Centro de Información e Investigación de Hortalizas, Universidad de California. Publicación 7246-Spanish. Davis, California. EUA. 3 p. [ Links ]
Townsend, G.R., and Heuberger, J.W. 1943. Methods for estimating losses caused by diseases in fungicide experiments. Plant Disease Reporter 60:340-343. [ Links ]
Vanhaarveld, A.B. 1984. Powdery mildew fungi in South Africa. Phytophylactica 16:155-166. [ Links ]
Yarwood, C.E., 1973. Pyrcnomycctes: Erysiphales. pp. 71-86. In: G.C. Ainsworth. F.K. Sparrow, and A.S. Sussman (eds.). The Fungi and Advanced Treatise. Volume IV. A Taxonomic Review with keys: Ascomycetes and Fungi Imperfecti. Academic Press. New York. USA. 621 p. [ Links ]
Zaracovitis. C. 1965. Attempts to identify powdery mildew fungi by conidial characters. Transactions of the British Mycological Society 48:553-558. [ Links ]
]]>Zitter, T.A., Hopkins, D.L., and Thomas, C.E. (eds.). 1996. Compendium of Cucurbit Diseases. APS press. St. Paul. Minnesota. USA. 87 p. [ Links ]
]]>