Seroepidemiología de la hepatitis A en México. Sensor de inequidad social e indicador de políticas de vacunación
Seroepidemiology of hepatitis A in Mexico. A detector of social inequity and monitor of immunization policies
José Luis Valdespino, MC, MSPI; Juan Ruiz-Gómez, MCII; Gustavo Olaiz-Fernández, MC, MSPIII; Eloísa Arias-Toledo, Ing BiotII; Carlos J Conde-González, QBP, M en C, D en CII; Oswaldo Palma, ActII; Jaime Sepúlveda, MC, M en C, D en C.II
IInstituto Nacional de Salud Pública; actualmente en el Laboratorio de Biológicos y Reactivos de México (Birmex)
IIInstituto Nacional de Salud Pública. México ]]>
IIISecretaría de Salud. México
RESUMEN
OBJETIVO: Estudiar la distribución y frecuencia de los anticuerpos contra el virus de la hepatitis A en una muestra probabilística en México con representatividad estatal, así como analizar los factores de riesgo y los patrones epidemiológicos.
MATERIAL Y MÉTODOS: A partir de la Encuesta Nacional de Salud se estudiaron 4 907 sueros seleccionados de forma aleatoria para anticuerpos contra VHA mediante ensayo inmunoenzimático. Los sueros se recolectaron de noviembre de 1999 a junio del 2000 a nivel nacional.
RESULTADOS: Se encontró seroprevalencia general de 81.3% (IC 78.6-84.2), y los resultados expandidos permiten inferir que existen 78.7 millones de mexicanos infectados. Los factores de riesgo en menores de nueve años incluyen residir en entidades sureñas (RM= 5.3), localidades rurales (RM= 3.1), provenir de familia con bajos ingresos (RM= 2.4) y habitar viviendas con acceso limitado a servicios sanitarios (agua, RM= 2.5; drenaje, RM= 2.7).
CONCLUSIONES: Los patrones de transmisión heterogéneos y las diferencias en las pre-valencias de infección indican inequidad en las poblaciones estudiadas, explicables por diferencias en las condiciones sanitarias y sociales. Se discuten las ventajas de intervenciones poblacionales tales como la vacunación y el fortalecimiento de las condiciones sanitarias y socioeconómicas.
Palabras clave: hepatitis A; seroepidemiología; inequidad; vacunación; México
ABSTRACT
]]> OBJECTIVE: Hepatitis A Virus (HAV) in Mexico has traditionally been considered a disease with a homogeneous pattern of transmission, high rates of infection at early ages, and infrequent complication rates. The purpose of this study was to take advantage of the 2000 NHS, a probabilistic population-based survey, in order to describe the seroepidemiology of HAV infection in Mexico.Key Words: viral hepatitis A; seroepidemiology; inequity; Mexico
El virus de la hepatitis tipo A (VHA) es un virus de RNA no envuelto perteneciente a la familia Pi-cornaviridae, género Hepatovirus. El mecanismo de transmisión más frecuente es la vía fecal-oral.1,2 La clasificación basada en la región VP1 que codifica la proteína mayor de la superficie incluye cinco genotipos;1 la basada en el gen VP1/ZA propone siete genotipos.3 En cualquier caso, los diferentes genotipos están relacionados desde el punto de vista antigénico entre sí. Las proteínas que codifican estos genes estimulan la producción de anticuerpos neutralizantes.1 A nivel global, el VHA es causante de 20 a 40% de los casos sintomáticos de hepatitis. El diagnóstico serológico de la enfermedad depende del hallazgo de anticuerpos del tipo IgM durante la fase aguda, los cuales persisten durante tres a seis meses. La presencia exclusiva de IgG contra VHA es indicadora sólo de infección pasada y persiste por décadas después del contacto inicial con el virus, sobre todo en áreas en donde existe transmisión frecuente.1,2
A nivel mundial se han descrito cuatro patrones epidemiológicos de la hepatitis A de acuerdo con su endemicidad. El patrón de endemicidad alto se caracteriza por afectar en particular al grupo de preescolares; la transmisión es de persona a persona, casi nunca hay informes de epidemias y la persistencia de la inmunidad es casi universal en adultos. El patrón de endemicidad moderado afecta sobre todo al grupo de escolares; la transmisión incluye vehículos (alimentos y agua) y los informes de epidemias en este grupo de edad son comunes. El patrón de transmisión bajo afecta en especial a los adolescentes y adultos; también se relaciona con vehículos y se registran epidemias. Por último, el patrón de transmisión muy bajo afecta las más de las veces a adultos; los casos notificados se vinculan con brotes y antecedentes importantes, entre ellos, los viajes a regiones con alta transmisión, el contacto con migrantes o la ingestión de alimentos frescos importados.2
En países con sistemas de vigilancia epidemiológica, para cada tipo etiológico de hepatitis viral se ha precisado el peso de la enfermedad. Por ejemplo, en Estados Unidos se notifican cada año 10 000 casos y se prevén 93 000 nuevas infecciones. La tasa de letalidad es de 0.3% en todos los grupos de edad y alcanza 1.8% en adultos mayores de 50 años.2
]]> De forma adicional, se calcula que 10 a 20% de los casos requiere de hospitalización. El promedio de incapacidad es de 27 días, los costos directos e indirectos de atención médica en adultos equivalen a 2 000 dólares en adultos y 1 000 en niños.1,2En Estados Unidos, la prevalencia de anticuerpos se ha estudiado a través de las encuestas nacionales de salud y nutrición. En la NHANES III efectuada de 1988 a 1994 se registraron seroprevalencias de 9% en escolares, 19% en adultos jóvenes, mientras que tres cuartas partes de la población mayor de 70 años ya había sufrido la infección.2 La prevalencia de infección en población estadounidense de origen mexicano es de 70% y es tres veces mayor que en la población de blancos no hispanos. En ese país una proporción considerable de los casos ocurre en individuos que tienen como antecedente viajar a zonas con alta prevalencia de hepatitis A. Algunos brotes epidémicos se han vinculado con productos provenientes de este país. Por último, se ha descrito el virus de la hepatitis A como uno de los contaminantes del agua en zonas costeras de Baja California, México y California en Estados Unidos.4-8
La expresión clínica de la infección por VHA es dependiente de la edad. A medida que aumenta la edad, la gravedad del cuadro clínico y la letalidad se incrementan.1,2
En la actualidad, la hepatitis A en países como México no se considera un problema de salud pública debido a que se asume que la infección ocurre durante los primeros años de la vida y, por tanto, produce una enfermedad "benigna" con repercusiones poco importantes en el peso de la enfermedad. En cambio, se ha documentado como problema de salud en los viajeros a regiones endémicas y, en fecha reciente, como un problema de contaminación ambiental (en alimentos frescos9 y agua para consumo humano) y marítima.4-8
La endemicidad de la infección por VHA depende de factores de riesgo semejantes a los de otras infecciones entéricas y por tanto se relaciona con el acceso a medidas sanitarias y las condiciones socioeconómicas.1
La transmisión fecal-oral y fecal-vehículo-oral son las principales formas de diseminación de la enfermedad1,2 y, por consiguiente, se ha demostrado que el contacto con niños en guarderías y escuelas es un factor importante en la génesis de epidemias.1 El consumo de agua y alimentos crudos o mal cocidos contaminados como moluscos bivalvos o cebollas verdes9 y la participación de reservorios humanos han conducido a la producción de epidemias.1 Con la mejoría de las condiciones sanitarias y sociales, la infección por VHA ha disminuido de manera sustancial en algunos países. Sin embargo, esto ha provocado que el número de susceptibles y la probabilidad de aparición de brotes epidémicos aumenten.2
Desde 1995 han ganado licencia dos vacunas de virus inactivado en Estados Unidos, la HAVRIX® y la VAQTA®.10,11 En ambos casos, los resultados de ensayos clínicos aleatorizados indican alta inmunogenicidad (97%), seguridad y adecuada efectividad. De forma inicial, las recomendaciones iniciales para la vacunación incluyeron a la población de 2-18 años y adultos residentes en áreas de gran transmisión. A partir de octubre de 2005 se amplió la recomendación para incluir al grupo de 1-18 años y en la actualidad forma parte del esquema de vacunación regular en niños y adolescentes. Un programa de control global del VHA requiere vacunación universal en la infancia. Para que esta intervención en salud pública sea efectiva en términos del costo es necesario combinar vacunas y que las disponibles reduzcan sus costos.12,13
En México existen varios antecedentes de encuestas seroepidemiológicas de hepatitis A, de las cuales ninguna tiene la propiedad de ser probabilística y nacional. En una encuesta seroepidemiológica realizada en 1973, Kumate y colaboradores informaron que la seroprevalencia de anticuerpos contra VHA era de 75 y 84% en 190 preescolares y 673 escolares, respectivamente.14 En 1982, Ruiz-Gómez y colaboradores informaron que la seroprevalencia en 275 niños menores de cinco años de edad fue de 45%.15 Bustamante y colaboradores, en una encuesta llevada a cabo en el sur del país (estado de Chiapas), describieron en 1986 seroprevalencia de 97.2% en 35 preescolares.16 En 1999, Tapia y colaboradores detectaron prevalencia de 40.5% en 850 preescolares residentes en áreas urbanas.17
En México, el Sistema de Vigilancia Epidemiológica de las hepatitis virales no incluye su distinción por factor etiológico. Por lo tanto, no existe un registro del número de casos y defunciones por este agente en particular.
El objetivo de esta investigación fue conocer la distribución y frecuencia de los anticuerpos contra el virus de la hepatitis A en una muestra probabilística de población residente en las 32 entidades federativas con representatividad estatal, así como analizar los factores de riesgo concomitantes, incluidas las variables sociales y sanitarias y precisar los patrones epidemiológicos de la transmisión por este virus.
]]>Material y métodos
Diseño
La Secretaría de Salud efectuó la Encuesta Nacional de Salud (ENSA 2000), cuyo diseño ya se ha descrito entre noviembre de 1999 y junio de 2000. De manera sinóptica, incluyó 43 479 hogares (con un total de 90 916 individuos) seleccionados mediante un muestreo probabilístico polietápico, con el fin de ser representativa de la población mexicana civil, no institucionalizada, en los niveles nacional y estatal. La recolección de la información estuvo a cargo de personal entrenado que recogió información sociodemográfica del estado actual de salud, uso de servicios de salud y comportamiento de los participantes, y recolectó muestras biológicas.
Tamaño de la muestra
El presente estudio se basa en la información de 4 836 individuos mayores de un año de edad de ambos sexos. La muestra se seleccionó del Banco de Sueros mediante muestreo aleatorio simple a partir de los 45 294 sujetos estudiados por la ENSA 2000. Se calcularon los tamaños de muestra para los tres grupos estudiados. En sujetos de 1-9 años el tamaño es de 500 y se consideró una probabilidad de infección de 0.4; en sueros de individuos de 10 a 19 años el tamaño de muestra fue de 2 100 y se tomó una probabilidad de 0.85, y en sujetos de 20 años y mayores la muestra fue de 2 400 con una p= 0.90. Las probabilidades de error tipo 1 y poder fueron los mismos. El tamaño de la muestra estudiado es menor para la Ciudad de México en comparación con las regiones que adicionan varios estados, algo atribuible a que el tamaño de la muestra es semejante para cada entidad federativa.
Análisis de laboratorio
Dentro de las muestras de suero de la ENSA 2000 se seleccionaron por muestreo aleatorio simple 5 000 muestras, de las cuales se procesaron 4 836 sueros para estudiar anticuerpos totales contra el virus de la hepatitis A, mediante la técnica de ensayo inmunoenzimático con micropartículas (MEIA) y un reactivo comercial (AxSYM® HAVAB 2.0® Abbott Laboratories); dicha prueba se basa en el principio de unión competitiva entre el anti-VHA de la muestra y el conjugado de anti-VHA con fosfatasa alcalina.
Análisis estadístico
Para el análisis estadístico se calculó la seroprevalencia de anticuerpos contra hepatitis A, según algunas características demográficas, socioeconómicas, geográficas, sanitarias y de servicios de salud. El ingreso mensual en el hogar se analizó en salarios mínimos a partir de los ingresos económicos informados por las personas mayores de 12 años, y se tomó como base el salario mínimo vigente por municipio en el año 2000. Para conocer la relación entre algunos factores adjuntos y la seropositividad a la VHA se obtuvieron razones de momios y se calcularon intervalos de confianza al 95%. En los procedimientos estadísticos se calcularon los factores de expansión poblacional. Los datos se procesaron con el paquete estadístico SAS 9.1 (SAS Institute, Cary NC) y SUDAAN 7.5.6. Las razones de momios y los intervalos de confianza se obtuvieron con este último paquete estadístico, el cual considera el tipo de muestreo utilizado en el diseño muestral de esta encuesta.
]]> Aspectos éticosEl protocolo específico obtuvo la aprobación de las comisiones de Investigación y Ética del Instituto Nacional de Salud Pública. De modo adicional, la recolección y presentación de los datos se realizaron bajo la observancia de los principios de confidencialidad y reserva señalados por la Ley de Información Estadística y Geográfica.
Resultados
En los 4 907 sujetos estudiados se encontró seroprevalencia de anticuerpos contra el VHA en 81.3% (78.6-84.2). Los resultados expandidos en la población mexicana para el año 2000 permiten inferir que este virus de transmisión entérica ya ha infectado a 78.7 millones de mexicanos.
En el grupo de preescolares (1-4 años), 28.7% (21.5-37.2) tenía anticuerpos contra VHA, lo que representa 2.9 millones de infectados a esa edad, y 7.4 millones pasaron a la edad escolar como susceptibles. En el grupo de escolares (5-14 años), 66.4% (61.7-70.8) de los muestreados tenía anticuerpos, lo que indica que 16.5 millones de escolares mexicanos ya se habían infectado a esa edad, pero 2.9 millones todavía eran susceptibles cuando pasaron a la adolescencia.
La prevalencia en adolescentes (15-19 años) fue de 86.9% (81.8-90.7), en adultos jóvenes (20-29 años) de 97.5% (95.1-98.7) y a partir de los 30 años de edad la seroprevalencia fue mayor de 98.2% (97.3-99.1). La seroprevalencia en todos los grupos de edad expandida es mayor en mujeres 82.6% (79.8-85.6) en comparación con hombres 80.0% (76.7-83.4).
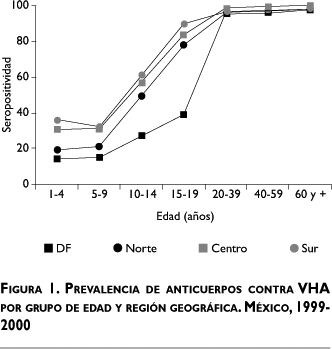
En la figura 1 se observan las diferencias en la distribución de las prevalencias de infección por VHA de acuerdo con grupos de edad entre la Ciudad de México y los estados del norte, centro y sur del país. En el sur 50% de las infecciones ocurre durante la edad preescolar (1-4 años); en cambio, en el centro y norte del país se alcanza esta proporción de infecciones hasta la etapa escolar (5-14 años). Por último, en la Ciudad de México no es sino hasta la adolescencia cuando se registra esta proporción de infecciones.
]]>
Distribución y frecuencia en sujetos de 1-9 años de edad
La región geográfica es un factor de riesgo de infección por VHA. En los estados del sur del país el riesgo de antecedente de infección es cinco veces mayor que en la Ciudad de México (RM= 5.2 [IC 2.5-10.8]). Estas diferencias son consistentes aunque menores en la región centro (RM= 3.0) y las entidades del norte del país (RM= 2.3). Las RM son mayores a la unidad en todos los casos a pesar del tamaño de muestra menor para la Ciudad de México. Residir en localidades rurales (menores de 15 000 habitantes) también se vincula con una mayor prevalencia de anticuerpos contra VHA (RM= 3.1 [IC 2.0-4.8]).
La variable socioeconómica "ingreso familiar" distribuida en cuartiles también se relaciona con un mayor riesgo en la población con ingresos más bajos (RM= 2.4 [IC 1.6-4.7]).
El análisis de las variables de acceso a servicios sanitarios, como disponibilidad de agua (RM= 2.5) y drenaje (RM= 2.7) o los niveles de cloro en el agua (RM= 3.3), permite predecir riesgos diferenciales en el grupo de uno a nueve años de edad sin acceso o con acceso deficiente a estos servicios sanitarios (cuadro I).
Distribución en el grupo de 10 a 19 años
En general se observan diferenciales por región geográfica (RM= 14.5) y tipo de localidad (RM= 5.4). Las diferencias en variables socioeconómicas (RM= 2.1) y variables sanitarias (RM= 8.6, 7.4 y 2.3) son menores que en la primera década de la vida (cuadro II).
Distribución en el grupo de 20 y más años
A partir de esa edad las prevalencias son mayores de 96% y prácticamente desaparecen las diferencias en las frecuencias de infección por VHA (cuadro III).
]]> ConclusiónÉste es el primer informe de una encuesta con base poblacional y probabilística en la que se describe la seroprevalencia de anticuerpos contra VHA en Mé–xico. Los resultados muestran que la frecuencia de anticuerpos es tres veces mayor que la informada en Estados Unidos en la encuesta NHANES-III.2 Al comparar los resultados con los de otros estudios mexicanos, la seroprevalencia detectada en este estudio es tres veces menor respecto de la que comunicó Kumate14 en una muestra no probabilística en los años setenta, y una tercera parte menor en comparación con la de Ruiz-Gómez en los ochenta15 y menor a la de Tapia a finales de los noventa.17
Las limitaciones de este trabajo son las propias de un estudio trasversal; para el cálculo de tamaño de la muestra se priorizaron las estimaciones poblacionales con base en el muestreo multietápico utilizado. Los factores de riesgo que se presentan tienen como limitante que las variables independientes y dependientes se recolectaron de forma simultánea, y además los tamaños de muestra en algunos casos no son las recomendadas para un diseño analítico. No obstante, los intervalos de confianza orientan sobre las fortalezas y limitaciones de las RM. A pesar de la relación de algunas variables independientes entre sí, no se calcularon RM multivariadas. Se prefirió computar RM simples a partir de las proporciones ponderadas poblacionales.
Los resultados de este trabajo muestran que no existe en la actualidad un patrón epidemiológico homogéneo de transmisión de hepatitis A en México. Esta variabilidad se muestra en la frecuencia de anticuerpos durante las primeras décadas de la vida y es posible identificar los siguientes patrones de transmisión:
| • | El patrón de endemicidad alto se observa en entidades federativas del sur del país, en estratos socioeconómicos bajos y en ocupantes de viviendas con deficiencias sanitarias (agua, drenaje y niveles de cloro en el agua). En estas áreas las tasas de prevalencia de infección en preescolares alcanzan cifras más elevadas. |
| • | El patrón de endemicidad moderado se presenta sobre todo en entidades federativas del centro y norte del país. También se vincula con variables socioeconómicas y sanitarias. |
| • | El patrón de transmisión bajo se empieza a observar en la Ciudad de México y los estratos socioeconómicos altos. |
| • | Todavía no se reconoce en México el patrón de transmisión muy bajo. |
Al comparar los resultados del presente estudio con los informes previos destaca la disminución de la frecuencia de infección por VHA en preescolares y su desplazamiento al grupo de escolares y adolescentes. Por lo tanto, es de esperar que ocurran epidemias de forma más frecuente en estos grupos de edad al concentrarse un mayor número de susceptibles a edades mayores.
Es recomendable que las definiciones de caso utilizadas para la vigilancia epidemiológica de las hepatitis virales en países como México evolucionen de la utilización de criterios sindromáticos al uso de criterios etiológicos, como sucede en la mayoría de los países desarrollados.2
Es posible que la tasa de letalidad y los días de incapacidad por hepatitis A en México sean todavía inferiores que en Estados Unidos (0.05-0.15%). Sin embargo, al incrementarse la edad de la infección es de esperarse que la letalidad en este país también se eleve.
El gran número de preescolares susceptibles a la infección detectados en la encuesta (7.4 millones) es argumento suficiente para justificar la evaluación de la posible incorporación de la vacuna contra la hepatitis A en el esquema regular de inmunizaciones de los niños en México. Una vez instalado el programa sería importante evaluar la duración de la inmunidad conferida por la vacuna mediante la vigilancia de los títulos de anticuerpos. En caso que se comprobara que la inmunidad es limitada en el tiempo, el programa de vacunación en niños tendría que acompañarse de medidas de revacunación en la adolescencia. Sería deseable que se redujeran los costos de las dos vacunas disponibles en el mercado al realizarse compras consolidadas.
]]> Este estudio muestra con claridad que pertenecer al nivel socioeconómico bajo y carecer de los servicios sanitarios inadecuados se vinculan con una mayor tasa de seropositividad hacia el VHA. Las elevadas tasas de seropositividad de los estados de la región sur del país coinciden con el alto grado de dispersión de la población y pobreza, presentes en estos lugares. Por otro lado, en el Distrito Federal así como en algunos estados del norte del país, se observaron tasas relativamente bajas. Estos resultados concuerdan con la inequidad social y de salud. En este mismo número se presentan los resultados de sarampión y poliomielitis en los que se ha logrado la equidad inmunológica gracias a los programas de vacunación; es por ello que los resultados de este trabajo son un indicador de la ausencia de vacunación en contra de esta enfermedad.Las diferencias de las seroprevalencias de infección por VHA, en particular en sujetos de 1-9 años, reflejan las divergencias en el acceso a los servicios sanitarios (agua y drenaje), que a su vez se relacionan con el tipo de localidad (urbano-rural) y el nivel socioeconómico (cuartiles de ingreso). La distribución de la infección por este virus transmitido de manera semejante a otras infecciones entéricas refleja las inequidades de las condiciones sanitarias y sociales en este país. A corto plazo, la intervención poblacional que podría resolver este problema es la vacunación, a mediano plazo el desarrollo sanitario y social y a largo plazo el desarrollo social y económico.
Ante una salud poblacional y económica más globalizada, la hepatitis A puede tener repercusiones económicas en el turismo y la exportación de alimentos frescos. Por otro lado, deben considerarse las repercusiones de tipo ambiental, por lo que la incorporación de intervenciones contra esta enfermedad puede ofrecer beneficios adicionales.
Los resultados de esta investigación muestran que el patrón de transmisión de la hepatitis viral tipo A en México es cambiante y heterogéneo. Las diferencias entre las prevalencias y factores de riesgo son evidencia de las desigualdades que existen entre los diferentes estratos de la población.
Las poblaciones en mayor riesgo de contraer la infección a edades tempranas residen en las áreas pobres de zonas rurales y con acceso limitado a los servicios sanitarios. Los habitantes de áreas urbanas, con niveles socioeconómicos altos y mejores condiciones sanitarias, tienen prevalencias más bajas. En contraparte, corren un mayor riesgo de presentar cuadros clínicos graves al sufrir la infección a edades más avanzadas.
La vacunación contra algunos inmunógenos como sarampión y poliomielitis ha logrado una cobertura cercana a 100% (véase en este mismo número los artículos correspondientes). Esto ha llevado a la eliminación de la transmisión autóctona. Para esas enfermedades, tales logros son independientes de la accesibilidad geográfica o socioeconómica. Esto último se ha definido como "equidad inmunológica".
En consecuencia, los resultados sobre la magnitud y distribución y frecuencia de la infección de una enfermedad prevenible por vacunación, como la hepatitis A, indican inequidad inmunológica y esto mismo es un signo de las políticas de vacunación.
Estos datos pueden ser de utilidad para las políticas públicas en dos vertientes. Por un lado, aportan elementos que justifican la evaluación de la incorporación de la vacunación contra hepatitis A en el esquema regular de vacunación y, por otro lado, destacan la necesidad de actualizar el sistema de vigilancia epidemiológica de la enfermedad que permita su caracterización desde el punto de vista etiológico al incorporar los resultados de laboratorio. Es recomendable asimismo realizar estudios sobre la relación costo-beneficio para la incorporación de la vacunación contra hepatitis A; esta intervención sanitaria podría ser recomendable en una primera etapa sólo para algunas regiones como la Ciudad de México y el norte del país.
Agradecimientos
]]> Proyecto financiado parcialmente por CONACyT: 37212-M y MO244-9911. Los autores expresan su agradecimiento al personal de laboratorio: Ing. Cruz Portugal García y Biól. Manuel Velázquez Meza por su valiosa labor.
Referencias
1. Cuthbert JA. Hepatitis A: old and new. Clin Microbiol Rev 2001;14(1):38-58. [ Links ]
2. Prevention of hepatitis A through active or passive immunization: Recommendations of the Advisory Committee on Immunization Practices (ACIP). MMWR Recomm Rep 1999;48(RR-12):1-37. [ Links ]
3. Costa-Mattioli M, Cristina J, Romero H, et al. Molecular evolution of hepatitis A virus: a new classification based on the complete VP1 protein. J Virol 2002;76(18):9516-9525. [ Links ]
4. Jong EC. United States epidemiology of hepatitis A: influenced by immigrants visiting friends and relatives in Mexico? Am J Med 2005;118(Suppl 10A):S50-S57. [ Links ]
5. Doyle TJ, Bryan RT. Infectious disease morbidity in the US region bordering Mexico, 1990-1998. J Infect Dis 2000;182(5):1503-1510. [ Links ]
6. Webster G, Barnes E, Dusheiko G, et al. Protecting travellers from hepatitis A. BMJ 2001;322(7296):1194-1195. [ Links ]
7. Mutsch M, Spicher VM, Gut C, et al. Hepatitis A virus infections in travelers, 1988-2004. Clin Infect Dis 2006;42(4):490-497. [ Links ]
8. Shapiro CN, Coleman PJ, McQuillan GM, et al. Epidemiology of hepatitis A: seroepidemiology and risk groups in the USA. Vaccine 1992;10(Suppl 1):S59-S62. [ Links ]
9. Wheeler C, Vogt TM, Armstrong GL, et al. An outbreak of hepatitis A associated with green onions. N Engl J Med 2005;353(9):890-897. [ Links ]
10. Notice to Readers: FDA Approval of Havrix® (Hepatitis A Vaccine, Inactivated) for Persons Aged 1-18 Years. MMWR Morb Mortal Wkly Rep 2005;54(48):1235-1236. [ Links ]
11. Notice To Readers: FDA Approval of VAQTA® (Hepatitis A Vaccine, Inactivated) for Children Aged >1 Year. MMWR Morb Mortal Wkly Rep 2005;54(40):1026. [ Links ]
12. Kershenobich D. Hepatitis A: is universal vaccination justified in Mexico? Rev Gastroenterol Mex 1996;61(4 Suppl 2):S69-S70. [ Links ]
13. Mazari-Hiriart M, López-Vidal Y, Ponce-de-Leon S, et al. Longitudinal study of microbial diversity and seasonality in the Mexico City metropolitan area water supply system. Appl Environ Microbiol 2005;71(9):5129-5137. [ Links ]
14. Kumate J, Alvizouri AM, Isibasi A. Serologic survey of hepatitis A antibodies in Mexican children. Bull Pan Am Health Organ 1982;16(2): 156-160. [ Links ]
15. Ruiz-Gómez J, Bustamante-Calvillo ME. Hepatitis A antibodies: prevalence and persistence in a group of Mexican children. Am J Epidemiol 1985;121(1):116-119. [ Links ]
16. Bustamante-Calvillo ME, Velázquez-Castillo FR, Padilla-Noriega L, et al. Seroepidemiology of hepatitis A virus infection in communities of the southern border of the State of Chiapas. Bol Med Hosp Infant Mex 1986;43(12):735-741. [ Links ]
17. Tapia-Conyer R, Santos JI, Cavalcanti AM, et al. Hepatitis A in Latin America: a changing epidemiologic pattern. Am J Trop Med Hyg 1999;61(5):825-829. [ Links ]
Fecha de recibido: 18 de abril de 2006
Fecha de aprobado: 8 de febrero de 2007
Solicitud de sobretiros: MSP José Luis Valdespino. Director general adjunto de Investigación, Desarrollo y Aseguramiento de la Calidad (IDyAC). Laboratorios de Biológicos y Reactivos de México (Birmex). Amores 1240, Col. Del Valle, 03100 México, DF, México. Correo electrónicol: jvaldesp@insp.mx
]]>