Resistencia a Colletotrichum lindemuthianum en frijol común transgénico, expresando el gen defensina de Arabidopsis thaliana*
Resistance to Colletotrichum lindemuthianum in transgenic common bean expressing an Arabidopsis thaliana defensin gene
Elsa Espinosa-Huerta1, Anareli Quintero-Jiménez1, Bertha María Sánchez-García2, Jorge Alberto Acosta-Gallegos3 y María Alejandra Mora-Avilés4§
1 Campo Experimental Bajío- INIFAP. Programa de Biotecnología. Carretera Celaya-San Miguel de Allende km 6.5. C. P. 38110, A. P. 112, Celaya, Guanajuato, México. Tel +52 461 6115323. Ext. 121. (espinosa.elsa@inifap.gob.mx). §Autora para correspondencia: mora.alejandra@inifap.gob.mx.
]]> 2 Programa de Sanidad Vegetal Tel +52 461 6115323. Ext 172, (sanchez.bertha@inifap.gob.mx).3 Programa de frijol. Tel +52 461 6115323. Ext. 112 (acosta.jorge@inifap.gob.mx).
4 Programa de Biotecnología +52 461 6115323. Ext. 186.
* Recibido: enero de 2013
Aceptado: junio de 2013
Resumen
El gen defensina de Arabidopsis thaliana es un péptido antimicrobiano que proporciona protección a una amplia gama de agentes patógenos. Las líneas transgénicas del frijol común (Phaseolus vulgaris L.) cv. Flor de Mayo Anita expresan constitutivamente el gen defensina pdf 1.2 siendo generados por la transformación de hipocotilos mediada por Agrobacterium sp. vía organogénesis directa. El gen pdf 1.2 es expresado bajo el control del promotor CaMV-35S en las plantas de frijol transformando a estas en resistentes al hongo fitopatógeno Colletotrichum lindemuthianum. La respuesta fue una reducción significativa en la formación de lesiones y la proliferación en masa de esporas en las líneas T0, T1 y T3 en comparación con las plantas no transformadas. Veinte plantas transgénicas T3 de frijol común fueron generadas a partir de 5 líneas independientes que expresaron el gen pdf1. 2, mostrando resistencia a razas 448 y 1472 de C. lindemuthianum en comparación con las plantas no transformadas. Un análisis del nivel de la expresión génica del gen pdf 1.2 por Q-PCR mostro que todas las plantas que fueron consideradas resistentes o tolerantes, tuvieron niveles similares de expresión transcripcional en oposición a las plantas susceptibles, las cuales no mostraron presencia de la transcripción pdf 1.2.
Palabras clave: Phaseolus vulgaris L., Agrobacterium tumefaciens, defensina, gen pdf1.2, regeneración.
]]>Abstract
The defensin gene from Arabidopsis thaliana is an antimicrobial peptide that provides protection to a wide array of pathogens. Transgenic common bean (Phaseolus vulgaris L.) plants of cv. Flor de Mayo Anita constitutively expressing the defensin pdf 1.2 gene were generated by Agrobacterium-mediated transformation via hypocotyls direct organogenic regeneration. The pdf 1. 2 gene under the control of promoter CaMV-35 S was expressed in transformed common bean plants challenged with Colletotrichum lindemuthianum. The observed response was a significant reduction in the formation of lesions and spore mass proliferation in T0, T1 and T3 lines as compared to non-transformed plants. Twenty-seven T3 common bean transgenic plants from 5 independent lines expressing pdf 1.2 gene showed resistance to C. lindemuthianum races 448 and 1472 compared to non-transformed plants. Analysis ofthe level of pdf 1.2 gene expression by Q-PCR indicated that all plants considered resistant or tolerant had similar levels of transcriptional expression as opposed to susceptible plants, which did not have detectable levels of gene expression.
Key words: Phaseolus vulgaris L., Agrobacterium tumefaciens, antimicrobial peptide, transformation, pdf 1.2 gene, regeneration.
Introducción
La transferencia de genes, aunado a los métodos de mejoramiento convencional pueden acelerar el desarrollo de nuevos cultivos con características específicas tales como resistencia a sequía, adaptación a suelos acidificados, tolerancia a temperaturas extremas, arquitectura de plantas eficaz, mayor vida de anaquel, calidad nutricional y resistencia a enfermedades. Un componente principal en la mayoría de los enfoques genómicos, es el tener un sistema de transformación consistente para desarrollar varias estrategias de identificación de genes, como la sobre expresión de genes, supresión de genes, análisis de promotores, T-DNA tagging y expresión de genes para el mejoramiento de cultivos.
Frijol común es un cultivo con gran diversidad genética que incluye germoplasma con características agronómicas superiores, como la resistencia a condiciones climáticas adversas, resistencia a plagas y enfermedades y una alta calidad nutricional (Cruz de Carvalho et al, 2000); sin embargo, algunos genes que confieren características específicas pueden estar o no presentes en el germoplasma del frijol común y el mejoramiento convencional puede llevar mucho tiempo.
La necesidad de contar con un protocolo que de cómo resultado una generación eficiente de plantas, es un requisito esencial para la transformación genética de plantas. La regeneración directa organogénica de frijol común para dos cultivos comerciales, fue reportada con una alta eficiencia de regeneración (Delgado-Sánchez et al., 2006; Quintero-Jiménez et al, 2010). Sin embargo, últimamente se han reportado eventos de transformación exitosa a través del bombardeo con partículas (Faria et al., 2006; Bonfim et al., 2007).
Debido a la diversidad agroecológica donde el frijol común es cultivado, las poblaciones de patógenos relacionados son muy diversos y su importancia económica es diferente entre regiones. Las enfermedades causadas por hongos son frecuentes y muy devastadoras sobre el cultivo del frijol común. Entre estas enfermedades encontramos rolla, antracnosis, mancha angular de la hoja y pudrición de raíces y muchas especies de Fusarium pueden causar hasta 80% de pérdidas en el rendimiento de semilla (Schwartz et al., 2005).
]]> Muchas proteínas antimicrobianas han sido identificadas y probado su actividad antimicrobiana ante hongos y bacterias. En algunas especies de plantas, las plantas transgénicas que expresan genes de proteínas antimicrobianas ajenos, en calidad adquirieron resistencia a los patógenos (Gao et al., 2000; Kanzaki et al, 2002; Kawata et al, 2003; Faria et al, 2006; Sjahril et al., 2006; Sridevi et al., 2006; Vijayan et al., 2008). Las defensinas son péptidos antimicrobianos con amplio espectro contra microorganismos como las bacterias patógenas de las plantas (Bohlmann, 1994) y hongos (Thevissen et al, 1996; 1999). Las defensinas son pequeños péptidos catiónicos básicos (de 45 a 54 aminoácidos) ricos en cisteina y 5 KDa de tamaño (Lay y Anderson, 2005). Las defensinas tienen la capacidad de actuar sobre las membranas de microorganismo específicos, interactuando bajo sitios específicos, con alta afinidad de unión en células de hongos que inducen los flujos de iones a través de las membranas plasmáticas de las hifas de los hongos vivos y por lo tanto la muerte del hongo (Thevissen et al, 1999).El gen pdf1.2 es una defensina específica de hoja que se expresa ante la presencia de patógenos (Thoma y Broekaert, 1998). Este gen fue aislado de Arabidopsis thaliana y posee una alta homología (> 85%) con los genes que codifican para proteínas antifúngicas. Se sugirió que la función principal de las defensinas en la planta es antifúngico, que actúa, ya sea en el sitio de inoculación o en regiones remotas no inoculadas del tejido (Brown et al, 2003).
El objetivo del presente estudio fue desarrollar plantas genéticamente modificadas de frijol común mediante la transformación mediada por Agrobacterium, que contiene el gen defensina pdf 1.2 proveniente de A. thaliana para conferir resistencia a hongos patógenos como C. lindemuthianum.
Materiales y métodos
Material vegetal
Las semillas de frijol común variedad Flor de Mayo Anita (FMA) (1494-FRI-032-2203 02/C) (Castellanos et al, 2003) fueron utilizados para los experimentos de transformación. Ambos transgénicos primarios T0 y plántulas resistentes a kanamicina a partir de plantas auto polinizadas (T1 y T3) que fueron usadas para experimentos adicionales. Generaciones T0 a T3 fueron genotipeados para ver la presencia del gen pdf 1.2, después de que mostraron resistencia a la kanamicina, rociando las plantas con 50 mg / l durante 4 días seguidos.
Construcción de defensina
El construeto pKYLX80-pdf1.2 contiene el gen defencina ADNe (pdfl.2) (0,438 kb) de Arabidopsis thaliana (Penninekx et al, 1996). El gen pdfl.2 fue regulada por un virus del mosaieo de la coliflor (CaMV) doble, el promotor 35S y el terminador rubiseo del guisante. El gen de la neomieina fosfotransferasa (nptIT) fue seleccionado como marcador que proporciona resistencia a la kanamieina bajo el control del promotor nopalina sintasa (nos) y el terminador nos dé A. tumefaciens (Figura 1). El plásmido se introdujo en la cepa de Agrobacterium GV2260 mediante transformación de choque térmico (Hoisington et al, 1994).
]]>
Procedimiento de transformación
La inducción y medio de multiplicación (IMM) para la germinación de la semilla, la disección de hipocotileos y componentes de los medios fueron deseritas anteriormente (Quintero-Jiménez et al, 2010). Este medio líquido se añadió a la cepa A. tumefaciens GV2260 crecido hasta una DO 600= 0.8 en una proporción 5:1 (v/v), respectivamente. Los hipocotileos se incubaron en esta solución durante 10 min; el líquido se descartó y el exceso eliminado. Los explantes se colocaron en un medio de co-cultivo, que consistia en IMM (Quintero-Jiménez et al, 2010) adicionado con 200 μM acetosiringona.
El medio de eliminación para Agrobacterium consistia de IMM adicionado con 300 mg/L de Timentin (GlaxoSmithKline®). Los hipocotileos se mantuvieron en este medio durante 10 días en las mismas condiciones de cultivo. Los explantes se transfirieron a medio de selección, en los mismos componentes del medio de eliminación de Agrobaeterium modificado con 50 mg/l de kanamieina.
Una vez regenerados los brotes via organogenica, hipocotilcos con grupos de yemas se transfirieron a un medio de selección freseo cada semana y se mantuvieron en los hipocotileos hasta que una planta completa estuviera formada. En todos los pasos las placas Petri fueron selladas e inubadas a 25 °C con un fotoperiodo de 16 h. La intensidad de luz fue 45-70 µmol/m2/seg.
Los brotes difereneiados que permanecieron verdes en el medio de selección se separaron y cultivaron individualmente en cajas Magenta® con medio MTC (Quintero-Jiménez et al., 2010) modificado con 50 mg/l de kanamieina y 300 mg/l de Timentin. Las condiciones de cultivo fueron idénticas a la etapa anterior. Plántulas regeneradas se transfirieron a macetas llenas de Sunshine® Universal Mix (Sun Gro Horticulture Canada Ltd.) y climatizada ex vitro. Las nuevas plantas se colocaron en invernadero a 25-28 °C y 170-285 µmol/m2/sec hasta producción de semilla madura.
Analisis por PCR punto final
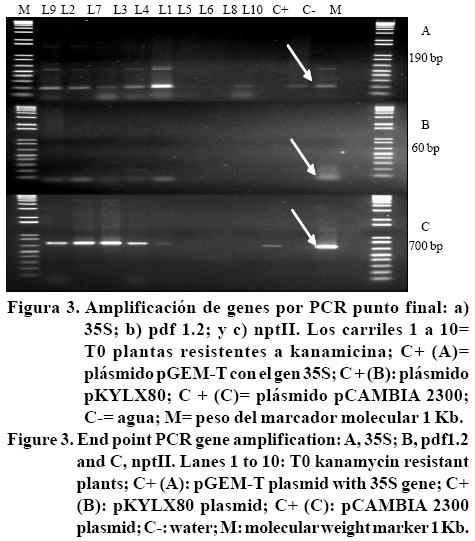
Se aisló el ADN de acuerdo con Murray y Thompson (1980) usando 200 mg de tejido de la hoja por muestra. Las reacciones consistieron en la muestra de ADN (30 ng), iniciadores (0,2 mM), dNTP (0,25 mM), polimerasa Taq (1 U), cloruro de magnesio (2 mM), y amortiguador Taq (1X). El análisis por PCR se hizo utilizando iniciadores nptII, pdf. 2 y promotor 35S. Los iniciadores pdf1.2 (pGV2260-PDF 1.2) y npt II consistieron en sentido defensina 5'- CAT CAT GGC TAA GTT TGC TTC C-3'; defensinas antisentido 3'-CTC ATA GAG TGA CAG AGA CT -5'; sentido nptII 5'-TCG TCGATGACT GGG CAC AACAGA -3 '; antisentido nptII 3'-AAGAAG GCGATA GAA GGC GAT GCG -5'. Los iniciadores para detectar el promotor 35S fue en sentido 35S 5' GATAGT GGG ATT GTG CTG CA 3', antisentido 35S 5 'GCA CCT ACA AAT GCC ATC A 3'. Las condiciones de amplificción para todos los conjuntos de iniciadores fueron 3 min 94 °C durante un cielo, 1 min a 94 °C, 1 min a 55 °C (iniciadores pdf 1.2 y nptII) o 54 °C (iniciadores 35S), y 2 min a 72 °C durante 3 5 cielos y una extensión final de 7 minutos a 72 °C. Los fragmentos esperados eran 60 pb para pdf1.2, 700 pb para gen nptII y 195 pb para el promotor 35S.
Análisis en tiempo real por PCR cuantitativa
Análisis de detección de transgen
]]> Los iniciadores y la sonda fueron diseñados utilizando el programa Primer Expres v2.0 (Applied Biosystems, Foster City, CA) a partir de la secuencia del gen pdf 1.2 (NCBI, NM_123809). El gen defensina, iniciadores específicos y sondas para detectar el gen pdf 1.2 son sentido 5'-AGT TGT GCG AGAAGC CAA GT-3 ', antisentido 3'-GCA TGC ATT ACT GTTTCC GCAAA-5' y la sonda Taq Man® 5 '-CCC TGA CCA TGT CCC -3' con una etiqueta colorante FAM™ y el enlazante al surco menor (MGB) en el extremo 5 ', y el colorante desactivador de fluorescencia (NFQ) en el extremo 3'. El control interno 18S ribosomal (4319413E, Applied Biosystem) fue marcado con fluoroforo VIC. Las condiciones de amplificación consistieron en 95 °C, 10 min (desnaturalización), 45 cielos (amplificación PCR), 95 °C, 15 segundos (desnaturalización) y 60 °C, 1 min (extensión) (ABI PRISM®7000 Sequence).Análisis de la expresión de genes
El ARN celular total se extrajo del tejido de las hojas utilizando Trizol® (Reagent, Carisbald, CA, USA) siguiendo las instrucciones del fabricante. La primera cadena de ADNe se sintetizó usando RT-PCR mediante One-Step RT-PCR Master Mix de Applied Biosystems (Catalago N ° 4309169). El sistema TaqMan® mencionado anteriormente se utilizó para la amplificación de genes. Las condiciones de amplificación consistieron en 48 °C por 30 min (transcripción inversa), 95 °C por 10 min (desnaturalización), 45 cielos (amplificación por PCR), 95 °C por 15 seg y 60 °C por 1 min (extensión) (ABI PRISM®, Sistemas de detección de secuencias 7000, Applied Biosystems).
La proporción de la expresión relativa se calculó mediante la normalización del gen objetivo Ct (pdf 1.2) con referencia al gen control Ct (18S) para obtener sólo la eficiencia del gen defensina (ΔCt= Ctpdff1.2-Ct18Sr) (Livak y Sehmittgen, 2001).
Ensayos de plantas transgénicas para resistencia a hongos
Condiciones de crecimiento para Colletotrichum lindemutianum
Los patotipos 448 y 1472 (ATCC MYA-2277) de C. lindemuthianum (Pastor-Corrales, 1991) fueron cultivados en agar (Difeo®), harina de maíz durante diez días. Las esporas fueron recuperadas mediante la adición de 1 -2 ml de agua estéril y añadiendo 0.5% de Tween 20 y se cuantificaron ajustando la concentración del medio de inoculación a 1.5 x 106 conidios / ml (IM).
Inoculación de hojas tomadas de plantas T0 y plántulas T1 con C. lindemuthianum
Tres hojas trifoliadas fueron tomadas de tres líneas T0 transformadas y plantas FMA no transformadas 60 días después de la transferencia al invernadero. Los trifolios fueron colocados en cámaras húmedas e inoculadas mediante el rociado de IM con patotipo 1 472 de C. lindemuthianum.
Plántulas T1 resistentes a kanamieina fueron germinadas en macetas planas con Sunshine® Growing Mix # 6, (Canadá) en un invernadero a22-25 °C. Cincuenta plantas fueron inoculadas con homocigotos y heterocigotos a 17 días después de que germinaran con IM patotipo 1 472 de C. lindemuthianum. El desarrollo de la enfermedad se evaluó 10 días después de la inoculación sobre la superficie de la hoja cubiertos con lesiones en T0 y plantas T1 (Garrido-Ramírez y Romero-Cova, 1989).
]]> Inoculación de plantulas T3 con C. lindemuthianumCien semillas de Cada línea T3 transformada y los genotipos control FMA, Vietoire (susceptible) (Dufresne et al., 2000.), y Pinto Saltillo (tolerantes) (PV - Reg. Núm. FRI-052-140890) (Acosta-Gallegos et al., 1995) fueron germinadas en macetas planas con Sunshine® Growing Mix # 6 (Canadá) en un invernadero a22-25 °C. Cincuenta plantas fueron inoculadas a los 17 días después de la germinación con la cepa 448 de C. lindemuthianum y cincuenta con la cepa 1472. Las plantas fueron inoculadas rociando 2 ml de IM en la parte de atrás de las hojas simples. Las plantas inoculadas se incubaron en una cámara de crecimiento húmeda por 72 h con una humedad relativa de 90% y una intensidad luz de 45 nmol/m2/sec. Una vez transcurrido este tiempo, las plantas se mantuvieron durante diez días bajo condiciones normales de invernadero hasta la evaluación de la enfermedad.
La enfermedad se evaluó con una escala de 0 a 3, donde 0: es una planta resistente y sin sintomas visibles de la enfermedad; 1 corresponde a una planta tolerante con unos pequeños puntos necrótieos en la parte posterior de la hoja; 2 corresponde a una planta con daños moderada como cireulos necrótieos en ambos lados de la hoja y lesiones en el peciolo o tallo; y 3 corresponde a plantas atacadas severamente con decoloraeión y pérdida de hojas, abundantes lesiones necrótieas en el tallo y peciolos (Garrido Ramirez y Romero-Cova, 1989).
Análisis de la progenie de plantas transgénicas
Después de esto, de 40 a 50 semillas de 5 líneas endogámieas de frijol común transgénieos fueron analizadas por PCR de amplificación fragmentada para el gen pdf 1.2. Las plantas que amplifican el fragmento del gen pdf1.2 fueron evaluadas y el análisis estadistico Chi-cuadrado se realizó para determinar las proporciones de segregación y el número de eventos de inserción.
Resultados y discusión
Transformación de plantas
La transformación mediada por A. tumefaciens de P. vulgaris fue desarrollado en base a los reportes publicados anteriormente sobre regeneración exitosa (Delgado-Sánchez et al., 2006; Quintero-Jiménez et al., 2010). Nos referiremos al explante principal como hipocotileo en lugar del eje del embrión como se informó anteriormente, debido a que las estructuras derivadas de la germinación y la ampliación del embrión deriva en la estructura del hipocotileo (Figura 2a). A partir de los cuatro diferentes ensayos de transformación con A. tumefaciens en var. Flor de Mayo Anita, se observo una respuesta positiva de la organogénesis directa de los hipocotileos. El eomplejo de tejido de brotes organogénicos formados cerea de las células suspensoras indica que el potencial germinativo y regenerador es trasladado a ese lugar facilitando y promoviendo el desarrollo de 2-3 brotes, cada brote tiene plena capacidad para el desarrollo de una planta entera (Figura 2b). Sin embargo, no todos los nuevos brotes se desarrollan con éxito en una planta completa, de hecho la mayoría de los casos el potencial morfogénico fue concentrado en un solo brote (Figura 2e).
Una vez formados los brotes organogénicos, estos permanecieron en los hipocotileos hasta el desarrollo de la planta completa (Figura 2d). En cada transferencia de medio fresco, una capa delgada del hipocotileo fue eliminado hasta que la planta era independiente del hipocotileo. Después de la una formación completa de la planta, las raices formadas en la base del tallo indica que la nueva planta es independiente del hipocotileo, esta fase tomo 2 meses para elongacion y enraizamiento completo (Figura 2e). Todas las líneas T0 mostraron estados fenológieos similares (Figura 2f) en comparación con las plantas no transformadas, estas florecieron y produjeron semillas al mismo ritmo que las plantas testigo (Figura 2g y 2h).
]]> De acuerdo con nuestras observaciones, algunos de los factores que deben ser tomados en consideración para una regeneración constante de plantas transformadas son edad de la semilla (semillas cosechadas el año previo a los experimentos no son adecuados para una regeneración razonable, generalmente las poblaciones de frijol común cosechadas dos a tres años anteriores al experimento tienen mejor capacidad fisiológica para la regeneración), y el tamaño y color de la semilla tiene que ser homogénea dentro de la población a utilizar.Análisis genómico
Lineas T0 aT3 resistentes a la kanamieina fueron analizadas por PCR punto final para verificar la inserción de los principales genes en el genoma de la planta (nptII, 700 pb; 35S, 190 pb, y pdf 1.2, 60 pb) (Figura 3). Éstos resultados fueron confirmados por Q-PCR que muestra la amplificación del gen pdf 1.2 en plantas T1 a T3 amplificadas para todos los componentes del árbol previamente (L2, L3, L4, L7 y L9) (Figura 4).


Inoculación de plantas y detección de resistencia a antracnosis
T0 y T1 líneas transformadas
Diez días después de la inoculación de T0 se desprendieron hojas de frijol común con hongos patógenos de C. lindemuthianum con la cepa 1472, las líneas L3, L4 y L9 tuvieron menor superficie de hoja dañada con bajos niveles de resistencia (14, 50 y 33%, respectivamente), en comparación con las plantas no transformadas (Tabla 1). Sin embargo, una prueba adicional de tolerancia fue el hecho de que habia 80% menos de masas de esporas en los peciolos de la línea L3 que en el control, que muestran 100% de la superficie cubierta con esporas (Figura 5a y 5b). El análisis de varianza indicó diferencias significativas entre las medías de las evaluaciones de la enfermedad (p< 0.001).
]]>

Plantas inoculadas T1 L3 y L4 con la cepa 1 472 mostraron una alta susceptibilidad, similar a las plantas control transformadas (no pdf 1.2), y a las plantas no transformadas, indicando diferencias en la respuesta entre los dos bioensayos para T0 y T1 (Tabla 1). Las líneas L2, L7 y L9 mostraron evidencia de menor lesión de antracnosis (37 a 58% menos daños que las plantas no transformadas) (Tabla 1, Figura 5e y 5d). Comparación por pares de Tukey mostró que las líneas transgénieas L2, L4, L7 y L9 tenian evaluaciones de enfermedad más bajas que las plantas control y que estas evaluaciones diferian entre líneas transgénicas aumentando los niveles de protección en líneas L7 y L9 (Tabla 1).
Expresión transcripcional del gen pdf 1.2 y el análisis del bioensayo para hongos en plantas T1
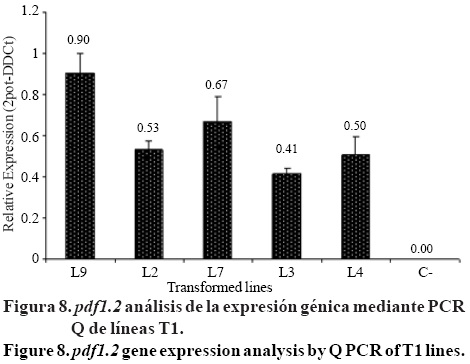
El análisis de la expresión génica de pdf 1.2 en líneas T1 mostraron que la línea transgénica L9 (0.90) tuvieron mayor expresión relativa del gen pdf 1.2 que las otras cuatro líneas T1; L7 (0.66), L2 (0.53), L4 (0.50) y L3 (0.41) (p< 0.001) (Figura 6). Cuando se compararon los valores de expresión relativa con el promedio de la superficie de la hoja cubierta con las lesiones en las plantas T1 resistentes a kanamieina, se encontró que eran inversamente proporcional, por la disminución de la superficie cubierta con lesiones conforme la expresión relativa del gen pdf 1.2 incrementaba (Tabla 1).

Otros parámetros no cuantitativos, tales como las colonias que cubren el peciolo o el nivel de infestación sobre las venas principales, son elementos que deben ser tomadas en consideración en la medición de la resistencia debido algen pdf1.2. Observaciones similares fueron heehas por Kanzaki etal. (2002) en líneas de arroz transformadas con el gen defensina de wasabi, que mostró resistencia al añublo del arroz en diferentes niveles, no necesariamente asociado con el nivel de la expresión génica.
]]> En contraste con los resultados de Vijayan et al. (2008) observaron la inhibición de la clongación de las raices de plantas de A. thaliana, disminuyendo la posterior ampliación de pelos radicales, lo que indica el potencial de la defensina para afectar el crecimiento vegetal de las plantas transformadas, en la investigación reportada en este documento, no hay evidencia de alteraciones fenotipicas derivados de la expresión del gen pdf 1.2 en plantas de frijol transformadas.Expresión transcripcional del gen PDF 1.2 y el análisis de bioensayo por hongos en plantas T3
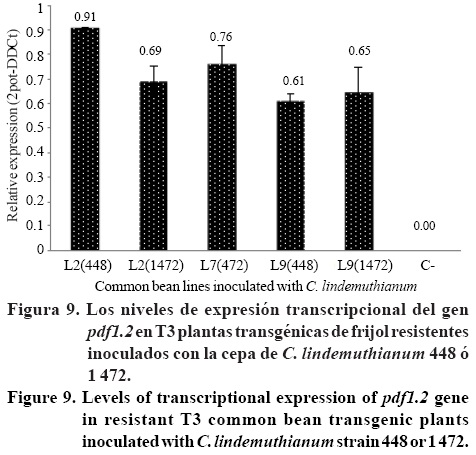
La expresión transeripcional del gen PDF 1.2 en plantas tolerantes y resistentes a T3 C. lindemuthianum mostró que las plantas L2 resistentes a la cepa 448 expresaron el nivel más alto de gen pdf1.2 (0.91), mientras que las plantas de las líneas L2 (1 472), L7 (1 472) y L9 (448 ó 1 472) tenian niveles más bajos de expresión, ya sea una respuesta de resistencia o tolerancia (0.61 - 0.76) (Figura 7). Por otra parte, no hubo diferencia estadistica en los niveles de expresión entre las plantas resistentes y tolerantes.

El análisis de plantas T3 inoculadas con cepas 448 ó 1 472 de C. lindemuthianum identificó 27 plantas resistentes. Tres plantas de la línea L2 y dos L9 de fueron resistentes a la cepa 448, mientras que seis L2, tres L3, siete L7 y seis plantas L9 fueron resistentes a la cepa 1 472. Se observó un análisis de la interacción de dos vias de la varianza entre las líneas transgénieas y cepas C. lindemuthianum (p<0.028), donde las plantas de las líneas L2, L3, L7 y L9 fueron resistentes a la cepa 1472 y las plantas de las líneas L2 y L9 fueron resistentes a la cepa 448 en comparación con el control FMA y Vietoire (Figura 8 y 9). El resto de las plantas de la población fueron tolerantes o susceptibles, incluyendo las plantas FMA no transformadas.
Terras et al. (1995) transformaron tabaeo con el gen defensina AFP2 aislado de Raphanus que confiere resistencia contra Alternaria longipes, reduciendo el área cubierta con lesiones de las plantas T2 entre 7 y 8 veces menos que las plantas heterocigotas y no transformada, respectivamente. De la misma manera, Sjahril etal. (2006) insertaron el gen defensina WjAMP-1 aislado de wasabi en el genoma de Phalaenopsis Watoboushi '# 6.13' que confiere una alta resistencia contra Erwinia carotovora; plantas transformadas fueron asintomáticas una semana después de la inoculación de las bacterias en la superficie de la hoja, mientras que las plantas control, no inoculadas murieron en el mismo periodo de tiempo. Gao et al. (2000) trabajó con un gen defensina alfAFP de alfalfa (Medicago sativa), que se insertó en papa otorgándole una fuerte resistencia contra Verticillium dahliae con valores de ABCPE (área bajo la curva de progreso de la enfermedad) menores que las plantas control resistentes. Además, Koike et al. (2002) transformaron tomate con Rs-AFP2 que proporciona resistencia a un amplio espectro de patógenos como Fusarium oxysporum, Phytophthora infestans, Rhizoctonia solani y Verticillium dahliae.
En los ensayos in vitro realizados por Terras et al. (1995) quien estudió la actividad in vitro de Rs-AFP2 en el crecimiento del hongo Alternaria longipes, informes de fragmentación y reducción en la tasa de crecimiento de hongos. En otro ensayo in vitro de Gao et al. (2000) demostró que el gen alfAFP a una concentración de 5 ug/ ml redujo el número de esporas germinadas de V. dahliae en un 50%. De la misma manera, Sjahril et al. (2006) inoculo E. carotovora directamente en cuatro puntos en la hoja de Phalaenopsis transformada con el gen WjAMP obteniendo una alta resistencia contra éstas bacterias, mientras que las plantas control fueron altamente susceptibles a la enfermedad.
En todos estos reportes, asi como en esta investigación, se resalta la importancia de los genes defensina contra patógenos, principalmente hongos. La reducción en el daño de la hoja y menor formación de esporas en ensayos in vitro de T0, líneas L3, L4 y L9 derivadas de la actividad de gen pdf 1.2 contra C. lindemuhtianum, inhibiendo la germinación y el crecimiento de esporas, de manera similar a los informes anteriores en otras plantas transformadas con el gen defensina (Terras et al., 1995; Wang et al., 1999; Parashina et al., 2000; Gao et al., 2000; Swathi et al., 2008).
A pesar de que los ensayos in vitro podrian mostrar información razonable sobre los niveles de tolerancia o resistencia proporcionada por el gen pdf 1.2, en nuestra experiencia, los bioensayos realizados en plántulas fueron reproducibles y consistentes. Se eree que la reducción en el área cubierta con lesiones y esporas de las líneas transformadas de Flor de Mayo Anita, está relacionado con la actividad del gen pdf 1.2, posiblemente a través de dos mecanismos diferentes, uno es el papel del péptido antimicrobiano codificado por el gen directamente contra el patógeno potenciando la permeabilidad de las membranas, alterando su crecimiento y por la inducción de otras AMP in situ a través de la activación de sus mecanismos de defensa sistémicos (Yedidia et al., 1999; Mora-Avilés y Earle, 2004). Thevissen et al. (1999) establecieron que en defensinas de Raphanus (Rs-AFP2) y dalia (Dm-AMP1) podrían inducir la afluencia de Ca+ 2 y emanación de K+ cuando se pegan sobre las hifas de los hongos, lo que sugiere la inhibieión del crecimiento, lo cual se debe a una disipaeión del gradiente de protones a partir de la célula fúngica haeia el apoplasto provocando una alteración general y la muerte celular.
Análisis de segregación
Las proporciones de segregación y el análisis X2 indicaron que las 5 líneas transgénicas evaluadas mostraron una segregación 3:1 indicando una inserción de genes (<0.05).
Conclusiones
El nivel de protección a partir de la expresión del gen pdf 1.2 fue variable entre y dentro de las líneas; sin embargo, hay evidencia de plantas resistentes sin ningún tipo de lesiones causadas por la cepa 1 472 ó 448, proporcionando evidencia del efecto del gen pdf 1.2 en la protección de las plantas. La reducción en el daño de la hoja y menor formación de esporas en ensayos in vitro de T0, líneas L3, L4 y L9 derivadas de la actividad de gen pdf 1.2 contra C. lindemuhtianum, inhibiendo la germinación y el crecimiento de las esporas, mostrando la importancia de los genes defensina contra los patógenos, principalmente hongos.
]]> Los avances relacionados con el uso de genes que pueden proporcionar resistencia a un amplio espectro se han desarrollado, estos avances y el hecho de que el frijol común puede ser modificado fácilmente; por lo tanto los requisitos están en su lugar para proporcionar una herramienta de transformación que podria estar integrada en el proceso de mejoramiento de frijol común.
Agradecimientos
This project was supported by the Consejo Nacional de Ciencia y Tecnología and Secretaría de Agricultura, Ganadería, Pesca y Alimentación (CONACYT-SAGARPA 2003 002 Núm. 080).
Literatura citada
Acosta-Gallegos J.A.; Ochoa-Márquez R.; Arrieta-Montiel M. P.; Ibarra Pérez F.A.; Pajarito-Ravelero A. and Sánchez-Valdez I. 1995. Registration of "Pinto Villa" common bean. Crop Sci 35:1211. [ Links ]
Bohlmann, H, Broekaert, W. 1994. The role of thionins in plant protection. Crit Rev Plant Sci 13:1-16. [ Links ]
]]>Bonfim, K.; Faria, J. C.; Nogueira, E. O. P. L.; Mendes, E. A. and Aragao, F. J. L. 2007. RNAi-mediated resistance to bean golden mosaie virus in genetieally engincered common bean (Phaseolus vulgaris). MPMI. 20:717-726. [ Links ]
Brown, R. L.; Kazan, K.; MeGrath, K. C.; Maelean, D. J. and Manners, J. M. 2003. A role for the GCC-box injasmonate-mediated activation ofthe PDF1.2 gene of Arabidopsis. Plant Physiol 132:1020-1032. [ Links ]
Castellanos-Ramos, J. Z.; Guzmán-Maldonado, S. H.; Muñoz-Ramos, J. J. and Acosta-Gallegos, J. A. 2003. Flor de Mayo Anita, a new common bean cultivar for the central region of Mexico. Rev. Fitotec. Mex. 26:209-211. [ Links ]
Cruz de Carvalho, M. H.; Van Le, B.; Zuily-Fodil, Y.; Pham, Thi A. T. and Thanh, Van K. T. 2000. Efficient whole plant regeneration of common bean (Phaseolus vulgaris L.) using thin-cell layer culture and silver nitrate. Plant Sci. 159:223-232. [ Links ]
Delgado-Sánchez, P.; Saucedo-Ruiz, M.; Guzmán-Maldonado, S. H.; Villordo-Pineda, E.; González-Chavira, M.; Fraire-Velázquez, S.; Acosta-Gallegos, J. A. and Mora-Avilés, A. 2006. An organogenic plant regeneration system for common bean (Phaseolus vulgaris L.). Plant Sci. 170:822-827. [ Links ]
]]>Dufresne, M.; Perfeet, S.; Pellier,A-L.; Bailey, J.A. and Langin, T.A. 2000. GAL4-like protein is involved in the switeh between biotrophie andncerotrophie phases ofthe infection process of Colletotrichum lindemuthianum on common bean. Plant Cell. 12:1579-1590. [ Links ]
Estrada-Navarrete, G.; Alvarado-Affantranger, X.; Olivares, J. E.; Diaz-Camino, C.; Santana, O.; Murillo, E.; Guillén, G.; Sánehez-Guevara, N.; Acosta, G. J. A.; Quinto, C.; Li, D.; Gresshoff, P. M. and Sánchez F. 2006. Agrobacterium rhizogenes transformation of the Phaseolus spp.: a tool for functional genomies. MPMI 19:1385-1393. [ Links ]
Faria, J. C.; Albino, M. M. C.; Dias, B. B. A.; Caneado, L. J.; da Cunha, N. B.; Silva, L. M.; Vianna, G. R. and Aragao, F. J. L. 2006. Partial resistance to Bean golden mosaic virus in a transgenic common bean (Phaseolus vulgaris) line expressing a mutated rep gene. Plant Sci. 171:565-571. [ Links ]
Gao,A. G.; Hakimi, S. M.; Mittanek, C.A.; Wu, Y.; Woerner, B. M.; Stark, D. M.; Shah, D. M.; Liang, J. and Rommens, C. M. T. 2000. Fungal pathogen protection in potato by expression of a plant defensin peptide. Nat Biotechnol. 18:1307-1310. [ Links ]
Garrido-Ramirez, E. R. and Romero-Cova, S. 1989. Identificación de razas de Colletotrichum lindemuthianum (Saec. & Magn.) Serib. en México y búsqueda de resistencia genética a este hongo. Agrociencia 77:139-156. [ Links ]
]]>Hoisington, D.; Khairallah, M. and González, de L. D. 1994. Laboratory protocols: CIMMYT Applied Molecular Geneties Laboratory. 2th Edition. Mexico, D. F. [ Links ]
Kanzaki, H.; Nirasawa, S.; Saitoh, H.; Ito, M.; Nishihara, M.; Terauehi, R. and Nakamura, I. 2002. Overexpression of the wasabi defensin gene confers enhaneed resistance to blast fungus (Magnaporthe grisea) in transgenic rice. Theor. Appl. Genet. 105:809-814. [ Links ]
Kawata, M.; Nakajima, T.; Yamamoto, T.; Mori, K.; Oikawa, T.; Fukumoto, F. and Kuroda, S. 2003. Genetic engincering for disease resistance in rice (Oriza sativa L.) using antimicrobial peptides. JARQ. 37:71-76. [ Links ]
Koike, M.; Okamoto, T.; Tsuda, S. and Imai, R. 2002. Anovel plant defensin-like gene of winter wheat is specifieally induced during cold aeclimation. Bioch. Biophys Res. Commun. 298:46-53. [ Links ]
Lay, F. T. and Anderson, M.A. 2005. Defensins-components of the innate immune system in plants. Curr Prot Pept. Sci. 6:85-101. [ Links ]
]]>Livak, K. J. and Sehmittgen, T. D. 2001. Analysis of relative gene expression data using real-time quantitative PCR and the 2(-delta delta C(T)) method. Methods 25:402-408. [ Links ]
Murray, M. G. and Thompson, W. F. 1980. Rapid isolation of high molecular weight plant DNA. Nuel Acids Res. 8:4321-4326. [ Links ]
Parashina, E. V.; Serdobinskii, L.A.; Kalle, E. G.; Lavrova, N. V.; Avetisov, V. A.; Lunin, V. G. and Naroditskii, B. S. 2000. Genetic engineering of oilsced rape and tomato plants expressing a radish defensin gene. Rus. J. Plant Physiol. 47:417-423. [ Links ]
Pastor-Corrales, M.A. 1991. Estandarización de variedades diferenciales y de designación de razas de Colletotrichum lindemuthianum. Phytopathology 81:694. [ Links ]
Penninekx I, A. M. A.; Eggermont, K.; Terras, F. R. G.; Thomma, B. P. H. J.; De Samblanx, G. W.; Buehala, A.; Metraux, J. P.; Manners, J. M. and Broekaert, W. F. 1996. Pathogen-induced systemic activation of a plant defensin gene in Arabidopsis follows a salieylie acid-independent pathway. Plant Cell 8:2309-2323. [ Links ]
]]>Quintero-Jiménez, A.; Espinosa-Huerta, E.; Acosta-Gallegos, J.A.; Guzmán-Maldonado, H. S. and Mora-Avilés, M. A. 2010. Enhaneed shoot organogenesis and regeneration in the common bean (Phaseolus vulgaris L.). Plant Cell Tiss. Org. Cult. 102:381-386. [ Links ]
Schwartz, H. F.; Steadman, J. R.; Hall, R. and Forster, R. L. 2005. Compendium of beandiseases. ISBN0-89054-327-5 viii+109 pp. [ Links ]
Sjahril, R.; Chin, P. D.; Khan, R. S.; Yamamura, S.; Nakamura, I.; Amemiya, Y and Mii, M. 2006. Transgenie Phalaenopsis plants with resistance to Erwinia carotovora produced by introducing wasabi defensin gene using Agrobacterium method. Plant Bioteeh. 23:191-194. [ Links ]
Sridevi, G.; Parameswari, C.; Rajamuni, P. and Veluthambi, K. 2006. Identification of hemizygous and homozygous transgenic rice plants in T1 generation by DNA blot analysis. Plant Biotechnol. 23:531-534. [ Links ]
Swathi, A. T.; Divya, K.; Jami, S. K. and Kirti, P. B. 2008. Transgenie tobaeeo and peanut plants expressing a mustard defensin show resistance to fungal pathogens Plant Cell. Rep. 27:1777-1786. [ Links ]
]]>Terras, F. R. G.; Eggermont, K.; Kovaleva, V.; Raikhel, N. V.; Osborn, R. W.; Kester, A.; Rees, S. B.; Torrekens, S.; Van Leuven, F.; Vanderleyden, J.; Cammue, B. P. A. and Broekaert, W. F. 1995. Small eysteine-rich antifungal proteins from radish: their role in host defense. Plant Cell. 7:573-588. [ Links ]
Thevissen K.; Ghazi, A.; De Samblanx, G. W.; Brownlee, C.; Osborn, R. W. and Broekaert, W. F. 1996. Fungal membrane responses induced by plant defensins and thionins. J. Biol. Chem. 271:15018-15025. [ Links ]
Thevissen, K.; Terras, F. R. G. and Broekaert, W. F. 1999. Permeabilization of fungal membranes by plant defensins inhibits fungal growth. Appl. Environ. Mierobiol. 65:5451-5458. [ Links ]
Thomma, B. P. H. J. and Broekaert, W. F. 1998. Tissue-speeifie expression of plant defensin genes PDF2.1 and PDF2.2 in Arabidopsis thaliana. Plant Physiol. Bioehem. 36:533-537. [ Links ]
Vijayan, S.; Guruprasad, L. and Kirti, P. B. 2008. Prokaryotie expression of a constitutively expressed Tephrosia villosa defensin and its potent antifungal aetivity. Appl. Mierobiol. Bioteehnol. 80:1023-1032. [ Links ]
]]>Wang, Y.; Nowak, G.; Culley, D.; Hadwiger, L.A. and Fristensky, B. 1999. Constitutive expression of pea defense gene DRR206 confers resistanee to blaekleg (Leptosphaeria maculans) disease in transgenie canola (Brassica napus). MPMI 12:410-418. [ Links ]
]]>