
Efecto de los campos eléctricos pulsantes sobre la estructura de la α-lactoalbúmina bovina
Effect of pulsed electric fields on the structure of bovine α-lactalbumin
M.R. Robles-López1,2, R. Robles de la Torre2, M. Camarillo-Cadena3, A. Hemández-Arana3, J.S. Welti-Chanes4 y H. Hernández-Sánchez1*
1 Depto. Graduados e Inv. Alimentos, Escuela Nacional de Ciencias Biológicas, Instituto Politécnico Nacional, Carpió y Plan de Ayala, México, DF México. * Autor para la correspondencia. E-mail: hhernan1955@yahoo.com Tel.57-29-60-00 ext 62461, Fax ext 62463
]]> 2 Centro de Investigación en Biotecnología Aplicada, Instituto Politécnico Nacional, Tepetitla, Tlaxcala, México.3Depto. de Química, Universidad Autónoma Metropolitana Unidad Iztapalapa, México, DF, México.
4Instituto Tecnológico y de Estudios Superiores de Monterrey Campus Monterrey, Monterrey, NL, México
Recibido 20 de Septiembre 2012
Aceptado 9 de Octubre 2012
Resumen
El procesamiento por campos eléctricos pulsantes (CEP) es una tecnología no térmica de conservación de alimentos que usa descargas muy cortas de electricidad para la inactivación de enzimas y microorganismos sin alterar las propiedades del alimento. El objetivo del presente trabajo fue aplicar CEP para provocar cambios estructurales en la α-lactoalbúmina bovina (α-LA). Los tratamientos se realizaron en un electroporador usando intensidades de campo de 4.5, 9 y 10 kV/cm con 2, 4 y 10 pulsos de onda cuadrada con frecuencia de 0.2 Hz. Los cambios se evaluaron a valores de pH de 3, 7, y 10. Los análisis de fluorescencia (ANS), mostraron que a mayor intensidad de campo y número de pulsos se incrementa la hidrofobicidad. Con dicroísmo circular se observaron cambios moderados en las estructuras secundaria y terciaria provocados por Oou CEP. Con estos resultados es posible concluir que los CEP pueden usarse para modificar la estructura de proteínas como la α-LA sin llegar a desnaturalizarlas, con la posibilidad de generar características funcionales específicas para aplicaciones particulares.
Palabras clave: campos eléctricos pulsantes, α-lactoalbúmina bovina, estructusa de proteínas, glóbulo fundido, hidrofobicidad.
]]>Abstract
Pulsed electric field (PEF) processing is a non-thermal method of food preservation that uses short bursts of electricity for enzyme and microbial inactivation causing minimal effect on food quality. The purpose of this work was to apply PEF to induce structural changes in bovine α-lactaltamin (α-LA). 'The treatments were performed in an electroporator with field intensities of 4.5, 9 and 10 kV/cm, using 2, 4 and 10 squate wave pulses and a 0.2 Hz frequency. Changes were evaluated in PEF-treated protein solutions buffered at pH values of 3, 7 and 10. ANS fluorescence analysis indicated that the higher the field intensity and number of pulses, the higher the protein hydrophobicity. PEF induced moderate changes in the protein secondary and tertiary structure as determined by circular dichro ism. These retults indicate that PEF can idduce non-denaturing changes in the structure of proteins such as α-LA with the possibility of generating beneficial changes in their functional properties for specific food uses.
Keywords: pulsed electric fields, bovine α-lactalbumin, protein structure, molten globule, hydrophobicity.
1 Introducción
El uso de nuevos factores de conservación en alimentos ha dado origen al desarrollo de tecnologías emergentes con un enfoque particular al desarrollo de alimentos mínimamente procesados. Un proceso de conservación que ha despertado interés dentro de las tecnologías emergentes es la aplicación de campos eléctricos pulsantes (CEP) (Barbosa-Cánovas y col., 1998; Bendicho y col., 2002, 2005). Esta tecnología tiene como característica principal la de ser un tratamiento no termico, de corta duración, de bajo impacto sobre el material tratado y que ha demostrado su eficiencia en la inactivación de enzimas y microorganismos patógenos, principalmente en alimentos líquidos. Este proceso es una aplicación de la electricidad totalmente diferente a otras previamente utilizadas como la electroforesis (Aguilar y col., 2009; Garza-García y Lapizco-Encinas, 2010), electro coagulación (Piña-Soberanis y col., 2011) y electro incineración (Solís-Obay col., 2009).
La aplicación de los CEP se ha estudiado para demostrar su capacidad de disminuir cargas microbianas y/o actividades enzimaíticas no deseadas (Sale y Hamilton, 1968; Qin y col., 1995; Zhang y col., 1994; Zhang y col., 1995; Gongora-Nieto y col., 2002; Bendicho y col., 2002; Elez-Martínez y col., 2006). Existen diversos estudios en que se evalua la inactivación de enzimas con CEP, como es el caso de la inactivación de polifenoloxidasas de diversos productos vegetales (González y col., 1999; Zhong y col., 2005; Mayer, 2006), papaína, (Yeom y col., 1999), lipoxigenasas de jitomate (Min y col., 2003), proteasas microbianas (Bendicho y col., 2005). Se ha propuesto que los CEP afectan los enlaces más débiles que le dan estabilidad a las proteínas, como son los puentes de hidrogeno, fuerzas electrostáticas y fuerzas de van der Waals (Yeom y col., 2002).
Las propiedades funcionales de las proteínas están estrechamente relacionadas a su hidrofobicidad superficial y de ella depende su capacidad para formar espumas o emulsiones. Cuando se hace alguna modificación en la estructura de alguna proteína sin cambiar la secuencia de los aminoácidos de su cadena principal, se obtienen cambios en la respuesta de las propiedades funcionales (Ju y col., 2001; Liu y col., 2009).
En la aplicación de otras tecnologías emergentes se ha observado que al someter la α-LA a altas presiones hidrostáticas (HHP), la estructura primaria permanece intacta durante el proceso, mientras que la estructura secundaria y terciaria si se ven afectadas en diversos grados produciendo cambios en la funcionalidad. (Rodiles-López y col., 2008).
]]> Adicionalmente, la espectroscopía de fluorescencia permite observar cambios en los residuos de triptofano como resultado de variaciones en la estructura de las proteínas y sus interacciones (Vivian y Callis, 2001). Si los fluorocromos que dan respuesta son los propios aminoácidos de la proteína como el triptofano, tirosina o fenilalanina, el fenómeno se conoce como fluorescencia intrínseca. Si se desea en cambio conocer la hidrofobicidad superficial es necesario usar marcadores como compuestos anionicos alifaíticos (ácido cis-parinárico) o aromaticos (ácido 1-anilino-naftaleno-8-sulfonico o ANS) que se unen a compuestos no polares de la superficie de la molecula proteíca (Alizadeh-Pasdar y Li-Chan, 2000). De esta forma se han reportado los efectos de los CEP en proteínas por medio de un anaílisis de fluorescencia como en el caso de la β-lactoglobulina (Pérez y Pilosof, 2004), clara de huevo (Jeantet y col., 1999), peroxidasa de rábano (Zhong y col., 2005) y pectin metil esterasa (Zhong y col., 2005). Adicionalmente el dicroísmo circular es una técnica ampliamente utilizada para analizar la estructura secundaria de proteínas en solución, cuyo principio se basa en la actividad optica de cada uno de los aminoácidos y de los enlaces al desviar la luz ultravioleta polarizada. Los diferentes tipos de estructura secundaria pueden producir espectros característicos y cada espectro de una determinada proteína puede utilizarse para estimar el porcentaje de las diferentes clases de estructuras secundarias, (Pérez-Iratxeta y Andrade-Navarro, 2008).El presente trabajo tiene como objetivo aplicar campos eléctricos pulsantes (CEP) para provocar cambios estructurales en la α-LA bovina y evaluar los efectos de estos cambios sobre las características estructurales de dicha proteína del suero lácteo.
2 Materiales y métodos
2.1 Proteína y tratamientos con CEP
Se utilizó la proteína α-lactoalbúmina bovina (α-LA) donada por Davisco Foods International Inc. (Eden Prairie, MN, EUA). Para los tratamientos con los CEP se disolvió la proteína al 10%p/v en agua desionizada. Los tratamientos de CEP se aplicaron con un equipo de electroporación Gene Pulser X Cell de Bio-Rad Laboratories (Hercules, CA, EUA) con onda cuadrada y una intensidad de campo de 10, 9 y 4.5 kV/cm, 0.2 Hz de frecuencia y duración del pulso de 5 μ, con 2, 4, y 10 pulsos. En todos los casos la temperatura se midió después de cada pulso y no excedió a 50°C. Las muestras tratadas fueron congeladas y liofilizadas en un equipo FreeZone Freeze Dry de Labconco (Kansas City, MO, EUA), a condiciones de operación de 50 -60 x 10-3 milibares y temperatura del condensador -28 a -49 °C.
Para cuantificar los cambios provocados por el tratamiento con los CEP, las muestras de proteína liofilizada se disolvieron en soluciones buffer de fosfato (0.1M) con valores de pH de 3, 7, 10. La selección de los valores se basó en los siguientes hechos: a pH 3 se tiene a la α-LA en un estado conocido como glóbulo fundido ácido que ha sido estudiado a profundidad (Kelkar y col., 2010); a pH 10 se tiene un estado similar aunque no tan evidente (Kronman y col., 1967) y a pH 7 se tiene el estado nativo de la proteína, el cual sirve de testigo en este caso. Los glóbulos fundidos son estados de plegamiento parcial que se piensa se asemejan a las estructuras formadas durante el plegamiento de las proteínas (Demarest y col., 1999).
2.2 Hidrofobicidad superficial
La determinación de hidrofobicidad de la α-LA se realizó, de acuerdo a la técnica propuesta por Kato y Nakai (1980) usando como sonda de fluorescencia al ANS. La excitación de la molecula se realizó con luz de longitud de onda de 380 nm y el pico de máxima respuesta se observó a 450 nm. Las mediciones de fluorescencia se realizaron en un equipo K2 Multifrecuency Phase Fluorometer (ISS, Inc., Champaign, IL, EUA) con muestras diluidas en buffer de fosfatos 0.1M con pH de 3, 7, y 10, con una concentración final de proteína de 50 mg/ml y con temperatura controlada a 25°C.
]]>2.3 Dicroísmo circular (DC)
Los espectros de DC fueron obtenidos en un espectropolarímetro Jasco J-715 (Jasco Co. Ltd., Hachioji, Japon), las determinaciones se realizaron con temperatura constante y controlada a 25 ± 0.1°C, con un ancho de banda de 2 nm, y con pasos de 0.2 nm, una velocidad de análisis de 5 nm/min. Para la obtención de los espectros de DC en UV lejano se utilizó una cubeta de 1 mm longitud y soluciones de 0.15 mg/ml de α-LA de acuerdo a lo propuesto por Rodiles-López y col. (2010). Para evaluar los cambios en las estructuras secundarias de la proteína en estudio, se uso el programa D2K2 (Pérez-Iratxeta1 y Andrade-Navarro, 2008). Los espectros de DC con UV cercano se registraron en una cubeta de 1cm y soluciones de 1 mg/ml de α-LA.
Todos los datos obtenidos fueron sometidos a un análisis de varianza de una vía (ANOVA) a un nivel de significancia de 5%, los tratamientos involucrados en un experimento se consideraron significativamente diferentes cuando al valor de F le correspondió una p ≤ 0.05.
3 Resultados y discusión
3.1 Efecto del tratamiento con CEP sobre la hidrofobicidad de la α-LA
En las figs. 1, 2 y 3 se muestran los resultados de los cambios de hidrofobicidad en la α-LA con y sin tratamiento evaluada a través de los estudios de fluorescencia, a los tres niveles de pH considerados en este estudio.



La concentración de la proteína (50 μg/ml) de cada muestra fue medida previamente por absorbancia a 280 nm e igualada en todas las muestras, de tal forma que los cambios en altura del pico máximo representan solamente el efecto de los tratamientos con CEP. En la Fig. 1 el pico máximo corresponde al mayor efecto provocado por los CEP sobre la α-LA (9 kV y 10 pulsos).
En la Fig. 1 se puede observar que las muestras tratadas con CEP y disueltas a pH 3, muestran cambios de zonas hidrofóbicas con respecto a la muestra sin tratar. Las muestras tratadas con un campo menor (4.5 kV/cm) y menor número de pulsos no mostraron cambios importantes en relación a la muestra sin tratar. Se observa en la Fig. 1 que la muestra tratada con 9 kV/cm y 10 pulsos presenta los mayores cambios en fluorescencia con referencia a la muestra no tratada; ese incremento se refleja en una mayor hidrofobicidad de la proteína. En concordancia con los resultados obtenidos, Zhon y col. (2005), relacionaron la inactivación de peroxidasas de rábano al aplicar CEP con una disminución de las estructuras alfa hélice medida por dicroísmo circular y fluorescencia. Li y col. (2007) sugieren que a mayor tiempo de tratamiento con CEP se induce un desdoblamiento molecular en las proteínas causando la exposición de grupos hidrofóbicos y cuando la intensidad del campo y el tiempo de exposición aumentan, la solubilidad decrece probablemente debido a la agregación de moléculas por interacciones hidrofobicas.
Cuando la muestra se disolvió a pH 7, se pudo observar en la Fig. 2 que se presentan cambios tanto en la forma de los espectros, como en la intensidad de fluorescencia con ANS. Estos cambios son respuesta a los efectos de los CEP; hay que destacar que la α-LA es más estable en pH 7 (Robbins y Holmes, 1970) y hay diferencias entre todas las muestras. La mayor hidrofobicidad se obtuvo a 10 kV y 2 pulsos y la menor hidrofobicidad fue al aplicar 4.5 kV y 2 pulsos.
En la Fig. 3 se puede observar que los valores de fluorescencia son menores que los obtenidos en las muestras disueltas en los buffers de menor pH (figs. 1 y 2). Cuando las muestras se solubilizaron a pH 10, todas presentaron un espectro de emisión similar indicando que posiblemente la proteína estaba parcialmente desnaturalizada a causa del pH, además de los efectos de la aplicación de los CEP. Peng y col. (1995) describen que las interacciones hidrofóbicas juegan un papel importante en las estructuras secundarias. En este estudio, al disminuir la hidrofobicidad se provocan cambios en la estructura y probablemente la molécula se compacta observándose entonces una posible desnaturalización en la Fig. 3. Es por esta razón que todos los espectros son similares tanto en intensidad de los picos como en la forma del espectro.
]]> Se observa, con estos resultados de fluorescencia, que la aplicación de CEP afecta la estructura terciaria de la α-LA y que cuando esta proteína desnaturalizada se solubiliza a diferente pH su comportamiento difiere entre tratamientos, principalmente a pH de 3 y 7. La estructura terciaria de las proteínas depende en gran medida de las interacciones electrostáticas del medio (pH) y de su fuerza ionica. Estos factores influyen tanto en la carga de los aminoácidos que forman la cadena principal como en la disposición espacial de los mismos. Los resultados del tratamiento con CEP podrían indicar que efectivamente estos provocan un cambio estructural en la proteína y que el medio influye directamente en la estructura proteica.Li y col. (2007) encontraron que la hidrofobicidad de un extracto proteica de soya aumenta al ser tratada con CEP, sugiriendo que este fenómeno ocurre debido a un desdoblamiento de la cadena principal destruyendo las interacciones hidrofóbicas y causando la exposición en la superficie de la proteína de los grupos hidrofóbicos. Por otra parte Jeantet y col. (1999) reportaron que la aplicación de campos de 20-35 kV/cm y de 2-8 pulsos no induce cambios en hidrofobicidad ni desnaturalización en las proteínas de clara de huevo.
En los resultados obtenidos por Permyakov y col. (1985), se muestra que los medios tanto acidos como alcalinos provocan modificación en la estructura de la α-LA detectados por fluorescencia y atribuidos a los residuos de triptofano que quedaron más expuestos por desdoblamiento de la proteína. Estos cambios al parecer son producidos por una protonación de los residuos de aminoácidos.
3.2 Efecto del tratamiento con CEP sobre los cambios en la estructura terciaria de la α-LA evaluados por dicroísmo circular en UV cercano
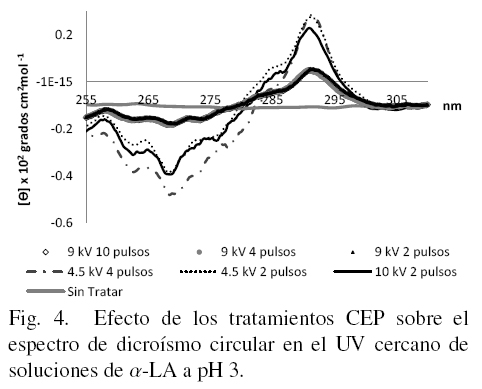
La evaluación de los cambios estructurales en las muestras de α-LA tratadas con CEP observados a través de DC en UV cercano se presenta en las figs. 4, 5 y 6. En la Fig . 4 se presentan los espectros de la α-LA disuelta en medio ácido (pH 3) y se puede concluir en base a los trabajos de investigación de Robbins y Holmes (1970) acerca de los espectros de la α-LA a diferentes valores de pH, que la proteína sin tratar estaba en estado de glóbulo fundido porque el espectro no presenta los picos y valles característicos de la proteína nativa. Aquí se pueden observar líneas casi paralelas al eje de las abscisas. Esto se debe a que parte de la estructura terciaria se ha perdido por efecto del pH. Un comportamiento similar se presenta con el tratamiento de 9 kV/cm con 2 y 4 pulsos. Sin embargo, las muestras tratadas con 4.5 kV/cm aparentemente muestran mas resistencia al medio ácido y no se pierde tanto su estructura terciaria.
]]>


La proteína nativa en un intervalo de pH donde es estable (5.4 a 8.0) presenta espectros de DC con bandas negativas cercanas a 296 nm, por la presencia de triptofano, (Robbins y Holmes, 1970). Cuando el pH baja, las bandas de elipticidad a 296 y 272 nm también bajan e indica que los residuos de triptofano tienen una mayor libertad de movimiento a pH ácido y alcalino por la desnaturalización proteica. Se sabe que en la α-LA control a pH 3 (en estado de glóbulo fundido) los triptofanos están en un ambiente que restringe su movimiento (Kelkar y col., 2010). En este caso los tratamientos con CEP logran eliminar en parte estas restricciones creando estructuras nuevas.
Las señales que presentan los espectros de las figs. 4, 5 y 6 en la cercanía a 270 nm corresponden a residuos de fenilalanina, a 290 nm al triptofano y a tirosina en los 280 nm. Las señales ausentes (picos) indican desnaturalización de la proteína.
En la Fig. 5 se muestran los espectros de la proteína disuelta a pH 7. En este caso la muestra tratada con 10 kV/cm y 2 pulsos muestra un mayor cambio en las zonas donde se ubican los residuos de tirosina (270nm) y los de fenilalanina (de 255 a 270 nm) y el triptofano (296 nm) (Kelly y Price, 2000). Estos cambios indican un posible aumento en la libertad de movimiento en la proteína tratada, en comparación con la proteína nativa, aunque es importante señalar que las muestras de proteína tratada no se encuentran en estado desnaturalizado sino en diferentes estados intermedios del tipo glóbulo fundido.
Las diferencias observadas en la Fig. 5 indican que si hay cambios provocados por el tratamiento con CEP y que dependen además en gran medida, del medio donde se encuentren. El efecto del pH aquí encontrado están de acuerdo con lo reportado por Robbins y Holmes (1970), quienes señalaron que el espectro de la α-LA en estado nativo en un intervalo de pH 5.4 a 8 es independiente del pH mostrando un espectro negativo cerca de 290 nm, el máximo cercano a 272 nm; pero cuando la muestra se encuentra en un intervalo de pH mayor de 10.2 la elipticidad en la región de 275 a 295 nm se ve disminuida del 75 al 80 % y a pH 11.5 la desnaturalización es completa y la elipticidad empieza a ser positiva.
En la Fig. 6 se presentan los espectros obtenidos de DC en el UV cercano para α-LA disuelta a pH 10. Es posible observar que la muestra sin tratar se encuentra en el centro de los espectros, existiendo cambios entre las muestras con los diferentes tratamientos aumentando o disminuyendo la elipticidad, (Kelly y Price, 2000), causada por la aplicación de los pulsos, la máxima elipticidad se obtuvo en la muestra de 4.5 kV con 4 pulsos.
Los cambios en los espectros ponen de manifiesto que los residuos de aminoácidos aromáticos tirosina, triptofano y fenilalanina, que son hidrofóbicos y que se encuentran al interior del glóbulo proteíco, por efecto de los tratamientos de CEP quedaron expuestos hacia la zona hidrofílica.; hay que notar, sin embargo, que las muestras presentan patrones diferentes, en función del pH de disolución de la proteína, es decir; en medio ácido (Fig. 4), neutro (Fig. 5), o básico (Fig. 6).
]]> Peng y col. (1995) han demostrado que la α-LA posee un sitio de union de alta afinidad por cationes divalentes (Ca2+, Mg2+, Mn2+) y que el enlace provoca un cambio conformacional que resulta en una exposición de algunos residuos de triptofano de la superficie de la proteína a un interior rígido y no polar de la macromolécula de proteína. Este cambio asemeja lo que ocurre durante la transición a pH ácido de la proteína nativa. Estos autores sugieren que la transición acida conocida en α-LA es debida a un reemplazo cooperativo competitivo del Ca2+ por tres H+.
3.3 Efecto del tratamiento con CEP sobre los cambios en la estructura secundaria de α-LA evaluados por dicroismo circular (DC) en el UV lejano
Los estudios de DC en UV lejano permiten tener una evaluación más detallada de los cambios en la estructura secundaria de la proteína. Los espectros obtenidos en esta región se muestran en las figs. 7, 8 y 9 a cada uno de los valores de pH en los que la proteína fue disuelta después de los tratamientos.


]]>
Las muestras de α-LA tratadas con CEP y sin tratar evaluadas a pH 3 y 10 muestran algunas diferencias en el espectro obtenido en el UV lejano, esto es, se observan algunos cambios en la elipticidad (espectros), sin que se pierdan las estructuras originales de la proteína, es muy probable que alguno(s) de los aminoácidos cambien de carga y provoquen el rompimiento de interacciones electroestadísticas y/o formen nuevas interacciones con aminoácidos cercanos.
No se detectaron cambios en el caso de la α-LA tratada con CEP con respecto a la muestra sin tratar para el caso de pH 7 (Fig. 8), donde se sabe que la proteína es más estable.
Todas las muestras tratadas con CEP parecen tener un comportamiento similar en su estructura secundaria y no se observan cambios muy grandes; la muestra con mayores diferencias en relación a la muestra sin tratar es la que recibió un tratamiento de 9 kV/cm y 2 pulsos.
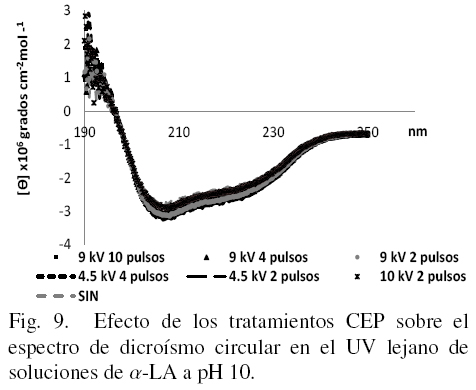
En la Fig. 9 se presentan los resultados de las muestras tratadas con CEP y diluidas en buffer de fosfatos a pH de 10.
En el presente estudio todos los tratamientos parecen haber afectado o modificado la forma nativa de la proteína de alguna forma aunque sin llegar a una desnaturalización total de la misma ya que solo se manifiestan algunas diferencias en hidrofobicidad superficial y estructura terciaria principalmente. Para apreciar mejor si también existen cambios en la estructura secundaria se introdujeron los datos de DC en el UV lejano en el software K2D2 (Pérez-Iratxeta1 y Andrade-Navarro, 2008) para obtener los porcentajes de los tres tipos principales de estructura secundaria, los cuales se muestran en la Tabla 1. Si se comparan los datos para los tres valores de pH en las muestras sin tratamiento, se puede observar que mientras más ácido o más básico es el medio en que se disuelve la α-LA, menos porcentaje de estructura al azar tiene, siendo esto a expensas principalmente de un incremento en la estructura del tipo alfa-hélice.

]]> De acuerdo con Robbins y Holmes (1970), la α-LA esta formada por aproximadamente un 25% de estructura alfa hélice, un 15 % de hojas beta y un 60 % de estructura al azar, estos valores son similares a los presentados en la Tabla 1 específicamente cuando la proteína están a pH 7; se observa también en este Cuadro que aunque el pH juega un papel muy importante en la estructura secundaria de la proteína, también se observan cambios provocados por el tratamiento con CEP; a pH 3 las variaciones van desde un 12 % hasta un 24 % de cambios en relación a la muestra sin tratamiento, a pH 7 no hay diferencias significativas debidas a la aplicación de los diferentes tratamientos y a pH 10 las diferencias por efectos de CEP oscilan desde 6.4 hasta casi un 12%, concluyendo que los CEP provocan una disminución en los proporciones de alfa hélices: hojas beta de la α-LA detectables solo a valores de pH de 3 y 10. También se puede observar de la Tabla 1, que los cambios son mas grandes a mayores intensidades de campo y que el número de pulsos no ejerce una diferencia significativa.
Con los resultados aquí obtenidos se ha demostrado que se producen cambios ligeros en la estructura terciaria, una variación en la hidrofobicidad superficial dependiente del tratamiento y una disminución en la cantidad de estructura alfa-hélice concomitante a un incremento en hoja beta por efecto del tratamiento con CEP con relación a la α-LA sin tratar. Al parecer la aplicación de los CEP favorece la conversión de alfa hélices a hojas beta en medios ácidos o alcalinos. Este efecto fue observado también por Rodiles-López y col. (2010) cuando aplicaron altas presiones hidrostáticas a la α-LA. Cabe la posibilidad de que estos cambios puedan ser atribuidos a modificaciones de los ángulos formados por los puentes de hidrogeno en las alfahelices y a la desnaturalización ocurrida por ruptura de interacciones hidrofóbicas y electroestáticas por efecto de los CEP (Rogers y Sternberg, 1984).
Conclusiones
La aplicación de CEP en la α-LA provocan diferentes niveles de hidrofobicidad, causando cambios en los espectros de fluorescencia. Los cambios observados dependen en gran medida de los diferentes niveles de las condiciones del tratamiento (especialmente de la intensidad de campo eléctrico); los cambios provocados por el tratamiento con CEP también fueron detectados en los espectros de dicroísmo circular, tanto en el UV cercano como en el lejano. Se observó un efecto adicional en las moléculas de α-LA causado por el medio donde se solubilizaron las muestras, sin embargo, dentro de cada valor de pH también se observaron diferentes comportamientos debidos a los CEP y que incluyen principalmente leves cambios en la estructura terciaria y variaciones en los diferentes tipos de estructura secundaria, principalmente alfa-hélice y hojas beta. El gran número de estructuras diferentes de α-LA obtenidas a través de la variación de pH y los tratamientos con CEP permite predecir que las propiedades funcionales resultantes también serán variadas y con gran potencial de aplicación en alimentos. Todas estas estructuras son intermedias entre el estado nativo y el desnaturalizado.
Agradecimientos
El primer autor (Robles-López) agradece el apoyo del Comité Técnico de Prestaciones a Becarios (COTEPABE) del IPN por la licencia parcial otorgada para cursar el Doctorado en Alimentos en la Escuela Nacional de Ciencias Biológicas del Instituto Politécnico Nacional, reconocido por el CONACyT dentro del Padrón Nacional de Posgrados de Calidad como Programa Competente a Nivel Internacional.
Referencias
]]>Aguilar, O., Rito-Palomares, M. y Glatz, C.E. (2009). Caracterización tridimensional de proteínas de soya mediante electroforesis de dos dimensiones y partición en fases acuosas. Revista Mexicana de Ingeniería Química 8, 5765. [ Links ]
Alizadeh-Pasdar, N. y Li-Chan, C.Y. (2000). Comparison of protein surface hydrophobicity measured at various pH values using three different fluorescent probes. Journal of Agricultural and Food Chemistry 48, 328-334. [ Links ]
Barbosa-Cánovas, G., Pothakamury, U. R. y Palou, E. (1998). Nonthermal Preservation of Foods. Ed. Marcel Dekker, Inc., Nueva York. [ Links ]
Bendicho, S., Barbosa-Cánovas, G. y Martin O. (2002). Milk processing by high intensity pulsed electric fields. Trends in Food Science & Technology 13, 195-204. [ Links ]
Bendicho, S., Marsellés F., Barbosa-Cánovas G. y Martin-Belloso O. (2005). High intensity pulsed electric fields and heat treatments applied to a protease from Bacillus subtilis. A comparison study of multiple systems. Journal of Food Engineering 69, 317-323. [ Links ]
]]>Demarest, S.J., Boice, J.A., Fairman, R. y Raleigh, D.P. (1999). Defining the core structure of the α-lactalbumin molten globule state. Journal of Molecular Biology 294, 213-221. [ Links ]
Elez-Martínez, P., Aguiló-Aguayo, I. y Martin-Belloso, O. (2006). Inactivation of orange juice peroxidase by high-intensity pulsed electric fields as influenced by process parameters. Journal of the Science of Food and Agriculture 86,71-81. [ Links ]
Garza-García, L.D. y Lapizco-Encinas, B.H. (2010). Estado del arte en la manipulation de proteínas empleando electroforesis. Revista Mexicana de Ingeniería Química 9, 125-137. [ Links ]
Gongora-Nieto, M.M., Sepúlveda, D., Pedrow, P., Barbosa, C. y Swanson, B. (2002). Food processing by pulsed electric fields: treatment delivery, inactivation level, and regulatory aspects. Lebensmittel-Wissenschaft und-Technologie 33, 275-288. [ Links ]
González, E., Ancos, B. y Cano, M. (1999). Partial characterization of polyphenol oxidase activity in raspberry fruits. Journal of Agricultural and Food Chemistry 47, 4068-4072. [ Links ]
]]>Jeantet,R., Baron, F., Nau, F., Roignant, M. y Brule, G. (1999). High intensity pulsed electric fields applied to egg white: effect on Salmonella enteritidis inactivation and protein denaturation. Journal of Food Protection 62, 1381-1386. [ Links ]
Ju, Z.Y., Hettiarrachchy, N.S. y Rath N. (2001). Extraction, denaturation and hydrophobic properties of rice flour proteins. Journal of Food Science 66, 229-232 [ Links ]
Kato, A. y Nakai, S. (1980). Hydrophobicity determined by a fluorescence probe method and its correlation with surface properties of proteins. Biochimica et Biophysica Acta 624, 13-20. [ Links ]
Kelkar, D.A., Chaudhuri, A., Haldar, S. y Chattopadhyay, A. 2010. Exploring tryptophan dynamics in acid-induced molten globule state of bovine alpha-lactalbumin: a wavelength-selective fluorescence approach. European Biophysics Journal 39, 1453-1463. [ Links ]
Kelly, S.M. y Price, N.C. (2000). The use of circular dichroism in the investigation of protein structure and function. Current Protein and Peptide Science 1, 349-384. [ Links ]
Kronman, M.J., Holmes, L.G. y Robbins, F.M. (1967). Inter- and intramolecular interactions of α-lactalbumin. VIII. The alkaline conformational change. Biochimica et Biophysica Acta 133, 46-55. [ Links ]
Li, Y., Chen, Z. y Mo, H. (2007). Effects of pulsed electric fields on physicochemical properties of soybean protein isolates. Lebensmittel Wissenschaft und-Technologie 40, 1167-1175. [ Links ]
Liu, X., Ning, J. y Clark, S. (2009). Changes in structure and functional properties of whey proteins induced by high hydrostatic pressure: a review. Frontiers of Chemical Engineering in China 3, 436-442. [ Links ]
Mayer A. (2006). Polyphenol oxidases in plants and fungi: going places? a review. Phytochemistry 67,2318-2331. [ Links ]
Min, S., Min, S.K. y Zhang, Q.H. (2003). Inactivation kinetics of tomato juice lipoxygenase by pulsed electric fields. Journal of Food Science 68, 1995-2001. [ Links ]
Peng, Z.Y., Wu, L.C. y Kim, P.S. (1995). Local structural preferences in the α-lactalbumin molten globule. Biochemistry 34, 3248-3252. [ Links ]
Pérez, E.O. y Pilosof, A.M.R. (2004). Pulsed electric fields effects on the molecular structure and gelation of β-lactoglobulin concentrate and egg white. Food Research International 37, 102-110. [ Links ]
Pérez-Iratxetal, C. y Andrade-Navarro, M.A. (2008). K2D2: estimation of protein secondary structure from circular dichroism spectra. BMC Structural Biology 8, 25. [ Links ]
Permyakov, E.A., Morozova, L.A. y Burstein, E.A. (1985). Cation binding effects on the pH, thermal and urea denaturation transitions in α-lactalbumin. Biophysical Chemistry 21, 21-31. [ Links ]
Piña-Soberanis, M., Martín-Domínguez, A., González-Ramírez, C.A., Prieto-García, F., Guevara-lara, A. y García-Espinoza, J.E. (2011). Revisión de variables de diseño y condiciones de operation en la electrocoagulación. Revista Mexicana de Ingeniería Química 10, 257-271. [ Links ]
Qin, B., Chang, F., Barbosa, C. y Swanson, B. (1995). Nonthermal inactivation of Saccharomyces cerevisiae in apple juice using pulsed electric fields. LebensmittelWissenschaft und-Technologie 28, 564-568. [ Links ]
Robbins, F.M. y Holmes, L.G. (1970). Circular dichroism spectra of alpha lactoalbumin. Biochimica et Biophysica Acta 221, 234-240. [ Links ]
Rodiles-López, J.O., Jaramillo-Flores, M.E., Gutieírrez-Loípez, G.F., Hernaíndez-Arana, A. Fosado-Quiroz, R.E., Barbosa-Cánovas, G.V. y Hernandez-Sanchez, H. (2008). Effect of high hydrostatic pressure on bovine α-lactalbumin functional properties. Journal of Food Engineering 87, 363-370. [ Links ]
Rodiles-López, J.O., Arroyo-Maya, I.J., Jaramillo-Flores, M.E., Gutierrez-López, G.F., Hernandez-Arana, A., Barbosa-Cánovas, G.V., Niranjan, K. y Hernandez-Sanchez, H. (2010). Effect of high hydrostatic pressure on the structure of bovine α-lactalbumin. Journal of Dairy Science 93, 1420-1428. [ Links ]
Rogers, N.K. y Sternberg, M.J. (1984). Electrostatic interactions in globular proteins. Different dielectric models applied to the packing of alpha-helices. Journal of Molecular Biology 174, 527-542. [ Links ]
Sale, A.J.H. y Hamilton, W.A. (1968). Effects of high electric fields on microorganisms. III Lysis of erithrocytes and protoplasts. Biochimica et Biophysica Acta 163, 34-43. [ Links ]
Solís-Oba, M., Eloy-Juarez, M., Teutli, M., Nava, J.L. y González, I. (2009). Comparison of advanced techniques for the treatment of an indigo model solution: electroincineration, chemical coagulation and enzymatic. Revista Mexicana de Ingeniería Química 8, 275-282. [ Links ]
Vivian, J.T. y Callis, P.R. (2001). Mechanisms of tryptophan fluorescente shifts in proteins. Biophysical Journal 80, 2093-2109. [ Links ]
Yeom, H.W., Zhang, Q.H. y Dunne, C.P. (1999). Inactivation of papain by pulsed electric fields in a continuous system. Food Chemistry 67, 5359. [ Links ]
Yeom, H.W., Zhang, Q. H. y Chism, G. W. (2002). Inactivation of pectin methylesterase in orange juice by pulsed electric fields. Journal of Food Science 67, 2154-2159. [ Links ]
Zhang, Q.H., Barbosa-Cánovas, G.V. y Swanson, B.G. (1995). Engineering aspects of pulsed electric field pasteurization. Journal of Food Engineering 25, 261-281. [ Links ]
Zhang, Q.H, Monsalve-González, A., Qin, B., Barbosa-Cánovas, G.V. y Swanson, B.G. (1994). Inactivation of Saccharomyces cerevisiae in apple juice by square-wave and exponential-decay pulsed electric fields. Journal of Food Process Engineering 17, 469478. [ Links ]
Zhong, K., Hu, X., Guanghua, Z., Chen, F. y Liao, X. (2005). Inactivation and conformational change of horseradish peroxidase induced by pulsed electric field. Food Chemistry 92, 473-479. [ Links ]
]]>