Diseño de aleaciones para ánodos de sacrificio sustentables
Designing alloys for sustainable sacrificial anodes
Guillermo Salas-Banuet* y Laura Verduzco-Flores
Facultad de Química, Universidad Nacional Autónoma de México. Av. Universidad 3000, Ciudad Universitaria, C.P. 05410, Deleg. Coyoacán, México, D.F. Correo: *salasb@unam.mx
]]>Artículo recibido el 12 de marzo de 2012.
Aceptado el 13 de febrero de 2013.
Resumen
Se presenta: un proceso de diseño de aleaciones para fabricar ánodos de sacrificio, usados en ambientes marinos; la propuesta de sustituir al In con Ag, en aleaciones Al-Zn-In, buscando sustentar el medio ambiente; y la proposición de incluir los parámetros de los procesos de fabricación de ánodos y los estructurales en la normatividad sobre ánodos de sacrificio.
Se manufacturaron en el laboratorio, se ensayaron y compararon ocho aleaciones Al-Zn 2% (contenido menor al que señala la norma para aleaciones con In (de 3.5 a 5%) y con Sn (de 4 a 5%), buscando mayor sustentabilidad); cuatro se alearon con In (de 0.59 a 0.766%) y cuatro con Ag (de 0.23 a 0.428%). Se usaron dos rapideces de enfriamiento durante la solidificación, buscando modificar la estructura y cambiar propiedades y comportamientos ante la corrosión -el potencial de corrosión, la rapidez de corrosión, la activación del ánodo, el tipo de corrosión y la eficiencia de corriente-. se evaluaron las estructuras y se midieron sus potenciales; se encontró que la variación de la rapidez de enfriamiento modificó la estructura de las aleaciones, sus propiedades y comportamientos ante la corrosión y que el comportamiento general de algunas de las aleaciones con Ag es superior a las que contienen in. Las mayores eficiencias se dieron en las aleaciones con menor contenido de In (69%) y de Ag (71%).
Palabras Clave: Ánodos de sacrificio, diseño, estructura, protección catódica, sustentabilidad.
Abstract
]]> In this paper we present: a) a design process for manufacturing alloys to be used as sacrificial anodes in marine environments; b) the proposal to replace in with Ag, in search of alloys that could contribute to environmental sustain; and c) the proposal to include the parameters related to anode structure and their manufacturing process in the regulation of sacrificial anodes.Eight Al-Zn 2% alloys were manufactured, tested, and compared in our laboratory. These had a lower content than the one indicated by the alloy standards - 3.5-5% and 4-5% content for in and Sn respectively- looking for a more sustainable environment. Four of them were alloyed with In (from 0.59 to 0.766%), and four with Ag (from 0.23 to 0.428%). in order to modify the structure, two cooling rates were used during solidification, seeking to modify their properties, and hence their behavior against corrosion, i.e. corrosion potential, corrosion rate, anode activation, type of corrosion and current efficiency. It was found that the variation of the cooling rate changes the structure of the alloys, their properties and corrosion behaviors. The overall behavior of some of the Ag alloys is superior to those containing In. The higher efficiencies were obtained for alloys with the lower amount of In (69%) and Ag (71%).
Key Words: Sacrificial anodes, design, structure, cathodic protection, sustainability.
Introducción
Alrededor del 90% de la producción metálica mundial es de Fe, en múltiples aleaciones de hierro y acero. Esto se explica por sus características especiales; en general, los aceros presentan un alto valor en sus distintas resistencias mecánicas, además de gran ductilidad y maleabilidad y el menor costo entre los metales; así, sus aleaciones se utilizan para fabricar enormes estructuras marinas y terrestres, como trasatlánticos, rascacielos, largos puentes, plataformas extractivas, redes de ductos, tanques de almacenamiento, ferrocarriles, etc. Sin embargo, el Fe tiene una gran desventaja: es muy reactivo químicamente y por ello forma bastantes sustancias o compuestos con otros elementos; existen reportados treinta y seis: veintiún óxidos e hidróxidos; siete cloruros; cinco sulfuros y sulfatos; y tres carbonatos[1]; esta reactividad hace que el Fe (en aceros y hierros) tienda a su estado energético más estable, formando los compuestos minerales de donde se extrajo, deteriorándose rápidamente en un proceso conocido como corrosión, sobre todo cuando está en contacto con aire húmedo y a altas temperaturas.
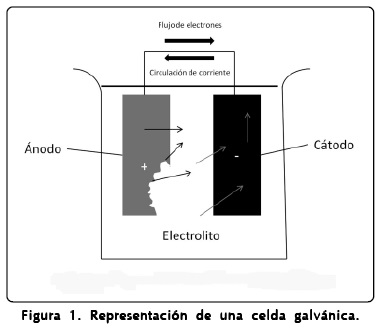
La corrosión se inicia cuando un metal se encuentra en un electrolito (sustancia que se comporta como un medio conductor de electricidad, por contener iones libres); si es acuoso, se dice que el proceso es de naturaleza electroquímica. Por otro lado, y en el mismo sentido, cada metal tiene un diferente valor de potencial electroquímico, por lo que si dos metales están en contacto eléctrico -formando un par galvánico- existirá un gradiente de potencial; si esto se da en el interior de un electrolito formarán una celda galvánica; con la diferencia entre los potenciales se obtiene un flujo de electrones y una corriente eléctrica, cuya circulación es contraria, lo que acelerará la corrosión del metal más activo y disminuirá la del más noble (Fig. 1). El metal de mayor potencial emite los electrones -el ánodo, donde sucede la oxidación- y el que los recibe es el cátodo, donde acontece la reducción. Al oxidarse, el ánodo se corroerá, se sacrificará (de aquí el concepto de ánodo de sacrificio), mientras que el cátodo permanecerá estable, protegido; el comportamiento de cada par galvánico será distinto, dependiendo del electrolito en que se encuentre.

El entendimiento de la celda galvánica fue la base para desarrollar los procesos de protección catódica. En uno de ellos, la estructura metálica que se desea proteger funcionará como cátodo, si se conecta eléctricamente a un metal o aleación que funcione como ánodo, el cual se sacrificará al corroerse.
]]> Aunque existen varios procesos para evitar o retardar la corrosión, el descrito anteriormente es el más adecuado para proteger a las grandes estructuras enterradas o inmersas en un líquido.
Motivación
La disolución de los ánodos de sacrificio usados para proteger a las estructuras de acero sumergidas en el mar, deposita en él los elementos metálicos de la aleación, contaminándolo. La contaminación marina en la sonda de Campeche -la prolongación submarina de la península de Yucatán, en el golfo de México, lugar donde se ubican los principales yacimientos petroleros mexicanos explotables de hoy- es muy grande y diversa, pues a la costa llegan todo tipo de materiales, tales como partículas sólidas, aguas residuales, petróleo, agroquímicos, fertilizantes y elementos tóxicos; muchos de éstos son desechos industriales. El origen de los elementos tóxicos es variado, pero no escapa al entendimiento la afectación que pueden ejercer en la salud de personas, animales y plantas y el mantenimiento del medio ambiente. La cadena trófica y los diversos mecanismos de alimentación de presas y depredadores de un ecosistema, incluido el humano, concentran en ellos una cantidad atípicamente alta de elementos tóxicos, haciéndolos muy peligrosos para la salud. El In es uno de los más tóxicos y actualmente sirve como elemento aleante en ánodos de sacrificio. La experimentación en animales de laboratorio indica que su consumo provoca síntomas de envenenamiento, como pérdida de peso, edema pulmonar, neumonía necrótica, daño en la sangre y cambio degenerativo en el hígado y los riñones; en cambio, se ha demostrado que el envenenamiento con Ag es raro, por lo que el metal no es, en general, considerado tóxico[2].
Los problemas de este tipo son multidisciplinarios, por lo que no existe remedio único, total, ni inmediato; la solución al problema de contaminación existente en la sonda de Campeche, requiere de una actitud constante de enfoque desde cada una de las múltiples áreas del conocimiento involucradas. Desde la trinchera de la ciencia e ingeniería de los materiales, una propuesta es diseñar aleaciones que contengan una cantidad menor de elementos aleantes, que éstos sean menos dañinos que los que actualmente se utilizan y que se usen para fabricar ánodos de sacrificio, manufacturados de tal manera que sus estructuras presenten un buen comportamiento general ante la corrosión.
Antecedentes
Despic et al.[3], investigaron el comportamiento electroquímico de aleaciones binarias de Al con pequeñas cantidades (arriba del 0.2%) de In, Ga y Th y una ternaria con 0.01% In y 0.01% de Ga, buscando reemplazar al Zn. Concluyeron que las aleaciones propuestas son económica y electroquímicamente adecuadas para sustituir a las que contienen Zn.
Salinas y Bessone[4], estudiaron el efecto del Sn y del Zn en el proceso de activación del Al en la aleación Al-Zn 5%-Sn 0.1%, modificando las condiciones de colada y de tratamiento térmico realizadas a la aleación. Encontraron que las zonas enriquecidas con Zn y Sn controlan el proceso de activación del Al y que son las responsables del inicio y propagación del ataque. Esas zonas ricas en Zn y Sn se ubican en los espacios entre los brazos secundarios de las dendritas (EDS), por lo que al incrementar la rapidez de enfriamiento se disminuye el EDS y esas zonas se segregan a los límites del grano, concentrándolas, lo que baja la eficiencia de corriente del ánodo de 58.9 a 39.8%. Señalan que el tratamiento térmico de solubilización y posterior temple, parece facilitar una mejor distribución de las zonas ricas en Zn y Sn, incrementando la eficiencia de corriente del ánodo a 74.5%.
En otro trabajo[5], se fundieron en el laboratorio muestras de siete ánodos comerciales de Mg, con diferencias grandes en la cantidad de sus elementos contaminantes, los cuales se solidificaron bajo diferente rapidez de enfriamiento: 0.24, 1.24 y 15.3°C/s, evaluando su rapidez de corrosión. Los especímenes se analizaron con microscopía óptica, encontrando que todos habían modificado la forma, el tamaño y la cantidad relativa de los componentes de la estructura; éstos fueron medidos y comparados, buscando una posible relación con el comportamiento encontrado ante la corrosión.
]]> Los resultados de rapidez de corrosión mostraron que la diferencia en composición química de las aleaciones y su rapidez de enfriamiento, que representan los cambios estructurales, afectan el comportamiento ante la corrosión; la pérdida de peso se vio modificada hasta en nueve veces por la composición química y hasta en 4.6 por la rapidez de enfriamiento.No hubo manera de relacionar la diferencia microestructural a la rapidez de corrosión; sin embargo, se encontró una tendencia clara en las diferencias macroestructurales: a mayor cantidad relativa de granos equiaxiales, mayor rapidez de corrosión y a mayor cantidad relativa de granos columnares, menor rapidez de corrosión. Como existen fases formadas por el exceso de los elementos químicos contenidos en el Mg (sitios de actividad catódica) y éstos se ubican en los límites de los granos, se llegó a la conclusión de que a mayor número de límites de grano en el espécimen, valores más altos de rapidez de corrosión y pérdida de peso. Esto haría deseable obtener ánodos de magnesio con la mayor cantidad posible de granos columnares grandes -que representan menor cantidad de límites de grano- los cuales pueden obtenerse controlando la dirección y la velocidad del enfriamiento durante su solidificación.
Juárez et al.[6] solidificaron y aplicaron un tratamiento térmico a muestras de ánodos de Mg, para compararlas en ambos estados. Reportan una eficiencia de 53.2%, con una mayor pérdida de peso para la muestra de colada; y una eficiencia de 68.6%, con una corrosión más uniforme para la muestra tratada térmicamente. Observan que, en la muestra de colada la corrosión es por picado y ocurre preferentemente en los límites de grano, donde abundan precipitados de segundas fases, ricos en Fe; en comparación, en la muestra con tratamiento térmico, la corrosión está más uniformemente distribuida y las picaduras se dan preferencialmente en los límites de las subceldas, donde se ubican las partículas de segunda fase, ricas en Fe. Afirman que estos valores de eficiencia están directamente relacionados a la microestructura.
Partiendo de la premisa de que la baja eficiencia de un ánodo de Mg está relacionada a la heterogeneidad de su composición química, Campillo et al.[7] trataron térmicamente muestras de un ánodo de Mg comercial, con estructura de granos columnares, con tres rapideces de enfriamiento. Además, aplicaron tratamientos de envejecimiento, usando dos temperaturas de solución a diferentes tiempos, seguidos de un temple en agua. Calcularon la eficiencia de las muestras, que presentó un rango desde 22.98 a63.85%. Encontraron granos columnares y partículas insolubles de Fe-Mn, ricas en Fe, y Mn segregado; midieron los granos y las partículas, analizaron los elementos que las componen, definieron la morfología de éstas y notaron su distribución. Observaron que la corrosión del Mg sucede preferentemente en las regiones ricas en segunda fase, heterogéneamente distribuidas, y que la eficiencia de la muestra se incrementaba conforme disminuía el tamaño de las partículas, sobre todo para un tratamiento térmico específico.
Valdés et al.[8] prepararon tres aleaciones base Al, con Zn (4.17.77% at.), Mg (5.84-10.67% at.) y Li (0.12-0.15% at.) y analizaron las fases presentes. Definieron una matriz de dendritas de una solución sólida de Al α, con precipitados, dentro de ella, de τ Al2Mg3Zn3, Mg7Zn3, y δ AlLi, así como un eutéctico formado por la solución sólida de Al α y τ Al2Mg3Zn3, que cuantificaron, y partículas de Mg7Zn3. El cálculo de la eficiencia de las muestras de colada les dio de 61.43% y encontraron que cumplen con el criterio de potencial e indican que la presencia de granos equiaxiales favorece la disminución de la presencia del eutéctico y, con ello, la disolución del ánodo es más uniforme y se aumenta la eficiencia; y que la precipitación de la fase intermedia τ Al2Mg3Zn3 en la matriz Al α, junto con las fases Mg7Zn3, y δ AlLi, evitan la formación de la capa protectora de óxido de Al.
En el mismo sentido, Valdés et al. [9] fabricaron muestras de una aleación de Al con 4.8% at. de Zn, 5.1% at. de Mg y 0.09% at. de Li y les aplicaron tratamientos de envejecimiento, para comparar las estructuras y el comportamiento electroquímico entre ellas y las muestras de colada. En las 7 muestras se encontraron varias fases, básicamente una solución sólida a con otras fases intermedias, principalmente binarias, algunas ternarias y dos cuaternarias. Notaron que la dispersión de la fase τ Al2Mg3Zn3 en la solución sólida de Al α, en las muestras con un tratamiento térmico específico, era buena y que esto explicaba un mayor valor relativo de eficiencias encontradas de 65 y 67%, comparado con el de las muestras de colada que tuvieron, en promedio, 62%. También apreciaron que la presencia de la fase insoluble Mg7Zn3 en la región interdendrítica, provoca el aislamiento de algunas dendritas de solución sólida, dando lugar al mecanismo de corrosión por picadura localizado. Las fases τ Al2Mg3Zn3 y del tipo δ-AlLi, juegan un papel importante en el rompimiento de la capa pasivante de óxido de Al y, por tanto, en una disolución uniforme del ánodo.
Basándose en el sistema Al-Zn-Mg, González et al.[10] prepararon por fusión y colada, ocho muestras de cuatro aleaciones base Al con 12% de Zn y con 4.4, 5.2, 5.4 y 6.3% de Mg, cada una; después, a cuatro de las muestras se les practicó un tratamiento térmico y se compararon, entre ellas, los microconstituyentes y la eficiencia que presentaron. En todas se encontró una solución sólida de Al a, la fase τ y dos eutécticos, uno formado por (α + τ) -cuya cantidad depende de la composición de la aleación- y otro por (α + Si), cuya cuantía depende del total de Si presente, el cual está como impureza, entre 0.155 y 0.204%. En las muestras de colada, conforme contenían mayor cantidad de Mg, la presencia de solución sólida Al a y la del eutéctico (α + τ) disminuyó; el eutéctico (α + Si) se encontró en la proporción de la cantidad de Si en la muestra. Las eficiencias que reportan muestran que aumentan en el sentido del aumento del Mg y del eutéctico (α + Ï), de 68 a 78%, así como también existe un aumento para cada muestra después del tratamiento térmico, la menor de 68 a 69% y las mayores desde 73 a 87%.
Orozco et al.realizaron un trabajo enfocado en la influencia del contenido de Mg en el comportamiento electroquímico y la eficiencia de aleaciones Al-Zn 5.3% at.-Mg (5.3, 6.6, 7.2 y 11.3 % at.), para ser usadas como ánodos de sacrificio. Reportan que la microestructura de colada está compuesta de dendritas de Al a, eutéctico (α + τ) y la fase τ, ambos interdendríticos; esta fase se observó principalmente en las tres muestras con mayor cantidad de Mg. La eficiencia electroquímica calculada para la muestra con 5.3% Mg es de 68% y para la que contiene 11.3% Mg es de 75%, con lo que concluyen que el incremento en la cantidad de Mg es el responsable del aumento en eficiencia.
En otro trabajo[12], Medrano fabricó a nivel laboratorio la aleación Al-Zn 4.2% -In 0.04%, de acuerdo a Morgan[13] (basada en la recomendación NACE TMO190-98, DNV-RP-B-401 del 2010), utilizada comercialmente como ánodo de sacrificio; se solidificaron 5 muestras con diferente rapidez de enfriamiento: 0. 04, 0.116, 0.124, 0.143 y 7.23°C/s. A cada muestra se le midió la rapidez de corrosión, el tamaño de grano (TG), el espaciamiento dendrítico secundario (EDS) y los grosores de las láminas de los microconstituyentes secundarios presentes entre los EDS.
El objetivo estaba en entender las relaciones entre la rapidez de enfriamiento durante la solidificación, la modificación estructural y la rapidez de corrosión.
]]> Se encontró: 1) que ninguna de las muestras se pasivó, 2) una tendencia clara de que a mayor rapidez de enfriamiento durante la solidificación se tiene una menor rapidez de corrosión, 3) una tendencia evidente de que a mayor rapidez de enfriamiento se obtiene un tamaño menor de EDS (el espacio entre los brazos dendríticos secundarios), por lo que a menor tamaño de éste, habrá una menor rapidez de corrosión; como los microconstituyentes secundarios se encuentran en los espacios interdendríticos, la modificación de éstos afecta a los primeros, influyendo en la rapidez de corrosión.Los trabajos anteriores evidenciaron tres ideas: 1) La modificación de los parámetros de los procesos aplicados a las aleaciones durante la solidificación o usando un tratamiento térmico, que transforma la estructura de la aleación usada como ánodo de sacrificio. 2) La modificación de los factores estructurales afecta el comportamiento de la aleación ante la corrosión, entre ellos la eficiencia. 3) La necesidad de que cada material debe ser estudiado por separado, ya que sus estructuras y, por ende, sus distintas propiedades y comportamientos ante la corrosión, se ven afectados de manera diferente.
Fundamentos del diseño
Casi no existen reportes sobre el diseño de ánodos de sacrificio; esta situación es entendible, pero limita la bibliografía disponible. Se presentan los fundamentos encontrados en la literatura y los establecidos con la experiencia.
1. Fundamentos electroquímicos
Los metales que pueden servir como base para fabricar ánodos de sacrificio para proteger estructuras de hierro y acero en agua de mar, deben de ser más reactivos que el Fe; así, se tienen los siguientes: Cr, Zn, Al, Mn, V, Mg, Na, Ca, Sr, Be, Cs, K y Li, porque son los que poseen valores más negativos que el del Fe, en la serie electromotriz para metales de potenciales estándar de electrodo[14]. Sin embargo, la mayoría de ellos son muy reactivos -como los ocho últimos- por lo que pueden corroerse rápidamente y durar poco; pueden pasivarse -como el primero- y dejar de corroerse, con lo que se dañaría la estructura a proteger; y la mayoría son caros. Las alternativas más viables son el Mg, el Zn y el Al; como el Mg y el Zn son muy activos y se disuelven rápidamente cuando son sumergidos en agua marina, se recurre a las aleaciones de Al para proteger las estructuras petroleras de acero, como los barcos, las plataformas extractivas y los ductos transportadores de petróleo, hecho que se explica con la posición que exhiben en la serie galvánica para metales sumergidos en un flujo de agua de mar[15].
Los comportamientos solicitados para los ánodos de sacrificio son: poca reactividad, para que duren; no pasividad, para que sigan funcionando; dilución homogénea, para aumentar su eficiencia; buena colabilidad, para que adquieran las formas y texturas superficiales requeridas; bajo costo y accesibilidad.
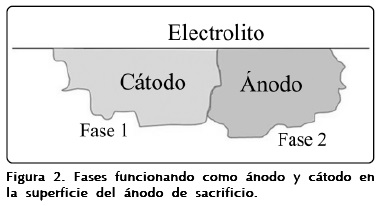
A lo largo del tiempo, se han usado diferentes aleaciones base aluminio para los ánodos de sacrificio: Al-Sn-Hg, Al-Bi-Hg, Al-Zn-Hg, Al-Zn-Sn y Al-Zn-In; actualmente, la última es la más popular. Es importante notar que los valores de potencial de los distintos elementos aleantes del Al son más positivos que el suyo; los elementos aleantes forman diferentes macro y microconstituyentes en la aleación, los cuales están determinados por los diagramas de fase y pueden ser modificados por diversos medios. De esta forma, funcionarán como pequeñas celdas galvánicas en la superficie del ánodo de sacrificio (Fig. 2), evitando la pasivación del Al, que se da al formarse una delgada capa de óxido, muy estable e impermeable al oxígeno.
]]>
2. Fundamentos metalúrgicos.
La problemática planteada para los ánodos de sacrificio, desde la ciencia e ingeniería de los materiales, requiere saber que las micro y macro estructuras de una aleación: a) son las formas físicas en que se conforman las fases presentes; b) juegan un papel importante en todas las propiedades de la aleación y c) pueden modificarse en tamaño, forma, distribución, ubicación y cantidad relativa, al incidir en los parámetros de los procesos de fusión y solidificación. Las modificaciones estructurales también pueden lograrse a través de otros procesos, como los mecánicos y térmicos, y aunque se reportan aumentos en la eficiencia, encarecen la fabricación del ánodo por ser necesariamente posteriores al de fundición; así, se hace necesario calcular si el aumento de eficiencia compensa el gasto del tratamiento térmico o mecánico.
Las normas relativas a las especificaciones de los ánodos de sacrificio se refieren, principalmente, a los rangos necesarios de los elementos aleantes; en ninguna de ellas y casi en ningún otro tipo de literatura, se especifica el papel que juegan la micro y macroestructura, aún cuando resulta obvio que influyen en sus distintos comportamientos.
La aleación de un ánodo de sacrificio puede tener diferente rapidez de enfriamiento si se modifica el volumen y/o el espesor del ánodo y, con ello, obtener diferentes estructuras.
Hipótesis
Cualquier cambio químico o estructural en una aleación usada como ánodo de sacrificio, modificará el tamaño, forma, distribución, ubicación y cantidad relativa de los pequeños ánodos y cátodos que lo conforman, modificando sus distintas propiedades y comportamientos ante la corrosión. Así, se tienen dos ideas fundamentales: 1) el que un ánodo de sacrificio tenga un comportamiento general adecuado (que no se pasive, se corroa poco, lo haga homogéneamente y presente alta eficiencia) requerirá del control de los elementos químicos y de los estructurales; y 2) es posible diseñar aleaciones más sustentables que las actualmente usadas en los ánodos de sacrificio.
Propuesta
]]> Para formular la propuesta, se analizaron los diagramas de fase relativos a las aleaciones comerciales, las tradicionalmente usadas para fabricar los ánodos de sacrificio. Se encontró que en todas ellas se forman microconstituyentes estructurados por dos fases -como los eutécticos- que coexisten con soluciones sólidas y/o con alguna otra fase intermedia. Entonces, se buscaron las posibles nuevas aleaciones (Al-Zn-X) que pudieran cumplir con estas características estructurales, encontrándose más de veinte.Considerando los fundamentos y sus antecedentes, de entre las más de veinte posibilidades de elementos de aleación, se escogió a la Ag para sustituir al In, en las aleaciones Al-Zn, porque: 1) su toxicidad es mucho más baja; 2) tiene el valor de potencial más positivo respecto al Al, que cualquiera de los elementos aleantes tradicionales; 3) México es el segundo productor de Ag a nivel mundial, después de Perú y se buscan aplicaciones para ella y; 4) es diez veces más barata que el In.
Materiales y métodos
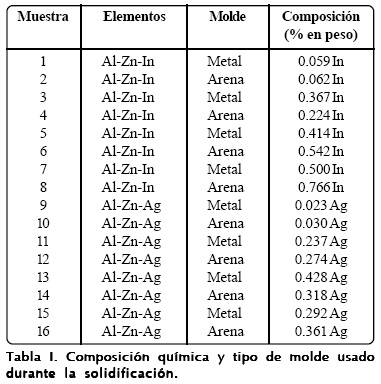
En el laboratorio se fabricaron cuatro aleaciones Al-Zn-In (de 0.59 a 0.766%) y cuatro aleaciones Al-Zn-Ag (de 0.23 a 0.428%) (Tabla I), propuestas en base a los correspondientes diagramas de fase; se amplió el rango del porcentaje presente del In para ampliar la posibilidad de encontrar nuevos comportamientos. Se solidificaron empleando dos rapideces de enfriamiento -para modificar las estructuras y evaluar sus particulares propiedades y comportamientos ante la corrosión-colando en dos tipos de molde: uno metálico (rapidez de enfriamiento mayor) y otro refractario (de arena). Las diferencias en composición química, para cada par de aleaciones, se debieron a las pérdidas normales, debidas a la oxidación de los elementos aleantes durante su fusión y al tiempo en que permanecieron líquidas. La cantidad de Zn agregada fue de 2%, en vez del porcentaje señalado por la norma para aleaciones de In (de 3.5 a 5%) y de Sn (de 4 a 5%).
Se armó una celda electroquímica para medir los potenciales de las muestras, las cuales constituyeron el electrodo de trabajo; como electrodo de referencia se empleó uno de calomel -saturado con KCl- y como electrodo auxiliar, uno de grafito. El electrolito fue agua de mar sintética, de acuerdo a la norma ASTM D 1141-75.
Con un equipo Auto-Tafel, para cada muestra se obtuvo una curva de polarización (con potenciales de -300 a 1000 mV y una rapidez de barrido de 86 mV/min) y 6 curvas de Tafel (con un intervalo de sobrepotencial entre -300 a 300 mV y una rapidez de barrido de 60 mV/min).
Con ellas se calculó el potencial de corrosión (mV), la corriente de corrosión (A) y la rapidez de corrosión, en milipulgadas por año (mpy).
]]>Resultados y discusión
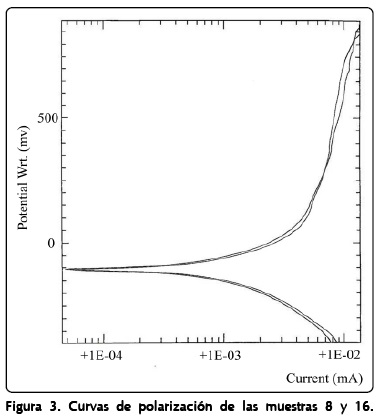
Las pendientes anódicas de todas las curvas de polarización fueron muy similares e indican que ninguna se pasivará, a pesar de que el rango de potencial aplicado fue alto; las más reactivas fueron las número 8 (0.766% In) y 16 (0.361% Ag), que son las de mayor contenido de elemento aleante; la Figura 3 presenta sus curvas de polarización, que son prácticamente iguales.
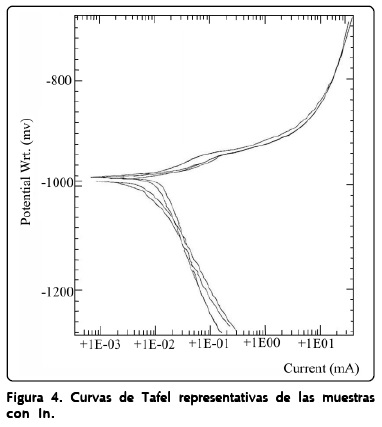
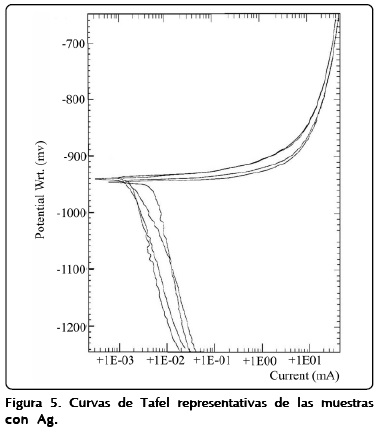
Las curvas de Tafel para cada muestra son muy parecidas; las Figuras 4 y 5 presentan cuatro curvas representativas de las aleaciones de Ag e In, respectivamente. La comparación de las curvas indica que -en general- ninguna de las aleaciones se pasivará.
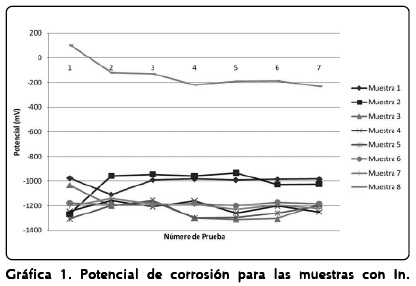
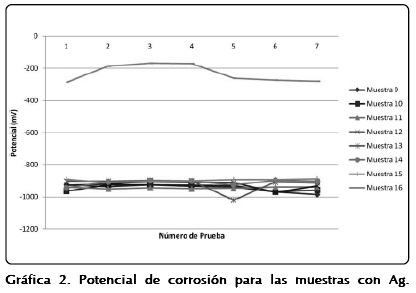
La Gráfica 3 permite visualizar el efecto de la composición química y la rapidez de enfriamiento, en la rapidez de corrosión; en general, a mayor cantidad de In en la muestra, menor rapidez de corrosión, para ambas rapideces de enfriamiento; esta tendencia no se observa en las muestras con Ag. Los valores más bajos de rapidez de corrosión fueron presentados por las muestras 8 (0.766% In) y 16 (0.361% Ag), las de más alto contenido de elementos aleantes que, a su vez, presentaron los valores de potencial más cercanos a los del Fe. También es posible apreciar que, para la mayoría de los pares de muestras, las nones -aquellas solidificadas con una mayor rapidez de enfriamiento- son las que tienen una mayor rapidez de corrosión; la que reportó la mayor rapidez de corrosión fue la 9 (0.023% de Ag), con un valor de casi 7 mpy; no tan alta si se compara con valores de rapidez de corrosión de alrededor de 200 mpy, reportados para otros ánodos.
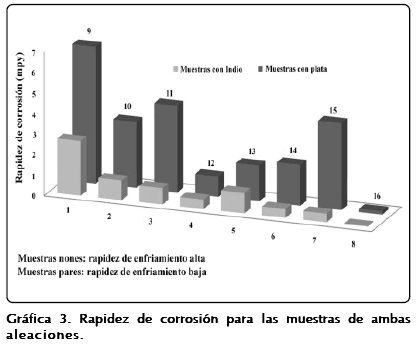
La fotomicrografía 1 es la representativa de todas las aleaciones; en ella se aprecian los granos equiaxiales de la solución sólida de Al (el microconstituyente primario o matriz) y, en sus límites, los microconstituyentes secundarios. Se cuantificó la cantidad relativa de estos últimos, así como su número por área; juntos, representan su tamaño. La Tabla II muestra estos datos y la rapidez de corrosión promedio para cada una de las muestras solidificadas en el molde metálico y la Tabla III lo hace para las solidificadas en el refractario.
El resultado de la comparación de las Tablas II y III, respecto a la rapidez de corrosión y la cuantificación de los segundos microconstituyentes, indica que los de las muestras solidificadas en el molde refractario -con una relativa rapidez de enfriamiento menor- ocupan un porcentaje mayor de área, se encuentran en menor cantidad -lo que concuerda con su mayor tamaño- y, en general, tienen una rapidez de corrosión menor. Con estas tablas y la Gráfica 3, es posible apreciar que el valor de la rapidez de corrosión de las muestras con la misma composición química, es dos y tres veces mayor en las solidificadas en el molde refractario, encontrando el extremo en la muestra 15, que tiene un valor de rapidez de corrosión 10 veces mayor que la 16. Así, desde el punto de vista estructural, si se desea una aleación con menor rapidez de corrosión para estas aleaciones, se deberá disminuir la rapidez de enfriamiento durante su solidificación, lo cual favorecerá un tamaño mayor, un número menor y una cantidad relativa mayor de segundas fases (sitios anódicos/ catódicos), aunque no exista una correlación directa entre la rapidez y estos parámetros estructurales.
]]> Una inspección visual de las muestras puso de manifiesto que, sin importar la rapidez de enfriamiento a la que fueron obtenidas, todas aquéllas con In se corroen de manera agresiva y localizada, mientras que las de Ag lo hacen de manera uniforme, lo que incidirá en una vida efectiva mayor del ánodo. Las mayores eficiencias se encontraron en las aleaciones con menor contenido de In (una eficiencia del 69%) y de Ag (71%), solidificadas con mayor rapidez de enfriamiento, lo que significa que los segundos microconstituyentes ocupan un porcentaje de área menor, que se encuentran en mayor cantidad y que la velocidad de corrosión es mayor.La mayoría de las aleaciones de In exhiben menor rapidez de corrosión que las de Ag, aunque se encontró que las de mayor contenido de Ag (las número 12, 13, 14 y 16), tienen una equivalente a las de In.
Por otro lado, las aleaciones de Ag muestran adecuados y más homogéneos potenciales de corrosión que las de In, ninguna posibilidad de pasivación y un tipo de corrosión más homogéneo, lo que las catalogaría como muy adecuadas para fabricar ánodos de sacrificio.
Conclusiones
1. El comportamiento general ante la corrosión de una aleación del tipo estudiado estará definido por la cantidad del elemento aleante, pero también por su microestructura -específicamente por el tamaño y la cantidad relativa de los segundos microconstituyentes- modificada por la rapidez de solidificación de la aleación.
2. El elemento aleante influye en el tipo de corrosión y, por tanto, en una vida efectiva mayor del ánodo.
3. Ánodos fabricados con las aleaciones propuestas, que tengan mayor volumen, tendrán menor rapidez de enfriamiento y, con ello, menor rapidez de corrosión, aunque una relativa menor eficiencia.
4. El comportamiento general de varias de las aleaciones de Al propuestas, con menor cantidad de Zn y aleadas con Ag, las hace susceptibles de ser usadas como ánodos de sacrificio, con la ventaja extra de ser mucho menos tóxicas.
5. Es necesario incluir los aspectos microestructurales y de control del proceso de solidificación en las normas relativas a los ánodos de sacrificio.
]]> 6. Es posible validar el proceso presentado para diseñar aleaciones que puedan ser usadas como ánodos de sacrificio en agua de mar; su divulgación ayudará a caminar en el sentido sustentable.
Agradecimientos
Los autores deseamos reconocer el apoyo decidido del Ing. José Ramírez Vieyra para la culminación del trabajo.
Referencias
1. Barin, I. Termochemical Data of Pure Substances (VCH, Weinheim, 1993). [ Links ]
2. Patty, A. Patty's Industrial Hygiene and Toxicology (Wiley-interscience, New York, 1991). [ Links ]
]]>3. Despic, A. et al. Electrochemical properties of aluminium alloys containing indium, gallium and thalium. Journal of Applied Electrochemistry 6, 527-542 (1976). [ Links ]
4. Salinas, D. & Bessone, J. Electrochemical behavior of Al-5%Zn-0.1%Sn sacrificial anode in aggressive media. Corrosion 47(9), 665-674 (1991). [ Links ]
5. Salas, G. et al. Cooling Rate effect in the as cast magnesium sacrificial anodes structure and its corrosion evaluation. Memorias del Primer Congreso de Corrosión NACE Región Latinoamericana y Primer Congreso Venezolano de Corrosión, Maracaibo, Venezuela, 2, 1-12/94064 (1994). [ Links ]
6. Juárez, J. et al. Improving the efficiency of magnesium sacrificial anodes. JOM 45(9), 42-44 (1993). [ Links ]
7. Campillo, B. et al. Effect of heat treatment on efficiency of Mg anodes. Journal of Materials Engineering and Performance 6(4), 449-453 (1997). [ Links ]
]]>8. Valdés, S. et al. Activation of an Al-Zn-Mg-Li alloy by the presence of precipitates to be used as sacrificial anode. Mat. Res. Soc. Symp. Proc. 654, AA3.5.1-AA3.5.6 (2001). [ Links ]
9. Valdés, S. et al. Evaluation of an Al-Zn-Mg-Li alloy/potencial candidate as Al-sacrificial anode. Journal of Materials Engineering and Performance 10(5), 596-601 (2001). [ Links ]
10. González, C. et al. Solidification of chill-cast Al-Zn-Mg alloys to be used as sacrificial anodes. Metallurgical and Meterials Transactions A. 34A, 2991-2997 (2003). [ Links ]
11. Orozco, R. et al. Effect of Mg content on the performance of Al-Zn-Mg sacrificial anodes. Journal of Materials Engineeringand Performance 16(2), 229-235 (2007). [ Links ]
12. Medrano, W. Caracterización microestructural de ánodos de sacrificio de Al-Zn-In. Tesis. Facultad de Química, Universidad Nacional Autónoma de México (2007). [ Links ]
]]>13. Morgan, J. Cathodic Protection (NACE, USA, 1993). [ Links ]
14. Metals Handbook, Corrosion. Vol. 13 (ASM International, EUA, 1987). [ Links ]
15. ASTM G 82-83 (Reapproved 1989). Standard Guide for Development and Use of a Galvanic Series for Predicting Galvanic Corrosion Performance (ASTM International, USA). Pp. 334-340. [ Links ]
Información sobre los autores
Guillermo Salas-Banuet
Guillermo Salas-Banuet es egresado de la licenciatura y el posgrado de la Facultad de Química, UNAM. Es profesor de carrera Titular "C" de la misma institución en donde labora como académico, investigador y divulgador desde hace 38 años, tiempo completo. Su principal interés es la docencia. Su campo de trabajo principal radica en los materiales, principalmente los metálicos, específicamente en las relaciones estructura-propiedades, nuevos procesos, diseño y sustitución de aleaciones, reciclaje y desarrollo e impacto de la ciencia y la tecnología; otros campos de interés son el pensamiento, las ideas, la historia, la sociología, la arqueología, el crecimiento humano, el derecho, la economía y las funciones cerebrales, entre otros. Ha impartido cursos teórico-prácticos a nivel licenciatura y posgrado (más de 165); publicado en revistas arbitradas internacionales (más de 30) y nacionales (más de 10); publicado en memorias de congresos internacionales (más de 80) y nacionales (más de 25) e impartido conferencias por invitación (más de 25), algunas magistrales.
]]> Laura Verduzco-FloresLaura Verduzco-Flores trabaja actualmente para Chevron Corporation con el título de "Lead Planning Engineer", buscando implementar soluciones para reducir las emisiones de gases de invernadero en las operaciones de la empresa. Tiene experiencia en las áreas de desarrollo sustentable, biocombustibles, energía eólica, ciclo de vida y celdas de hidrógeno, entre otras. Durante 3 años dirigió el departamento de políticas de sustentabilidad en la empresa Catchlight Energy, la cual es una "joint venture" entre Chevron y Weyerhaeuser, para producir biocombustibles de segunda generación. Recientemente participó en el desarrollo del reporte de adaptación al cambio climático para el Congreso de Estados Unidos. Representa a su compañía en varios grupos de la industriapetrolera, incluyendo MECA y USDRTVE. Anterior a Chevron, dio apoyo técnico a la Oficina de Hidrógeno del Departamento de Energía de Estados Unidos y fue gerente de una compañía de manufactura de sacos de polipropileno en Michoacán, México.
Recibió el título de Ingeniera Química de la Universidad Nacional Autónoma de México en 1998 con una tesis de investigación de aleaciones para ánodos de sacrificio y el de Doctora en Ciencias en "Environmental and Energy Management" en 2006 de "The George Washington University" con una tesis en la que modeló diferentes avenidas para producir electricidad y vapor para uso residencial e hidrógeno para uso vehicular por medio de una celda de hidrógeno.
]]>