
Criterios termodinámicos para la selección de una membrana polimérica, empleada en el proceso de pervaporación para la separación de MMA, ISB y PRP
Arturo Sánchez y Joaquín Palacios*
Laboratorio de Fisicoquímica de Macromoléculas, Facultad de Química, Universidad Nacional Autónoma de México. México 04510, D. F.
Recibido el 28 de septiembre del 2000.
Aceptado el 3 de noviembre del 2000.
Resumen
Este trabajo se refiere a la separación de una mezcla de compuestos que son previamente obtenidos como los productos del proceso de degradación térmica de poli (metacrilato de metilo), PMMA. El compuesto que deseamos purificar es el monómero de metacrilato de metilo MMA, que se obtiene como producto de la degradación con una pureza del 95% en peso y se desea lavar hasta una concentración mayor del 99.9% en peso por medio del proceso de pervaporación. El objetivo de este trabajo es estudiar la teoría de pervaporación y aplicar los principales criterios termodinámicos para la selección de membranas poliméricas para la separación de la mezcla MMA/PRP/ISB, estos criterios termodinámicos se basan en los parámetros de interacción y las solubilidades de los monómeros en la membrana. La ventaja de esta técnica de separación es principalmente, el bajo requerimiento de energía comparado con el de otros procesos tales como: destilación, cristalización, etc.
Palabras clave: termodinámica, membrana polimérica, pervaporación, polímeros.
Abstract
This work refers a separations of the that of the mixture of the one of the compounds that son previously obtained as the products of the process of the thermal one of the degradation of the poly (methyl methacrylate), PMMA. The compound that we want to purify is the monomer of methyl methacrylate MMA that one obtains as product of the degradation with a purity of 95% in weight and it is wanted to wash until a concentration bigger than 99.9% in weight by means of the pervaporation process. The objective of this work is to study the pervaporation theory and to apply the main thermodynamic approaches for the selection of membranes polymeric for the separation of the mixture MMA/PRP/ISB, these thermodynamic approaches are based on the interaction parameters and the solubility of the monomers in the membrane. The advantage of this separation technique is mainly, the first floor energy requirement compared with that of other such processes as: distillation, crystallization, etc.
Keywords: thermodynamics, polymeric membranes, pervaporation, polymers.
Introducción
]]> La selección de una membrana polimérica que pueda emplearse en el proceso de pervaporación, para la separación de mezclas de substancias orgánicas, es un problema interesante y a la vez complejo ya que existen muchas posibilidades en cuanto a los polímeros que podrían usarse para este fin.Por lo tanto, es importante establecer criterios termodinámicos que nos auxilien de manera científica para la solución del problema, esto es en la selección preliminar de algunas membranas útiles para lograr una separación específica.
El parámetro que más se emplea como un criterio fundamental para la selección de una membrana de pervaporación, es el valor del parámetro de interacción χAB disolvente-polímero. Este valor se calcula a partir de los datos de los parámetros de solubilidad de los compuestos a separar y de los polímeros afines, de acuerdo con sus propiedades fisicoquímicas.
En este artículo se presenta y discute un conjunto de criterios termodinámicos útiles para la selección de una membrana polimérica eficaz para la separación del metacrilcato de metilo MMA, a partir de una mezcla del mismo componente con isobutirato de metilo ISB y propionato de metilo PRP.
En nuestro trabajo se emplearon modelos termodinámicos así como datos de la literatura, para calcular los parámetros que sirven como criterios básicos para la selección de la membrana útil en la separación del MMA por medio del proceso de pervaporación.
Por la importancia que reviste para el problema de la separación del monómero MMA, la adecuada selección de la membrana y considerando la complejidad del proceso de selección de la misma, pensamos que el establecer criterios generales para este propósito, es en sí una contribución significativa pues con estos antecedentes se facilita y prepara el trabajo experimental, a la vez que se permite el poner a prueba los modelos de la termodinámica de las disoluciones poliméricas así como establecer sus limitaciones y aciertos.
El presente trabajo trata también el tema de pervaporación, el proceso de separación de mezclas líquidas en el que se utiliza una membrana polimérica como medio de separación. En esta ocasión se aborda la separación de una mezcla de compuestos derivados del ácido acrílico, los cuales son: el MMA, ISB y PRP, que son los productos principales del proceso de degradación térmica del poli(metacrilato de metilo) PMMA, como señala Avilés [1].
El compuesto que deseamos purificar es el monómero MMA, el cual se obtiene como un líquido en el proceso de degradación térmica con una concentración aproximada de 95% en peso, por lo cual necesitamos purificarlo, eliminando los otros dos compuestos presentes, mediante la tecnología de pervaporación. En esta alternativa de purificación, no se requiere de una gran cantidad de energía en forma de calor, cuando se le compara con la destilación, lo que hace que la pervaporación presente una alta eficiencia energética.
En los procesos de separación donde se utilizan membranas, estas tienen la característica de seleccionar entre dos o más tipos de moléculas, debido a sus diferencias en: tamaño, forma, carga, afinidad o estructura química y así se logra alcanzar un grado de separación en la mezcla de alimentación.
La pervaporación es un proceso de separación complejo donde las características de separación pueden ser influenciadas en gran medida por la composición del líquido a separar. El proceso se usa comúnmente para remover uno de los componentes de una mezcla líquida, el contaminante. La pervaporación es por lo tanto muy atractiva cuando la mezcla líquida exhibe una composición azeotrópica.
]]> Para obtener un incremento en el flujo del compuesto que permea, es conveniente que el material polimérico de la membrana se encuentre en estado viscoelástico, porque así se obtiene una mayor solubilidad de las impurezas a separar, en contraste con el proceso de separación de gases donde la membrana usada se encuentra generalmente en estado cristalino o semicristalino [2].El mecanismo generalmente aceptado para explicar el proceso de pervaporación es el mecanismo de disolución-difusión, el cual describe de manera adecuada la separación de mezclas orgánicas, tales como: mezclas de hidrocarburos o de hidrocarburos halogenados.
La permeación de mezclas líquidas también difiere de la permeación de un sólo componente, debido a que la solubilidad y la difusividad de un componente en una mezcla líquida podrían estar influenciadas significativamente por la permeación de los otros componentes. Este hecho puede observarse en los resultados de los experimentos de permeación hechos por Huang y Lin [3], donde se presentan los resultados de mezclas que permean considerablemente más rápido que cualquiera de los componentes puros, para un sistema benceno / hexano / poli(etileno). Estos resultados inesperados de permeación pueden ser atribuidos al incremento en la velocidad de difusión de las especies lentas retenidas debido a la presencia de las otras especies coexistentes. Conclusiones similares sobre el acoplamiento en los flujos de permeación fueron encontradas y se reportan en la literatura reciente [4-10].
En el modelo del fenómeno de difusión de una mezcla líquida a través de una membrana polimérica, se han usado relaciones lineales o exponenciales, en donde la difusividad de algún componente se relaciona con las concentraciones de los componentes en el sistema penetrante/polímero. Estas relaciones son empíricas, sin embargo, Fiels y Huang [4] ampliaron el modelo de volumen libre, para aplicarlo a la difusión de mezclas líquidas en polímeros, estos sistemas muestran buenos resultados comparados con la parte experimental. El uso del modelo de volumen libre para la permeación de mezclas líquidas es muy empleado con propósitos prácticos.
Greenlaw [11] y Long [12] investigaron mezclas líquidas que conducen casi a la idealidad. Una relación lineal entre permeabilidad y concentración puede adoptarse en estos casos. Mulder y Smolders [13] propusieron una relación de tipo exponencial entre el coeficiente de difusión y la concentración para mezclas agua-etanol, sólo que esta no considera interacciones mutuas entre los penetrantes y la membrana. Huang y Wei [14] aplicaron varias mejoras al modelo para mezclas etanol-agua a través de membranas de látex.
Aquí, se presenta una serie de cálculos teóricos que nos conducen a establecer los criterios termodinámicos útiles para la selección de una membrana empleada para llevar a cabo la separación de la mezcla de compuestos que deseamos separar por medio del proceso de pervaporación. Una vez seleccionada la membrana, se aplicó el modelo sencillo de disolución-difusión desarrollado por Matsura [15], para explicar la separación de una mezcla líquida binaria mediante el proceso de pervaporación. En este trabajo se presentan y discuten los valores calculados para:
— Los parámetros de interacción de diez polímeros con cada uno de nuestros compuestos a separar.
— Las isotermas de absorción para el MMA y para las impurezas W, en los sistemas Poli(metil propil siloxano) PMPS/MMA y PMPS/W.
— Los coeficientes de difusión a dilución infinita Do para el MMA y W en el sistema PMPS/MMA/W.
]]> — Los coeficientes de difusión Di, para los sistemas PMPS/MMA y PMPS/W.— Los coeficientes de plasticidad γ´ del PMPS en presencia del MMA y de W.
— La relación de mojado γ/γc para el PMPS en presencia de MMA, ISB y PRP.
Estos cinco parámetros se emplearon como criterios termodinámicos para la selección de las membranas que pueden ser empleadas en pervaporación para la separación de MMA, ISB y PRP.
Antecedentes teóricos
Procesos de separación
Dos sustancias i y j se mezclarán de forma espontánea cuando la energía libre del producto resultante o sea la mezcla sea menor que la suma de las energías libres de las sustancias puras.
Para lograr la separación de una mezcla formada espontáneamente, es necesario suministrar una cantidad de energía igual o mayor a la energía libre de mezclado ΔGm, a esta cantidad de energía se le conoce como el trabajo mínimo para efectuar la separación Wmin, y puede ser proporcionada por medio de energía en forma de calor o de trabajo mecánico.


En la práctica, la energía requerida para la separación podría ser varias veces mayor en magnitud que el valor del trabajo mínimo. La cristalización y la destilación llevan consigo una transición de fase, lo cual significa que se debe suministrar el calor necesario para la vaporización o solidificación.
Los procesos que utilizan membranas, tales como: ósmosis inversa o electrodiálisis se llevan acabo sin transición de fase y con bajo consumo de energía. En el proceso de pervaporación, el vacío ejercido en el lado del permeato facilita en gran medida el cambio de fase del líquido a vapor, puesto que la presión parcial ejercida por un componente dentro de la membrana, es mayor que la presión de vacío en el lado del permeato.
Mecanismo de disolución-difusión para una mezcla binaria
El gradiente de potencial químico a través de la membrana es considerado como la fuerza impulsora para la transferencia de masa en el proceso de pervaporación. El gradiente de potencial químico puede escribirse como:

Donde ∇µ es el gradiente de potencial químico a través de la membrana para cada componente, aim se refiere a la actividad de cada componente i en la membrana, Vi se refiere al volumen molar de cualquier componente, ∇p es el gradiente de presión entre ambas caras de la membrana y T es la temperatura del sistema
Si se considera que la presión de alimentación permanece constante al entrar los componentes en la membrana, como se muestra en la Figura1. La ecuación de transporte de acuerdo con la primera ley de Fick, queda de la siguiente forma:


El equilibrio termodinámico que se establece entre ambas caras de la membrana se puede representar mediante las siguientes ecuaciones:

Los subíndices 2 y 3 de las ecuaciones anteriores se refieren a la cara de la membrana en contacto con la disolución de entrada y a la cara de la membrana en contacto con el permeato respectivamente. Además se sabe que:

Donde µ0 es el potencial químico del compuesto puro a una presión de referencia, el equilibrio termodinámico entre ambas caras de la membrana para la especie i se puede escribir como:

Con la consideración de que la presión de la disolución de entrada, p2, prevalece a través de la membrana, y dicha presión decrece hasta la frontera entre la membrana y el permeato, entonces las ecuaciones (8 y 9) se pueden escribir de la siguiente forma:


Si se define al coeficiente de partición, K, como la relación de coeficientes de actividad para cada componente (γi2 / γim2 o γi3 / γim3), sustituyendo su valor en las ecuaciones (12 y 13), obtenemos:
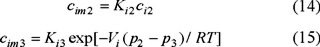
Introduciendo las ecuaciones anteriores en la ecuación (4), obtenemos:

Lo cual nos permite calcular el flujo del componente i a través de la membrana.
Absorción de disolventes en una red polimérica
Las isotermas de absorción, especialmente en el caso de compuestos orgánicos sobre materiales elastoméricos, se pueden describir de acuerdo con Favre [16] por medio de la expresión:


Donde χs es el término de contribución entrópica y χh el término de contribución entálpica, δs y δp son los parámetros de solubilidad del disolvente y polímero respectivamente
Difusión de disolventes dentro de redes poliméricas
Diferentes expresiones relacionan la difusividad del disolvente con la concentración de este en el polímero, las cuales fueron derivadas bajo argumentos de la teoría de volumen libre. A continuación se muestra una sencilla relación exponencial donde se observa la dependencia del coeficiente de difusión con la fracción en volumen del disolvente en la membrana φs, esta expresión es muy usada por su simplicidad y porque describe adecuadamente la dependencia de coeficiente de difusión con la concentración, como lo señala Favre [17]:

Donde Do es el coeficiente de difusión a disolución infinita y γ´ es el llamado coeficiente de plasticidad, el cual refleja el incremento en el volumen libre en la red de polímero, después de la absorción del disolvente. Esta expresión se empleó para calcular el coeficiente de plasticidad a partir de datos de Doi reportados por Favre (1994) y los valores de D calculados con la ecuación (23).
Mojado de membranas poliméricas sólidas por medio de líquidos
La relación de tensiones superficiales γ / γc , permite predecir el mojado de un material sólido, como una membrana de tensión superficial crítica γc, por un líquido de tensión superficial γ. Una membrana de polímero sólido, no es mojada cuando se cumple la relación γ / γc > 1.
El ángulo de contacto θ para el mojado, se forma por el efecto de las tres tensiones interfaciales entre el sólido, el líquido y el gas, de acuerdo con la ecuación de Young:
]]>
Donde el subíndice s, se refiere al sólido, v al vapor y l al líquido.
Para encontrar experimentalmente la tensión superficial crítica, se miden ángulos de contacto a temperatura constante entre la membrana polimérica sólida con varios líquidos, corresponde al valor de γc el valor de la tensión superficial del líquido cuando el valor de cos θ = 1. Entonces, la γc esta dada por la siguiente ecuación:

Proceso de cálculo
Para proceder a la selección de una membrana útil para nuestro problema de separación, primero se obtuvieron de la literatura valores de los parámetros de solubilidad para nuestros compuestos y para diversos polímeros, después se calculó el parámetro de interacción χ con la ecuación (18) y una vez seleccionada la membrana adecuada para nuestro propósito, se calculó la relación de mojado γ / γc, los coeficientes de difusión a dilución infinita Doi, ecuación (22), los coeficientes de difusión Di, ecuación (23), los coeficientes de plasticidad γ´, con la ecuación (25), para el sistema seleccionado. También se pudo aplicar un modelo de disolución-difusión sencillo, para obtener los valores de la permeabilidad Pi, flujos Ji y los factores de separación SFi j. Estos resultados se presentan y discuten a continuación.
Resultados y discusión
Cálculo de los parámetros de solubilidad
]]> Un criterio termodinámico aplicable para la elección de un disolvente adecuado para un polímero dado, es el uso de los parámetros de solubilidad tanto del polímero, δp como del disolvente δs, estos parámetros están relacionados con la polaridad del material, entre más grande sea el valor de δ aumenta la polaridad del material. De manera general, cuando el parámetro de solubilidad del disolvente se encuentra dentro del intervalo: δp - 1.1 < δs < δp + 1.1, se tiene un disolvente adecuado para ese polímero. Más adelante se muestra la Tabla 1, la cual contiene diversos parámetros de solubilidad reportados por F. Allan [18] y ordenados de acuerdo a su polaridad.
Cálculo de los parámetros de interacción χ
De acuerdo con los criterios termodinámicos de miscibilidad y compatibilidad, la elección de una membrana útil para separar una mezcla de líquidos, puede hacerse mediante el uso de los parámetros de interacción polímero-disolvente χ. Cuando el valor de χ es cero, se tendrá una disolución total. Favre [16] reporta que cuando el valor de χ es menor de 0.8 se tiene un buen disolvente para sistemas de pervaporación: PDMS/diversos disolventes.
El valor de χ se determinó mediante el uso de la expresión semi-empírica, ecuación (18), con la cual se calcularon los parámetros χ, para nueve sistemas entre ellos el sistema PMPS/MMA-ISB-PRP, los valores se reportan en la Tabla 2.

Para el cálculo del término entálpico χh de la ecuación (18), se utilizaron los valores de δ reportados en la Tabla 1, mientras que el valor del termino entrópico se consideró constante e igual a 0.35, valor aceptado para este tipo de sistemas de pervaporación. Los resultados se muestran en la Tabla 2, donde se marcan con negritas aquellos polímeros que muestran una gran interacción con las impurezas (ISB y PRP) y una interacción menor con el MMA, de tal manera que las impurezas pueden hinchar al polímero mas rápidamente que el MMA y por lo tanto dichas impurezas pueden atravesar la membrana más fácilmente que el MMA. Como se aprecia en la Tabla 2, el PMPS y el PMOS muestran diferencias en los valores de χ, que favorecen la separación de las impurezas.
Cálculo de los valores de las isotermas de absorción para un sistema polímero-disolvente
]]> De acuerdo con el criterio termodinámico del parámetro de interacción χ, se procedió a estudiar el comportamiento de los líquidos problema frente a una membrana de PMPS.Para calcular las isotermas de absorción del sistema: PMPS / MMA y PMPS / W, se utilizó la ecuación (17), donde el término W, se empleó para definir a las impurezas que como sabemos son: el ISB y el PRP principalmente.
Se dieron valores de composición φi, para el sistema, se calcularon las actividades correspondientes para el MMA y para las impurezas W. Se observó que el valor de la actividad igual a uno, aMMA = 1, se alcanza para el MMA cuando la composición del sistema es φMMA = 0.612 y para las impurezas, aW = 1 para una composición φW = 0.797 . (Figs. 2 y 3).


Correlación entre el coeficiente de difusión a dilución infinita con el volumen molar del penetrante
Sabemos que un parámetro muy importante para cuantificar la difusión de un penetrante a través de una membrana es el coeficiente de difusión a dilución infinita Do,i. Se ha reportado en investigaciones hechas por Favre (1994), una relación de tipo lineal entre el ln Do,i y el volumen molar del penetrante Vi, para diversos sistemas polímero / penetrante de acuerdo con la expresión (22):

Favre [17] reportó diversos valores de Do,i, para el sistema PDMS/diversos penetrantes, entre los que se encuentran algunas moléculas que muestran cierto parecido en el tamaño y la estructura química con nuestras sustancias a separar.
En la figura 5, a los datos de Do,i se les aplicó un ajuste de línea recta y se hicieron las interpolaciones sobre esa línea, para encontrar los valores de Do,i de nuestras substancias a separar.

Cálculo de los coeficientes de difusión y de plasticidad en los sistemas PMPS/MMA y PMPS/W
Se han propuesto varias relaciones matemáticas para explicar la variación del coeficiente de difusión con la concentración:

En la ecuación (24), cuando el sistema se acerca a la idealidad, es decir, cuando la fracción en volumen de penetrante es muy pequeña φi → 0, entonces, [d ln ai / d ln φi] → 1.

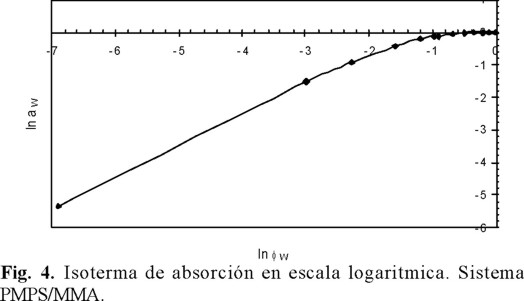
Otro método para conocer el valor de [d ln ai / d ln φi], es el método gráfico, mediante el cálculo de las pendientes de la gráfica de ln ai vs. ln φi, como se presenta en la figura 4.
Se probaron las dos opciones mencionadas arriba para conocer el valor de [d ln ai / d ln φi], este valor se introdujo en la ecuación (23), con el fin de encontrar el valor del coeficiente difusión Di,j y entonces calcular el coeficiente de plasticidad γ', que describe de manera adecuada el comportamiento para nuestro sistema, es decir, aquel que muestre la mejor correlación entre el coeficiente de difusión y la concentración del penetrante. Linearizando la ecuación (19), obtenemos la ecuación 25:

Donde γ' es el llamado coeficiente de plasticidad característico de cada sistema penetrante-polímero. El valor del coeficiente γ', es un criterio importante en la selección de la membrana polimérica adecuada para lograr la separación de nuestros compuestos.
Se prepararon las gráficas de Ln Di vs. φi, para los sistemas PMPS/MMA y PMPS/W con el fin de conocer los valores de γ'. Las figuras 6 y 7 describen en forma adecuada el comportamiento del coeficiente de difusión en función de la concentración.

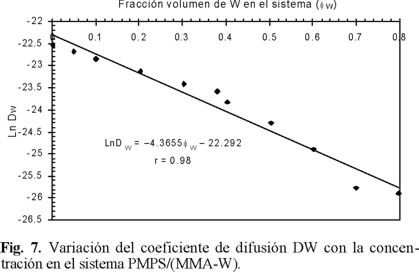
Como se puede apreciar en la figura 5, a medida que las concentraciones de MMA en el sistema aumenta, el valor de su coeficiente de difusión disminuye sensiblemente. El mismo comportamiento se observó para las impurezas representadas por W, en este caso la variación de DW con φW es menor, lo cual favorece que se presente una separación de los componentes de la mezcla.
Criterio de mojado para la membrana en contacto con los compuestos a separar
De acuerdo con la teoría del ángulo de contacto, en el proceso de pervaporación la membrana de polímero sólido no es mojada cuando la relación de tensiones superficiales γ / γc es mayor que la unidad. A continuación en la Tabla 3, se muestran valores de tensión superficial crítica γc para membranas hidrofóbicas e hidrofilicas, también se muestran los valores de tensión superficial γ para los compuestos a separar, los datos fueron tomados de Rodríguez [19].
En la figura 8 se presentan los valores de la relación γ / γc en función de la temperatura en K, la cual se preparó con los valores de γ calculados con la ecuación (26) y el valor de γc para el PDMS, este valor se consideró constante e igual al valor que se reporta en la Tabla 3.


En la ecuación (26) A y B son constantes características para cada compuesto a separar y Tr es la temperatura reducida correspondientemente.
]]> Este criterio nos permitió la selección de una temperatura de trabajo óptima, para la separación de los compuestos de la mezcla. Es decir, si queremos que el MMA quede retenido, es conveniente trabajar a una temperatura a la cual el MMA no moje fácilmente al PDMS o al PMPS, mientras que el ISB y el PRP si los mojen, dicha temperatura deberá estar entre 273 K (0 °C) y 287 K (14 °C). Para temperaturas mayores a 14 °C, como es la temperatura ambiente en la ciudad de México, 20 a 25 °C, el MMA mojará a la membrana de PDMS, pero siempre en menor proporción que el ISB y el PRP, lo que permitirá que estos últimos se absorban y atraviesen la membrana con mayor facilidad.
Conclusiones
En el presente trabajo se estudiaron algunos aspectos fisico-químicos que involucra el proceso de pervaporación, además se establecieron y se aplicaron diversos criterios termodinámicos para la selección de una membrana adecuada para la separación de nuestra mezcla de compuestos, los resultados obtenidos en relación con estos criterios termodinámicos se resumen a continuación.
El criterio termodinámico que nos dice cual es una membrana adecuada, es el uso de los parámetros de interacción polímero-penetrante χ, pues dicho criterio considera el efecto de la polaridad del polímero y del penetrante y el efecto del tamaño del penetrante.
Se detectaron dos membranas útiles para la separación, las cuales fueron el poli(metil propil siloxano) PMPS y el poli(metil octil siloxano) PMOS, de acuerdo con los valores de χ calculados.
En las isotermas de absorción para el sistema PMPS/ MMA el valor de actividad igual a uno se alcanza para una concentración de φMMA = 0.612, mientras que para el sistema PMPS/W se alcanza el valor de aW = 1 para una concentración de φW = 0.797.
De acuerdo con el modelo aplicado, al aumentar el volumen molar de los penetrantes MMA, ISB y PRP, el coeficiente de difusión a dilución infinita Doi disminuye en forma semi-logarítmica.
Al aumentar la concentración de alguno de los penetrantes, su coeficiente de difusión disminuye en forma semi-logarítmica. Sin embargo, para bajas concentraciones, las impurezas se difunden mas rápidamente que el MMA, lo cual permite la eliminación de las mismas. Cuando se aplicó el criterio de mojado γ / γc, este nos permite decir que por debajo de 287 K el MMA no moja a la membrana de PDMS, mientras que las impurezas si la mojan, lo cual facilita sensiblemente la separación de las impurezas.
]]> Referencias
1. Avilés Palacios, J. E., Tesis. Universidad Autónoma del Estado de México, 1994.
2. Mulder, M. V .H., Basic Principles of Membrane Technology. Kluver Dordcrecht, 1990. [ Links ]
3. Huang, R. Y. M.; Lin, V. J. C. J. Appl. Polym. Sci., 1968, 12, 2615. [ Links ]
4. Fiels, M.; Huang, R. Y. M. J. Macromol. Sci. Phys., 1971, B5, 89. [ Links ]
5. Suzuki, F.; Onazato, K. J. Appl. Polym. Sci. 1982, 27, 4229. [ Links ]
]]>6. Rautenbach, R.; Albrecht, R. J. J. Membrane Sci. 1985, 25, 1. [ Links ]
7. Brun, J. P.; Larchet, R. J. Membrane Sci. 1985, 23, 257. [ Links ]
8. Rhim, J. W.; Huang, R. Y. M. Separation characteristics of pervaporation membranes separation process, in: R.Y.M. Huang (Ed.) Pervaporation Membrane Separation Process, Elsevier, Amsterdam, 1991. [ Links ]
9. Yeom, C. K.; Huang, R. Y. M. J. Memb. Sci. 1992, 67, 39. [ Links ]
10. Heintz, A.; Stephan, W. J. Membrane Sci. 1994, 89, 143. [ Links ]
]]>11. Greenlaw, F. W.; Pince, W D.; Shelden, R. A. J. Membr. Sci., 1977, 2, 333. [ Links ]
12. Long, R. B. Ind. Eng. Chem. Fundam., 1965, 4, 445. [ Links ]
13. Mulder, M. V. H.; Smolder, C. A. J. Membrane. Sci. 1994, 17, 289. [ Links ]
14. Huang, R. Y. M.; Wei, Y. Sep. Sci. Technol. 1994, 29, 1193. [ Links ]
15. Matsura, T. Synthetic membranes and membranes separation process. CRC Press. New York , 1995. [ Links ]
]]>16. Favre, E.; Nguyen, Q.; Schaetzel, P.; Clément, R.; Neél, J., J. Chem Soc. Faraday Trans. 1993, 98, 4339. [ Links ]
17. Favre, E.; Shaetzel, P.; Nguygen, Q. T.; Clement, R.; Neel, J. J. Membrane Sci. 1994, 92, 169. [ Links ]
18. Bartron, A. F., Handbook of polymer liquid interaction parameter and parameters solubility. CRC Press, 1995. [ Links ]
19. Rodriguez, F. Principles of polymer systems, Mc Graw-Hill. New York 1985. [ Links ]
]]>