
Photoelectrochemical oxidation of phenol and 4–chlorophenol using a titanium electrode coated with a TiO2 film
Gonzalo Cuauhtémoc LÓPEZ–OJEDA1, Aída Viridiana VARGAS–ZAVALA1, Ma. Rafaela GUTIÉRREZ–LARA1, Rosa María RAMÍREZ–ZAMORA2 y Alfonso DURÁN–MORENO1*
1 Facultad de Química, UNAM, Edificio E, Laboratorio 301, Ciudad Universitaria, C.P. 04510. México, D.F. Tel. (55) 56225293, Fax (55) 56225303. Correos electrónicos: unilquadium@hotmail.com, viv@correo.unam.mx, rafaelag@servidor.unam.mx, alfdur@servidor.unam.mx*
2 Instituto de Ingeniería, UNAM, Coordinación de Ingeniería Ambiental, Edificio 5, Ciudad Universitaria, C.P. 04510, México, D.F. Tel. 56233600 Ext. 8657. Correo electrónico: rramirezz@ii.unam.mx
Recibido enero 2010 ]]> Aceptado diciembre 2010
RESUMEN
El objetivo de este trabajo fue evaluar el desempeño de un sistema de oxidación fotoelectrocatalítica para la degradación de fenol y 4–clorofenol presentes en soluciones acuosas. Para las pruebas experimentales se utilizó una celda de 1.5 L como fotorreactor y un soporte de titanio como ánodo, el cual fue recubierto con dióxido de titanio (TiO2). La inmovilización del TiO2 sobre el soporte de titanio se realizó mediante la técnica de depósito de electroforesis, seguida de una activación térmica a 450 ºC. El material recubierto se caracterizó por microscopía electrónica de barrido (SEM, por sus siglas en inglés), observándose la formación de una película uniforme sobre el soporte de titanio. En este fotorreactor se realizó la oxidación del fenol y del 4–clorofenol en condiciones ácidas y una lámpara de luz UV. Los resultados mostraron una rápida transformación del fenol y del 4–clorofenol debida al ataque de los radicales hidroxilo formados a partir del agua. En concentraciones bajas de 50 y 100 mg/L de solución sintética, se obtuvieron porcentajes de remoción significativos para ambos compuestos fenólicos siendo estos del 80 y 100 % para el caso del fenol; sin embargo, se observó que al incrementar la concentración inicial de estos compuestos hasta 300 y 500 mg/L, las soluciones de fenol y 4–clorofenol finales adquirieron una coloración obscura debido a la formación de subproductos de la oxidación que impidieron la transmisión de luz hacia el catalizador, interfiriendo con ello en el mecanismo de reacción. Las reacciones electroquímicas, inducidas por la aplicación de otros potenciales, no fueron capaces de degradar los subproductos formados en los experimentos con concentraciones iniciales mayores a 300 mg/L. Los resultados de remoción de carbono orgánico total (COT) mayores al 80 %, demuestran que el sistema de oxidación fotoelectrocatalítica es efectivo para la mineralización de fenol y 4–clorofenol en concentraciones inferiores a 100 mg/L. Futuros estudios se enfocarán a evaluar la viabilidad de utilizar el sistema de oxidación fotoelectrocatalítica como pretratamiento de un proceso biológico para el tratamiento de aguas residuales con altas concentraciones de fenol y de 4–clorofenol.
Palabras clave: fotoelectrocatálisis, fotocatálisis, fenol, 4–clorofenol, foto–ánodo, TiO2, luz UV.
ABSTRACT
The aim of this work was to evaluate the performance of a photoelectrochemical system for the degradation of phenol and 4–chlorophenol in aqueous solutions. Experiments were carried out in a 1.5 L cell using a titanium electrode coated with titanium dioxide (TiO2) as anode. The anode was prepared by immobilizing TiO2 (Degussa P25) on a titanium substrate using an electrophoretic deposition method, followed by heat treatment at 450 ºC. The TiO2 film was characterized using scanning electron microscopy (SEM); a uniform surface was observed all over the titanium substrate. This electrode was utilized as the anode of a photoreactor for the oxidation of phenol and 4–chlorophenol under acidic conditions and an ultraviolet lamp. Results showed a rapid transformation of phenol and 4–chlorophenol by the action of hydroxyl radicals yielded from water. It was found that at low concentrations (50–100 mg/L) both compounds were significantly degraded (80–100 %), however, at higher initial concentrations (300–500mg/L), by–product formation of phenol and 4–chlorophenol oxidation imparted a dark color to the solutions, which hindered light transmission to the catalyst and interfered with the reaction mechanism. Attempts to degrade by–products by applying other potentials in the experiments of concentrations greater than 300 mg/L did not succeed. Removals of total organic carbon (TOC) higher than 80 %, showed that the photoelectrochemical oxidation system was effective in mineralizing phenol and 4–chlorophenol at concentrations lower than 100 mg/L. Future studies will focus on evaluating the photochemical oxidation system as a pre–treatment for a biological process used for the treatment of wastewater with high phenol and 4–chlorophenol concentrations.
Key words: photoelectrocatalysis, photocatalysis, phenol, 4–chlorophenol, photoanode, TiO2, UV light.
]]> INTRODUCCIÓN
En la actualidad los procesos fotoquímicos son considerados como una alternativa tecnológica para el tratamiento de efluentes industriales con propiedades fisicoquímicas difíciles de manejar por medio de tratamientos biológicos convencionales. Es por ello que se emplean materiales semiconductores, los cuales poseen una actividad catalítica alta, activada mediante la acción de una fuente de radiación UV. Tal actividad tiene la capacidad de propiciar reacciones de oxidación en fase acuosa. Entre los materiales empleados para este tipo de procesos se tiene el TiO2 en forma anatasa, el cual ha destacado por su bajo costo, baja toxicidad, buena estabilidad mecánica y capacidad fotocatalítica alta. El TiO2 se utiliza en forma de polvo, para la preparación de soluciones coloidales o bien, inmovilizar al soporte que servirá de ánodo. Para llevar a cabo la inmovilización del soporte se emplean técnicas de síntesis del TiO2 como la llamada de sol–gel, en la cual el catalizador se genera a partir de un precursor como el isopropóxido de titanio o TiCl3 (Alam et al. 2002, Alemany et al. 1997, Djaoued et al. 2002, Horikoshi et al. 2002, Lee et al. 2004, Shaojing et al. 2004, Tasbihi et al. 2007, Zhou et al. 2002, Zoppi et al. 2003); mientras que Hitchman et al. (2002) utilizaron tetra–butóxido de titanio como reactivo base y Enríquez et al. (2007) probaron cinco catalizadores diferentes obtenidos a partir de la hidrólisis de TiOSO4.
Otra técnica que ha revelado ser de mucho interés práctico es el preparar una solución a partir de óxido de titanio nanoparticulado para recubrir el soporte, teniendo la opción de aplicar o no una diferencia de potencial con tal de mejorar la adherencia y las propiedades morfológicas de la capa final resultante, seguida de una activación térmica a más de 400 ºC, lo anterior fue citado en los trabajos de Esquivel et al. (2009), Ku et al. (2006), Mbindyo et al. (1997), Peralta et al. (2006), Peralta et al. (2008), Vohra et al. (2003) y Waldner et al. (2005).
Autores como Alemany et al. (1997), An et al. (2002), Horikoshi et al. (2002), Peralta et al. (2006) y Peralta et al. (2008) estudiaron el mecanismo de reacción que involucra la interacción entre el material fotocatalizador y la radiación UV, generando "huecos de pares de electrones" en la superficie del semiconductor cargados eléctricamente, los cuales reaccionan con las sustancias orgánicas y con el agua. La iluminación con energía irradiada es más grande que la energía del ancho de banda (Egb) del semiconductor (hn > Egb = 3.2 eV en el caso de TiO2 en forma anatasa) generando hoyos en la banda de valencia (h+nb) y electrones en la capa de conducción (e—cb), lo que se muestra en la Ecuación 1:

Debido a esta característica energética, el TiO2 en forma anatasa sólo puede ser activado por luz ultravioleta a longitudes de onda menores a 400 nm. Los hoyos fotogenerados en la banda de valencia (h+nb) y los electrones de la banda de conducción (e—cb), pueden recombinarse para liberar calor o dirigirse por vías separadas hacia la superficie del TiO2, en donde pueden reaccionar con las especies adsorbidas en la superficie del catalizador como en el caso de los compuestos orgánicos (Ecuación 2):

También puede ocurrir la generación de radicales libres de acuerdo a las reacciones mostradas en las ecuaciones 3 y 4:

Durante la oxidación del agua o de los iones de hidróxido realizada por el "agujero" en la capa de valencia (h+nb) se pueden generar radicales hidroxilo (OH •). La banda de conducción de electrones (e—cb) puede reaccionar con el oxígeno molecular para formar radicales en forma de aniones de superóxido, O2—, los cuales pueden ser el punto inicial para otro tipo de reacciones. En un primer caso, se generan mecanismos de reacción de tipo redox, mediante los cuales se oxidan directamente los compuestos de tipo orgánico sobre la superficie del semiconductor. En el segundo caso, la reacción de ruptura del agua forma radicales OH•. En caso de no ser posible la degradación total de los contaminantes, al menos se logra un cambio estructural de las sustancias, ayudando a que se vuelvan aptas para un tratamiento posterior o lograr la disminución de la toxicidad de los efluentes por medio de oxidaciones parciales. La aplicación de voltaje externo al proceso netamente fotocatalítico (llamado entonces proceso fotoelectrocatalítico), convierte al fotocatalizador en un fotoánodo, de tal manera que los procesos de recombinación de los electrones generados debido a la radiación UV se retardan, así como la reacción de fotorreducción misma del oxígeno (Ecuación 5):
]]>
La reacción anterior se minimiza debido a que el electrón no actúa sobre el semiconductor sino que se incorpora al circuito eléctrico (Alemany et al. 1997, An et al. 2002, Horikoshi et al. 2002, Peralta et al. 2006 y Peralta et al. 2008).
En este trabajo se empleó la técnica de electroforesis aplicando una diferencia de potencial de 4 V para recubrir una malla de titanio con polvo de TiO2 (Degussa P–25); posteriormente se activó el soporte por medio de una calcinación a 450 ºC. Los experimentos de oxidación fueron realizados utilizando un foto–reactor de geometría cilíndrica, en medio ácido de pH entre 3 y 3.5, Na2SO4 0.1 M como electrolito de soporte y una lámpara de luz UV de 254 nm, se emplearon soluciones sintéticas de fenol de concentraciones 50, 100, 300 y 500 mg/L y 4–clorofenol de 100, 300 y 500 mg/L como contaminantes. Durante las pruebas realizadas la disminución de estos compuestos fenólicos fue evaluada por medio de la reacción con 4–aminoantipirina, la demanda química de oxígeno (DQO) y el carbono orgánico total (COT). Los resultados experimentales a concentraciones mayores de 300 y 500 mg/L presentaron una reacción secundaria, la cual fue la generación de polímeros insolubles, cuya presencia se incrementó conforme se aumentó la concentración de las soluciones a oxidar.
MATERIALES Y METODOLOGÍA
Preparación del soporte de Ti en TiO2
Se utilizó una malla de titanio de tipo micro como fotoánodo, la cual se limpió con una solución de ácido clorhídrico (HCl) y ácido nítrico (HNO3) concentrados en una relación 50/50 en volumen, a una temperatura de 80 ºC durante 1 hora. Para la preparación de la solución precursora de TiO2, se utilizó polvo Degussa P–25 (80 % anatasa, 20 % rutilo, con diámetro de partícula de 20 nm) disuelto en 2–propanol (>99.8 % Sigma Aldrich) y agua destilada, formándose una solución coloidal. Posteriormente, se sumergió totalmente el soporte en la solución, empleando un ánodo de acero inoxidable y el soporte como cátodo; se aplicó una diferencia de potencial de 4V durante 1 minuto, para finalmente calcinar a 450 ºC por 30 minutos y enfriar a temperatura ambiente. Este método se realizó 5 veces para tener finalmente la malla con 5 capas de TiO2. Se empleó la técnica de microscopía electrónica de barrido (SEM) para observar la superficie de la malla de titanio recubierta, de manera que se examinaran los aspectos morfológicos obtenidos con la técnica de preparación del TiO2.
Reactor fotoelectroquímico
Los experimentos fueron realizados a temperatura ambiente en un reactor cilíndrico de 1.5 L como volumen útil. La figura 1 muestra la distribución en la que fueron colocados los elementos dentro del reactor, que incluyó difusores de aire con el fin de mejorar la turbulencia, aumentar el efecto de mezclado y saturar la solución con oxígeno. El cátodo consistió en una barra de grafito.
]]>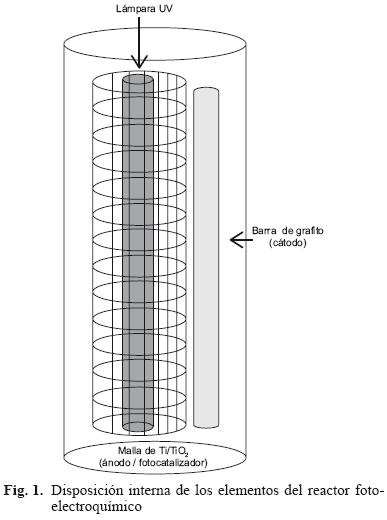
La figura 2 muestra la distribución en la que fueron colocados los elementos dentro del reactor, el soporte o fotoánodo se colocó en el interior, la lámpara UV en la parte central y la malla en la parte externa, la barra de grafito fue colocada en uno de los extremos del fotoánodo. El soporte de Ti y la barra de grafito, de aproximadamente 14.0 cm2 de área superficial, se conectaron en un circuito electroquímico utilizando una fuente de poder Laboratory DC Power Supply GPR–3060D, con la que se aplicó una diferencia de potencial de 0.7 V con la finalidad de retardar las reacciones secundarias de recombinación de acuerdo al mecanismo antes mencionado. Como fuente de radiación UV se empleó una lámpara de 6 W a 254 nm de Levitec, colocada en un tubo de cuarzo de 3 mm de espesor.

El flujo de alimentación de electrolito fue de 1.66 x 10—7 m3/s (10 mL/min), el cual se recirculó al reactor para incrementar el efecto de oxidación del soporte de TiO2 sobre los compuestos orgánicos presentes. El electrolito utilizado fue Na2SO4 0.1 M, ajustado a un pH de 3 a 3.5 mediante la adición de H2SO4 concentrado (>98 % J.T. Baker). El volumen utilizado de las soluciones sintéticas fue de 1 L, estas fueron preparadas con agua destilada, fenol (>99 % J.T. Baker) y 4–clorofenol (>98 % Sigma Aldrich). En el caso del fenol la concentración utilizada fue de 50 mg/L y para el 4–clorofenol los experimentos se realizaron utilizando tres concentraciones 100, 300 y 500 mg/L. Para cuantificar la disminución de la concentración de fenol, se utilizó el método espectrofotométrico del cambio de coloración por reacción con 4–aminoantipirina empleando un fotómetro Spectronic 21D de Milton Roy (NMX–AA–050–SCFI–2001); las mediciones de la DQO (NMX–AA–030–SCFI–2001), tanto para fenol como para 4–clorofenol, se hicieron utilizando la técnica a reflujo cerrado; finalmente, el análisis de COT se realizó con un equipo Shimadzu TOC–V Total Organic Carbon Analyser.
RESULTADOS Y DISCUSIÓN
Análisis de la superficie del electrodo por microscopía electrónica de barrido (SEM)
Las fotografías de microscopía electrónica de barrido obtenidas a las resoluciones de (a) 1 μm, (b) 500 μm, (c) 100 μm y (d) 50 μm se muestran en la figura 3. Se observa que con la técnica empleada para preparación del soporte, el TiO2 formó una película uniforme sobre todo el sustrato de titanio. Además, se aprecia que al utilizar polvo nanoparticulado como el TiO2 Degussa P–25, se formaron gránulos de distintos tamaños repartidos sobre la superficie de la malla, producto del depósito del material de TiO2.
Los gránulos depositados, según lo que se observa en la figura 3, presentaron dimensiones entre 30 y 50 Mm, formando a su vez agregados entre ellos. El recubrimiento mostró características mecánicas estables y resistencia a la abrasión mecánica, permaneciendo adherido a la malla aún tras lavados continuos y al montar y desmontar el equipo. Además se presenta una resistencia al ataque químico debido al contacto con las diversas soluciones de electrolito y fenol, así como al uso de H2SO4 concentrado.
]]> Oxidación de fenolEl mecanismo de reacción involucra la activación de la molécula de fenol con los radicales OH•. El primer paso comprende el ataque electrofílico de los radicales hidroxilo a la molécula de fenol, para formar un radical fenoxi adsorbido (Ecuación 6):

Además de los procesos llevados a cabo con el radical OH•, también se toman en cuenta las reacciones directas entre el sustrato orgánico con los hoyos fotogenerados en la capa de valencia del fotocatalizador o con otro tipo de radicales como O2•; procesos que, aunque de menor relevancia, pueden intervenir en la interfase entre el semiconductor y el fluido. Así, el radical fenoxi también puede ser oxidado directamente en la superficie del catalizador de TiO2 formando un catión fenoxio (Ecuación 7):

En el primer caso, las reacciones de hidroxilación del radical fenoxi resultan en la formación de hidroquinona o catecol, mientras que en el segundo caso los mismos subproductos pueden generarse si existe hidrólisis del catión fenoxio (Alemany et al. 1997, Guillard et al. 1999). Los subproductos finales son ácidos carboxílicos, y en caso de llevarse a cabo la oxidación completa, CO2 y agua (Peiró et al. 2001).
Como se observa en la figura 4, hay una rápida disminución en la concentración del fenol, a causa del mecanismo de oxidación favorecido por los radicales hidroxilo formados por la reacción entre la capa de TiO2 y el agua del medio, debido a la activación del fotocatalizador por la radiación UV.

Para una concentración de 50 mg/L de fenol se remueve el 60 % del mismo en una hora de reacción, lográndose la remoción casi completa en 6 horas de irradiación. Al duplicar la concentración inicial (100 mg/L) de fenol, se logra una remoción de hasta un 88 % para las mismas horas de irradiación. Los resultados anteriores prueban que existe un efecto de oxidación y disminución de la cantidad inicial de fenol por la acción conjunta de la malla recubierta de TiO2, la luz UV y el circuito electroquímico auxiliar. Dado que el fenol no puede oxidarse a CO2 en un sólo paso, los resultados indican que la molécula original se oxida y genera otros subproductos derivados, de acuerdo al mecanismo de reacción anteriormente descrito.
]]> Las constantes cinéticas fueron evaluadas asumiendo que las reacciones de oxidación del fenol siguen un comportamiento de pseudo primer orden, lo que permite que la cinética pueda representarse con una expresión semejante a la de una ecuación de velocidad de primer orden. Para este caso, se asume que la concentración de los radicales hidroxilo generados por la interacción entre el TiO2 y la radiación UV se encuentran en exceso, por lo que la cinética es considerada de primer orden, así la concentración del otro reactivo (el compuesto orgánico a degradar) disminuirá exponencialmente, pero con una velocidad que es proporcional a la concentración del reactivo en exceso (Alemany et al. 1997). Los valores de las constantes cinéticas para los experimentos a 50 y 100 mg/L se muestran en el cuadro I.
Remoción de la DQO en soluciones de fenol
La tendencia del comportamiento en la disminución de DQO se muestra en la Figura 5. La disminución en el valor de DQO para la solución de 50 mg/L fue del 27.7 % al pasar de 162 a 117 mg/L en 7 horas. Con una concentración de 100 mg/L de fenol, el valor de DQO disminuyó un 31.5 % al pasar de 308 a 211 mg/L. En esta tendencia se observa que existe un incremento proporcional entre la tasa de oxidación del fenol y la concentración inicial de la solución en estudio, esto se explica en términos del incremento de la transferencia de masa del fenol a la superficie del fotoánodo, si existe más fenol en la solución, aumenta la cantidad de materia orgánica que puede entrar en contacto con dicho soporte en un determinado tiempo y por ende, es oxidada de manera más efectiva (Tasbihi et al. 2007). El mecanismo necesita de interacción entre la superficie y la molécula. El ataque de los radicales OH● ocurre no sólo en la superficie, sino también en la interfase entre el dispositivo y el medio. La reacción de descarboxilación se ve favorecida por el ataque combinado de generación de radicales libres y la interacción con la superficie del catalizador a través de los hoyos en la capa de valencia.

A 300 mg/L de fenol, la DQO se redujo sólo un 17.6 %, pasando de 890 a 733 mg/L en 7 horas. El valor de la DQO para 500 mg/L se redujo un 32.6 %, de un valor inicial de 1398 a 942 mg/L en el mismo lapso de 7 horas. Estos valores de remoción bajos a las concentraciones de fenol inicial de 300 y 500 mg/L, pueden atribuirse a una consecuencia inesperada del mecanismo de ataque por radicales libres, lo cual modifica las características de las soluciones tratadas pasando de ser incoloras a amarillentas (por la generación de benzoquinona y catecol como productos iniciales de oxidación), incrementándose la coloración al transcurrir el tiempo de experimentación hasta un café oscuro, casi negro y obteniéndose además residuos en forma de precipitados en el fondo del reactor, los cuales no pudieron ser oxidados. Dado que el mecanismo de fotocatálisis depende de que exista una transmisión de la luz al soporte de TiO2, si hay algo que pueda interferir con esa transmisión (en este caso el cambio de coloración y la posible adsorción de parte de tales precipitados sobre la superficie del TiO2 dando un efecto de envenenamiento o pasivación del soporte), se frenarían las reacciones de oxidación, reduciendo los valores de remoción, de ahí el declive paulatino de la velocidad de degradación.
Remoción de COT en soluciones de fenol
]]> La figura 6 muestra los resultados de los experimentos de remoción de COT. En este caso el tiempo de experimentación se fijó en 8 horas. Para la solución de 50 mg/L de fenol inicial se obtuvo una remoción del 84.6 %. Con 100 mg/L la eficiencia fue de 93.2 %; para el caso de la solución de 300 mg/L se obtuvo una remoción del 17.47 %, mientras que a una concentración de 500 mg/L el valor de COT inicial se redujo en un 28.8 %. A concentraciones mayores se observa una baja eficiencia, producto del cambio de color, sumándose el fenómeno adicional al que varios autores han descrito como un conjunto de reacciones de polimerización en la que dos o más radicales fenoxi se acoplan, dando lugar a la formación de otros intermediarios más complejos, los que pueden ser moléculas con hasta dos anillos aromáticos unidos entre sí, teniendo la capacidad de agregarse y formar largas cadenas (Peiró et al. 2001, Santos et al. 2002). Se obtienen por lo tanto compuestos no solubles en agua que precipitan y cambian la coloración de las soluciones tratadas, además de provocar la inactivación paulatina del soporte de TiO2 al quedar adheridos a su superficie.
Según los resultados de las cinéticas obtenidos para las reacciones de descomposición del fenol, la constante k está directamente relacionada con la concentración de las soluciones de fenol. Las constantes evaluadas mediante la disminución de fenol con base en la concentración de la DQO y del COT, muestran que hay un incremento en el valor de la constante mientras mayor es la concentración (como en el caso del incremento obtenido en los experimentos a 50 y 100 mg/L). Sin embargo, debido a que existen reacciones secundarias que afectan al proceso fotocatalítico, ocurre lo contrario, disminuyendo tanto el valor de remoción final como el de la velocidad de oxidación y la constante cinética. En el cuadro II se presentan los resultados del cálculo de las constantes para estos experimentos.
Oxidación de 4–clorofenol
Para las pruebas experimentales con 4–clorofenol, se utilizaron soluciones de 100, 300 y 500 mg/L, realizando sólo mediciones de la DQO y el COT, ya que la reacción del 4–clorofenol con 4–aminoantipirina no produjo un color estable con el que fuera posible medir la disminución de compuestos fenólicos derivados, debido a la posible liberación de cloruros y a las desviaciones propias del método cuando los compuestos analizados son para sustituidos. A continuación se mencionan los resultados obtenidos de estos dos parámetros.
Remoción de la DQO
La figura 7 muestra los resultados obtenidos para la remoción de la DQO. A una concentración de 100 mg/L de 4–clorofenol inicial se logró una disminución de 214 mg/L de la DQO, pasando de 417 a 203 mg/L, lo que corresponde a un 51.32 % de remoción; con 300 mg/L de 4–clorofenol, el valor de la DQO disminuyó de 750 a 523.2 mg/L, equivalente a un 30.23 % de remoción y, finalmente con la solución de 500 mg/L, la concentración de la DQO disminuyó 230 mg/L, al reducirse desde 921 a 690.53 mg/L, obteniéndose el 25.02 % de degradación.
]]>
Las reacciones de oxidación de 4–clorofenol, de acuerdo a la bibliografía, siguen un esquema de ataque por radicales OH● análogo al de las reacciones con fenol, generando subproductos tales como benzoquinona y catecol pero produciéndose otros derivados clorados como clorocatecol y clorohidroquinona, además de ácidos carboxílicos tales como ácido maleico y en oxidación completa, CO2 y agua (Enríquez et al. 2007, Mbindyo et al. 1997).
De manera similar a las pruebas con fenol, utilizando 4–clorofenol se volvió a presentar el fenómeno de cambio de coloración y formación de compuestos insolubles, proceso que inhibió la capacidad oxidante del soporte.
Remoción de COT
En las pruebas de determinación de COT, cuyos resultados se presentan en la figura 8, para la solución de 100 mg/L se obtuvo una remoción del 82 % en 19 horas de reacción, a 300 mg/L la materia orgánica sólo disminuyó en 36.6 % . Con la concentración mayor de 500 mg/L, la remoción fue del 28.9 %. Aunque también se presentó el fenómeno del cambio en la coloración de las soluciones tratadas, la tonalidad de la solución con una concentración de 100 mg/L de fenol no fue tan intensa como en el caso de las concentraciones iniciales de 300 y 500 mg/L.

Al igual que en el caso del fenol, se asume una cinética de pseudo primer orden y se observa de igual forma que el valor de k es menor mientras mayor es la concentración inicial de la solución estudiada, tanto para el valor de la DQO, como para el del COT. En el cuadro III se muestran los resultados obtenidos para esta prueba cinética y es evidente que la constante es mayor al aumentar la concentración inicial del 4–clorofenol. Esto es congruente, puesto que hay un incremento de la transferencia de masa de los compuestos orgánicos del medio a la superficie del fotoánodo donde pueden ser oxidados de manera efectiva. Cabe mencionar que con el 4–clorofenol no se presentó un cambio de coloración tan intenso como en el caso de fenol, y además, en tiempos mayores de 12 horas, la tonalidad oscura se fue perdiendo gradualmente, por lo que las reacciones fotocatalíticas no fueron minimizadas.
La inactivación del soporte debido a los compuestos de oxidación formados es provocada por las reacciones llevadas a cabo sobre la superficie del catalizador, de acuerdo a la Ecuación 2, en la que el ataque mediado por los radicales OH● necesita que tales sustancias se adsorban en la interfase del soporte. Mientras más de estas sustancias se generan, una mayor cantidad es adsorbida, minimizando el poder oxidante conforme pasa el tiempo, generándose de esta forma una capa que recubre el soporte y al TiO2, con lo cual a su vez se minimiza el efecto de la luz UV sobre éstos.
El potencial aplicado de 0.7 V no es lo suficientemente alto como para promover otro tipo de reacciones redox complementarias que puedan ayudar a la oxidación y destrucción de los subproductos formados. El cambio de coloración en las soluciones es otro factor que va disminuyendo la capacidad oxidante del soporte de TiO2 al impedir una buena transmisión de la luz UV proveniente de la lámpara, creando una barrera que hace inaccesible parcialmente al catalizador.
]]> Observando las gráficas de remoción de la DQO y del COT a concentraciones altas para los dos compuestos estudiados, puede verse que aunque la velocidad de reacción es cada vez menor, los procesos de degradación no se detienen. Esto puede deberse al efecto de aireación dado por los difusores empleados en el reactor, debido a que su acción ayuda a que la capa de compuestos adheridos sea removida de la superficie de la malla por la turbulencia que generan, logrando de esta forma que las reacciones de oxidación continúen. Sin embargo, conforme más cantidad de subproductos se genera, la acción remediadora se ve minimizada.
CONCLUSIONES
Durante el desarrollo de la presente investigación se logró la oxidación de fenol y 4–clorofenol en medio ácido a diferentes concentraciones, empleando TiO2 en forma anatasa inmovilizada en un soporte de titanio. El método de preparación del fotoánodo proporcionó una buena estabilidad química y mecánica al catalizador adherido a la malla de titanio. Los resultados experimentales mostraron que los compuestos originales de fenol y 4–clorofenol, son transformados rápidamente por la acción de los radicales hidroxilos formados por las reacciones entre el agua del medio y su interacción con la superficie del catalizador. A concentraciones bajas se obtienen velocidades de oxidación y porcentajes de remoción aceptables, pero a altas concentraciones ocurren reacciones secundarias, generándose compuestos insolubles como parte de los subproductos formados, de acuerdo a lo descrito en la bibliografía. Estos compuestos no pudieron ser degradados bajo las condiciones de operación del reactor y minimizan la capacidad oxidante del soporte de TiO2 al modificar las propiedades de las soluciones tratadas y envenenar el material fotocatalítico. El potencial auxiliar aplicado sólo retarda las reacciones de recombinación fotoquímicas, pero no es el suficiente para ayudar a minimizar o destruir los subproductos insolubles que no pueden ser oxidados.
AGRADECIMIENTOS
Se agradece el apoyo del Consejo Nacional de Ciencia y Tecnología (CONACyT) por la beca para la realización de estudios de maestría de Gonzalo Cuauhtémoc López Ojeda, así como a la Facultad de Química de la UNAM por el apoyo financiero otorgado a través del Programa de Apoyo a la Investigación en Posgrado (PAIP).
REFERENCIAS
Alam M.J. y Cameron D.C. (2002). Preparation and characterization of TiO2 thin films by sol–gel method. J. Sol–gel Sci. Techn. 25, 137–145. [ Links ]
Alemany L.J., Bañares M.A., Pardo E., Martin F., Galán Fereres M. y Blasco J.M. (1997). Photo degradation of phenol in water using silica–supported titania catalyst. Appl. Catal. B: Environ. 13, 289–297. [ Links ]
An T.C., Zhu X.H. y Xiong Y. (2002). Feasibility study of photo electrochemical degradation of methylene blue with three–dimensional electrode–photo catalytic reactor. Chemosphere 46, 897–903. [ Links ]
Djaoued Y., Badilescu S., Ashrit P.V., Bersani D., Lottici P.P. y Brüning R. (2002). Low temperature sol–gel preparation of nanocrystalline TiO2 thin films. J. Sol–gel Sci. Techn. 24, 247–254. [ Links ]
Enríquez R., Agrios A.G. y Pichat P. (2007). Probing multiple effects of TiO2 sintering temperature on photocatalytic activity in water by use of a series of organic pollutant molecules. Catal. Today 120, 196–202. [ Links ]
Esquivel K., Arriaga L.G., Rodríguez F.J., Martínez L. y Godínez L.A. (2009). Development of a TiO2 modified optical fiber electrode and its incorporation into a photoelectrochemical reactor for wastewater treatment. Water Res. 43, 3593–3603. [ Links ]
Guillard C., Disdier J., Herrmann J.M., Lehaut C., Chopin T., Malato S. y Blanco J. (1999). Comparison of various titania samples of industrial origin in the solar photocatalytic detoxification of water containing 4–chlorophenol. Catal. Today 54, 217–228. [ Links ]
Hitchman M.L. y Tian F. (2002). Studies of TiO2 thin films prepared by chemical vapor deposition for photocatalytic and photoelectrocatalytic degradation of 4–chlorophenol. J. Electroanal. Chem. 538–539, 165–172. [ Links ]
Horikoshi S., Watanabe N., Onishi H., Hidaka H. y Serpone N. (2002). Photodecomposition of a nonylphenol polyethoxylate surfactant in a cylindrical photoreactor with TiO2 immobilized fiberglass cloth. Appl. Catal. B: Environ. 37, 117–129. [ Links ]
Ku Y., Lee Y.C., Wang W.Y. (2006). Photocatalitic decomposition of 2–chrophenol in aqueous solution by UV/TiO2 process with applied external bias voltage. J. Hazard. Mater. B 138, 350–356. [ Links ]
Lee J. M., Kim M.S. y Kim B.W. (2004). Photodegration of bisphenol–A with TiO2 immobilized on the glass tubes including the UV light lamps. Water Res. 38, 3605–3613. [ Links ]
Mbindyo J.K.N., Ahmadi M.F. y Rusling J.F. (1997). Pollutant decomposition with simultaneous generation of hydrogen and electricity in a photogalvanic reactor. J. Electrochem. Soc. 144, 3153–3158. [ Links ]
Peiró A.M., Ayllón J.A., Perla J. y Doménech X. (2001). TiO2–photocatalyzed degradation of phenol and ortho–substituted phenolic compounds. Appl. Catal. B: Environ. 30; 359–373. [ Links ]
Peralta Hernández J.M., Meas Vong Y., Rodríguez F.J., Chapman T.W., Maldonado M.I. y Godínez L.A. (2006). In situ electrochemical and photo–electrochemical generation of the fenton reagent: A potentially important new water treatment technology. Water Res. 40, 1754–1762. [ Links ]
Peralta Hernández J.M., Meas Vong Y., Rodríguez F.J., Chapman T.W., Maldonado M.I. y Godínez L.A. (2008). Comparison of hydrogen peroxide–based processes for treating dye–containing wastewater: decolorization and destruction of Orange II azo dye in dilute solution. Dyes Pigments 76, 656–662. [ Links ]
Santos A., Yustos P., Quintanilla A., Rodríguez S. y García Ochoa F. (2002). Route of the catalytic oxidation of phenol in aqueous phase. Appl. Catal. B: Environ. 39; 97–113. [ Links ]
Shaojing B., Zhengguo J., Xiaoxin L., Haiyan D. y Zhijie C. (2004). Preparation and formation mechanism of porous TiO2 films using PEG and alcohol solvent as double templates. J. Sol–gel Sci. Techn. 30, 239–248. [ Links ]
Tasbihi M., Ngah C.R., Aziz N., Mansor A., Abdullah A.Z., Teong L.K. y Mohamed A.R. (2007). Lifetime and regeneration studies of various supported TiO2 photocatalysts for the degradation of phenol under UV–C light in a batch reactor. Ind. Eng. Chem. Res. 46, 9006–9014. [ Links ]
Vohra M.S. y Tanaka K. (2003). Photocatalytic degradation of aqueous pollutants using silica–modified TiO2. Water Res. 37, 3992–3996. [ Links ]
Waldner G. y Krysa J. (2005). Photocurrents and degradation rates on particulate TiO2 layers. Effect of layer thickness, concentration of oxidizable substance and illumination direction. Electrochim. Acta 50, 4498–4504. [ Links ]
Zhou X.F., Chu D.B., Wang S.W., Lin C.J. y Tian Z.Q. (2002). New route to prepare nanocrystalline TiO2 and its reaction mechanism. Mater. Res. Bull. 37, 1851–1857. [ Links ]
Zoppi R. A, Trasferetti B.C. y Davanzo C.U. (2003). Sol–gel titanium dioxide thin films on platinum substrates: preparation and characterization. J. Electroanal. Chem 544, 47–57. [ Links ]
]]>