Masas relativas y el mol. Una demostración simple de un concepto difícil
Relative masses and mole, a simple demonstration of a difficult concept
Armando Marín-Becerra y Rafael Moreno-Esparza*
* Departamento de Química Inorgánica, Facultad de Química. Universidad Nacional Autónoma de México. Ciudad Universitaria, 04360, México, DF. Correos electrónicos: amarin@unam.mx; moresp@unam.mx
]]>Fecha de recepción: 22 de septiembre 2009.
Fecha de aceptación: 4 de enero 2010.
Resumen
Un mol como unidad de la cantidad de sustancia la masa molar y la masa atómica, así como la relación que guardan con el número de Avogadro son, en general, conceptos que a los estudiantes les resultan difíciles de asimilar. Con el empleo de una balanza de dos brazos y una analogía simple es fácil de demostrar que 12 g de carbono necesariamente contienen el mismo número de átomos que los que hay en 1 g de hidrógeno, sin necesidad de saber cuántos átomos son ésos.
Abstract
Amount of substance, molecular and molar mass and their relation with Avogadro's number are concepts that students often find difficult to understand. Using a two–plate balance and a simple analogy, it is easy to demonstrate that one gram of hydrogen contains the same number of atoms as those contained in twelve grams of carbon, without needing to know the actual quantity of the atoms involved.
Keywords: first–year undergraduate; general chemistry; demonstrations; analogies; constructivism.
]]>Introducción
Un mol —como unidad de la cantidad de sustancia— la masa molar y la masa atómica, así como la relación que guardan con el número de Avogadro son, en general, conceptos que a res han documentado la dificultad y confusión que existe entre ellos, así como las diferentes estrategias usadas para su enseñanza (Case, 1999; Furió et al., 1999; 2000; 2002; 2006; Garritz et al., 2002; Padilla et al., 2008).
La forma en que los profesores abordamos estos temas sin duda no ayuda a esclarecer la gran diferencia que existe entre estos diferentes conceptos.
El vínculo, al parecer inseparable, entre el concepto de mol y el número de Avogadro se refleja en muchas de las publicaciones que han abordado el tema, pues en general el concepto mero de Avogadro (Bindel, 1992; 2002; Goh, Subramaniam y Chia, 1994; Solomon y Chinhyu, 1993; Kruglak, 1988; Boyko y Blliveau, 1986; Feinstein y Sisson, 1982; Seiglie, 2003; Singh, Pike, Szafran, Davis, y Leone, 1995; Széll, Dannis, Jouas y Wong, 1980) o presentando analogías que ilustran lo enorme de este número, empleando para ello objetos macroscópicos tales como chocolates, monedas, granos de arena, etc. (Uthe, 2002; Diemente, 1998; Johns, 1993; Hoyt, 1992; van Lubeck, 1989; Poskozim, Wazorick, Tiempetpaisal y Poskozim, 1986; Todd, 1985; Fulkrod, 1981).
Pensamos que estas comparaciones sólo consiguen ilustrar que los átomos son entidades extraordinariamente pequeñas, un concepto que probablemente ya la mayoría de los estudiantes entiende. Sin embargo, en general se hace poco énfasis en el concepto central que subyace: la cantidad de sustancia1 y su unidad, el mol.
El objetivo del presente trabajo es presentar una analogía que permite ilustrar el concepto de mol sin la necesidad de conocer la magnitud del número de Avogadro.
Es nuestro parecer que demostrar que 12g de carbono necesariamente contienen el mismo número de átomos que los que hay en 1 g de hidrógeno, es un hecho mucho más importante que saber cuántos átomos son ésos.
Hoy en día las siguientes dos oraciones parecen equivalentes:
]]> — 1 g de hidrógeno contiene un mol de átomos de hidrógeno.— 1 g de hidrogeno contiene 6.02×1023 átomos de hidrógeno.
Sin embargo, históricamente la química avanzó empleando las consecuencias de la primera oración, sin necesidad de conocer la segunda.
Una vez que fueron establecidas con cierta precisión un conjunto de masas atómicas relativas, la composición másica porcentual de las sustancias puede ser traducida a las fórmulas químicas correspondientes y fue con la ayuda de éstas que D. Mendeleev construyó su tabla periódica.
Así, es sin duda la hipótesis de Avogadro, y no el número de Avogadro, una de las aportaciones más importantes a la química moderna, pues con base en ella fue posible generar un conjunto confiable de masas atómicas relativas.
De esta manera, la pregunta que debemos resolver no es: ¿cuántos átomos tiene 1g de hidrógeno? sino ¿cómo podemos estar seguros que éstos son los mismos que los contenidos en 12g de carbono?
Afortunadamente esta pregunta puede demostrarse fácilmente tanto en el laboratorio como en el salón de clase. La analogía que se desarrolla a continuación nos permitirá ilustrar cómo, una vez establecida una escala de masas relativas, el concepto de mol queda implícito al expresar esta masa relativa en una unidad de masa distinta.
La analogía
En el salón de clase: La idea central es pedirle a los alumnos se imaginen que trabajan en un taller, en el cual cuentan con una balanza de dos platos, así como con una variedad de objetos como clavos, tornillos, tuercas y rondanas, tales que todos los elementos dentro de cada uno de estos grupos de objetos sean iguales, en particular que tengan la misma masa, pero diferente de aquella de los elementos de otro grupo; es decir, todos los tornillos tienen la misma masa, pero la de un tornillo es diferente que la de una tuerca, que es a su vez diferente de la de un clavo, etc.
]]>Descripción de la estrategia
Empleando la balanza de dos platos, es posible establecer la masa relativa de los objetos en el taller con el siguiente procedimiento:
• Primero debemos decidir cuál de los objetos habremos de emplear como estándar. En nuestro experimento imaginario usaremos al objeto de menor masa como nuestra unidad de medida —es importante mencionar que no importa cuál objeto se seleccione como estándar, los resultados serán equivalentes, pero a fin de mantener la analogía lo más cercana a la tabla periódica es conveniente usar aquel que se considere como el de menor masa.
• Nuestro experimento imaginario requiere que en uno de los platos de la balanza se coloque un puñado de tuercas mientras que en el otro se coloquen tantos clavos como sean necesarios para equilibrar la balanza. Dado que la masa de una tuerca es diferente de la de un clavo, el número de objetos en cada plato de la balanza necesariamente es distinto.
• Una vez hecho lo anterior, se pide a los alumnos que sugieran el número de objetos que hay en cada plato de la balanza. Los alumnos propondrán números como: 38 tuercas se equilibran con 175 clavos, 60 tornillos se equilibran con 1 530 clavos, etc.
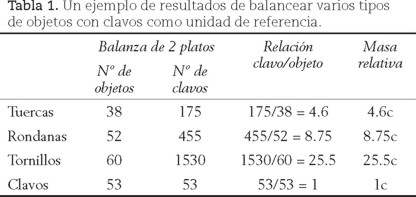
• Una vez establecidos estos números se podrán calcular las masas relativas de todos los objetos del taller, por ejemplo: 175 clavos / 38 tuercas = 4.6 clavos / 1 tuerca; es decir, que la masa de una tuerca equivale a la de 4.6 clavos o lo que es lo mismo la masa de 1 tuerca es de 4.6 "clavones" o 4.6 c (donde esta unidad de masa: "clavón" la abreviamos como "c"). Un ejemplo de resultados se ilustra en la tabla 1.

25.5 c + 3(8.75) + 4.6 c = 56.35 c
Una vez establecida la masa relativa de los objetos de estudio (en este ejemplo: 1 clavo = 1c, 1 tornillo = 25.5 c y 1 tuerca = 4.6 c) se les pide a los alumnos que calculen el número de objetos contenidos en cada uno de los siguientes lotes:
• 1 kg de clavos.
• 4.6 kg de tuercas.
• 25.5 kg de tornillos.
• 8.75 kg de rondanas.
• 56.35 kg de ensamblajes o arreglos (cada uno de ellos formado por un tornillo, tres rondanas y una tuerca).
Los alumnos rápidamente advierten que es imposible realizar este cálculo si no se conoce la masa de un clavo.
]]> Se les pide entonces que formen equipos de tres o cuatro a los que se les sugiere que estimen la masa en gramos (o miligramos) de un clavo y con ella calculen la cantidad de objetos contenidos en las cantidades indicadas anteriormente.Cuando cada equipo anota sus resultados en el pizarrón es claro que independientemente de la masa que cada equipo haya asignado al clavo, la cantidad de tuercas contenidas en 4.6 kg de éstas es la misma cantidad que los tornillos contenidos en 25.5 kg de éstos. En la tabla 2 se ejemplifican los resultados.

Claramente el número de objetos es constante en cada equipo, pero diferente del obtenido por los otros equipos, pues depende de la masa que cada uno de ellos haya asignado al clavo. Además, puede notarse que entre menor sea la masa asignada al clavo de referencia, la cantidad de objetos calculados por cada equipo será mayor —si la masa del clavo es de 1 g,56.35 kg de ensamblajes contienen 1×103 de éstos, mientras que si la masa asignada al clavo es de 1.5 mg, 56.35 kg de ensamblajes contienen 6.66 × 105 de estos arreglos.
Al final de esta demostración debe hacerse énfasis en que este mismo principio se puede aplicar a la masa de los átomos y que, una vez que se determina la masa relativa de los mismos —esto es: la masa atómica; p. ej. H = 1 uma, C = 12.01 uma y Cl = 35.45 uma— podemos estar seguros que la cantidad de átomos de hidrógeno contenidos en 1 g de esta sustancia son los mismos que los átomos de carbono contenidos en 12 g de carbono, así como los átomos de cloro contenidos en 35.45 g de esta sustancia, sin necesidad de saber cuántos son.
En este punto conviene hacer patente que esta cantidad "indeterminada" pero fija de átomos es lo que llamamos número de átomos por mol, por lo que 35.45 g de cloro representa la masa de un mol de átomos de cloro o lo que es lo mismo, es la masa molar del cloro —expresada como g/mol o "gramos por cada mol".
Los alumnos podrán extrapolar fácilmente que, dado que la masa de los átomos es extremadamente pequeña —pues 1 uma es una cantidad muy pequeña de masa expresada en gramos— la cantidad de átomos que contiene un mol debe ser enorme.
La ventaja de esta analogía es que es muy fácil llevarla a cabo también en el laboratorio, empleando preferentemente una balanza de dos platos, además de una balanza común y el mismo tipo de objetos mencionados, lo más pequeños posible. Este tipo de objetos tienen algunas ventajas sobre el uso de, por ejemplo, semillas (Garritz et al., 2002), pues el hecho de ser manufacturados por máquinas les confiere una masa muy regular, además de que con ellos es posible construir ensamblajes —en clara analogía a las moléculas.
Las masas relativas se determinan con el mismo procedimiento descrito con anterioridad, colocando un puñado de tuercas en un plato y equilibrando la balanza con el elemento seleccionado como estándar.
]]> Es cierto que pueden establecerse las masas relativas empleando una balanza analítica en lugar de una de dos platos; sin embargo, esto no es muy recomendable pues el estándar que emplea la balanza analítica, "el gramo", no pertenece al conjunto de elementos en estudio (tuercas, tornillos, rondanas, etc.). Usar una balanza de dos platos permite mantener la analogía lo más cercana posible a los átomos, cuyas masas relativas fueron originalmente establecidas usando como estándar al más ligero de los elementos del conjunto: al átomo de hidrógeno.Una vez establecidas las masas relativas se solicita a los alumnos midan, empleando la balanza común, la cantidad correspondiente en onzas de cada uno de los objetos estudiados para después contar los objetos que este lote contiene. Por ejemplo, si la tuerca tiene una masa de 5.7 c (c = "clavones"), deben medir la cantidad más cercana posible a 5.7 onzas de tuercas en la balanza y luego contar cuántas tuercas están contenidas en este lote (como 1 onza = 28.35 gramos, al medir 5.7 onzas de tuercas los alumnos deben medir 161.595 gramos). El usar onzas en lugar de gramos tiene dos propósitos, el primero es que el número de objetos contenidos en cada lote sea el mayor posible y el segundo demostrar que este método funciona independientemente del estándar de masa empleado (gramos, onzas, libras o kilogramos). Si se desea puede repetirse el procedimiento empleando ahora el gramo como estándar de masa en lugar de la onza y corroborar esas afirmaciones.
Después de esta demostración debería quedar claro que el numero de objetos contenidos en un mol (6.02 × 1023), no es un número mágico, sino una consecuencia de que en el sistema internacional de unidades la unidad de masa es el kilogramo y que el número de Avogadro sería distinto si en lugar de gramos usáramos onzas como estándar de medida —en este caso 1 mol sería la cantidad de átomos contenida en 12 onzas de 12C, donde claramente el concepto de mol es invariante pero el número de Avogadro depende del estándar de masa empleado.
Esta demostración en el laboratorio funciona muy bien si los objetos estudiados tienen masas menores que 1 g y la masa del estándar empleado es de alrededor de 1/10 de la de los objetos estudiados.
Sólo queda una pregunta por resolver: en estas demostraciones podemos establecer fácilmente las masas relativas de los objetos en estudio debido a que podemos contarlos con facilidad. Entonces, ¿cómo podemos establecer la masa relativa de los átomos si no podemos contarlos?
Es por esto que la hipótesis de Avogadro es tan importante: si un litro del gas hidrógeno contiene el mismo número de partículas que un litro de gas cloro (ambos bajo las mismas condiciones de temperatura y presión), aun sin saber cuántas partículas están contenidas en estas muestras, la relación de las masas que es posible medir en ellas es igual a la relación de las masas que deben presentar las partículas que los forman, y sabiendo que tanto las partículas del cloro gaseoso como las del hidrógeno gaseoso están constituidas cada una por dos átomos —esto es: ambas sustancias forman moléculas diatómicas— esta relación se extiende hasta los átomos:

O lo que es lo mismo: la masa de un átomo de cloro es 35.45 veces la masa de un átomo de hidrógeno.
Conclusiones
]]> Creemos que la presente analogía ilustra convenientemente el concepto de mol, y que realizar las actividades propuestas permite a los estudiantes asimilar más fácilmente este concepto. Adicionalmente, esta analogía permite ilustrar que el número de Avogadro es una consecuencia del estándar de masa del Sistema Internacional de Unidades y no un número "mágico".Por último, vale la pena mencionar que la presente analogía emplea implícitamente la definición de átomo enunciada por John Dalton en donde la masa de todos los átomos de un elemento es la misma —no se contempla la existencia de isótopos. Sin embargo, si así se desea, puede modificarse la metodología a fin de incluir la existencia de "isótopos", añadiendo objetos similares pero de masa distinta, aunque de proporciones bien definidas —por ejemplo añadiendo 30% de tornillos grandes y 70% de pequeños, etc. Sin embargo en ese caso, a pesar de que el modelo es más cercano a la realidad, éste pierde algo de la simplicidad en el manejo de los números.
Referencias
Bindel, T. H., Avogadro's number: Surprise!, Journal of Chemical Education, 69, 305-306, 1992. [ Links ]
Bindel, T. H., Crystal models made from clear plastic boxes and their use in determining Avogadro's number, Journal of Chemical Education, 79, 468-472, 2002. [ Links ]
Boyko, E.R.; Blliveau, J. F., Surface tension and Avogadro's number, Journal of Chemical Education, 63, 671-672, 1986. [ Links ]
]]>Case, J. M. y Fraser, D. M., An investigation into chemical engineering students' understanding of the mole and the use of concrete activities to promote conceptual change, International Journal of Science Education, 21(12), 1237-1249, 1999. [ Links ]
Diemente, D., Demonstrations of the enormity of the Avogadro's number, Journal of Chemical Education, 75, 1565-1566, 1998. [ Links ]
Feinstein, H. I.; Sisson, R. F., The Estimation of Avogadro's number using cetyl alcohol as the monolayer, Journal of Chemical Education, 59, 751, 1982. [ Links ]
Fulkrod, J. E. How big is Avogadro's number (or how small are atoms, molecules, and ions), Journal of Chemical Education, 58, 508, 1981. [ Links ]
Furió, C., Azcona, R. y Guisasola, J., Dificultades conceptuales y epistemológicas del profesorado en la enseñanza de los conceptos de cantidad de sustancia y de mol, Enseñanza de las Ciencias, 17(3), 359-376, 1999. [ Links ]
]]>Furió, C.; Azcona, R.; Guisasola, J. y Ratcliffe, M., Difficulties in teaching the concepts of 'amount of substance' and 'mole', International Journal of Science Education, 22(12), 1285-1304, 2000. [ Links ]
Furió, C., Azcona, R., Guisasola, J., Revisión de investigaciones sobre la enseñanza–aprendizaje de los conceptos cantidad de sustancia y mol, Enseñanza de las Ciencias, 20(2), 229-242, 2002. [ Links ]
Furio,C., Azcona, R., Guisasola, J., Enseñanza de los conceptos de cantidad de sustancia y de mol basada en un modelo de aprendizaje como investigación orientada, Enseñanza de las Ciencias, 24(1), 43-58, 2006. [ Links ]
Garritz, A., Gasque, L., Hernandez, G. y Martínez, A.M., El mol: un concepto evasivo. Una estrategia didáctica para enseñarlo, Alambique 33, 99-109, 2002. [ Links ]
Goh, N. K.; Subramaniam, R.; Chia, L. S., A More Direct Feeling for Avogadro's number Journal of Chemical Education, 71, 656-657, 1994. [ Links ]
]]>Hoyt, W.,A mole of salt crystals–Or,How big is the Avogadro's number?, Journal of Chemical Education, 69, 496, 1992. [ Links ]
Johns, P., Demonstrating the magnitude of Avogadro's number, Journal of Chemical Education, 70, 774-775, 1993. [ Links ]
Kruglak, H., Brownian movement and Avogadro's number: A biophysical chemistry experiment, Journal of Chemical Education, 65,732–734, 1988. [ Links ]
Padilla, K.; PoncedeLeón, A. M.; Rembado, F. M. y Garritz A., Undergraduate Professors' Pedagogical Content Knowledge: The case of 'amount of substance', Journal of Science Education, 30(10), 1389-1404, 2008. [ Links ]
Poskozim, P. S.; Wazorick, J. W.; Tiempetpaisal, P.; Poskozim, J. A., Analogies for Avogadro's number Journal of Chemical Education, 63, 125-126, 1986. [ Links ]
]]>Seiglie, C. A., Determination of Avogadro's number by improving electroplating, Journal of Chemical Education, 80, 668-669, 2003. [ Links ]
Singh, M., M.; Pike, R. M.; Szafran, Z.; Davis, J. D.; Leone, S. A., Microscale electrolysis: synthesis of iodoform, its characterization, Faraday's Laws, and Avogadro's number, Journal of Chemical Education, 72, A4-A6, 1995. [ Links ]
Solomon, S.; Chinhyu, H., Measuring Avogadro's number on the overhead projector, Journal of Chemical Education, 70, 252-253, 1993. [ Links ]
Széll, T.; Dannis, D.; Jouas, J. P.; Wong, M., An approximate determination of Avogadro's constant, Journal of Chemical Education, 57, 735-736, 1980. [ Links ]
Todd, D., Five Avogadro's number problems, Journal of Chemical Education, 62, 76, 1985. [ Links ]
]]>Uthe, R. E., For mole problems, call Avogadro: 602-1023, Journal of Chemical Education, 79, 12-13, 2002. [ Links ]
van Lubeck, H., How to visualize Avogadro's number, Journal of Chemical Education, 66, 762, 1989. [ Links ]
1 Ésta es una de las siete magnitudes fundamentales del SI y se le ha dado muy poco énfasis en los textos de química. Cada vez que citemos "el mol" en este artículo hay que tener presente que detrás está la magnitud "cantidad de sustancia".
]]>