La melatonina induce la síntesis y liberación de las encefalinas en el cerebro de la rata
Melatonin induces enkephalins synthesis and release in the rat brain
Miguel Asai1*, Marcela Valdés–Tovar1, Gilberto Matamoros–Trejo1, David García1
1 Laboratorio de Análisis Químicos. División de Investigaciones en Neurociencias. Instituto Nacional de Psiquiatría Ramón de la Fuente Muñiz.
]]> *Correspondencia:
Recibido primera versión: 6 de noviembre de 2008.
Segunda versión: 1° de octubre de 2009.
Aceptado: 16 de octubre de 2009.
Abstract
Since enkephalins discovery in 1975, several opioid peptides have been included in neuroscience research. Enkephalins have been involved in the homeostasis maintenance of the organism, mostly with cellular and molecular mechanisms implicated in antinociception and narcotic responses. Moreover, enkephalins have been shown to be involved in the control of stress, regulation of cardiovascular functions, modulating primary immune responses, in addition to cellular differentiation processes. As opioid peptides appear to modulate several bioactivities and physiological responses in organisms, this posits that several modifications should occur during their synthesis, cell release, and receptor binding in target cells.
At present, it has been demonstrated that the endogenous opioid system (EOS), displays a circadian rhythm, in which its tissue content, presynaptic release, and receptor's number reaches its maximal concentration during the dark phase (24:00h) and the minimal during the early morning (05:00 h). Recently, our group reported that functional pinealectomy disrupts the enkephalin circadian rhythm and significantly reduces the tissue content of opioid peptides in the rat brain. However, the effect was shown to be specific to the hour along the 24h daytime. There were no significant changes during the light period, only during the dark period (01:00h), when the enkephalin tissue content decreased in the experimental group. The effect was reverted when pinealectomized rats were injected with single doses of melatonin (MEL) (150µg/kg i.p.). If the lack of melatonin in the rat brain significantly reduced the enkephalin tissue content, and its exogenous administration re–established the enkephalin tissue levels, it is possible that the hormone is involved in the enkephalin synthesis. In this paper we provide further evidence that supports the relation between melatonin and opioid peptides synthesis and release. In addition, we studied the effect of darkness and melatonin administration in enkephalin tissue levels. Finally, we analyzed the luzindole effect as a melatonin receptor antagonist in the pinealectomized rat brain.
Material and methods
]]> Subjects: Male Wistar rats were housed in a light and temperature controlled room. Water and pellet food were available ad libitum. This group was subdivided in: 1. Functional pinealectomy group (FP). Rats were housed individually during 15 days in a room with continuous light (<50lux). 2. FP rats were housed in a dark room during four or six hours. 3. FP rats were injected with melatonin (150, 300, 600µg/kg s.c.). 4. FP rats were injected with Luzindole (187.5, 375, 750µg/kg i.p.). After 30 min, the animals were injected with melatonin (150µg/kg). 5. FP rats were injected with melatonin (800µg/ kg) and subjected to the in vitro release processes. The rats were sacrificed by decapitation and the blood collected for melatonin serum determination. The brains were removed and processed for an analytical preparative procedure for the enkephalin determination by radioimmunoassay technique. The in vitro release methodology was performed as follows: tissue samples were homogenized by applying 8 strokes with a Thomas grinder system. The homogenates were centrifuged at 4,000rpm, 4°C during 10 min. Supernatants were recovered and centrifuged at 12,000rpm at 4°C for 20 min. Supernatants were discarded and pellets were resuspended in the homogeneization buffer (1:9 w/v). Samples were placed on top of a Percoll gradient density (23%, 15%, and 10%) and centrifuged at 20,000 rpm at 4°C for 25min. The synaptosomal enriched fraction (15–23%) was obtained and diluted in 1mL of Krebs buffer (mM: NaCl 119, KCl 4.6, CaCl2·2H2O 1.25, KH2PO4 0.85 MgSO4 0.84, NaHCO3 24.8, sucrose 10). Buffer was gasified with a mixture of C02 95% and O2 5%, pH 7.4. 800µL aliquots were placed into plastic chambers.After 20 min of stabilization with Krebs buffer, three different superfusates were collected: 1. basal, 2. potassium [50mM], and 3. post–stimulus (Krebs buffer without potassium). Samples were collected into HCl 0.1N, boiled and subsequently loaded into Amberlite XAD–2 columns (8 × 0.7cm) for solid–phase peptide extraction. The flow rate was held constant at 0.5 mL min–1 and elution of the whole peptide fraction was carried out using a continuous gradient with absolute methanol. Eluted samples were lyophilized and resuspended in 2mL of distilled water and finally stored at –20°C for further quantification of IR–Enkephalin using standard radioimmunoassay procedures.
The results showed that functional pinealectomy reduced the opioid tissue content in the different brain structures assayed. The lack of melatonin significantly decreased the enkephalin tissue content when compared to the control group. However, tissue levels of enkephalin material were completely restored after four and six hours of administration of different doses of exogenous melatonin administration to the rats.
As continuous light decreases the melatonin content in the brain, darkness should be able to counteract the aforementioned effect. Our results showed that tissue levels of enkephalin material were increased over 200% and 300%, after exposing animals to a four or six–hour period of darkness, when compared to animals exposed to continuous light. Luzindole was used to abolish any melatonin activity via activation of its membrane brain receptors. Our experiments showed that different doses of the antagonist were not able to obliterate the increased content of opioid peptides induced with melatonin administration in the tested brain tissues.
Finally, enkephalin release showed a significant decrease in pinealectomized rats, showing a complete restoration of released peptide levels as shown by control group, after hormone administration. Thus, melatonin appears to counteract the neuronal decrease of the releasable pool of opioid peptide within the nerve terminals, reaching the released rate values detected in the control group.
Our results suggest four relevant features: 1. Functional pinealectomy induces a significant decrease in the tissue content of opioid peptide material that seems to correlate with a decrease in the presynaptic release of enkephalins. 2. Darkness and MEL administration counteracted the light induced effects, namely the decreased content of opioid peptide material in tissue and the reduced peptide release from nerve terminals. 3. Nonetheless, the presence of luzindole was not able to inhibit the synthesis of opioid peptides. Melatonin is a hormone that synchronizes cell activity with photoperiod. Beyond this physiological property, MEL has been related to neuropeptide synthesis. Previous reports have shown that surgical or functional pinealectomy reduces the Met–Enkephalin tissue content in the rat brain. Also, it has been demonstrated that MEL stimulates the Proopiomelanocortin (POMC) gene expression in the immune system.
In this paper, we showed further evidence that melatonin participates in the biosynthetic regulation of opioid peptides. Dark stimulation after continuous light exposure on rats produced an increase of tissue content of enkephalin above 300%, when compared with tested animals subjected to functional pinealectomy. Similar results were obtained with the exogenous melatonin administration. These evidences support the hypothesis that hormone treatment may be able to interact with protein kinase C (in the active–state of the enzyme). In addition, the hormone could modulate the cellular responses of several transcription factors (c–Fos, c–Jun, AP–1) responsible for the enkephalin gene expression. On the other hand, rats exposed to MEL–receptor antagonist luzindole, injected before MEL administration, showed that the tissue content of opioid peptide was not totally abolished by the melatonin antagonist. It has been proposed that melatonin not only interacts with its membrane receptor, but it is able to cross the cytoplasmic membrane and interact directly with the intracellular signal transduction system via the biomolecules that operate within.
In conclusion, the physiology of melatonin appears to control the synthesis and presynaptic release of the endogenous opioid system in the rat brain.
Key words: Melatonin, opioid peptides, synthesis, release.
]]> Resumen
En la actualidad se reconoce que el Sistema Endógeno Opioide (SEO) participa en la regulación y control de la homeostasis; por lo tanto se requiere que los procesos bioquímicos que dan lugar a su síntesis, liberación y unión a receptores se encuentren reguladas de manera endocrina. Diversas líneas de investigación han demostrado que la concentración y liberación presináptica de las encefalinas no permanece constante durante un ciclo de 24 horas. Por el contrario, su síntesis y liberación alcanzan su máxima concentración durante la fase de oscuridad y la mínima durante las primeras horas de la mañana. Recientemente, nuestro grupo de trabajo ha demostrado que la ausencia de melatonina (MEL), por efecto de la pinealectomía funcional, rompe el ritmo circádico y reduce significativamente la concentración de las encefalinas durante la fase de oscuridad. Si la ausencia de la hormona abate la concentración de opioides, es factible que la MEL se encuentre involucrada en la síntesis de las encefalinas. En el presente trabajo se muestran los resultados del efecto de la pinealectomía funcional sobre la concentración tisular y la liberación de los opioides, así como el efecto de la administración exógena de MEL y de su antagonista el luzindol (LZ).
Diseño experimental
Control Naive. Se utilizaron ratas macho de la cepa Wistar (200–250g), que permanecieron en un cuarto con un ciclo de luz y oscuridad controlada. La fase de luz duró 12 horas y comenzó a las 06:00h. A su vez, este grupo fue subdividido en: 1. Luz Continua (LC): Para abatir la concentración sérica de la hormona, se usó el modelo experimental conocido como pinealectomía funcional. 2. Luz Continua + Oscuridad: La luz abate la concentración de MEL y la exposición a la oscuridad revierte dicho efecto. Un grupo de ratas sometido a la luz continua se colocó en un cuarto con oscuridad durante cuatro y seis horas. 3. Luz continua+melatonina: Para analizar el efecto de la MEL sobre el contenido tisular de opioides, se administró una dosis de MEL (150, 300 y 600µg/Kg s.c.). 4. Luz continua+luzindol (LZ)+MEL: Si la melatonina ejerce su mecanismo de acción al unirse a sus receptores presentes en la membrana plasmática, entonces su efecto podría ser revertido por la presencia del LZ. Por lo tanto, a tres grupos de ratas sometidas a la pinealectomía funcional se les inyectó con LZ a una dosis de 187.5, 375, 750 µg/kg. s.c. Después de transcurridos 30min., los animales fueron inyectados con MEL (150µg/kg. s.c.). 5. Liberación: Se utilizaron tres grupos de ratas: a) control, b) luz continua y c) luz continua+MEL (800µg/kg. s.c.). Post mortem la amígdala fue sometida al proceso preparativo para la obtención de los sinaptosomas.
Resultados
Los resultados obtenidos en el presente trabajo nos muestran que la pinealectomía funcional reduce significativamente la concentración de encefalinas en todas las estructuras cerebrales analizadas. Sin embargo, el efecto es revertido tanto por la administración exógena de MEL, como por la exposición a la oscuridad. Las diferentes dosis administradas del LZ bloquearon parcialmente el efecto estimulante de la MEL sobre la síntesis de los opioides. Por último, la pinealectomía funcional redujo significativamente la liberación presináptica de encefalinas, misma que se pudo reestablecer con la administración exógena de la hormona.
Discusión
Las evidencias experimentales del presente trabajo sugieren que la MEL se encuentra relacionada con la síntesis y la liberación de las encefalinas. Por un lado, la pinealectomía funcional redujo significativamente el contenido tisular de encefalinas, pero el efecto fue revertido tanto con la administración exógena de la hormona como con la exposición a la oscuridad. La administración del LZ sólo fue capaz de bloquear parcialmente el efecto estimulante de la MEL sobre la síntesis de encefalinas. El efecto de la MEL sobre la liberación de opioides pone de manifiesto la relación funcional entre ambos sistemas. A menor cantidad de opioides por efecto de la pinealectomía, menor liberación presináptica y por el contrario, una vez administrada la hormona los valores de la síntesis–liberación se restablecen.
Conclusión
La MEL puede estar involucrada en la síntesis y la liberación de los péptidos opioides.
]]> Palabras clave: Melatonina, encefalinas, síntesis, liberación.
INTRODUCCIÓN
Las encefalinas fueron descubiertas en 1975 por el grupo de John Hughes. Estos investigadores aislaron y purificaron del cerebro del ganado porcino, dos pentapéptidos que mimetizaban in vitro la acción de la morfina.1 Su secuencia [NH2–Tyr1–Gly2–Gly3–Phe4–Met5–COOH] y [NH2–Tyr1–Gly2–Gly3–Phe4–Leu5–COOH] mostró que sólo diferían de un aminoácido en su porción carboxilo terminal, por ello fueron llamados metionina y leucina–encefalina, respectivamente. La relevancia fisiológica de este hallazgo no se hizo esperar porque gracias a estos péptidos se podían comenzar a estudiar, a nivel bioquímico, los mecanismos de acción de los narcóticos y las vías del dolor. Por otro lado, por primera vez se descubrió que un neurotransmisor podía ser de naturaleza peptídica y tener sus propias características de almacenamiento, transporte y secreción, propiedades que les permitieron incorporarse a los mecanismos moleculares que constituyen la transmisión sináptica.2 En poco tiempo fueron purificados, identificados y caracterizados un gran número de péptidos opioides.3 En la actualidad al conjunto de los péptidos opioides se le conoce como Sistema Endógeno Opioide (SEO).
Debido a la extensa distribución anatómica y subcelular de las encefalinas y la de sus receptores, la fisiología del SEO se ha relacionado con la secreción hipofisiaria e hipotalámica de varios neurotransmisores4,5 en los sistemas neurales involucrados en las respuestas somáticas a los estímulos dolorosos,6 en las vías del dolor,7 en la proliferación celular,8 en el control cardiovascular,9 con el estrés10 y en el sistema inmune.11–13 Si el SEO participa en el control de la homeostasis, los mecanismos bioquímicos que regulan su síntesis y liberación deben de estar sujetos a un refinado control endógeno a fin de proveer al organismo de la concentración basal necesaria para que los péptidos opioides ejerzan su función a lo largo del día. Diversas evidencias experimentales han demostrado que el contenido de los péptidos opioides no permanece constante en un ciclo de 24 horas. Por el contrario, su contenido tisular14 y su liberación15 alcanzan su concentración máxima durante la fase de oscuridad (24:00h) y la mínima durante las primeras horas de la mañana (05:00h), lo que pone de manifiesto que el SEO posee un ritmo circádico bien establecido. Sin embargo, son desconocidos los mecanismos que regulan el control de dicho ritmo.
En la actualidad se reconoce la participación de la melatonina (MEL) en la integración de la información del fotoperiodo con la actividad celular. Esta hormona, sintetizada principalmente en la glándula pineal, es la responsable de controlar el ritmo circádico de las hormonas, enzimas y neurotransmisores.16,17 Aunado a esta propiedad, se ha demostrado que la MEL tiene diversas funciones en el organismo entre las que destacan la de ser un eficiente captador de radicales libres,18 la de mantener la integridad funcional del citoesqueleto,19 ser un agente oncostático20 y estimular la respuesta inmune primaria.11,12
Recientemente, nuestro grupo de trabajo demostró que la pinealectomía funcional rompe el ritmo circádico de los opioides y reduce significativamente su contenido tisular.21 Si la ausencia de MEL abate la concentración de las encefalinas presente en el tejido nervioso, es posible que se encuentre involucrada con la síntesis y liberación de las encefalinas. Por lo tanto el objetivo del presente trabajo fue el de estudiar si la ausencia y presencia de la MEL, modifica el contenido tisular y la liberación presináptica de encefalinas en el Sistema Nervioso Central (SNC) de la rata.
MATERIAL Y MÉTODOS
Diseño experimental
]]> Sujetos1. Control Naive. Se utilizaron ratas macho de la cepa Wistar (200–250 g), que permanecieron en un cuarto con un ciclo de luz y oscuridad controlada. La fase de luz duró 12 horas y comenzó a las 06:00 h. La temperatura promedio del cuarto fue de 21±1°C. El alimento y el agua fueron administrados ad libitum. A su vez este grupo fue subdividido en:
a) Luz continua (LC). Para abatir la concentración sérica de la hormona, se usó el modelo experimental conocido como pinealectomía funcional.18 Este método se basa en la propiedad que tiene la luz de inhibir la actividad de la enzima N–acetiltransferasa involucrada en la síntesis de la hormona. Para conseguir dicho efecto se requiere colocar a los animales en un cuarto con luz continua durante 15 días. Para evitar el estrés producido por la presencia constante de la luz, la intensidad de la misma fue <50 lux.
b) Luz continua+oscuridad. Si la luz continua abate la concentración de MEL, la oscuridad revierte dicho efecto. Por lo tanto, un grupo de ratas sometido a la luz continua se colocó en un cuarto con oscuridad durante cuatro y seis horas (tiempo necesario para dar lugar a la síntesis de novo de los opioides). En el interior del cuarto la manipulación y sacrificio de los animales se llevó a cabo con luz roja.
c) Luz continua+MEL: Para analizar el efecto de la MEL sobre el contenido tisular de opioides, a un grupo de ratas sometidas a la luz continua se le inyectó una dosis única de MEL en las siguientes concentraciones: 150, 300 y 600µg/kg. s.c. Después de la inyección, los animales permanecieron en el cuarto de luz continua las siguientes cuatro horas antes de ser sacrificados.
d) Luz continua+luzindol+melatonina: Si la MEL ejerce su mecanismo de acción al unirse a sus receptores presentes en la membrana plasmática, entonces su efecto podría ser revertido por la presencia de su antagonista específico, el LZ. Por lo tanto, tres grupos de ratas sometidas a la luz continua fueron inyectados con luzindol a una dosis de 187.5, 375 y 750µg/kg. s.c. Después de transcurridos 30 min., los animales fueron inyectados con MEL (150µg/kg. s.c.). En forma semejante al inciso C, los animales permanecieron en el cuarto con luz continua durante cuatro horas antes de ser sacrificados.
e) Liberación. Si la MEL modifica la concentración tisular de opioides, es posible que la liberación presináptica de los mismos también se encuentre alterada. Por lo tanto, en este bloque de experimentos utilizamos tres grupos de ratas: a) control naive, b) luz continua y c) luz continua+MEL (800µg/kg. s.c.). Las ratas se sacrificaron y la amígdala basolateral fue disecada y sometida al proceso preparativo para la obtención de la fracción enriquecida de las terminales nerviosas aisladas (sinaptosomas).
Drogas: La MEL (N–acetil–5–metoxitriptamina) y el LZ fueron comprados a Sigma Chemical Co., y el Percoll a AmershamTM Biosciences. La hormona se disolvió en la mínima cantidad de etanol y para alcanzar la concentración deseada se aforó con solución salina isotónica (SSI). El LZ se disolvió en una relación de 1mg/5ml de Dimetil–sulfóxido y se aforó con SSI.
]]> Obtención de la muestra: Los animales se sacrificaron por decapitación, su cerebro fue removido y colocado en SSI a 4°C. La amígdala basolateral, el cuerpo estriado, el hipotálamo y el hipocampo se disecaron de acuerdo a los criterios anatómicos previamente descritos.22,23 Las estructuras se homogeneizaron y centrifugaron a 50,000 × g a 4°C durante 1h. El sobrenadante fue congelado a –20°C hasta el momento de purificar la muestra.Liberación in vitro: La amígdala fue obtenida de acuerdo a la técnica descrita en el inciso anterior. La fracción enriquecida de sinaptosomas se obtuvo de acuerdo a los procedimientos descritos por Nagy y Whittaker.24,25 Una alícuota de la muestra se añadió a la cámara de perfusión en donde se estabilizaron durante 20 minutos en amortiguador Krebs. El estímulo despolarizante fue inducido con la presencia de potasio [55 mM] y se recolectó una alícuota de 10 ml. Posteriormente el potasio fue retirado del medio añadiendo amortiguador Krebs normal. Para evitar la acción de las endopeptidasas las muestras se recolectaron en 1ml de HCL0.1N y se hirvieron en baño María durante 15min.
Purificación de la muestra. Los homogenados provenientes del tejido cerebral y los perfusados se sometieron a un proceso de purificación mediante la cromatografía de adsorción. Las muestras se añadieron a una columna de vidrio que contenía XAD–2®, se lavaron con agua y se eluyó en un gradiente continuo con 20 ml de metanol absoluto. Las muestras fueron evaporadas a sequedad y resuspendidas en 2mL de agua destilada y almacenadas a –20°C.
Determinación de los péptidos opioides
La determinación de los péptidos opioides se llevó a cabo con la técnica del radioinmunoensayo (RIA). El ensayo se realizó por triplicado y se utilizaron anticuerpos obtenidos previamente en nuestro laboratorio. Los cruzamientos y la caracterización de los anticuerpos han sido previamente publicados.8,15 El contenido de los péptidos opioides se reportó como la inmunoreactividad (IR) péptido/mg de proteína.
Determinación de la melatonina en el suero
La cuantificación de la MEL en el suero de la rata se llevó a cabo mediante la técnica de ELISA (estuche comercial Immuno–Biological Laboratories). La reacción enzima–sustrato forma un producto colorido cuya densidad óptica se determinó en un lector de ELISA a una longitud de onda de 405nm.
Determinación de las proteínas
Se empleó la técnica de Lowry,26 utilizando Albúmina Sérica Bovina como sustancia patrón. La sensibilidad del ensayo fue de 5µg a 700nm.
Estadística. La prueba estadística utilizada fue el Análisis de la Varianza de una vía y la prueba post hoc de Tukey. El nivel de significancia aceptada fue p<0.05.
]]>RESULTADOS
Los resultados que se muestran en el cuadro 1 nos indican que en comparación con el grupo control, la pinealectomía funcional redujo significativamente el contenido tisular de IR–MET en todas las estructuras cerebrales analizadas. Las estructuras más afectadas por la pinealectomía fueron el hipotálamo y el hipocampo, en donde la reducción en el contenido del péptido con respecto al grupo control fue mayor a 50% y 70% respectivamente.
La administración de la dosis más baja de MEL (150µg/ kg) tuvo un efecto selectivo en el contenido tisular de MET–Encefalina, ya que sólo fue capaz de revertir el efecto de la pinealectomía en el hipotálamo (p<0.05) y en el hipocampo (p<0.05), pero no en el cuerpo estriado y la amígdala basolateral. La dosis de 300µg/kg produjo un incremento significativo en la concentración de IR–MET en todas las estructuras, excepto en el estriado, en donde, a diferencia de la dosis menor, encontramos una clara tendencia a incrementar el contenido de este péptido. La dosis de 600µg/kg produjo, en todas las estructuras cerebrales, un incremento significativo en el contenido tisular de la encefalina comparado con el grupo pinealectomizado. Incluso, en el hipotálamo no sólo rebasó el valor en los animales sometidos a la luz continua sino que fue mayor al grupo control. En cuanto a la concentración sérica de la hormona, nuestros resultados nos indican que la pinealectomía funcional redujo significativamente (p<0.05) la concentración de MEL en el organismo al compararlo con el grupo control. En el resto de las mediciones se observa un claro incremento producido por la administración exógena de la MEL.
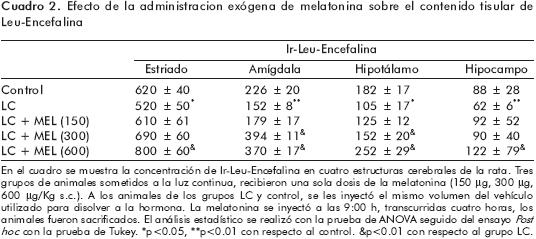
En el cuadro 2 mostramos el efecto de la pinealectomía funcional sobre la concentración tisular de la IR–Leu–Encefalina. Los resultados nos indican que la falta de la hormona redujo (en forma semejante a la Met–Encefalina) el contenido tisular de dicho péptido. La dosis de 150µg/kg de MEL no produjo cambios significativos en ninguna de las estructuras analizadas, aunque sí se observa una tendencia a incrementar su concentración. La dosis de 300µg/kg aumentó de manera significativa el contenido del péptido en la amígdala y el hipotálamo, pero no en el estriado y ni en el hipocampo. Sólo la dosis más alta (600µg/kg) fue capaz de inducir un incremento significativo en todas las estructuras analizadas. Como se mostró para la Met–Encefalina, la estructura del hipotálamo fue la más sensible a los cambios de concentración de la hormona, dando lugar a un incremento mayor al 100% cuando lo comparamos con el grupo pinealectomizado.

El efecto del antagonista específico de la MEL, el luzindol (LZ), se muestra en el cuadro 3. Como se ha descrito en los cuadros 1 y 2 la pinealectomía redujo el contenido tisular de los opioides, pero la administración exógena de MEL no fue capaz de revertir el efecto de la pinealectomía con ninguna de las tres dosis utilizadas del antagonista. De hecho, la concentración de Met–Encefalina posterior a la administración del LZ es menor en el grupo pinealectomizado en estructuras como el cuerpo estriado.


En la figura 1 se muestra la liberación in vitro de encefalinas, a partir de las terminales nerviosas aisladas de la amígdala. Además de medir la liberación de Met–Encefalina se determinó la liberación de otros dos péptidos representativos de la Proencefalina A, el Heptapéptido (Met–Encefalina–Arg6–Phe7) y la porción no opioide de la Proencefalina A, la Synencefalina (SYN). Nuestros resultados muestran que la pinealectomía reduce significativamente (p<0.05) la liberación presináptica de los tres péptidos analizados cuando se comparan con el grupo control. Sin embargo, la administración exógena de MEL (800µg/kg s.c.) revierte el efecto y la liberación tanto de la Met–Encefalina como del Heptapéptido, mostró aumentos significativos (p<0.05) al compararlos con el grupo pinealectomizado. Si bien se observó un incremento en la liberación de la SYN estos valores no alcanzaron a ser significativos.

DISCUSIÓN
Los resultados más relevantes del presente trabajo se resumen en los siguientes incisos: 1. La pinealectomía funcional reduce significativamente la concentración tisular y la liberación presináptica de las encefalinas en el cerebro de la rata. 2. El efecto es revertido con la administración exógena de MEL o cuando los animales son expuestos a cuatro y seis horas de oscuridad. 3. La administración del LZ es capaz de bloquear el incremento de la concentración tisular de IR–Met–Encefalina inducida por la administración exógena de la MEL.
Diversas líneas de investigación han demostrado que la concentración tisular y la liberación presináptica de los péptidos opioides tienen un ritmo circádico bien establecido. En el cerebro la concentración más alta de encefalinas se alcanza durante la fase de oscuridad y la mínima durante las primeras horas de la mañana.14,15 Nuestro grupo de trabajo demostró que la pinealectomía funcional rompe el ritmo circádico de los opioides, debido a que durante la fase de oscuridad la ausencia de la hormona abate la concentración tisular de encefalinas.21 En el presente estudio se aportan evidencias experimentales acerca de la fisiología de la MEL en el control de la síntesis de los opioides. Como se muestra en los cuadros 1 y 2 la ausencia de la hormona reduce de manera significativa el contenido tisular de las encefalinas en las cuatro estructuras cerebrales analizadas, efecto que puede ser revertido por la administración exógena de la hormona. Si bien la síntesis de encefalinas ha sido previamente documentada,27–31 la señal endocrina que regula la vía de señalización de dicha síntesis se desconoce. No obstante, factores de transcripción como el CREB, c–fos y AP–1 presentes en el SNC de la rata, son capaces de activar a los genes que dan lugar a los péptidos derivados del SEO.28,30,32 Para ejercer su función bioquímica, los factores de transcripción requieren ser activados, en particular por enzimas del tipo de las cinasas como la proteína cinasa C (PKC). Los experimentos realizados in vitro, indican que la MEL es capaz de unirse y activar a la PKC purificada del cerebro de la rata.33 Esta evidencia indica un estadio inicial de los eventos en cascada que la hormona produce intracelularmente y que pueden terminar en la expresión de los genes de los opioides. Wajs et al.34 han señalado que en estructuras del sistema inmune, como los nódulos linfáticos y la médula ósea, la MEL puede inducir la activación del gen que codifica para la Proopiomelanocortina (POMC) y que su actividad puede estar mediada por el factor de transcripción CREB. Evidencias posteriores confirman que la MEL es capaz de activar al CREB en la Pars tuberalis de la rata35 y que este efecto puede estar mediado por la PKC. La PKC se ha localizado tanto en el citoplasma como en los núcleos de varias estructuras del SNC.18 El grupo de Ventura et al.36 demostró que la exposición de núcleos aislados de los miocitos a la dinorfina B (agonista de los receptores kappa) aumenta la expresión génica de los opioides y que dicho efecto puede ser mediado por la PKC nuclear.
]]> Los mecanismos descritos previamente consideran que la concentración circádica de la hormona alcanza su máximo valor en el suero durante la fase de oscuridad (01:00h). La dosis más alta de 600µg/Kg de MEL se estableció en función de su farmacocinética37 y es cercana a la concentración fisiológica (1nM) que se encuentra en el suero de la rata a la 01:00am La dosis intermedia de MEL (300µg/Kg) mostró ser capaz de inducir un incremento significativo en el contenido tisular de las encefalinas. Sin embargo, la dosis más baja (150µg/Kg) tuvo un comportamiento selectivo en la concentración de la Met y la Leu–Encefalina, pues este último péptido no respondió a la dosis de MEL, mientras que la Met–Encefalina sí mostró cambios significativos pero sólo en dos estructuras cerebrales. Esta discrepancia puede explicarse debido a que en la molécula de la Proencefalina A sólo existe una copia de Leu–Encefalina y cuatro de Met–Encefalina.38 Por otro lado, desde los años 1970 se conoce que ambos péptidos se localizan en pozas liberables distintas en las terminales nerviosas.39 Una ventaja de inhibir la síntesis endógena de MEL40,41 por medio de una técnica no invasiva, en comparación con la pinealectomía quirúrgica o con el uso de fármacos, es que la concentración sérica de MEL se restablece de manera natural cuando se exponen a la oscuridad lo que nos permite medir los cambios en el contenido tisular de los péptidos opioides. Cuando el estímulo luminoso cesa y los animales pinealectomizados son expuestos a un periodo de oscuridad la síntesis endógena de MEL se activa e induce la síntesis de encefalinas. Después de cuatro horas de oscuridad el hipotálamo y el hipocampo presentaron un incremento significativo en el contenido de encefalinas cuando se comparan con el grupo pinealectomizado. Con seis horas de oscuridad la concentración de opioides alcanza valores del orden de un 350% de aumento con respecto al grupo de luz continua, de un 200% con respecto al grupo de cuatro horas y de un 100% con respecto al grupo control. Es necesario destacar que un aumento no significativo en la concentración sérica de la hormona (cuadro 1) produce un incremento considerable en el contenido tisular de los opioides, lo cual pone de manifiesto la avidez del organismo por la MEL y que su efecto sobre el SEO es inmediato. El uso del antagonista de la MEL el LZ refuerza la hipótesis de que la hormona participa en la síntesis de las encefalinas. En la actualidad se ha establecido la presencia del receptor de la MEL (Mt1) en estructuras del SNC que incluyen las aquí analizadas. Su afinidad, distribución y características de saturación han sido previamente descritas.42 Nuestros resultados demuestran que la presencia del LZ fue capaz de bloquear el incremento de encefalinas inducido por la administración de MEL en los animales pinealectomizados. Sin embargo, también es necesario mencionar que aun con el uso de tres diferentes dosis del antagonista no se encontraron cambios significativos entre los valores de encefalinas. El resultado puede ser explicado si consideramos que uno de los mecanismos de acción propuestos para MEL se basa en su propiedad de ser una sustancia liposoluble, por lo tanto es capaz de atravesar la membrana plasmática para interactuar con los segundos mensajeros.19Por último, la liberación presináptica de encefalinas es un dato que nos indica el aspecto funcional entre la MEL y las encefalinas. Por una parte los cambios observados en la liberación de opioides están en concordancia con su contenido en el tejido, es decir, a mayor concentración tisular mayor liberación y viceversa, la ausencia de la hormona reduce la liberación de encefalinas. En ambos casos el efecto se revierte al administrar MEL. Por otro lado, estos datos pueden comenzar a explicar el papel de la MEL en diversos aspectos de la fisiología y no sólo de la cronobiología. Un ejemplo de ello es la capacidad de la hormona de ser un agente inductor de la anestesia.43 Por el momento se ha establecido que a nivel molecular los anestésicos generales aumentan la función de los neurotransmisores inhibitorios como el ácido gama–aminobutírico (GABA) y de los receptores de glicina e inhiben la transmisión excitatoria producida como la mediada por los receptores N–metil–D–aspartato (NMDA).44 Ahora bien, previamente se ha demostrado que la síntesis y la liberación de GABA es regulada por la hormona45 aunado a que la analgesia inducida por la MEL no se debe a que se una a sus receptores, sino que promueve la liberación de beta–endorfina46 que, junto con las encefalinas, tienen un carácter inhibitorio en la transmisión sináptica.47 Los resultados de la liberación presináptica de opioides descrita en el presente trabajo refuerzan las hipótesis descritas, ya que nos sugieren que la MEL promueve la síntesis y en consecuencia la liberación no sólo de Met–Encefalina sino de varios péptidos representativos de la Proencefalina A (como la Met5–Arg6–Phe7 y la Synencefalina) y no sólo de la Proopiomelanocortina. Es decir afecta en su conjunto al Sistema Endógeno Opioide.
En conclusión, el presente trabajo aporta evidencias experimentales de que la MEL no sólo ejerce su acción en la cronobiología, sino que existe una relación funcional entre la MEL y la síntesis y liberación de los neuropéptidos como las encefalinas.
REFERENCIAS
1. Hughes J, Smith T, Kosterlitz H, Fothergill LA, Morgan B. Identification of two related pentapeptides from the brain with potent opiate agonist activity. Nature 1975;258:577–579. [ Links ]
2. Hokfelt T, Borberger C, Xu ZQ. Neuropeptides an overview. Neuropharmacology 2000;32(3);1337–1356. [ Links ]
3. Akil H, Watson SJ, Young E, Lewis ME, Khachaturian K et al. Endogenous opioids: Biology and function. Ann Rev Neurosci 1984;7:253–256. [ Links ]
4. Anderson KE. Neurotransmitters: central and periphereal mechanisms. Int J Impot Res Suppl 2000;4:S26–33. [ Links ]
5. Terenius L. From opiate pharmacology to opioid peptides physiology. Ups J Med Sci 2000;105(1):1–15. [ Links ]
6. Li S, Wang T, Wang R, Dai X, Chen Q et al. Melatonin enhances antinociceptive effects of ä–but not µ–opioid agonist in mice. Brain Res 2005;1043:132–138. [ Links ]
7. Przewlocki R, Przwelocka B. Opioids in chronic pain. Eur J Pharmacol 2001;429:79–91. [ Links ]
8. Padros MR, Vindrola O. Antibodies against the amino–terminal portion of pro–enkephalin inhibits DNA synthesis in human peripheral mononuclear cells. J Neuroimmunol 1995;61:79–83. [ Links ]
9. Younes A, Pepe S, Barron NB, Spurgeon HA. Circadian synthesis, processing, and coronary release of enkephalin–related peptides. AJP. Heart Circulatory Physiology 2000;279(4):H1989–1998. [ Links ]
10. Saravia F, Padrós MR, Ase A, Aloyz R, Duran S et al. Differential response to a stress stimulus of Proenkephalin peptide content in immune cells of naive and chronically stressed rats. Neuropeptides 1998;32:351–359. [ Links ]
11. Maestroni JM, Conti A. The melatonin–immune system–opioid network. En: Reiter RJ, Lukaszyk A (eds). Advances in pineal research 4. Londres: John Libbey; 1990. [ Links ]
12. Maestroni GJ, Conti A. The pineal–immuno–opioid network, mechanisms and significance. Ann NY Acad Sci 1992;650:56–59. [ Links ]
13. Roy S, Loh HH. Effects of opioids on the immune system. Neurochem Res 1996;21:1375–1386. [ Links ]
14. Asai M, Vindrola O, Zubieta M, Talavera E, Massarini A. Diurnal variations of IR–Met–enkephalin in the brain of pentylenetetrazol–kindled rats. Brain Res 1988;442:81–85. [ Links ]
15. Asai M, Zubieta M, Matamoros–Trejo G, Linares G, Agustin P. Diurnal variations of opioid peptides and synenkephalin in vitro release in the amygdala of kindled rats. Neuropeptides 1998;32(3):293–299. [ Links ]
16. Hardeland R: Melatonin: multiple functions in signaling and protection. En: Altmeyer P, Hoffmann K, Stucker M. (eds.). Skin cancer and UV radiation. Springer–Verlag Berlin Heidelger; 1997. [ Links ]
17. Reiter RJ. The melatonin rhythm: both a clock and a calendar. Experientia 1993;49:654–664. [ Links ]
18. Reiter RJ. Pineal melatonin: cell biology of its synthesis and of its physiological interactions. Endocrine Rev 1991;12:151–180. [ Links ]
19. Benitez–King G, Anton–Tay F: Calmodulin mediates melatonin cytoskeletal effects. Experientia 1993;49:635–641. [ Links ]
20. Blask DE, Sauer LA. Melatonin as a chronobiotic/anticancer agent: cellular, biochemical and molecular mechanisms of action and their implications for circadian–based cancer therapy. Curr Top Med Chem 2002;2:113–132. [ Links ]
21. Asai M, Mayagoitia L, García D, Matamoros G, Valdés M et al. Rat brain opioid peptides–circadian rhythm is under control of melatonin. Neuropeptides 2007;41:389–397. [ Links ]
22. Engel J Jr, Sharpless NS. Long–lasting depletion of dopamine in rat amygdala induced by kindling stimulation. Brain Res 1977;136:381–386. [ Links ]
23. Glowinski J, Iversen LL. Regional studies of catecholamines in rat brain. J Neurochem 1966;13:655–669. [ Links ]
24. Nagy A, Delgado–Escueta AV. Rapid preparation of synaptosomes from mammalian brain using nontoxic isoosmotic gradient material (Percoll). J Neurochem 1984;43:1114–1123. [ Links ]
25. Whittaker VP. Thirty years of synaptosome research. J Neurocytol 1993;9:735–42. [ Links ]
26. Lowry OH, Rosenbrough J, Farr AL, Randall RJ. Protein measurement with the folin phenol reagent. J Biol Chem 1951;193:265–275. [ Links ]
27. Kanamatsu T, Obie K, Grimes L, McGinty JF, Yoshikawa K. Kainic acid alters the metabolism of Met5–Enkephalin and the level of dynorphin A in the rat hippocampus. J Neurosci 1986;6:3094–3102. [ Links ]
28. Kley N. Multiple regulation of Proenkephalin gene expression by Protein Kinase C. J Biol Chem 1988;263(4):2003–2008. [ Links ]
29. Noda M, Furutani Y, Takahashi H et al. Cloning and sequence analysis of cDNA for bovine adrenal preproenkephalin. Nature 1982;295:202–206. [ Links ]
30. Rodriguez–Vida, Nahmod VE, Vindrola O. Synenkephalin processing in embryonic rat brain. Dev Brain Res 1994;77:151–156. [ Links ]
31. Ziolkowska B, Przewlocka B, Mika J, Labuz D, Przewlocki R. Evidence for Fos involvement in the regulation of proenkephalin and prodynorphin gene expression in the rat hippocampus. Mol Brain Res 1998;54:243–251. [ Links ]
32. Suh HW, Hudson PM, Hong JS. Expression of the proenkephalin A gene and [Met5]–enkephalin secretion induced by arachidonic acid in bovine adrenal medullary chromaffin cells: involvement of second messengers. J Neurochem 1995;64(2):608–613. [ Links ]
33. Anton–Tay F, Ramírez G, Martínez I, Benítez–King G. Invitro stimulation of protein kinase C by melatonin. Neurochem Res 1998;23:601–606. [ Links ]
34. Wajs E, Kutoh E, Gupta D. Melatonin affects proopiomelanocortin gene expression in the immune organs of the rat. Eur J Endocrinol 1995;133(6):754–760. [ Links ]
35. McNulty S, Ross AW, Barrett P, Hastings MH, Morgan PJ. Melatonin regulates the phosphorylation of CREB in ovine pars tuberalis. J Neuroendocrinol 1994;6(5):523–532. [ Links ]
36. Ventura C, Maioli M, Pintus G, Posadino AM, Tadolini B. Nuclear opioid receptors activate opioid peptide gene transcription in isolated myocardial nuclei. J Biol Chem 1998;273(22):13383–13386. [ Links ]
37. Yeleswaram K, McLaughlin LG, Knipe JO, Schabdach D. Pharmacokinetics and oral bioavailability of exogenous melatonin in preclinical animal models and clinical implications. J Pineal Res 1997;22(1):45–51. [ Links ]
38. Asai M, Guitiérrez R. Neurobiología de los péptidos opioides. Salud Mental 1994;17(2):30–41. [ Links ]
39. Watson S, Akil H, Richard CW, Barchas J. Evidence for two separate opiate peptide neuronal systems. Nature 1978;275:226–228. [ Links ]
40. Lewy AJ, Wehr TA, Goodwin FW, Newsome DA, Markey SP. Light suppresses melatonin secretion in humans. Science 1980;210:1267–269. [ Links ]
41. Poeggleler BH, Barlow–Walden LR, Reiter RJ, Saarela S, Menendez–Pelaez A et al. Red–light–induced suppression of melatonin synthesis is mediated by N–methyl–Daspartate receptor activation in retinally normal and retinally degenerate rats. J Neurobiol 1995;28(1):1–8. [ Links ]
42. Dubocovich ML, Rivera–Bermudez MA, Gerdin MJ, Masana MI. Molecular pharmacology, regulation and function of mammalian melatonin receptors. Front Biosci 2003;8:d1093–108. [ Links ]
43. Naguib M, Gottumukkata V, Goldstein P. Melatonin and anesthesia: a clinical perspective. J Pineal Res 2007;42:12–21. [ Links ]
44. Hill–Venning C, Belelli D. Subunit dependent interaction of the general anaesthetic etomidate with ã–aminobutiric acidtype A receptor. Br J Pharmacol 1997;120:749–756. [ Links ]
45. Cardinali D, Golomek D. The rhythmic GABAergic system. Neurochem Res 1998;23(5):607–614. [ Links ]
46. Shavali S, Ho B, Govitrapong O. Melatonin exerts its analgesic actions not by binding to opioid receptor subtypes but by increasing the release of beta–endorphin an endogenous opioid. Brain Res Bull 2005;64:471–479. [ Links ]
47. Bodnar RJ. Endogenous opiates and behavior: 2007 Peptides 2008:29;2292–2375. [ Links ] ]]>