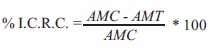
Aceites Esenciales y Extractos Acuosos para el Manejo in vitro de Fusarium oxysporum f. sp. lycopersici y F. solani
Essential Oils and Aqueous Extracts for the in vitro Management of Fusarium oxysporum f. sp. lycopersici and F. solani
Daniel Antonio Vásquez Covarrubias, Roberto Montes Belmont, Alfredo Jiménez Pérez e Hilda Elizabet Flores Moctezuma
Centro de Desarrollo de Productos Bióticos. Instituto Politécnico Nacional. Apartado postal 24. Yautepec, Morelos. Correspondencia: rbelmont@ipn.mx
]]>Recibido: Septiembre 09, 2013
Aceptado: Marzo 12, 2014
Resumen
El uso de fungicidas sintéticos favorece la aparición de hongos fitopatógenos resistentes, por lo que se requieren nuevos productos para el manejo de enfermedades. Una alternativa son los aceites esenciales (AE) y extractos acuosos (EA) de origen vegetal. En este trabajo se evaluaron distintas concentraciones de AE y EA de cinco especies de la familia Chenopodiaceae sobre el crecimiento micelial y esporulación de Fusarium oxysporum f. sp. lycopersici (FOL) y F. solani. Se encontró que existe una respuesta diferencial entre las razas 2 y 3 de FOL e incluso entre aislamientos de una misma raza. Los AE de Chenopodium album [0.3 %] y C. ambrosioides [2 %] inhibieron totalmente el crecimiento y esporulación en ambas especies de Fusarium. De los EA probados, el de Beta vulgaris ejerció la mayor reducción del crecimiento micelial (38 %) y esporulación (61 %). Los EA al 5 %, de las cinco especies evaluadas, mostraron una estimulación del 27 al 183 % en el crecimiento micelial en las cuatro cepas empleadas. Al 10 %o, Beta vulgaris, C. album, C. berlandieri subsp. nuttalliae y C. graveolens redujeron entre 11 y 38 % el crecimiento de F. solani y FOL raza 2 (aislamiento Yautepec) con respecto al testigo.
Palabras clave: Plantas antifúngicas, Chenopodiaceae, epazote, epazote de borrego, betabel.
Abstract
The use of synthetic pesticides favors the appearance of resistant pathogens and pest; therefore, new products are needed for disease management. The use of essential oils (EO) and aqueous extracts (AE) are an alternative option. In this work, different concentrations of EO and AE of five Chenopodiaceae species were evaluated on micelial growth and spore production of Fusarium oxysporum f. sp. lycopersici (FOL) and F. solani. It was found that there is a differential response between races 2 and 3 of FOL and even among isolates of the same race. EO of Chenopodium album [0.3 %] and C. ambrosioides [2 %] inhibited micelial growth and spore production on both Fusarium species. Of the EA tested, Beta vulgaris exercised the greatest reduction in mycelial growth (38 %) and sporulation (61 %). The EA 5 %, of the five species tested showed a stimulation by 27 to 183 % in mycelial growth on the four strains used. At 10 %, Beta vulgaris, C. album, C. berlandieri subsp. nuttalliae and C. graveolens reduced between 11 and 38 % growth of F. solani and FOL race 2 (isolate Yautepec) compared with the control.
]]> Keywords: Antifungal plants, Chenopodiaceae, american wormseed, lamb's quarters, beet.
En la familia Chenopodiaceae existen varias especies con metabolitos con un amplio espectro de acción contra hongos fitopatógenos dentro de los géneros Alternaria, Aspergillus, Cercospora, Colletotrichum, Erysiphe, Fusarium, Helminthosporium, Monilinia, Penicillium, Phyllachora, Puccinia, Pythium, Rhizoctonia. Sclerotinia y Tilletia (Grainge y Ahmed, 1988; Rodríguez, 2005). Estos metabolitos se detectan en extractos acuosos, etanólicos, metanólicos y aceites esenciales.
Rafiq et al., (1984) encontraron que el extracto acuoso de Chenopodium album inhibe el desarrollo de Cochliobolus carbonum y de Glomerella tucumanensis. Grainge y Ahmed (1988) en una revisión de literatura, indican la propiedad antifúngica en Beta vulgaris contra Alternaria tenuis, Aspergillus oryzae, Curvularia penniseti, Fusarium oxysporum, F. solani, Helminthosporium spp. y Rhizopus nigricans. También mencionan que C. album actúa sobre Colletotrichum lindemuthianum y Monilia fructicola, en tanto que C. ambrosioides inhibe a 20 especies de hongos incluyendo a dermatofitos de humanos.
En trabajo de campo, Montes-Belmont y Martínez (1992) aumentaron la producción de calabacita Cucurbita pepo en un 38 % con aplicaciones de extracto acuoso de C. album en comparación con plantas no tratadas contra Erysiphe cichoracearum. Bravo-Luna et al. (1998) reportaron que el aceite esencial de Chenopodium ambrosioides inhibió el crecimiento micelial de Fusarium moniliforme a una dosis de 500 ppm y la esporulación a 10000 ppm. Las saponinas de C. quinoa inhibieron el crecimiento de Candida albicans (Woldemichael y Wink, 2001). Montes-Belmont y Flores-Moctezuma (2001) en trabajo sobre el causante del ergot del sorgo Claviceps africana reportaron que el extracto acuoso de C. ambrosioides al 4 % y la mezcla de los extractos acuosos de Sizygium aromaticum (0.5 %) y C. ambrosioides (3.5 %) redujeron significativamente el crecimiento micelial in vitro. Sin embargo, en pruebas in vivo, los polvos, extractos acuosos y etanólicos de C. ambrosioides no redujeron el crecimiento de este hongo sobre semillas de sorgo. Los aceites esenciales de esta planta al 5 y 10 %, mostraron un efecto fungicida sobre F. thapsinum, pero afectaron significativamente el porcentaje de germinación y la altura en plantas de sorgo. El aceite esencial de las partes aéreas de C. botrys tuvo actividad fungicida contra Aspergillus niger y Candida albicans (Tzakou et al., 2006). Kumar et al. (2007) probaron que el aceite esencial de C. ambrosioides (100 µg/mL) actúa contra Aspergillus flavus, A. fumigatus, Lasiodiplodia theobromae, Fusarium oxysporum, Sclerotium rolfsii, Macrophomina phaseolina, Cladosporium cladosporioides, Bipolaris oryzae, y Pythium debaryanum.
Marangon et al. (2008) evaluaron el efecto del aceite esencial de C. ambrosioides, contra A. ochraceous, Colletotrichum gloeosporioides, C. musae, Fusarium oxysporum y F. semitectum, encontrando que a una concentración del 0.3% se inhibe completamente el crecimiento, y que al 0.1 % alcanza una reducción superior al 90 %o. Estos autores determinaron que el (Z)-ascaridol y E-ascaridol le confieren la actividad antifúngica a C. ambrosioides.
Saïdana et al. (2008) identificaron los compuestos volátiles y evaluaron el efecto de los aceites esenciales de Suaeda fructicosa (Chenopodiaceae) y Limonium echioides (Plumbaginaceae) sobre Fusarium oxysporum, Aspergillus niger, Penicillium spp. y Alternaria spp. sin encontrar efecto antifúngico. Javaid y Amin (2009) probaron Chenopodium album, C. murale y C. ambrosioides contra Macrophomina phaseolina, siendo la mejor especie C. album en extracto metanólico. Garduño-Pizaña et al. (2010) evaluaron el efecto de 15 especies de plantas contra F. oxysporum f. sp. gladioli, encontrando que el extracto acuoso (5 %) de C. ambrosioides estimuló significativamente el crecimiento y esporulación del hongo y redujo significativamente la germinación de los conidios.
Recientemente, Rauf y Javaid (2013) probaron diferentes concentraciones de extractos metanólicos de hojas, tallos, raíces e inflorescencias de Chenopodium album contra Fusarium oxysporum f. sp. cepae encontrando el mayor efecto en las inflorescencias.
Con base en estos antecedentes, el objetivo de este trabajo fue determinar la actividad biológica de aceites esenciales (AE) y extractos acuosos (EA) de Chenopodium album, C. graveolens, C. berlandieri subsp., nuttalliae, C. ambrosioides y Beta vulgaris, sobre el crecimiento micelial y producción de micro y macroconidios en Fusarium oxysporum f. sp. lycopersici y F. solani.
Especies de Fusarium. Tanto Fusarium oxysporum f. sp. lycopersici como F. solani se obtuvieron de la colección del Laboratorio de Fitopatología del Centro de Desarrollo de Productos Bióticos del Instituto Politécnico Nacional (México). Del primero se manejaron dos cepas de la raza 2 (una de Cuautla 2RC y otra de Yautepec, Morelos 2RY) y una de la raza 3 3R proveniente de Emiliano Zapata en el mismo estado. La cepa de F. solani provino de Tepoztlán, Morelos. Todas las cepas provenían de plantas de jitomate y fueron identificadas morfológica y molecularmente (Domínguez, 2012). Las cepas se mantuvieron en cajas de Petri de 15 x 90 mm con medio papa-dextrosa-agar (PDA, BDBioxon®). La temperatura se mantuvo en 25 ± 3 °C durante el transcurso de los bioensayos.
]]> Especies vegetales. Se utilizaron tres especies con antecedentes de propiedades antifúngicas: betabel (Beta vulgaris), epazote común (Chenopodium ambrosioides) y epazote de borrego (C. album). Una con efecto contra hormigas (epazote de zorrillo C. graveolens) (Grainge y Ahmed, 1988) y otra con propiedades alimenticias huauzontle (C. berlandieri subsp. Nuttalliae). Estas plantas se obtuvieron por colectas de campo en Jumiltepec, Morelos (epazote de borrego), Juchitepec, Edo. de México (epazote de zorrillo) y en la central de abastos de Cuautla, Morelos (epazote común, huauzontle y betabel).Procesamiento de las plantas. Se establecieron dos tipos de bioensayos uno para AE y otro para EA. Los AE se obtuvieron mediante destilación por arrastre de vapor de acuerdo al protocolo descrito por Marangon et al. (2008). Para esto, 4 L de material de la planta picada se introdujeron en un matraz de bola de 12 L y se sometió a ebullición; el vapor de agua se pasó a través de un condensador hasta que la destilación se detuvo y el destilado presentaba capa aceitosa. El destilado (hidrosol y AE) se congeló por un día con el propósito de congelar la fase acuosa (hidrosol) y facilitar la colecta del AE por decantación. Al hidrosol se le adicionó éter (Baker ®) en una proporción 1:10 (éter: hidrosol), se agitó por 30 seg y se congeló nuevamente para separar la fase etérea, la cual contenía trazas de AE. El éter se removió en baño maría a una temperatura entre 35 y 45 °C. El AE separado por congelación y por arrastre con éter se mezcló y secó adicionando sulfato de sodio anhidro (Sigma ®). El AE se separó por decantación y se almacenó en frascos ámbar en refrigeración a 4 °C hasta su uso.
Para obtener EA se siguió el protocolo señalado por Montes-Belmont et al. (2000) el material previamente triturado se colocó en charolas y se secó en una estufa entre 45 y 55 °C; a excepción del betabel, el cual se partió en rebanadas de 3-5 mm y se secó con un ventilador convencional durante cuatro días. Una vez deshidratado el material vegetal, se procedió a triturarlo en un molino eléctrico a un tamaño de malla No. 40. Este polvo fino se almacenó en recipientes de plástico protegidos de la luz, en un lugar fresco (20 ±3 °C) y seco hasta su uso.
Los EA se prepararon con agua destilada estéril, adicionando el polvo vegetal requerido para cada concentración [5, 10 ó 15 % p/v]. Cada matraz se colocó en agitación constante a 150 rpm durante 24 h. Pasado ese tiempo, se dejó reposar por 1 h y se filtró dos veces a través de gasas estériles. Inmediatamente después de filtrar cada EA, estos se incorporaron al medio de cultivo.
Los AE se incorporaron al medio de cultivo (PDA) después del proceso de esterilización del medio (15 lb/in durante 15 min) y hasta que el medio alcanzó una temperatura menor a 50 °C. Las concentraciones de AE empleadas fueron: 0.1, 0.3, 2 y 10 % v/v. Para facilitar la homogeneización de los AE en el medio, se agregó Tween 20 al 0.1 % en una proporción 1:5 (Tween:AE). Los tratamientos se establecieron bajo un diseño completamente al azar que incluyeron las 4 concentraciones y dos testigos: el control (únicamente PDA) y Tween 20 (proporción 1:5 respecto al AE). En todos los tratamientos se utilizaron seis repeticiones, considerando cada caja de Petri (90 x15 mm) como una unidad experimental. La temperatura de incubación fue a 25 ± 3 °C.
Con los EA, previamente filtrados, se prepararó el medio de cultivo PDA, empleando al extracto acuoso como la cantidad de agua requerida para la preparación del medio, según instrucciones del fabricante, en condiciones normales. Es decir, si el medio requería 1, 000 mL de agua, en su lugar se empleó 1000 mL de EA. Las concentraciones de EA empleadas fueron 5, 10 y 15 % (p/v). Una vez preparados los medios de cultivo, éstos se esterilizaron a 15 lb/in durante 15 min. El diseño experimental fue el mismo que para AE, además se incorporó un control (únicamente PDA).
Variables a medir:
a) Crecimiento micelial. El borde del micelio se marcó con un plumón indeleble cada 24 h después de la inoculación, hasta que el micelio del control (en al menos cuatro repeticiones) alcanzara el borde de la caja. Para determinar el área micelial se tomó una fotografía con una cámara digital fija en un tripie, manteniendo siempre las mismas condiciones (distancia, zoom, calidad en MPx y formato de imagen). En el programa ImageJ se calibró una distancia conocida para obtener la relación pixeles:mm. Una vez obtenida esta proporción, en Adobe Photoshop CS5®, se empleo la herramienta "lazo magnético" para señalar y medir el área micelial expresada como mm2.
Una vez tomadas las medidas de todas las fotografías (una por caja de Petri), se seleccionaron y exportaron a un documento txt delimitado por tabuladores, el cual se abrió en Excel y se guardó como hoja de cálculo para obtener el porcentaje de inhibición del crecimiento con respecto al control (% I.C.R.C.) mediante la fórmula:
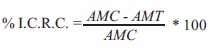
b) Producción de micro y macroconidios. A cada caja de Petri se le realizó un raspado micelial con una varilla de vidrio estéril. Se adicionaron 15 mL de agua destilada estéril y se vació en un vaso de precipitado estéril. El mismo procedimiento se realizó en cada tratamiento y al final se obtuvo una suspensión de esporas por tratamiento, a partir de la cual se realizaron tres conteos por repetición en una cámara de Neubauer marca Marienfeld® (Alemania). La determinación del número de esporas se realizó mediante la siguiente fórmula:

Se calculó el porcentaje de inhibición de la esporulación (% I.E.). de la siguiente manera:

Ambos bioensayos fueron repetidos en dos ocasiones para confirmar los resultados. Los datos de las dos repeticiones fueron sometidos a ANOVA seguido de separación de medias por Holm-Sidak. El análisis se llevó a cabo en el programa Sigma-Plot versión 10.0 y la probabilidad de rechazo fue de 5 %.
RESULTADOS
Crecimiento micelial. El AE de betabel al 0.3 % tuvo efecto fungistático con reducción significativa del crecimiento micelial de la cepa R2Y en un 71.12 %. Huauzontle y epazote de zorrillo, al 10 %, redujeron significativamente el crecimiento micelial de la cepa R3 (76.72 y 77 % respectivamente). Los AE de epazote de borrego y epazote común impidieron totalmente el crecimiento micelial de ambas especies Fusarium y las dos razas de F. oxysporum f. sp. lycopersici desde la inoculación del patógeno hasta la última lectura de crecimiento (11 d) (Figura 1A).
Los cinco EA presentaron un efecto fungistático en el crecimiento micelial. La reducción máxima de crecimiento micelial (I.C.R.C.) para cada especie fue; huauzontle 10 %, epazote común 23 %, epazote de zorrillo 24 %, epazote de borrego 28 % y betabel 38 % (Figura 1B).
]]> Producción de microconidios. Los AE de betabel (0.3 %) y AE de huauzontle (10 %) redujeron un 74 y 52 % (respectivamente) el número de microconidios en la cepa FOL R3. Los AE de epazote de borrego y epazote común (al 2 % y 0.3 % respectivamente) redujeron en 100 % el desarrollo micelial. y la producción de microconidios y macroconidios (Figura 2A).Únicamente los EA al 5 % redujeron la producción de microconidios. 8 % para epazote de borrego sobre R2C; 37 % para epazote común sobre FS, 46 % para epazote de zorrillo sobre R2Y, 51 % para huauzontle sobre R2Y y 61 % para betabel sobre R2Y (Figura 2B).
Producción de macroconidios. Los AE de huauzontle y betabel (al 0.3 %) redujeron 87 % la producción de macroconidios de FOL R2Y. El AE de epazote de zorrillo no mostró diferencias, con respecto al control, en el número de macroconidios (Figura 3A).
Únicamente los EA al 5 % redujeron la producción de macroconidios con respecto al control. La menor reducción se encontró con betabel contra FS y R2Y (64 % I.C.R.C.); mientras que la máxima reducción se registró con epazote de borrego sobre FS (90 % I.C.R.C.) (Figura 3B).
DISCUSIÓN
Aunque ya se había reportado el efecto antifúngico de B. vulgaris y C. ambrosioides sobre Fusarium oxysporum y F. solani (Grainge y Ahmed 1988) no se había comparado la susceptibilidad entre especies y aislamientos de estos dos patógenos ante un mismo aceite esencial o extracto acuoso.
Se encontraron diferencias en la susceptibilidad (crecimiento micelial y producción de conidios) entre Fusarium oxysporum f. sp. lycopersici y F. solani; también hubo una respuesta diferencial entre las razas 2 y 3 de FOL e incluso entre aislamientos de una misma raza. Esto concuerda con la diversidad de respuestas encontrada por otros autores desde un estímulo en el crecimiento de C. ambroioides sobre F.o. f. sp. gladioli (Garduño-Pizaña et al., 2010) hasta inhibición total de F.o. f. sp. cepae por parte de C. álbum (Raufy Javaid, 2013).
En el caso de C. album, este es el primer reporte de este efecto sobre Fusarium solani y Fusarium oxyporum f. sp. lycopersici razas 2 y 3. También se reporta por primera vez la actividad biológica de AE y EA de C. album, C. graveolens y C. berlandieri subsp. nuttalliae sobre el crecimiento micelial y producción de conidios de especies de Fusarium.
Aún cuando los AE de C. album y C. ambrosioides causan la reducción e inhibición del crecimiento y esporulación de las especies probadas, su composición química es diferente (Duke, 2008). Esta diferencia en la composición, así como diferencias en la concentración de los compuestos, podrían explicar el por qué los AE y EA de ambas especies provocan respuestas diferente en Fusarium spp.
]]> Bravo-Luna et al. (1998) y Kumar et al. (2007) mencionan que la susceptibilidad del patógeno a extractos vegetales será distinta según la especie, forma específica, raza y patogenicidad del hongo. Asimismo, esta susceptibilidad será distinta según la concentración del tratamiento a la que se someta al organismo.Esta respuesta diferencial puede atribuirse a mecanismos de resistencia (enzimáticos, estructurales, cambio de la permeabilidad de la membrana, etc.) que le permitan aprovechar, evitar o destoxificar alguno de los compuestos presentes en los extractos vegetales (Vivanco et al., 2005).
Otros compuestos, tales como ácido cafeico, ácido clorogénico, ácido ferúlico, formaldehido, kaempferol, ácido p-cumárico, quercetina, entre otros, presentes en B. vulgaris, C. ambrosioides y C. album (Duke 2008) se han reportado también como fungicidas y/o fungistáticos, por lo que es difícil atribuir el efecto antifúngico a algún compuesto, sin pruebas específicas.
Los EA al 10 y 15 % redujeron significativamente el crecimiento micelial, pero estimularon la producción de esporas; caso contrario con EA al 5 %o, donde estimularon el crecimiento micelial pero redujeron la producción de conidios.
La producción de estructuras de reproducción significa un gasto energético importante para el organismo, sin embargo, estas estructuras tienen un papel importante en el ciclo de vida del organismo. Su fabricación requiere del almacenamiento, síntesis o transformación de compuestos esenciales para lograr la formación de conidios funcionales (Ramachandran et al., 2008). Particularmente para Fusarium, se sabe que sus conidios poseen altas cantidades de compuestos grasos y que requieren de un sustrato rico en carbono y nitrógeno para la germinación (Palmero et al., 2008). Basado en los requerimientos energéticos y nutricionales del hongo para la formación de micro y macroconidios, se puede proponer que los EA proporcionan compuestos ricos en carbono y nitrógeno y que el hongo es capaz de asimilarlos y aprovecharlo para su beneficio en la producción de conidios (Garduño-Pizaña, 2010).
Los aceites esenciales (0.3 - 2 %) de C. album y C. ambrosioides mostraron ser antifúngicos para Fusarium solani, F. oxysporum f. sp. lycopersici razas 2 y 3, ya que causaron reducción significativa del crecimiento micelial y producción de conidios, resultando ser los tratamientos con mayor actividad antifúngica frente a las cuatro cepas evaluadas.
AGRADECIMIENTOS. Al Consejo Nacional de Ciencia y Tecnologia y al Instituto Politécnico Nacional por el apoyo económico brindado para la realización del presente trabajo. A los doctores Guillermo Fuentes Dávila y Luis Pérez Moreno por la revisión del presente trabajo.
LITERATURA CITADA
]]>Bravo-Luna L, Bermudez-Torres K y Montes-Belmont R. 1998. Inhibición del crecimiento micelial y esporulación de Fusarium moniliforme Sheld. mediante aceites esenciales vegetales y algunos de sus componentes químicos. Revista Mexicana de Fitopatología 16: 18-23. [ Links ]
Dominguez, A. G. 2012. Aislamiento, identificación y distribución de Fusarium spp. En jitomate cultivado en suelo bajo invernadero en Morelos, México. Tesis de Maestría en Ciencias. Instituto Politécnico Nacional. Centro de Desarrollo de Productos Bióticos. 107 p. [ Links ]
Duke, J. 2008. Duke's Handbook of Medicinal Plants of Latin America. CRC Press. Florida. 832 p. [ Links ]
Garduño-Pizaña C, Barrera-Necha LL and Rios Gomez MY. 2010. Evaluation of the fungicidal activity of leaves powders and extracts of fifteen mexican plants against Fusarium oxysporum f. sp. gadioli (Massey) Snyder and Hansen. Plant Pathology Journal 9: 103-111. [ Links ]
Grainge M and Ahmed S. 1988. Handbook of plants with pest control properties. John Wiley & Sons. New York, USA. [ Links ]
]]>Javaid A and Amin M. 2009. Antifungal activity of methanol and nhexane extracts of three Chenopodium species against Macrophomina phaseolina. Natural Products Research 23: 1120-1127. [ Links ]
Kumar R, Kumar AM, Dubey NK and Tripathi YB. 2007. Evaluation of Chenopodium ambrosioides oil as a potential source of antifungal, antiaflatoxigenic y antioxidant activity. International Journal of Food Microbiology 115: 159-164. [ Links ]
Marangon J, Newandram CG, Dev DJO and Moreira MF. 2008. Composition and antifungal activity of the essential oil of brazilian Chenopodium ambrosioides L. Journal of Chemical Ecology. 34: 1213-1218. [ Links ]
Montes Belmont R, Cruz Cruz, V, Martinez Martinez G, Sandoval García G, Garcia Licona R, Zilch Domínguez Susano, Bravo Luna L, Bermudez Torres K, Dlores Moctezuma HE y Carvajal Moreno M. 2000. Propiedades Antifúngicas en Plantas Superiores. Análisis Retrospectivo de Investigaciones. Revista Mexicana de Fitopatología 18: 125-131. [ Links ]
Montes-Belmont R y Flores-Moctezuma HE. 2001. Combate de Fusarium thapsinum y Claviceps africana mediante semillas de sorgo tratadas con productos naturales. Manejo Integrado de Plagas. 61: 23-30. [ Links ]
]]>Montes-Belmont R y Martínez GM. 1992. Control de la cenicilla Erysiphe cichoracearum y el mildiu de la calabacita Pseudoperonospora cubensis mediante extractos vegetales en Nazareno Xoxocotlán, Oaxaca. Revista Mexicana de Fitopatología 10: 86-91. [ Links ]
Palmero L., D., M. de Cara G., C. Iglesias G., G. Ruiz L and JC. Tello M. 2008. Effects of water potential on spore germination and viability of Fusarium species. Journal of Industrial Microbiology and Biotechnolog3 y 5: 1411-1418. [ Links ]
Rafiq M, Nassir MA and Bhatti, MAR. 1984. Antifungal properties of certain common wild plants against different fungi. Pakistan Journal of Agricultural Research 5: 236-238. [ Links ]
Ramachandran S., C. Larroche and A. Pandey. 2008. Production of spores. p: 231-246. In: Pandey, A., C. R. Soccol y C. Larroche (eds). Current Developments in Solid-State Fermentation. Springer Asiatech Publishers. New Delhi, India. [ Links ]
Rauf S and Javaid A. 2013. Antifungal activity of different extracts of Chenopodium album against Fusarium oxysporum f. sp. cepae, the cause of onion basal rot. International Journal of Agriculture and Biology 15: 367-371 [ Links ]
Rodríguez HC. 2005. Plantas contra plagas 2; epazote, hierba de la cucaracha, paraíso, higuerilla y sabadilla. Red de Acción en Plaguicidas y sus Alternativas en América Latina, Red de Acción sobre Plaguicidas y Alternativas en México, Sociedad Mexicana de Agricultura Sostenible, Colegio de Posgraduados e Instituto Tecnológico del Altiplano de Tlaxcala. Estado de México, México. 209 p. [ Links ]
Saïdana D, Mahjoub S, Boussaada O, Chriaa J, Mahjoub M, Chéraif I, Daami M, Mighri Z and Helal A. 2008. Antibacterial and antifungal activities of the essential oils of two saltcedar species from Tunisia. Journal of the American Oil Chemists' Society 85: 817-826. [ Links ]
Tzakou O, Pizzimenti A, Pizzimenti FC, Sdrafkakis V and Galati EM. 2006. Composition and antimicrobial activity of Chenopodium botrys L. Essential oil from Greece. Journal of Essential Oil Research 19: 292-294. [ Links ]
Vivanco JM, Cosio E, Loyola-Vargas VM y Flores HE. 2005. Mecanismos químicos de defensa en las plantas. Investigación y Ciencia 2: 68-75. [ Links ]
Woldemichael GM and Wink M. 2001. Identification and biological activities of triterpenoid saponins from Chenopodium quinoa. Journal of Agricultural Food Chemistry 49: 2327-2332. [ Links ]
]]>