Introducción
Los aneurismas aislados de la arteria ilíaca son menos frecuentes que los aneurismas de la aorta abdominal, con la misma etiología predominantemente aterosclerótica-degenerativa, la mayoría de los afectados son hombres mayores de 65 años. Los pacientes por lo general progresan de manera asintomática y se revelan de manera incidental, generalmente después de haber adquirido dimensiones significativas, y cuando presentan síntomas, estos son secundarios a la obstrucción de estructuras adyacentes o cuando el aneurisma se encuentra en etapa de ruptura1.
La reconstrucción abierta tradicional se asocia con altas tasas de morbilidad y mortalidad. La reparación endovascular se ha propuesto como una alternativa mínimamente invasiva, asociada a menores tasas de morbimortalidad, incluso en pacientes de alto riesgo quirúrgico. La calidad de las zonas de apoyo, importantes para el sellado, es decisiva para la eliminación del aneurisma. La eliminación se lleva a cabo mediante injertos de stent, a menudo en combinación con embolización. Debido al riesgo de claudicación glútea y disfunción eréctil se recomienda la preservación de la perfusión pélvica ipsilateral en casos de colateralización insuficiente. Para este propósito se encuentran disponibles dispositivos especiales de rama ilíaca o varias técnicas de endoprótesis paralelas1,2.
Metodología
Para la realización de la presente revisión bibliográfica se han utilizado diferentes fuentes bibliográficas primarias y secundarias obtenidas de motores de búsqueda como PubMed, Trip, Scopus y Google Scholar, por medio de las siguientes palabras clave y términos MeSH: “aneurysm”, “iliac artery”, “iliac aneurysm”, “risk factors”, “endovascular” y “endografts”, adicionalmente se formularon preguntas PICO en la búsqueda de los estudios relacionados con terapéutica utilizando el motor de búsqueda Trip. Como filtros adicionales se utilizaron en el tipo de artículo: “meta-analysis”, “randomized controlled trial”, “clinical trial”, “review”, “systematic review” y se filtró por los trabajos publicados en los últimos cinco años. La búsqueda arrojó 756 resultados y se los discriminó de acuerdo con la pertinencia y relevancia del título de los artículos. Luego de este proceso, se descartaron 708 trabajos y 48 artículos continuaron en el proceso de análisis. Los investigadores a continuación evaluaron el resumen. Finalmente, se descartaron 25 trabajos y 23 fueron seleccionados para la realización de este artículo de revisión.
Desarrollo
Definición
La definición más aceptada de aneurisma de la arteria ilíaca (AAI) es la dilatación del vaso a más de 1.5 veces su diámetro normal1. En general, una arteria ilíaca común (AIC) > 18 mm en hombres y > 15 mm en mujeres, y una arteria ilíaca interna (AII) > 8 mm se considera aneurismática1. Los AAI se asocian comúnmente con la dilatación aneurismática de la aorta abdominal como aneurismas aorto-ilíacos en aproximadamente el 10% de los aneurismas de aorta abdominal. El AAI aislado es un aneurisma de las arterias ilíacas sin un aneurisma de la aorta abdominal infrarrenal, esto incluye aneurismas de la AIC, de la AII, de la arteria ilíaca externa (AIE) y combinaciones de estos. Los aneurismas de la AIE, que tienen un origen embriológico diferente, son raros1,2.
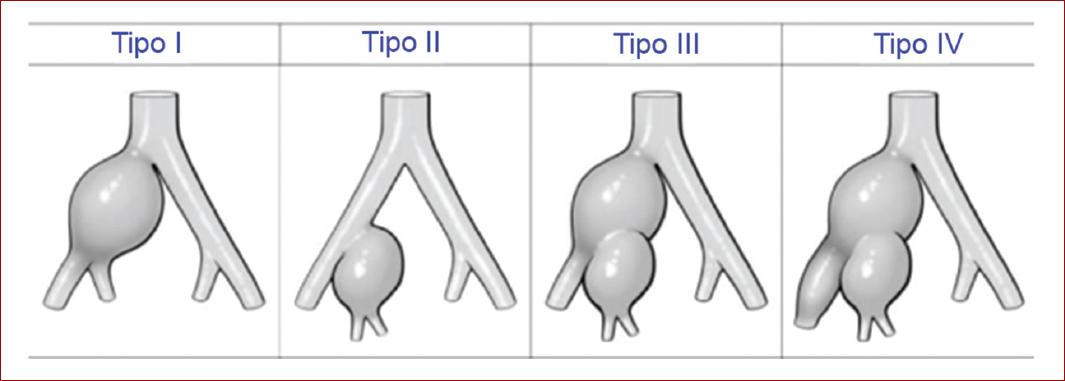
Existen varias clasificaciones para el AAI aislado. Una de ellas, la clasificación anatómica de Reber (Fig. 1), resulta adecuada para comparar los resultados de diferentes entidades anatómicas; por otro lado, la clasificación de Fahrni depende de la idoneidad del cuello para la reparación endovascular, que puede cambiar con el tiempo, el dispositivo y la técnica quirúrgica. Los AAI aislados se limitan con mayor frecuencia a la AIC (Reber I) y menos frecuentes a la AIE (Reber IV)2.
Sandhu y Pipinos han propuesto una clasificación anatómica según el segmento ilíaco aneurismático2:
- Tipo A: aneurisma de AIC con cuello proximal y distal 2.
- Tipo B: aneurisma de AIC con cuello proximal que alcanza la bifurcación ilíaca2.
- Tipo C: aneurisma de AIC con cuello proximal que afecta la bifurcación y se extiende a la AII2.
- Tipo D: aneurismas aislados de AII2.
- Tipo E: aneurisma de AIC sin cuello proximal, aneurismas de AIC bilaterales o combinación de aneurisma ilíaco y aneurisma de aorta abdominal (AAA)2.
Fisiopatología e historia natural
El desarrollo de un AAI es complejo, multifactorial y dinámico, y termina con un remodelado irreversible del tejido conjuntivo vascular; son cuatro los procesos que provocan la pérdida de la elasticidad y resistencia de la pared vascular: la proteólisis, el estrés oxidativo, una respuesta inmunitaria inflamatoria y la apoptosis de las células del músculo liso vascular. A su vez estos factores impiden la recuperación del diámetro vascular normal tras una pulsación2-4. Además, la pared arterial presenta un importante infiltrado inflamatorio consistente en linfocitos T y B, neutrófilos y macrófagos. Se desconoce el mecanismo que desencadena este proceso inflamatorio, pero es posible que los péptidos derivados de la degradación de los componentes de la matriz extracelular actúen como agentes quimiotácticos, promoviendo así la infiltración de macrófagos3-5. El debilitamiento de la pared vascular está asociado a la importante reducción en el contenido de células musculares lisas vasculares que mueren por apoptosis. Como compensación se produce una gran deposición de colágeno. La desestructuración de la capa media hace que la adventicia tenga que soportar fuerzas centrífugas inusuales, a las que responde generando respuestas inflamatorias, fibróticas y angiogénicas, lo que complica aún más el desarrollo de la patología. Una etiología sistémica común para la formación de aneurismas de vasos grandes está respaldada por la aparición de múltiples aneurismas de vasos grandes en el mismo paciente5,6.
La evolución natural de los AAI aislados o en asociación con AAA es la expansión continua a lo largo del tiempo con la tasa de expansión observada relacionada con el diámetro de la arteria ilíaca en el diagnóstico inicial; es así que en una revisión retrospectiva que evaluó las tasas de expansión de los aneurismas, los AAI aislados < 3 cm de diámetro se expandieron a una tasa promedio de 1.1 mm por año, mientras que los > 3 cm se expandieron 2.6 mm por año7.
Epidemiología y factores de riesgo
Los AAI aislados son poco frecuentes. Se estima que la incidencia global de AAI solitario en la población general es de aproximadamente el 0.03% y representa aproximadamente del 0.4 al 1.9% de todos los casos de enfermedad aneurismática. Los AAI solitarios son muy raros en la población pediátrica y suelen estar relacionados con trastornos del tejido conectivo. La incidencia de AAI asociada con AAA es mayor, siendo así que presenta una incidencia de aproximadamente el 5% según los estudios de detección, y que aproximadamente el 25% de los pacientes con AAA tienen un AAI8,9.
Los factores de riesgo para el AAI degenerativo son factores de riesgo similares para otros aneurismas degenerativos de grandes vasos (AAA, aneurisma poplíteo), por ende y con base en que la incidencia de AAI se asocia en su mayoría con el AAA, a continuación, se presentan los factores de riesgo para el desarrollo del AAA.
MAYOR EDAD Y SEXO MASCULINO
La prevalencia de AAA es insignificante en menores de 60 años. En cuanto al sexo, se ha demostrado que la prevalencia de AAA en varones es de cuatro a seis veces mayor que la de las mujeres8,9.
TABAQUISMO
Fumar tabaco es el principal factor de riesgo modificable vinculado al desarrollo y a la ruptura de los AAA. Entre el 18 y el 25% de las personas con AAA detectados en el cribado sistemático son fumadores actuales. Los AAA son más de siete veces más frecuentes en los fumadores que en los no fumadores. Varios estudios han demostrado que la duración del tabaquismo está directamente relacionada con un mayor riesgo de desarrollar AAA8,9.
RAZA CAUCÁSICA
Los AAA ocurren con mayor frecuencia entre los caucásicos que en cualquier otra raza. El estudio de cohortes Life Line Screening, que abarcó a más de 3 millones de personas, mostró una disminución del riesgo de desarrollar AAA en los hispanos (odds ratio [OR]: 0.69), los afroamericanos (OR: 0.72) y los asiáticos (OR: 0.72)8,10.
HISTORIA FAMILIAR
Una historia familiar positiva de AAA, particularmente entre familiares de primer grado, se asocia con un mayor riesgo de AAA incluso después de tener en cuenta las similitudes socioeconómicas y ambientales iniciales entre los familiares. Aunque los trastornos genéticos sindrómicos asociados con la formación de aneurismas, como el síndrome de Marfan (defecto de fibrilina 1), el síndrome de Ehlers-Danlos (procolágeno tipo III anormal) y el síndrome de Loeys-Dietz (mutación del factor de crecimiento transformante) están bien definidos, se asocian más comúnmente con aneurismas de la aorta ascendente y toracoabdominal8,9.
ANTECEDENTES DE OTROS ANEURISMAS DE GRANDES VASOS
Las personas con aneurisma de otros vasos grandes, comúnmente en extremidades y arterias carótidas, tienen un mayor riesgo de AAA. Los pacientes con aneurismas femorales o poplíteos tienen un AAA concomitante en hasta el 85 y el 60% de los casos, respectivamente8,9.
COMORBILIDADES
Una variedad de factores de riesgo principalmente ateroscleróticos también se ha asociado con el desarrollo de AAA, incluida la enfermedad arterial coronaria, la enfermedad cerebrovascular, la hipertensión y la hipercolesterolemia. En particular, se ha demostrado de forma fiable que la diabetes mellitus protege contra el AAA9,10.
Manifestaciones clínicas
Las manifestaciones clínicas del AAI dependen de su diámetro y su localización. Los aneurismas más grandes (diámetro > 6 cm) tienen más probabilidades de estar asociados con el desarrollo de síntomas (compresión, trombosis, tromboembolia) o ruptura de la arteria ilíaca10,11.
Aproximadamente la mitad de los pacientes son asintomáticos y el AAI se descubre incidentalmente en el momento de la imagen abdominal/pélvica para una indicación diferente10,11.
Los AAI se comportan más como un AAA con síntomas más comúnmente debidos a la expansión, compresión, erosión de las estructuras circundantes o ruptura en comparación con los síntomas relacionados con la trombosis o la tromboembolia que puede generar un aneurisma poplíteo10,11.
Los síntomas relacionados con la compresión pueden dar lugar a una o más de las siguientes manifestaciones clínicas: retención urinaria, cólico ureteral, pielonefritis e insuficiencia renal (debido a la obstrucción ureteral). La compresión del colon puede causar dolor a la defecación, tenesmo y estreñimiento secundario a la compresión rectal. Finalmente, la compresión del plexo lumbar puede provocar parestesia, paresia, neuralgia ciática o dolor lumbosacro10,12.
Por otro lado, la ruptura del AAI causa dolor agudo en el abdomen y el muslo o la ingle, a menudo acompañado de inestabilidad hemodinámica. La ruptura retroperitoneal puede contenerse, mientras que la intraperitoneal puede conducir a una rápida hemorragia. Es importante recalcar que las tasas de ruptura a cinco años para el AAI varían del 14 al 70%, y hasta el 33% de los pacientes con aneurismas ilíacos aislados presenta ruptura11,12.
La mortalidad por ruptura de un aneurisma ilíaco es alta, con una tasa de mortalidad de aproximadamente el 30% después de la reparación abierta, los peores resultados se encuentran relacionados con un retraso en su diagnóstico. La endoprótesis endovascular para la reparación de emergencia ha reducido las tasas de mortalidad perioperatoria10,11.
Diagnóstico
El diagnóstico del AAI se hace con base en una anamnesis adecuada, tomando en consideración los factores de riesgo del paciente y/o la presentación clínica9-11.
Es necesario que el examen físico incluya un examen abdominal, un examen rectal y un examen arterial periférico completo para identificar sospechas de AAI según la presencia de factores de riesgo o el diagnóstico de otro aneurisma de vaso grande. Aunque puede palparse una masa pulsátil que confirme el diagnóstico en el 70% de los casos, la ausencia de esta no excluye un AAI. Además, un soplo audible también puede indicar la presencia de un AAI10,11.
Una vez que exista la sospecha diagnóstica de un AAI con base en los factores de riesgo y el examen físico, las imágenes proporcionan información valiosa para su confirmación11,12.
La ecografía abdominal y pélvica es la prueba de detección de elección para pacientes asintomáticos, es una buena técnica no invasiva para demostrar la enfermedad de la arteria ilíaca, pero las imágenes pueden verse limitadas si los vasos ilíacos son tortuosos o profundos, y el gas intestinal suprayacente puede dificultar el examen, además de que la ubicación precisa del aneurisma puede ser difícil de determinar en la ecografía11,12.
Por otro lado, para pacientes con síntomas, la tomografía computarizada (TC) abdominal y pélvica proporciona un diagnóstico más preciso. En concreto, la angiografía por TC es muy precisa para el diagnóstico de AAI y proporciona detalles extensos de la anatomía aortoilíaca (Fig. 2). También permite la caracterización de AAA coexistentes u otros aneurismas de arterias periféricas. Su inconveniente es la necesidad de uso de medio de contraste intravenoso y la exposición a radiación12,13.
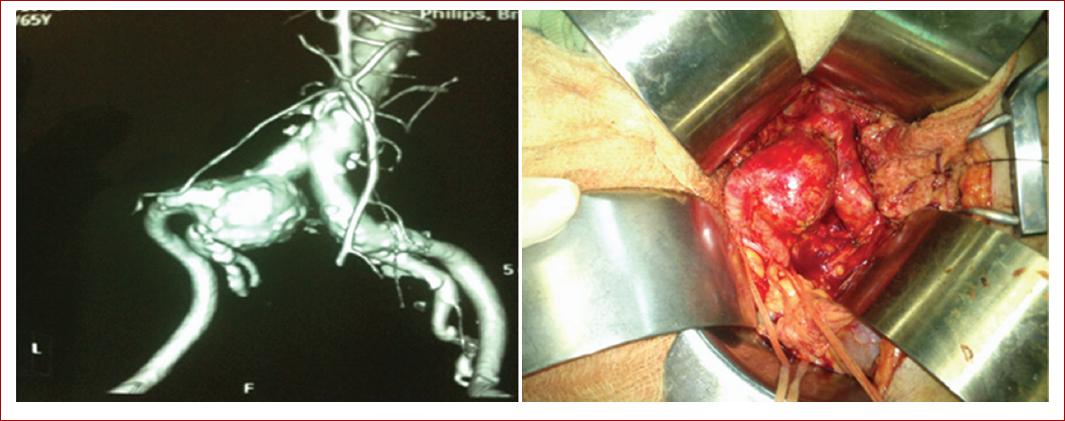
Figura 2 A: angiografía por tomografía computarizada que muestra un aneurisma aislado de la arteria ilíaca común derecha. B: fotografía intraoperatoria que muestra un aneurisma de la arteria ilíaca común derecha (tomada de Goyal et al., 20143).
Finalmente, cabe recalcar que la resonancia magnética (RM) es igual de eficaz que la TC para dar un diagnóstico preciso y detalles anatómicos, pero debido a su costo no suele usarse como estudio de imagen para el diagnóstico y seguimiento del AAI12,13.
Manejo
Es importante mencionar que el diagnóstico temprano, la vigilancia estricta de los aneurismas ilíacos pequeños y la reparación de los aneurismas ilíacos sintomáticos y más grandes reducen la morbilidad y la mortalidad asociadas con el AAI14,15.
El AAI asintomático se maneja de forma conservadora con estudios de imagen seriados (a intervalos de seis meses) o se repara. Un abordaje conservador es apropiado para los AAI asintomáticos pequeños y en aquellos pacientes con aneurisma sintomático que tienen una esperanza de vida baja o un estado funcional limitado. La reparación electiva de estos se basa en el riesgo de ruptura, que depende del tamaño del aneurisma (diámetro > 3 cm o incluso hasta 3.5 cm) y la tasa de expansión esperada del aneurisma en relación con la expectativa de vida del paciente; así como también la presencia de otros aneurismas y el riesgo de ruptura asociado con ellos, particularmente el AAA, también influye en la toma de decisiones (Fig. 3)14,15.
Además de la decisión del manejo expectante o la reparación del AAI, es fundamental el tratamiento para controlar los factores de riesgo de enfermedad cardiovascular14,15.
Por otro lado, para la elección de la reparación de urgencia o electiva se toman en cuenta las tasas de expansión (aproximadamente 1 mm/año para un aneurisma de 1 cm y 3 mm/año para un aneurisma de 3 cm), el riesgo de ruptura y la alta tasa de mortalidad asociada con la emergencia en comparación con la reparación electiva; por ende, se indica la reparación quirúrgica en casos de ruptura, un AAI sintomático (dado que los pacientes que presentan síntomas generalmente tienen aneurismas más grandes que tienen un alto riesgo de ruptura), un AAI de rápida expansión, un AAI asintomático > 3 cm y finalmente, en la reparación de un AAA coexistente14,16.
Para la reparación electiva del AAI en pacientes con anatomía aortoilíaca adecuada, de acuerdo con las guías de la Sociedad Vascular, se indica la reparación endovascular sobre la reparación quirúrgica abierta; esto debido a que aunque las tasas de permeabilidad y mortalidad de la arteria ilíaca primaria no son significativamente diferentes entre la reparación abierta y la endovascular. La reparación endovascular se asocia con una morbilidad perioperatoria significativamente menor, una ventaja importante dado que estos pacientes son mayores y con frecuencia tienen comorbilidades importantes, además de que se asocia con una estancia hospitalaria más corta, una disminución del tiempo operatorio y reducción de la pérdida de sangre14,16. Otras ventajas del manejo endovascular son que se evita un daño a los nervios simpáticos y parasimpáticos (o que resulta en disfunción eréctil o eyaculación retrógrada), y se evita también la interrupción de los vasos linfáticos15,16.
Las principales desventajas de la reparación endovascular son la necesidad de administración de contraste intravenoso y de vigilancia por imágenes de por vida, que pueden aumentar el riesgo de disfunción renal y secuelas relacionadas con la radiación, respectivamente15,16.
A pesar de que no existen ensayos aleatorizados que comparen la reparación endovascular ilíaca (REVI) (Fig. 4) vs. la reparación abierta, Zhorsel et al. (2019) concluyen que los AAI pueden tratarse de forma segura y eficaz con REVI o reparación abierta en cuanto a morbilidad, mortalidad y supervivencia a largo plazo a los 30 días, aunque la ausencia de reintervención es significativamente menor después de REVI16,17.
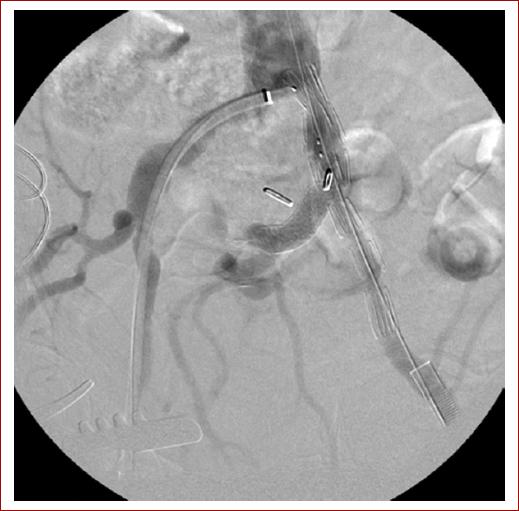
Figura 4 Reparación de aneurisma de la arteria ilíaca común con un dispositivo de endoinjerto ramificado ilíaco. La endoprótesis se extiende hacia las arterias ilíacas interna y externa (tomada de Perini et al., 202120)
En casos de ruptura de AAI, las tasas de mortalidad son más bajas en pacientes sometidos a REVI en comparación con la reparación abierta; sin embargo, esta última se elige más frecuentemente para la reparación de un AAI roto debido a la inestabilidad hemodinámica del paciente16,17.
La reparación abierta puede ser preferible si la preservación de la AII es crítica para el flujo pélvico con el fin de evitar la claudicación glútea, dado que mantener el flujo en la AII utilizando los dispositivos endovasculares disponibles sigue presentando desafíos técnicos, aunque dentro del enfoque de la REVI tanto el dispositivo de extensión de rama ilíaca (DERI) como la técnica de injerto paralelo (sándwich [(PG-ST]) han demostrado ser enfoques seguros y válidos17,18. Sin embargo, mientras que el DERI se ha establecido como un procedimiento duradero, faltan datos a mediano plazo sobre el rendimiento de los PG-ST y se requieren más estudios para certificar la durabilidad de este último procedimiento17,18.
La reparación abierta también puede ser superior para descomprimir el saco del aneurisma y aliviar los síntomas de compresión relacionados con los grandes AAI17,18.
Es importante la preparación previa a la cirugía del paciente con AAI, siendo así que en estos pacientes está indicada la tromboprofilaxis (dado el riesgo moderado a alto de trombosis venosa profunda), así como también la administración de antibióticos profilácticos y en caso de pacientes con nefropatía de base, la utilización de estrategias para reducir el riesgo de la nefrotoxicidad inducida por el contraste19.
Con respecto a la reparación abierta, esta depende del segmento del árbol ilíaco afectado (AIC, AII o AIE) y de la presencia de un AAA coexistente. Los pacientes con aneurismas bilaterales de la AIC o pacientes con AAA coexistente se tratan con la colocación de un injerto aorto-biilíaco o aorto-bifemoral20.
Los aneurismas aislados de la AIC pueden repararse sin exponer y pinzar necesariamente la aorta, siempre que la AIC proximal tenga una calcificación mínima, tenga un diámetro normal o, de lo contrario, pueda exponerse y pinzarse de manera segura. Evitar la disección aórtica y el pinzamiento también elimina la isquemia de la extremidad inferior contralateral, reduce el riesgo de complicaciones cardiacas y pulmonares y acorta el periodo de recuperación20,21.
Finalmente, el tratamiento quirúrgico de pacientes con un aneurisma de la AII puede consistir en endoaneurismorrafia con interposición de injerto (apertura del saco del aneurisma y colocación de un injerto), aneurismectomía (resección del aneurisma) o cirugía interna proximal y ligadura distal de la arteria ilíaca (Fig. 5)22.
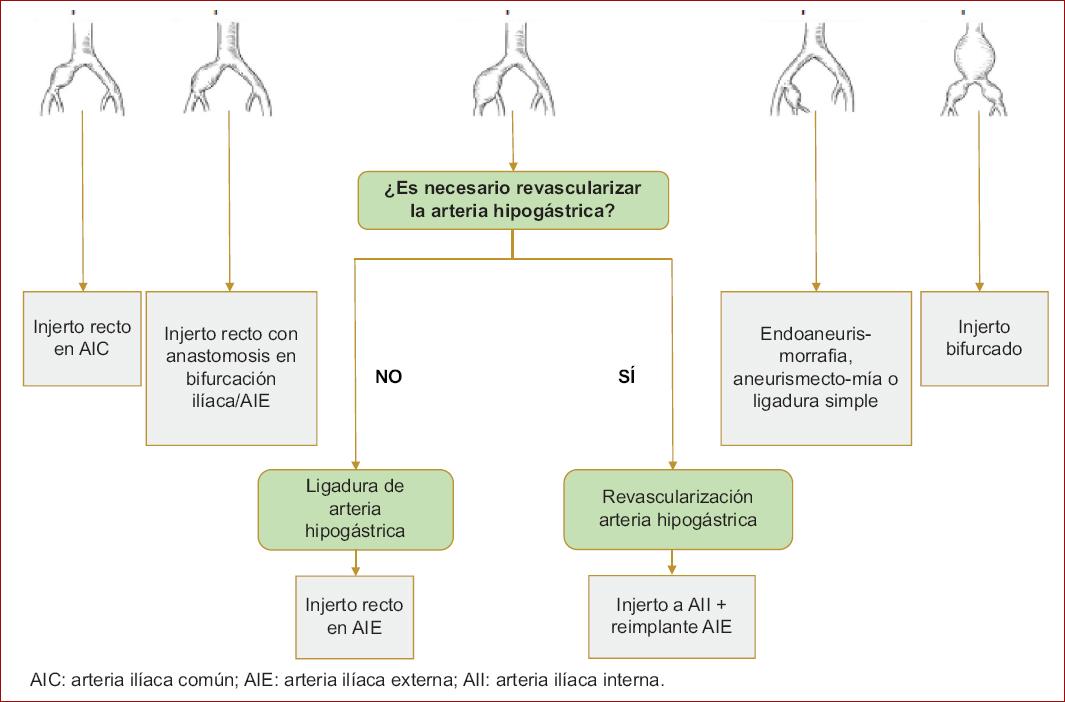
Figura 5 Opciones quirúrgicas de reparación mediante cirugía abierta, según el tipo de aneurisma ilíaco (tomada de Ballesteros, 201724).
Desde la introducción de las técnicas endovasculares, la reparación de los AAI se ha incrementado de forma exponencial. Hoy en día la reparación endovascular es la forma predominante de tratamiento de los AAI, y su hegemonía se justifica por su menor morbimortalidad. Por otro lado, los factores que influyen en el abordaje endovascular incluyen la longitud de la arteria normal proximal y distal al aneurisma, compromiso de la AII, enfermedad aneurismática bilateral vs. unilateral y presencia o ausencia de un AAA coexistente. El procedimiento específico puede implicar la colocación de una endoprótesis aórtica bifurcada o la colocación de una endoprótesis ilíaca aislada, cada una con o sin embolización complementaria de la AII22,23.
Cuando el aneurisma ilíaco se asocia a un AAA se realiza una reparación conjunta mediante una endoprótesis bifurcada con sellado distal en AIC. Si esta es aneurismática a nivel del ostium de la arteria hipogástrica, el sellado ha de extenderse a la AIE. En este caso hay varias opciones endovasculares, en relación con el manejo de la AII: a) técnicas que sacrifican la AII (cobertura simple, embolización de la hipogástrica selectiva y no selectiva)23, y b) técnicas que preservan la AII (ligadura con revascularización quirúrgica, técnica sándwich, DERI)23,24.
En la reparación combinada de un AAA y un AAI de pequeño tamaño (< 32 mm) puede realizarse la técnica bell-bottom manteniéndose permeable la AII. Esta técnica consiste en implantar una endoprótesis corta de mayor calibre por dentro del extremo final de la rama ilíaca. En cualquier caso, se requiere una zona final de la AIC aceptable y de longitud suficiente para garantizar el sellado distal23,24.
Con la técnica sándwich, dos stent-grafts, dispuestos en paralelo y por dentro de la parte final de la rama ilíaca endoprotésica, se extienden, uno hacia la AIE y el otro hacia la AII; la endoprótesis principal termina en la AIC, inmediatamente por encima de la bifurcación. Aunque existen pocas series publicadas y con seguimientos cortos, los resultados de esta técnica en términos de permeabilidad son más que aceptables23,24.
Como se discutió anteriormente, las ramas ilíacas representan una opción de tratamiento eficaz. Sin embargo, estos dispositivos tienen criterios anatómicos estrictos (longitud de AIC > 50-55 mm, diámetro a nivel de bifurcación > 18 mm, ausencia de tortuosidad ilíaca excesiva, etc.), lo que puede limitar su aplicabilidad. Tielliu et al., en una serie de 59 pacientes, reportaron que solo el 52% de los pacientes con aneurismas aortoilíacos o ilíacos aislados era morfológicamente aptos para rama ilíaca25.
Este dispositivo presenta un cuerpo principal que se extiende hasta la AIE con una rama lateral que encaja en la arteria hipogástrica, de modo que se mantiene el flujo anterógrado a la AII pero excluyéndose del saco aneurismático. A diferencia de otras técnicas que también preservan la AII, como la bell-bottom o la técnica sándwich, no compromete la zona de sellado en la AIC, siguiendo el principio vascular de extender la reparación de arteria sana proximal a arteria sana distal24,25.
Seguimiento
La vigilancia continua es importante para controlar las endofugas, el agrandamiento del saco o la migración del stent. Después de la reparación de un AAI, se debe realizar una evaluación anual que incluya un examen vascular completo para identificar el desarrollo de otros aneurismas de grandes vasos26.
La vigilancia de por vida es necesaria para los pacientes tratados con técnicas endovasculares. La angiografía por TC y las mediciones del índice tobillo-brazo deben realizarse a los 30 días, seis meses y un año. Si no se observan problemas al año, el seguimiento puede limitarse a una TC anual o una ecografía abdominal para evaluar la permeabilidad de la endoprótesis, identificar cualquier endofuga y evaluar los cambios en el diámetro del saco del aneurisma. Si hay un aumento en el diámetro del saco del aneurisma o el paciente desarrolla síntomas, puede estar indicada una vigilancia más frecuente o una arteriografía (Fig. 6)26.
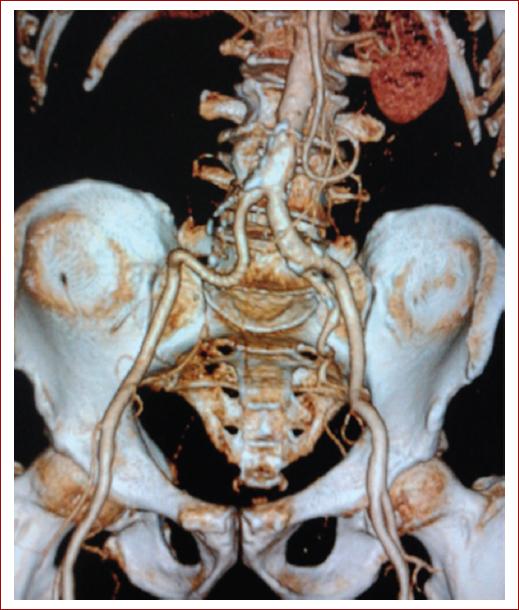
Figura 6 Angiografía por tomografía computarizada postoperatoria que muestra injerto permeable (tomada de Goyal et al., 20143).
Conclusiones
El AAI se define cuando un diámetro es 1.5 veces el diámetro normal de la arteria. Se asocian más estrechamente con el aneurisma de la aorta abdominal. Los factores de riesgo para un AAI verdadero son similares a otros aneurismas degenerativos de vasos grandes e incluyen tabaquismo, hipertensión, sexo masculino, edad avanzada y otros aneurismas de vasos grandes.
Los AAI a menudo se diagnostican de manera incidental como resultado de pruebas de imagen realizadas en pacientes que están siendo evaluados por otros problemas, como dolor abdominal o pélvico, otro aneurisma o enfermedad arterial periférica. Los AAI se diagnostican de manera confiable mediante ecografía, TC o RM.
El AAI se puede reparar mediante una variedad de técnicas abiertas o endovasculares. Los factores que influyen en la elección de la reparación incluyen el segmento del árbol ilíaco que está afectado (AIC, AII o AIE), AAA coexistente, longitud de la arteria normal proximal y distal al aneurisma, afectación de la AAI, aneurismas bilaterales vs. unilaterales, comorbilidades del paciente y recursos disponibles en el centro de tratamiento.











 nueva página del texto (beta)
nueva página del texto (beta)