Introducción
Antecedentes
La enfermedad de Buerger o tromboangeítis obliterante fue descrita por Leo Buerger en 1908, mientras trabajaba en el Hospital Monte Sinaí de Nueva York. Describió a detalle los hallazgos patológicos descritos de una nueva enfermedad con progresión inusual vasooclusiva presentada en 11 extremidades amputadas de jóvenes polacos, rusos e inmigrantes judíos. Con base en sus hallazgos, llamó a la enfermedad tromboangeítis obliterante, para distinguirla de la arterioesclerosis obliterante o síndrome de Winiwarter-Buerger, sugiriendo «un nuevo crecimiento de tejido en la capa íntima»1.
Hoy en día, continúa siendo una enfermedad de etiología desconocida, sin embargo, se atribuye su patogenia a diversos mecanismos, sobre todo de tipo autoinmune, proinflamatorios y estados de hipercoagulabilidad. Implica la afección de los vasos distales de las extremidades, a través de un proceso no ateroesclerótico, con fisiopatología inflamatoria y trombótica, siempre asociada a tabaquismo como el principal factor de riesgo potencial.
Es más frecuente en varones que en mujeres, puede ser causada por una bacteria conocida como Enterobacter cloacae y es una lesión en la que el tabaquismo juega un papel primordial, hasta el punto de que el abandono del tabaco mitiga o incluso detiene de una forma radical la evolución de la enfermedad. Es más frecuente en poblaciones mediterráneas, vascas y asiáticas. Su relación con haplotipos y posible componente genético es discutido.
En sus etapas iniciales, suele manifestarse como una lesión vascular con infiltración neutrofílica transmural. Se cree que el primer evento es la activación de las células presentadoras de antígeno posterior a daño endotelial producido por antígenos desconocidos (posiblemente glicoproteínas del tabaco). Se producen reacciones humorales y celulares que generan oclusión trombótica de los vasos, restringido a la capa íntima de las arterias, lo que define la enfermedad como una endarteritis, resultado de la infiltración de la íntima por células T, que causan su oclusión y que consiste en el hallazgo patognomónico de la enfermedad.
Histológicamente se genera una serie de cambios a nivel arterial dependiendo la fase de progresión de la enfermedad:
En su etapa aguda existe una panvasculitis dentro de las pequeñas y medianas arterias (1-5 mm de diámetro) y de las venas superficiales, generación de trombos arteriales con microabscesos.
En la fase subaguda existe una organización progresiva de los trombos oclusivos, la recanalización parcial o desaparición de los microabscesos y el depósito de factores de complemento y de inmunoglobulinas a lo largo de la lámina elástica.
Finalmente, en la fase crónica, los trombos oclusivos se reorganizan, existe importante vascularización de la capa media, fibrosis perivascular, mientras que existe una preservación de la arquitectura de las paredes de los vasos en todas sus etapas.
La enfermedad se suele presentar sobre la tercera o cuarta décadas de la vida, manifestándose en forma de claudicación o con lesiones necrosantes digitales que pueden evolucionar a la gangrena y precisar amputación. Igualmente afecta a venas superficiales de tobillos y pies, y origina tromboflebitis superficiales.
Diagnóstico
El diagnóstico es predominantemente clínico. Deben considerarse factores como la presencia de isquemia, necrosis o ulceraciones en la región distal de las extremidades, antecedente de tabaquismo, edad entre 30 y 50 años, utilizando criterios de exclusión como ateroesclerosis, enfermedad autoinmune, estado de hipercoagulabilidad o traumatismo.
Suelen utilizarse los criterios de Shionoya (Tabla 1) para el diagnóstico, aunque el estándar de oro continúa siendo la histopatología, con la demostración de células gigantes en la periferia de un trombo.
Tabla 1 Criterios diagnósticos de Shionoya en enfermedad de Buerger
| Criterios diagnósticos de Shionoya |
|---|
| Antecedente de tabaquismo |
| Inicio de la enfermedad antes de los 50 años de edad |
| Oclusiones arteriales infrapoplíteas |
| Cualquier compromiso en los miembros superiores o flebitis migratoria |
| Ausencia de factores de riesgo ateroescleróticos diferentes al tabaquismo |
Tratamiento
En su tratamiento es imprescindible el abandono del tabaco. La enfermedad de Buerger mejora radicalmente con ello, y es, por tanto, la piedra angular. Por desgracia, la mayoría de estos pacientes son grandes fumadores de difícil deshabituación. El resto de los procedimientos, como simpatectomía, terapia con prostaglandinas y otras renacientes opciones terapéuticas son elementos secundarios de eficacia variada.
Cuando ya existe compromiso isquémico de las extremidades, la abstinencia del tabaquismo suele ser por sí sola una medida insuficiente para aliviar el dolor en reposo y lograr la cicatrización de las heridas, por lo que deben establecerse otras medidas de tipo médico, quirúrgico o inclusive endovasculares para restaurar de manera adecuada el flujo sanguíneo requerido para la preservación de la extremidad.
Su pronóstico es relativamente bueno con el abandono del tabaco. En caso contrario, su evolución implica la amputación de las extremidades inferiores e incluso dedos de la mano. De acuerdo con la literatura, existe un riesgo de de amputación mayor del 25% a los 5 años, del 38% a los 10 años y del 46% a los 20 años2.
En la actualidad, a las opciones terapéuticas no invasivas se ha agregado el tratamiento con prostaglandinas en infusión intravenosa (p. ej., alprostadil 60-120 mcg/día por vía intravenosa por al menos 28 días), que mejora sustancialmente el estado de Rutherford en los pacientes con enfermedad de Buerger, disminuye el dolor y evita amputaciones mayores3. Estas maniobras generalmente se reservan para isquemias críticas no revascularizables.
La terapia endovascular con angioplastia transluminal percutánea ha tomado auge en recientes fechas como una opción terapéutica válida en pacientes con Buerger. En algunas series se evidencian resultados favorables, con una tasa de éxito a los 12 meses de hasta el 86.7% en salvamento de extremidades (LSR, limb salvage rate) y de hasta 66.7% en la mejora de la sintomatología, con una baja tasa de complicaciones, por lo que hoy en día resulta un procedimiento seguro y eficaz para la preservación de las extremidades4.
Resultados
En la tabla 2 resumimos las series de casos más extensas disponibles en la literatura de intervención por vía endovascular. Esta alternativa terapéutica mínimamente invasiva se ha expandido en los últimos años y, actualmente, centros con experiencia significativa lo recomiendan como la primera opción de tratamiento.
Tabla 2 Resumen de las características clínicas y resultados de las series de casos en la literatura
| Autor | Año | Número de pacientes | Edad | Género | Signos/síntomas | Tratamiento | Seguimiento | Resultados |
|---|---|---|---|---|---|---|---|---|
| Ghoneim BM | 2019 | 39 | 25-30 | N/A | N/A | Endovascular | 12 meses | 86.7% LSR |
| Kim DH | 2018 | 44 | 40 ± 9.6 | 43 masculino | Claudicación severa e isquemia crítica | Endovascular | 29 meses | 83.3% LSR al año y 67.9% LSR a los 3 años |
| Yuan L | 2014 | 2 | N/A | Masculino | N/A | Endovascular | 12 meses | 100% |
| Stoner MC | 2016 | 58 | 38 (21-50) | 55 masculino, 3 femenino | Cianosis, dolor, gangrena | 15 quirúrgico, 4 endovascular, 33 simpatectomía lumbar, 8 simpatectomía torácica | 12 | 20% requirió amputaciones |
| Kawarada | 2013 | 1 | 38 | Femenino | Infección de herida con pérdida de tejido, dolor severo, oclusión total femoropoplítea | Endovascular | 5 meses | Cicatrización completa |
| Graziani L | 2012 | 20 | 41.7 ± 1.7 | Isquemia crítica | Endovascular | 23 meses | 95% LSR | |
| Yuan L | 2014 | 9 | 35 (24-47) | Masculino | Claudicación severa, dolor en reposo, úlceras isquémicas | Endovascular | 20.9 meses | 100% LSR |
| Aragon Sanchez J | 2012 | 1 | 41 | Masculino | Isquemia crítica, dolor en reposo, úlcera del primer ortejo | Endovascular | 21 meses | 100% LSR |
| Kawarada O | 2014 | 1 | NA | Masculino | Falla de bypass | Endovascular | 12 meses | 100% LSR |
| Jun HJ | 2014 | 1 | NA | Masculino | Dolor en reposo, cianosis | Endovascular | 12 meses | 100% LSR |
| Kawarada O | 2015 | 1 | NA | Masculino | Isquemia crítica | Endovascular | 12 meses | 100% LSR |
| Lavie G | 2015 | 1 | 19 | Masculino | Dolor, cianosis | Endovascular | 9 meses | 100% LSR |
| Kilickesmez O | 2015 | 1 | 44 | Masculino | Claudicación intermitente, dolor severo | Endovascular | 6 meses | 100% LSR |
| Saravana K | 2015 | 3 | Na | Masculino | Isquemia crítica | Endovascular | 12 meses | 100% LSR |
| Kaçmaz Fehmi | 2016 | 1 | 42 | Masculino | Dolor en reposo y úlceras | Endovascular | 12 meses | 100% LSR |
| Lee JH | 2016 | 1 | NA | Masculino | Isquemia crítica | Endovascular | 12 meses | 100% LSR |
| Choi-Young | 2016 | 1 | 47 | Masculino | Dolor y úlcera | Endovascular | 12 meses | 100% LSR |
| Tomohiko Taniguchi MD | 2017 | 1 | 26 | Masculino | Dolor en reposo y ulceración | Endovascular | 12 meses | 100% LSR |
| Kawarada O | 2017 | 20 | 25 ± 8 | 16 masculino 4 femenino | Isquemia crítica y claudicación | Endovascular | 45 meses | 100% LSR |
| Ye K | 2017 | 75 | 25-40 | Masculino | Isquemia crítica | Endovascular | 3 años | 92.9% LSR |
| Tang J | 2017 | 30 | 46 (42-51.5) | Masculino | Isquemia crítica | Endovascular | 24 meses | 100% LSR |
| Li FQ | 2016 | 13 | 45 (36-53) | Masculino | Isquemia crítica | Endovascular | 46 meses | 63.9% LSR |
| Hafezi S | 2017 | 13 | NA | Masculino | Dolor en reposo, úlcera isquémica y gangrena | Endovascular | 6 meses | 92% LSR |
LSR: limb salvage rate.
Discusión
A continuación presentamos el caso de un hombre de 31 años con isquemia crítica de la extremidad, tratado de manera exitosa con angioplastia simple poplíteo-tibial.
Presentación de un caso exitoso y revisión de la literatura que apoya al tratamiento endovascular como una alternativa válida en el tratamiento de la enfermedad de Buerger.
Presentación de caso
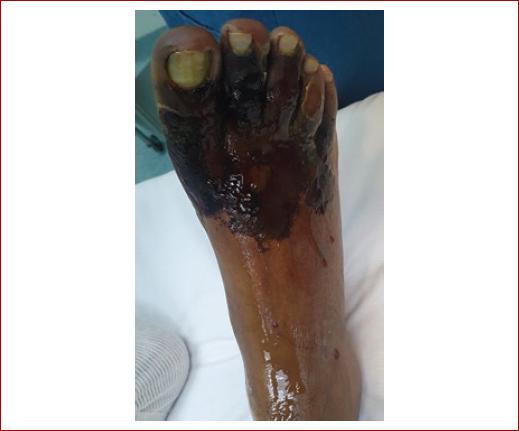
Paciente de sexo masculino de 31 años, previamente sano. Tabaquismo positivo, índice tabáquico de 6. Acude al mes de evolución, con necrosis irreversible de los dedos y dorso del pie en el miembro pélvico derecho (Fig. 1), y dolor isquémico en reposo.
A la exploración física se aprecia necrosis digital de los cuatro primeros dedos, pulsos femorales presentes y adecuados de manera bilateral, y pulsos poplíteos y distales ausentes. Al Doppler de onda continua, en el miembro pélvico derecho, pobre flujo poplíteo y ausencia de flujos distales, con índices tobillo-brazo de 0.2, derecho, y 0.6, izquierdo. Sin otros hallazgos de importancia.
En los estudios de laboratorio destacaron leucocitosis de 14.4 10^3/μl y trombocitosis de 546 10^3/μl. Un ultrasonido Doppler dúplex arterial confirmó ausencia de flujo a partir de la arteria poplítea, sin aparente recanalización distal. Con estos hallazgos, se opta por ofrecer manejo endovascular.
En la sala de hemodinamia, se realiza acceso ecoguiado anterógrado femoral común. La angiografía diagnóstica corrobora oclusión total crónica de la arteria poplítea en su segunda y tercera porciones (P2, P3) (Fig. 2), y de tres vasos tibiales, sin identificar adecuados vasos de salida (Fig. 3). Adicionalmente, se documentan colaterales «en tirabuzón», características (aunque no patognomónicas) de esta patología.

Figura 2 Oclusión completa de la arteria poplítea, P2 y P3. Colaterales «en tirabuzón». No se identifican los orígenes de las arterias tibiales.
Utilizando guía hidrofílica 0.014 y catéter de soporte, se exploró la arteria tibial anterior, sin lograr franquear oclusiones hasta el pie. Se realizaron intentos no exitosos de acceso retrógrado ecoguiado pedio y tibial posterior. Finalmente, se decide realizar angioplastia simple de la arteria tibial anterior y de la arteria poplítea. Se realiza angiografía de control, en la que se verifica reclutamiento de colaterales previamente no observadas (Fig. 4) y se detecta disección segmentaria de la arteria poplítea y tronco tibioperoneo no limitante de flujo.

Figura 4 Recanalización de la arteria poplítea, con recoil de su porción proximal y estenosis residual significativa del tronco tibioperoneo. Abundante reclutamiento de colaterales.
Al día siguiente y en el contexto de la infección sistémica, se realiza amputación transmetatarsiana en guillotina, sin complicaciones, verificando una adecuada perfusión del lecho cruento (Fig. 5). Se maneja en el postoperatorio con rivaroxabán 10 mg cada 24 horas por vía oral, cilostazol 100 mg vía oral y ácido acetilsalicílico 100 mg cada 24 horas por vía oral. Se egresa al paciente sin complicaciones.
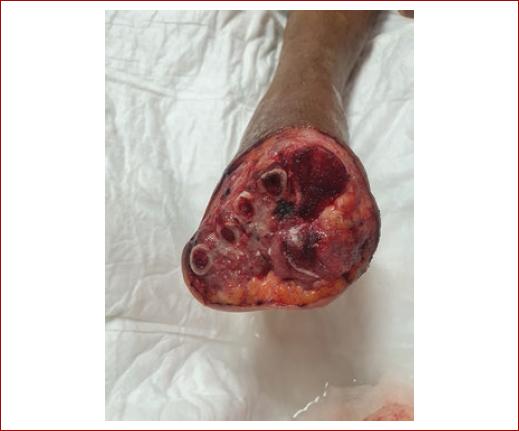
Figura 5 Amputación transmetatarsiana en guillotina, sin sangrado pulsátil, pero con adecuada viabilidad del tejido y microperfusión.
Seis meses después de la revascularización, el paciente continúa con evolución satisfactoria de la herida, sin recidiva del dolor, con adecuada granulación y sin reincidencia del dolor isquémico (Fig. 6). A la realización de Doppler de onda continua en miembros pélvicos se obtiene un índice tobillo -brazo de 0.6 derecho y de 0.6 izquierdo.
En el caso en cuestión, la ausencia de vasos de salida durante la angiografía inicial y la imposibilidad de ganar acceso ni anterógrado ni retrógrado conferían, en opinión nuestra, un pronóstico sombrío al paciente. La presencia de estenosis largas, fibróticas y de difícil recanalización subrayan la limitación en el armamento endovascular para el tratamiento de esta y otras arteritis fibróticas (p. ej., enfermedad de Takayasu), cuya fisiopatología está exenta de ateroesclerosis. Esto complica el manejo intervencionista, ya que la mayoría de los dispositivos actuales han sido diseñados y probados en estenosis ateroesclerosas. La incapacidad de recanalizar la arteria por vía subintimal y las características duras y poco elásticas de las arterias afectadas recuerdan más a las estenosis de venas centrales que a un padecimiento arterial puro.
A pesar de un resultado técnico cuestionable, la evolución clínica de nuestro paciente nos impulsó a reportar nuestra experiencia y a revisar la literatura, en donde centros de alto volumen presentan a la terapia endovascular como una opción atractiva de tratamiento.
La terapia endovascular con angioplastia transluminal percutánea es una opción terapéutica efectiva en pacientes con enfermedad de Buerger. En estudios recientes se han documentado resultados favorables, con una tasa de éxito al año de hasta el 86.7% en salvamento de extremidades (LSR) y 66.7%, de igual manera. En el caso de nuestro caso clínico, logró realizarse salvamento de la extremidad afectada con una remisión completa de la sintomatología, así como mejora en la calidad de vida de nuestro paciente, el cual hasta este momento no ha presentado complicaciones.
Conclusión
La enfermedad de Buerger es una entidad poco frecuente, que requiere un alto índice de sospecha. La necrosis distal es una manifestación clínica grave, que obligará a ofrecer tratamiento invasivo. En nuestro caso, la realización de dilataciones con balón demostró ser efectiva en la resolución de síntomas a 6 meses de seguimiento, con una adecuada evolución clínica a pesar de no haber reconstituido flujo lineal hasta el pie.
A manera comparativa se incluye en la tabla 2 los principales casos tratados de manera exitosa con terapia endovascular5-26.
Por lo tanto, «es importante enfocarnos en las opciones de tratamiento que han demostrado resultados prometedores y óptimos en instituciones de tercer nivel de atención como la terapia endovascular»27. El tratamiento endovascular debe considerarse dentro de las primeras opciones terapéuticas para esta compleja patología.











 nueva página del texto (beta)
nueva página del texto (beta)