Introducción
La diabetes mellitus tipo 2 (DM2) afecta a aproximadamente 415 millones de personas en el mundo1, con una prevalencia estimada del 9.2% en la población adulta mexicana2. La retinopatía diabética (RD) es una complicación microvascular de esta enfermedad y está presente en el 70% de los pacientes con DM2 en México3. El edema macular diabético (EMD) ocurre en cualquier etapa de la RD y su incidencia aumenta con la duración de la DM24. Junto con la RD, el EMD constituye una de las principales causas de discapacidad visual y ceguera legal entre los adultos en edad productiva4, lo que representa una carga para el sistema de salud mexicano en la actualidad.
La fotocoagulación con láser era el tratamiento estándar para el EMD antes de la aparición del tratamiento contra el factor de crecimiento endotelial vascular (VEGF), que mejora significativamente los resultados funcionales y anatómicos en comparación con el tratamiento con láser5. Varios estudios multicéntricos han evaluado la eficacia y la seguridad del ranibizumab intravítreo para el EMD. El estudio de fase II RESOLVE demostró la seguridad y la eficacia del ranibizumab mensual en el EMD durante 12 meses, lo que dio como resultado una ganancia de mejor agudeza visual corregida (MAVC) de +10.3 letras del ETDRS desde la situación basal6. El estudio de extensión de RESTORE demostró que el tratamiento individualizado con ranibizumab mejora y mantiene de manera efectiva los resultados funcionales y anatómicos durante más de 36 meses, con un número cada vez menor de inyecciones por año7. Además, el estudio RETAIN mostró la no inferioridad del régimen «tratar y extender» con ranibizumab versus ranibizumab por razón necesaria (PRN) durante 12 y 24 meses8.
Sin embargo, los ensayos clínicos aleatorizados tienen criterios de inclusión y exclusión restrictivos, que podrían limitar su capacidad para representar poblaciones más amplias. Por lo tanto, los datos del mundo real son necesarios para evaluar la efectividad del tratamiento en el entorno clínico, así como para informar del impacto económico tanto de las enfermedades como de las intervenciones en países e instituciones sanitarias específicos9. En este sentido, varios estudios han confirmado la efectividad del ranibizumab en la práctica clínica habitual10-12 y, hasta donde sabemos, no hay estudios que evalúen los resultados clínicos de ranibizumab en pacientes mexicanos con EMD.
Propósito
El objetivo de este estudio fue informar de los resultados visuales y anatómicos de ranibizumab en pacientes con EMD en un entorno del mundo real en México.
Métodos
Diseño del estudio
El presente estudio es un estudio multicéntrico intervencionista, prospectivo, de un solo grupo, abierto, realizado en cuatro hospitales de alta especialidad del Instituto de Seguridad y Servicios Sociales de los Trabajadores del Estado (ISSTE) en la Ciudad de México. Los pacientes recibieron inyecciones intravítreas de ranibizumab en uno o ambos ojos entre enero de 2015 y diciembre de 2015. El estudio fue aprobado por el Comité de Investigación del Centro Médico Nacional 20 de Noviembre del ISSSTE y se adhirió a los principios de la Declaración de Helsinki. Todos los participantes proporcionaron un consentimiento informado por escrito para la participación en el estudio. El estudio se registró con el número 507-2015.
Participantes
Sujetos reclutados ≥ 18 años de edad, hombres y mujeres, con alteración visual debida a EMD. Los pacientes tenían una MAVC basal entre 20/40 y 20/800 (equivalente Snellen), un grosor retiniano central (GRC) basal ≥ 250 µm medido con Cirrus HD - tomografía de coherencia óptica (OCT), estudios fluorangiográficos retinianos y hemoglobina glucosilada (HbA1c) ≤ 14% (130 mmol/mol).
Los pacientes con presencia o sospecha de infección intraocular fueron excluidos del estudio, así como aquellos con isquemia miocárdica o eventos cerebrovasculares 6 meses antes de ingresar en el estudio. Los pacientes con tracción vitreomacular, isquemia macular, cirugía ocular dentro de los 3 meses previos al inicio del estudio, hemorragia vítrea y pacientes que requieren tratamiento concomitante con esteroides, también fueron excluidos.
Los pacientes se retiraron del estudio si requerían cirugía intraocular, se negaban a seguir participando o se perdieron durante el seguimiento.
Intervención
Los pacientes fueron tratados de acuerdo con las directrices institucionales del ISSSTE para el diagnóstico y tratamiento del EMD13. Se administró una dosis de carga de 3 inyecciones mensuales de ranibizumab 0.5 mg (Lucentisâ, Novartis) a todos los pacientes, seguida de un monitoreo mensual que incluyó MAVC y OCT. El tratamiento se suspendía en caso de lograr una visión estable durante al menos 2 meses consecutivos y la resolución del edema. Los criterios de retratamiento incluyeron pérdida de ≥ 5 letras del ETDRS, aumento del GRC ≥ 10% con respecto a la visita anterior y/o edema persistente en las imágenes de OCT, con inyecciones subsiguientes hasta que se lograra una MAVC de 20/20 y/o se mantuviera estable durante 2 meses y/o el GRC fuera de < 250 µm.
Mediciones de resultados
El criterio de valoración clínico primario fue el cambio medio de la MAVC (número de letras obtenidas en la cartilla de agudeza visual del ETDRS) desde la situación basal hasta los 12 meses. Los criterios de valoración secundarios incluyeron el cambio medio del GRC obtenido mediante Cirrus HD-OCT (Carl Zeiss Meditec) desde la situación basal hasta los 12 meses, el tiempo medio para lograr un GRC < 250 µm, el cambio en la puntuación media de la Escala de severidad de la retinopatía diabética (DRSS) del ETDRS, el número de inyecciones intravítreas recibidas durante 12 meses y los factores que afectan los resultados de MAVC y GRC.
Análisis estadístico
Realizamos cálculos de tamaño de muestra para obtener el tamaño de muestra deseado para el estudio. Se realizó un cálculo del tamaño de la muestra para obtener un contraste de hipótesis de la diferencia de medias para los grupos dependientes, una diferencia de medias de 6.2 letras y una desviación estándar de 6.1, según los resultados del estudio RETAIN en su grupo de tratamiento PRN, con una media basal de 63.4 letras ± 11.15, utilizando un valor alfa de 0.05 y un poder de 0.8, lo que resultó en 41 ojos.
Se realizaron pruebas t de Student para comparar las medias de las variables continuas y cuantitativas y la prueba de McNemar X2 para el análisis de las variables dicotómicas. Se usó una curva de supervivencia de Kaplan-Meier para medir la fracción de sujetos que mostraban un GRC < 250 µm durante 12 meses. Se realizaron análisis de regresión logística binaria para determinar la relación entre las variables independientes y los resultados categorizados para MAVC y GRC, es decir, ganancia de MAVC > 10 y < 10 letras, pérdida o no pérdida de letras y GRC > 250 o < 250 µm en el mes 12. Se consideró un valor de p = 0.005 como estadísticamente significativo para todos los análisis. Se utilizó el software SPSS versión 21 (IBMâ).
Resultados
Características basales
Se incluyeron un total de 48 ojos de 34 pacientes. Diecinueve eran hombres (56%), la edad media de todos los pacientes fue de 61.6 años, con una duración media de la DM2 de 16.8 años (rango 1-33) y un valor medio de HbA1c de 7.9% (rango 5.5-13.1%) (63 mmol/mol, 37-120). La media basal de MAVC fue de 19 letras (rango 5-47) y la media basal de GRC fue de 362 µm (rango 215-839). El retiro del consentimiento fue la razón más común para el retiro del seguimiento; ocho pacientes fueron eliminados.
En la tabla 1 se resumen las características clínicas basales.
Tabla 1 Características basales
| Característica | Valor | Rango |
|---|---|---|
| Edad, años ± DE | 61.65 ± 7.9 | 35-75 |
| Género, número | ||
| Hombres (%) | 19 (56%) | |
| Mujeres (%) | 15 (44%) | |
| Duración de la DM2, años | 16.8 ± 5.4 | 1-33 |
| MAVC, letras ETDRS | 19 ± 14 | 5-47 |
| GRC, mm | 362 ± 98 | 215-839 |
| HbA1c, % (mmol/mol) | 7.9 ± 2.2 (63) | 5.5-13.1 (37-120) |
| Ojos tratados | ||
| Ojo izquierdo (%) | 27 (56.2%) | |
| Ojo derecho (%) | 21 (43.8%) | |
| Total de ojos | 48 | |
DE: desviación estándar; GRC: grosor retiniano central; MAVC: mejor agudeza visual corregida.
Mejor agudeza visual corregida
La media de MAVC después de 12 meses fue de 27.62 letras del ETDRS (rango 3-55). El cambio medio desde la situación basal hasta el mes 12 fue de +8.62 (± 4.3) letras (Fig. 1), lo que muestra una diferencia estadísticamente significativa desde la situación basal (p < 0.001). El valor medio máximo de MAVC (28 letras) se observó después de la tercera inyección de ranibizumab, y se mantuvo hasta el mes 12. Los ojos se clasificaron en tres grupos según los resultados de MAVC en el mes 12 (Tabla 2). El 77.08% de los ojos experimentó mejoría visual (n = 37); el 39.58% del total (n = 19) ganó ≥ 10 letras, mientras que 4.16% (n = 2) no tuvo cambios y el 18.75% (n = 9) perdió entre 1 y 3 letras.
Tabla 2 Clasificación de la mejor agudeza visual corregida (MAVC) final
| Resultados de MAVC | Número de ojos (rango de cambio de MAVC) | Total de ojos (%) |
|---|---|---|
| Mejoría visual | 37 (+4 a +40) | 77.08 |
| ≥ 10 letras ETDRS | 19 | 39.58 |
| ≤ 10 letras ETDRS | 18 | 37.5 |
| MAVC estable | 2 (0) | 4.16 |
| Pérdida visual | 9 (-1 a -3) | 18.75 |
+: ganancia de letras.
-: pérdida de letras.
Grosor retiniano central
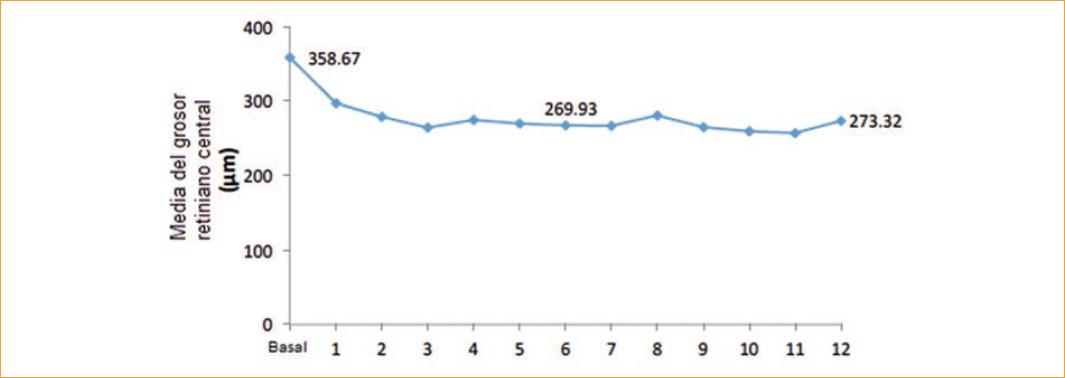
En el mes 12, la media del GRC fue de 273.32 µm, lo que representa una reducción media significativa de 85.34 (± 32.1) µm (23.79%) desde la situación basal (p < 0.001). La figura 2 muestra la media del GRC obtenida cada mes desde la situación basal hasta el mes 12.
La curva de supervivencia de Kaplan Meier (Fig. 3) demostró que el 41.3% de los ojos logró un GRC < 250 µm después de la primera inyección intravítrea, el 62.5%, después de la segunda dosis, y el 67%, al tercer mes, con una mediana de 3.37 meses (IC 95%: 2.42-4.38).
Severidad de la retinopatía diabética
La tabla 3 muestra la distribución de pacientes según la DRSS del ETDRS en la situación basal, a los 6 y 12 meses. En el mes 12 se observó una reducción numérica del porcentaje de pacientes con RD severa no proliferativa en comparación con la situación basal (de 20.83% a 10.41%). De manera similar, el porcentaje de casos de RD proliferativa disminuyó de 18.74% a 8.33%.
Tabla 3 Escala de severidad de retinopatía diabética del ETDRS en la situación basal, a los 6 y 12 meses
| Severidad de la retinopatía diabética | Número de pacientes (%) | ||
|---|---|---|---|
| Nivel numérico del ETDRS | Basal | 6 meses | 12 meses |
| Leve no proliferativa (35) | 0 | 0 | 5 (10.41%) |
| Moderada no proliferativa (47) | 24 (50.00%) | 29 (60.41%) | 33 (68.75%) |
| Severa no proliferativa (53) | 10 (20.83%) | 12 (25.00%) | 5 (10.41%) |
| Muy severa no proliferativa (57) | 5 (10.41%) | 3 (6.25%) | 1 (2.08%) |
| Proliferativa, sin alto riesgo (61) | 7 (14.58%) | 3 (6.25%) | 3 (6.25%) |
| Proliferativa de alto riesgo (71) | 2 (4.16%) | 1 (2.08%) | 1 (2.08%) |
La puntuación media de la DRSS del ETDRS mostró un cambio significativo de 50.59 (±7.9) a 45.79 (± 7.9) en el mes 12 (p < 0.001).
Número de inyecciones
Los pacientes recibieron una media de 6.7 inyecciones de ranibizumab por ojo tratado durante 12 meses. Este número incluye las 3 inyecciones mensuales de la fase de carga y las dosis posteriores de retratamiento PRN. El número total de inyecciones recibidas durante el estudio fue de 323.
Factores que afectan los resultados visuales y anatómicos
El análisis de regresión logística binaria mostró que ninguna de las variables predictoras tuvo un impacto estadísticamente significativo en el resultado de MAVC a los 12 meses (Tabla 4).
Tabla 4 Análisis de regresión logística binaria del resultado de MAVC a los 12 meses
| Variable | Pérdida de letras del ETDRS | Sin pérdida de letras del ETDRS | p (IC 95%) |
|---|---|---|---|
| Género femenino, n (%) | 6 (31.6%) | 13 (68.4%) | 0.29 (1.3-2.34) |
| Edad media, años ± | 56.4 ± 10 | 62.5 ± 6.7 | 0.074 (0.72-1.0) |
| Duración media de DM2, años ± | 18.0 ± 7.29 | 16.5 ± 4.95 | 0.915 (0.82-1.2) |
| Media de estadio basal de la RD, escala ETDRS ± | 50.1 | 50.7 | 0.91 (0.82-1.23) |
| Media de creatinina, mg/dl ± | 1.62 ± 0.78 | 1.25 ± 0.61 | 0.087 (0.73-9.7) |
| Media basal deMAVC, letras del ETDRS ± | 21 ± 15.6 | 18 ± 13.7 | 0.536 (0.91-1.1) |
| Media basal de HbA1c, % ± (mmol/mol) | 8.1 ± 2.1 (65) | 8.5 ± 1.49 (70) | 0.058 (0.16-0.9) |
| Media basal de GRC, μm ± | 335 ± 98 | 364± 99 | 0.844 (0.10-1.6) |
| Número medio de nyecciones | 10 | 6 | 0.562 (0.23-4.5) |
± Desviación estándar.
DM2: diabetes mellitus tipo 2; GRC: grosor retiniano central; MAVC: mejor agudeza visual corregida; RD: retinopatía diabética.
Además, el análisis de regresión logística binaria no encontró una asociación significativa entre ninguna variable y la mejoría visual de > 10 letras o < 10 letras al final del estudio (Tabla 5).
Tabla 5 Análisis de regresión logística binaria de la mejoría de MAVC a los 12 mese
| Variable | Media de MACV | Media de MACV | p (IC 95%) |
|---|---|---|---|
| Cambio > 10 letras | Cambio < 10 letras | ||
| Edad media, años ± | 62.41 ± 7.0 | 62.7 ± 7.0 | 0.626 (0.92-1.1) |
| Género masculino, n | 6 | 13 | 0.581 (0.79-4.1) |
| Duración media de la DM2, años ± | 16.52 ± 5.0 | 16.55 ± 5.0 | 0.187 (0.74-1.0) |
| Media del estadio basal de la RD, escala ETDRS ± | 50.91 ± 6.6 | 50.51 ± 9.24 | 0.980 (0.90-1.1) |
| Media basal de MAVC, letras del ETDRS ± | 18.2 ± 13.16 | 19.75 ± 14.54 | 0.75 (0.87-1.1) |
| Media basal de HbA1c, % ± (mmol/mol) | 8.2 ± 1.56 (66) | 8.7 ± 1.42 (72) | 0.476 (0.49-1.3) |
| Media de creatinina, mg/dl ± | 1.0 ± 0.48 | 1.42 ± 0.67 | 0.057 (0.42-0.98) |
| Media basal de GRC, µm ± | 340.52 ± 61.81 | 388.25 ± 121.59 | 0.102 (0.97-1.39) |
| Número medio de inyecciones | 10.47 | 6.0 | 0.102 (0.97-1.39) |
| Total de ojos | 19 | 18 |
± Desviación estándar.
DM2: diabetes mellitus tipo 2; GRC: grosor retiniano central; MAVC: mejor agudeza visual corregida; RD: retinopatía diabética.
Finalmente, el análisis de regresión logística binaria para el GRC final encontró que el GRC basal fue el único factor asociado significativamente con el grosor macular persistente en el mes 12 (p = 0.032, 95% CI) (Tabla 6).
Tabla 6 Análisis de regresión logística binaria del resultado de GRC a los 12 meses
| Variable | GRC < 250 μm | GRC > 250 μm | p (IC 95%) |
|---|---|---|---|
| Edad media, años ± | 60.37 ± 8.07 | 64.30 ± 7.00 | 0.691 (0.88-32.4) |
| Duración media de la DM2, años ± | 17.5 ± 5.1 | 14.9 ± 5.8 | 0.115 (0.96-1.34) |
| Media de estadio basal de la RD, escala ETDRS ± | 51.70 ± 7.8 | 47.61 ± 7.8 | 0.295 (0.88-1.05) |
| Media de creatinina, mg/dl ± | 1.38 ± 0.10 | 1.14 ± 0.18 | 0.848 (0.86-1.18) |
| Media basal de MAVC, letras del ETDRS ± | 18.97 ± 14.39 | 19.07 ± 13.26 | 0.315 (0.96-1.17) |
| Media de HbA1c, % ± (mmol/mol) | 8.5 ± 1.7 (69) | 8.3 ± 1.1 (67) | 0.182 (0.06-1.67) |
| Media basal de GRC, µm ± | 336.88 ± 66.46 | 420.38 ±136.4 | 0.032 (1.00-1.03) |
| Total de ojos | 35 | 13 |
± Desviación estándar.
DM2: diabetes mellitus tipo 2; GRC: grosor retiniano central; MAVC: mejor agudeza visual corregida.
Discusión
La alta prevalencia de DM2 es un problema de salud pública en México. El EMD es una de las principales causas de pérdida visual en pacientes que viven con DM24. El ISSSTE es una de las instituciones de salud más grandes de México, y brinda tratamiento con ranibizumab a pacientes con EMD clínicamente significativo. Este estudio es el primero en describir los resultados a los 12 meses de la terapia anti-VEGF en 48 ojos de 34 pacientes con EMD en México.
Las características basales en el presente estudio, incluida la duración de la DM2 y los niveles de HbA1c, fueron similares a las informadas en otros estudios clínicos. Nuestros resultados mostraron una ganancia media de 8.62 letras de MAVC desde la situación basal hasta el mes 12, que es similar a la informada en el estudio RETAIN (+7.4 letras del ETDRS en el mes 12 con ranibizumab y 0.5 mg PRN)8. La mejoría visual máxima se observó después de la tercera inyección y se mantuvo en el mes 12. De manera similar, un estudio observacional que evaluó el uso de ranibizumab en la atención clínica de rutina en Suecia informó de ganancias visuales significativas en el 50% de los pacientes con EMD después de 4 meses de tratamiento, que se mantuvieron durante 12 meses12.
En cuanto a los resultados anatómicos, observamos una reducción media de 23.79% del GRC desde la situación basal hasta el mes 12 en el presente estudio. Esto es similar a la reducción del 27.09% que se muestra en el grupo de régimen PRN con ranibizumab del estudio RETAIN a pesar de que el GRC basal no es numéricamente similar en ambos estudios (362 µm frente a 432 µm, respectivamente)8. La curva de supervivencia de Kaplan-Meier encontró que después de recibir tres inyecciones mensuales, el 67% de los ojos tenía un GRC < 250 µm. Esto confirma la importancia de la dosis de carga para lograr el objetivo del tratamiento. Con un 41.3% de los pacientes que muestran una reducción favorable del GRC en el primer mes, podría ser razonable realizar una evaluación preliminar de la respuesta al tratamiento después de recibir la primera inyección de ranibizumab.
Se ha encontrado que los agentes anti-VEGF son beneficiosos en la RD proliferativa14. Además de la mejora visual y los resultados anatómicos en el EMD, en el presente estudio hubo numéricamente menos pacientes que presentaban RD severa no proliferativa y proliferativa a los 12 meses en comparación con la situación basal. La puntuación de la DRSS disminuyó significativamente, de 50.59 a 45.79 (p < 0.001). De manera similar, un análisis post-hoc de los estudios RISE y RIDE encontró que el 56.8% de los pacientes tratados con ranibizumab experimentaron una mejoría de 1 paso o más de la DRSS desde la situación basal hasta el mes 24; el 40% no tuvo cambios y el 3.2% experimentó un empeoramiento de la DRSS15. Además, el 17.1% de los pacientes en el grupo de 0.5 mg de ranibizumab desarrollaron RD proliferativa durante 36 meses en comparación con el 39.1% de los pacientes en el grupo placebo, lo que sugirió que en los ojos tratados con ranibizumab, una mejoría mayor de la DRSS se relaciona con mejores resultados clínicos15.
En nuestro estudio, el tratamiento consistió en tres inyecciones mensuales seguidas de un régimen PRN según lo recomendado por las guías clínicas para el manejo del EMD en el ISSSTE13. El número medio de inyecciones por ojo tratado fue de 6.7 en 12 meses. Esto es consistente con el número de inyecciones informadas por el estudio RETAIN, en el que los pacientes del grupo PRN de ranibizumab recibieron una media de 7 inyecciones en 12 meses8. En el estudio de extensión RESTORE, los pacientes recibieron un número decreciente de inyecciones por año, es decir, 7.9 el primer año; 3.9 el segundo, y 2.9 el tercero7. Por lo tanto, este régimen de tratamiento tiene el potencial de reducir la carga del tratamiento en las instituciones de salud.
Un gran estudio epidemiológico realizado en el Servicio de Oftalmología del Hospital General de México (n = 13,670) encontró que el 71% de los pacientes diabéticos tenía algún tipo de RD, de los cuales el 63% tenía la variante no proliferativa y el 37% RD proliferativa, con 16% de pacientes que presentan EMD en cualquier etapa de la RD3. En contraste, la prevalencia de RD en una gran cohorte de pacientes diabéticos (n = 369,047) en el Reino Unido fue del 43%, de los cuales, el 11% tenía RD proliferativa16. Esto sugiere que la prevalencia de RD y RD proliferativa es mayor en la población mexicana, posiblemente debido a factores genéticos y de estilo de vida, así como a diferencias sustanciales en la detección y el manejo de la DM2 y la RD entre ambos países. La mayoría de los estudios clínicos aleatorizados en EMD se realizaron en países desarrollados; por lo tanto, es importante considerar si la variabilidad de la población ejerce un efecto sobre los resultados clínicos en el EMD. Aunque esta pregunta permanece fuera del alcance de este estudio, exploramos si las características basales de nuestra muestra de pacientes afectaron los resultados del tratamiento en el mes 12.
El análisis de regresión logística encontró una asociación significativa entre el GRC basal y el grosor macular persistente en el mes 12. Por lo tanto, podría ser razonable considerar el GRC basal para determinar la frecuencia óptima de seguimiento y retratamiento en cada paciente. Por otro lado, se ha encontrado que la MAVC basal es un factor predictivo para el resultado final de la MAVC17. En el presente estudio, sin embargo, no encontramos una asociación entre la agudeza visual inicial y final.
Las limitaciones del estudio incluyen el tamaño de la muestra. Se necesitan estudios adicionales con muestras más grandes para determinar los factores de predicción de los resultados de MAVC y GRC.
Conclusión
En este estudio, los pacientes experimentaron una mejoría visual y anatómica después de recibir inyecciones de ranibizumab en un entorno real. Observamos que el seguimiento mensual y el retratamiento individualizado, basados en criterios visuales y anatómicos, dan como resultado desenlaces clínicos potencialmente similares a los informados en los grandes estudios multicéntricos. La adherencia al régimen de PRN también podría ser útil para reducir la carga del tratamiento dentro de las instituciones de salud pública en México. Se necesitan más estudios para determinar la efectividad en una población más amplia, la mejoría de la calidad de vida relacionada con la visión y la rentabilidad de ranibizumab en las instituciones de salud mexicanas.











 nueva página del texto (beta)
nueva página del texto (beta)