Introducción
Determinados tumores sólidos (TS) con frecuencia presentan metástasis a hueso, siendo mama, próstata, pulmón y renal los que conllevan un mayor riesgo de desarrollar metástasis óseas. Se estima que hasta dos tercios de los pacientes con cáncer de mama o próstata en etapa avanzada se verán afectados con metástasis óseas1,2.
Las complicaciones óseas, llamadas también eventos relacionados con el esqueleto (ERE), son comunes en los pacientes con TS en etapas avanzadas e incluyen fracturas patológicas, radioterapia a hueso, compresión medular y cirugía ósea. Los ERE se asocian con un peor pronóstico y generan una carga considerable en morbilidad y mortalidad1,3. Los ERE también provocan pérdidas significativas en la calidad de vida relacionada con la salud, afectando distintos aspectos en las escalas física, emocional y funcional4,5. Además, debido a su elevada frecuencia y al consumo importante de recursos médicos que se destinan para cada caso, los ERE imponen un costo sustancial3,6-8. Es importante destacar que los pacientes con ERE son significativamente más propensos a sufrir un evento subsecuente1.
La aparición de los bifosfonatos ha jugado un papel importante en el manejo de los pacientes con neoplasias malignas avanzadas, ayudando a evitar o al menos retrasar la aparición de ERE9. El ácido zoledrónico (AZ), bifosfonato de tercera generación, ha demostrado eficacia y seguridad10. No obstante, todavía un alto porcentaje (entre 30 y 45%) de los pacientes experimenta al menos una complicación ósea11. Por otra parte, la toxicidad renal limita el uso de bifosfonatos administrados por vía intravenosa, requiriendo monitoreo previo a cada dosis, así como ajustes de dosis o suspensión de tratamiento.
El denosumab posee un mecanismo de acción innovador, distinto al de los bifosfonatos. En múltiples ensayos clínicos controlados el denosumab ha demostrado superioridad frente al AZ para prevenir ERE en pacientes con neoplasias malignas avanzadas12,13. El objetivo del presente estudio fue comparar los costos y la efectividad del uso de denosumab con respecto al empleo del AZ o no tratamiento (en aquellos donde el AZ está contraindicado por tener insuficiencia renal grave) desde la perspectiva del Instituto Mexicano del Seguro Social (IMSS), como pagador.
Material y métodos
Descripción general
El análisis se desarrolló conforme a la Guía para la Conducción de Estudios de Evaluación Económica para la Actualización del Cuadro Básico de Insumos del Sector Salud en México14. Se trata de un análisis de costo-efectividad, utilizando como medida de desenlace el número de ERE.
Población objetivo
Pacientes adultos, derechohabientes del IMSS, con TS y metástasis ósea. La población objetivo se dividió en tres categorías: cáncer de próstata (CaPr), cáncer de mama (CaMa) y otros tumores sólidos (OTS). Con base en la incidencia reportada por GLOBOCAN15 para CaPr, CaMa y OTS (pulmón, colorrectal, gastrointestinal, ginecológico, melanoma maligno y renal) y la proporción de pacientes que cumple con criterios para indicación de terapia dirigida al hueso en cada tipo de tumor (definida como el producto de la proporción de pacientes diagnosticados en etapa IV16-23 y la incidencia a 10 años de metástasis óseas1), se estimó la siguiente distribución proporcional: 63% CaPr, 14% CaMa y 23% OTS.
Intervenciones competitivas
Se comparó a denosumab a dosis de 120 mg administrada por vía subcutánea una vez cada cuatro semanas contra un escenario mixto en donde los pacientes pueden recibir AZ a dosis de 4 mg administrada mediante infusión intravenosa una vez cada cuatro semanas o no tratamiento (Mix AZ/No Trt). La proporción de pacientes del escenario mixto que no reciben tratamiento es 8.1%24, y corresponde a los individuos que presentan contraindicación al AZ debido a insuficiencia renal grave25.
Horizonte temporal y tasas de descuento intertemporal
Puesto que los pacientes con TS y metástasis ósea se encuentran en riesgo permanente de experimentar ERE se contempló un horizonte temporal de por vida, definido operacionalmente como 200 ciclos de 28 días (≈ 15.33 años)26-28. Los costos y ERE se descontaron a una tasa anual del 5% en el caso base14.
Modelo de decisión
El modelo que publicaron Stopeck et al.26 fue adaptado al contexto mexicano. Se trata de un modelo de Markov con tres estados de salud: «En tratamiento con terapia dirigida al hueso», «Fuera de tratamiento» y «Muerto». Los pacientes asignados a denosumab o AZ inician en el estado de salud «En tratamiento con terapia dirigida al hueso», en tanto que los pacientes con enfermedad renal grave del brazo Mix AZ/No Trt comienzan directamente en el estado de salud «Fuera de tratamiento». Los pacientes bajo tratamiento pueden suspender la terapia asignada, transitando así al estado «Fuera de tratamiento», en el cual enfrentan riesgos mayores de sufrir un ERE y, por lo tanto, los costos para ese rubro de gasto también se incrementan. El análisis considera también la posibilidad de muerte. El horizonte temporal transcurre en ciclos de 28 días para ser consistente con el periodo de administración de los medicamentos. La estructura es idéntica para las tres categorías de tumor sólido (CaPr, CaMa y OTS), aunque los parámetros individuales varían en función de la categoría considerada. El modelo reporta la ocurrencia de cuatro tipos de ERE (fractura patológica, radioterapia a hueso, compresión medular, cirugía ósea) y de cuatro eventos adversos serios (osteonecrosis de la mandíbula, reacción de fase aguda, hipocalcemia, toxicidad renal).
Parámetros clínicos
La tabla 1 presenta los parámetros clínicos más importantes. La frecuencia de ERE para el grupo tratado con AZ se modeló utilizando las tasas crudas anualizadas reportadas por Cristino et al.27, las cuales se definieron con información recolectada en cada uno de los tres ensayos clínicos pivotales29-31. Las respectivas tasas crudas anualizadas para denosumab se determinan aplicando la razón de riesgos (RR) para el primer y subsecuente ERE con dicho agente vs. AZ (publicada en cada uno de los tres ensayos clínicos previamente referidos) al valor de la tasa cruda anualizada con AZ que corresponda. Los pacientes que inician sin tratamiento (por tener contraindicación al AZ) o que abandonan el tratamiento con denosumab o AZ durante el seguimiento del modelo enfrentan una tasa de ERE un 75% más alta que con AZ27,28. Al igual que en otras evaluaciones económicas, las tasas crudas se ajustaron al alza permitiendo que sean más representativas de lo que se observa en el mundo real28. Las tasas crudas anualizadas de ERE ajustadas para el mundo real se transforman a tasas por ciclo dividiéndolas por el número de ciclos de 28 días que hay en promedio por año; esto es, dividiéndolas por 13.04 ≈ 365.25/28.
Tabla 1 Principales parámetros clínicos del modelo
| Variable | Mínimo | Caso base | Máximo | Referencia |
|---|---|---|---|---|
| Contraindicación a AZ | 7.6% | 8.1% | 8.6% | Arellano et al., 201524 |
| Tasa cruda anualizada de ERE, AZ | Cristino et al., 201727 | |||
| CaPr | NA | 0.947 | NA | |
| CaMa | NA | 0.631 | NA | |
| OTS | NA | 0.936 | NA | |
| RRERE denosumab vs. AZ | ||||
| CaPr | 0.71 | 0.82 | 0.94 | Fizazi et al., 201129 |
| CaMa | 0.66 | 0.77 | 0.89 | Stopeck et al., 201030 |
| OTS | 0.72 | 0.85 | 1.00 | Henry et al., 201431 |
| Análisis integrado | NA | 0.81* | NA | Lipton et al., 201632 |
| RRERE No Trt vs. AZ | 1.22 | 1.75 | 2.38 | Stopeck et al., 202028 |
| Factor de ajuste a mundo real | 1.00 | 2.84 | 4.00 | Stopeck et al., 202028 |
| Distribución ERE, CaPr† | Cristino et al., 201727 | |||
| Fractura patológica | NA | 26.8% | NA | |
| Radioterapia a hueso | NA | 66.1% | NA | |
| Cirugía ósea | NA | 1.5% | NA | |
| Distribución ERE, CaMa† | Cristino et al., 201727 | |||
| Fractura patológica | NA | 58.2% | NA | |
| Radioterapia a hueso | NA | 35.4% | NA | |
| Cirugía ósea | NA | 4.7% | NA | |
| Distribución ERE, OTS† | Cristino et al., 201727 | |||
| Fractura patológica | NA | 31.4% | NA | |
| Radioterapia a hueso | NA | 57.5% | NA | |
| Cirugía ósea | NA | 6.2% | NA | |
| Gamma generalizada, SG | Cristino et al., 201727 | |||
| CaPr, intercepto | 6.498 | 6.582 | 6.666 | |
| CaPr, escala | 0.825 | 0.924 | 1.023 | |
| CaPr, forma | 0.405 | 0.624 | 0.843 | |
| CaMa, intercepto | 7.128 | 7.217 | 7.306 | |
| CaMa, escala | 0.609 | 0.858 | 1.107 | |
| CaMa, forma | 0.416 | 0.850 | 1.284 | |
| OTS, intercepto | 5.737 | 5.851 | 5.965 | |
| OTS, escala | 1.130 | 1.214 | 1.298 | |
| OTS, forma | - 0.067 | 0.134 | 0.335 | |
| Intensidad de dosis | 0.80 | 0.90 | 1.00 | Stopeck et al., 201226 |
| Probabilidad de discontinuación‡ | Cristino et al., 201727 | |||
| Denosumab, CaPr | NA | 0.031 | NA | |
| Denosumab, CaMa | NA | 0.022 | NA | |
| Denosumab, OTS | NA | 0.047 | NA | |
| AZ, CaPr | NA | 0.036 | NA | |
| AZ, CaMa | NA | 0.022 | NA | |
| AZ, OTS | NA | 0.047 | NA |
*El análisis integrado de los datos para las tres categorías de tumor, publicado por Lipton et al.32, únicamente se emplea en un escenario evaluado como parte del análisis de sensibilidad.
†El valor del complemento (es decir, el porcentaje que falta para 100%) corresponde a compresión medular.
‡Por ciclo de tratamiento de 28 días. AZ: ácido zoledrónico; CaMa: cáncer de mama; CaPr: cáncer de próstata; ERE: eventos relacionados con el esqueleto; NA: no aplica; No Trt: sin tratamiento; OTS: otros tumores sólidos; RR: razón de riesgos; SG: supervivencia global.
La distribución porcentual por tipo de ERE en cada categoría de TS se muestra en la tabla 1. La radioterapia a hueso fue el evento más frecuente en los pacientes con CaPr y OTS, mientras que la fractura patológica lo fue en las pacientes con CaMa. Las curvas de supervivencia global (SG) de denosumab y AZ en los tres ensayos clínicos pivotales de TS están casi empalmadas, con estimaciones puntuales de hazard ratio con valores situados alrededor de 1 (que representa el valor nulo) y diferencias no significativas desde el punto de vista estadístico29-31. Por tal motivo, en cada categoría de TS se decidió utilizar una sola curva de SG, que aplica para las tres modalidades de tratamiento (denosumab, AZ y No Trt). De acuerdo con Cristino et al.27, la distribución gamma generalizada ofrece la mejor bondad de ajuste. Los parámetros estimados para dicha distribución se presentan en la tabla 1. Se asumió que no existen diferencias entre denosumab y AZ en relación con el cumplimiento terapéutico (intensidad de dosis igual a 90%)26 y que la discontinuación del tratamiento con ambos agentes sigue una distribución exponencial, lo que significa que las probabilidades de discontinuación son constantes en cada ciclo de tratamiento. Las tasas anuales de eventos adversos serios se calcularon combinando la información por brazo de tratamiento de los tres ensayos clínicos pivotales. Las tasas anuales estimadas para denosumab fueron: 0.017 (osteonecrosis de la mandíbula), 0.001 (reacción de fase aguda), 0.013 (hipocalcemia) y 0.026 (toxicidad renal); para AZ, las tasas fueron 0.012, 0.006, 0.006 y 0.033 respectivamente27.
Uso de recursos y costos unitarios
Se evaluaron los costos directos médicos; específicamente, los siguientes rubros de gasto: adquisición de ambos agentes, administración de AZ mediante infusión intravenosa, manejo habitual de los pacientes, atención de ERE y tratamiento de eventos adversos serios. Los valores se reportan en pesos mexicanos (de septiembre) del año 2020.
El precio de un envase con un frasco ámpula de 120 mg de denosumab fue obtenido en Compranet33. El precio de un envase con un frasco ámpula de 4.0 mg de AZ se derivó con la información del Portal IMSS Compró34. A la administración de AZ se le asignó un costo de $606.73, cifra equivalente a la diferencia entre el costo de una sesión de quimioterapia ($7,113) y el valor que de este corresponde a medicamentos ($6,558) en el IMSS35, actualizada por inflación. Para efectos del presente análisis, el manejo de rutina por cada ciclo de cuatro semanas consiste en una consulta de especialidad más (en el caso de AZ, y solamente durante el tiempo de tratamiento con dicho agente) un estudio de laboratorio para monitorear el nivel de creatinina sérica25. Los costos unitarios de la consulta de especialidad ($1,549.57) y del estudio de laboratorio ($93.42) se determinaron actualizando por inflación los valores correspondientes para tercer nivel de atención en el IMSS35.
El costo por la atención de ERE involucra los recursos destinados durante la fase inicial del tratamiento (es decir, la atención de urgencia en el hospital) y las consultas médicas brindadas posterior al egreso. En el caso de las fracturas patológicas (Tabla 2), se añade el costo asociado con las sesiones de fisioterapia, y su estimación se generó con datos publicados en diversos artículos2,6,36,37,39 y con los costos unitarios de una consulta de especialidad y de una sesión de fisioterapia en tercer nivel de atención35 y los costos de ciertos grupos relacionados con el diagnóstico (GRD) en el IMSS,38 actualizados por inflación. Los costos para cada uno de los otros tres tipos de ERE (Tabla 3) fueron estimados como la suma del costo del GRD correspondiente38 y del producto obtenido al multiplicar la frecuencia de consultas de especialidad reportada por Body et al.2 y el costo unitario de una consulta de especialidad en tercer nivel de atención en el IMSS35. Por tratarse de eventos adversos serios, en la determinación de sus costos se asumió que todos los pacientes afectados ingresan a hospitalización, siendo el costo por evento definido en función del valor actualizado por inflación del GRD38 que se consideró apropiado en cada caso (Tabla 3). Es importante señalar que los costos unitarios por servicios35 y los costos de GRD38 utilizados en el análisis son a nivel operativo-sustantivo.
Tabla 2 Estimación del costo por episodio de fractura patológica según categoría de tumor. Los costos unitarios y de GRD corresponden a sus respectivos valores a nivel operativo-sustantivo y se actualizaron por inflación a 2020. Cifras redondeadas
| Descripción | CaPr | CaMa | OTS |
|---|---|---|---|
| Costo durante la fase aguda (A)* | $82,462.90 | $86,503.90 | $82,462.90 |
| Proporción de casos quirúrgicos† | 50.75% | 55.83% | 53.29% |
| Costo de un caso quirúrgico‡ | $121,645.83 | $121,645.83 | $121,645.83 |
| Costo de un caso no quirúrgico§ | $42,086.58 | $42,086.58 | $42,086.58 |
| Costo por consultas ambulatorias (B) | $4,926.00 | $4,926.00 | $4,926.00 |
| Frecuencia de consultas¶ | 3.2 | 3.2 | 3.2 |
| Costo unitario por consulta** | $1,549.57 | $1,549.57 | $1,549.57 |
| Costo por sesiones de fisioterapia (C) | $15,411.96 | $13,958.28 | $14,685.12 |
| Frecuencia de sesiones†† | 14.5 | 13.2 | 13.9 |
| Costo unitario por sesión‡‡ | $1,059.57 | $1,059.57 | $1,059.57 |
| Costo total (A + B + C) | $102,800.86 | $105,388.18 | $104,094.52 |
*Promedio ponderado de casos quirúrgicos y no quirúrgicos.
†Estimación basada en Barlev et al.6
‡Estimación basada en Narazaki et al.,36 Trujillo González y cols.37 y Costos GRD 2018.38
§Costo del GRD número 542 (Costos GRD 2018).38
¶Estimación basada en Narazaki et al.36 y Body et al.2
**Costo de una consulta de especialidad en tercer nivel de atención en el IMSS.35
††Estimación basada en Narazaki et al.36 y Dimai et al.39
‡‡Costo de una sesión de fisioterapia en tercer nivel de atención en el IMSS.35 CaMa: cáncer de mama; CaPr: cáncer de próstata; GRD: grupo relacionado con el diagnóstico; IMSS: Instituto Mexicano del Seguro Social; OTS: otros tumores sólidos.
Tabla 3 Estimación del costo de otros ERE y de los eventos adversos serios
| Evento | Costos a valores de 2018 | Costos actualizados a valores 2020 | ||
|---|---|---|---|---|
| Atención aguda* | Consultas ambulatorias† | Total | ||
| Radioterapia a hueso | $65,232.50 | $5,953.33 | $71,185.83 | $77,820.35 |
| Cirugía ósea | $228,891.60 | $3,827.14 | $232,718.74 | $254,408.13 |
| Compresión medular | $275,541.50 | $5,811.59 | $281,353.09 | $307,575.19 |
| Osteonecrosis de la mandíbula | $41,564.50 | NA | $41,564.50 | $45,438.31 |
| Reacción de fase aguda | $25,977.73 | NA | $25,977.73 | $28,398.85 |
| Hipocalcemia | $23,721.08 | NA | $23,721.08 | $25,931.88 |
| Toxicidad renal | $35,302.76 | NA | $35,302.76 | $38,592.98 |
*Costos a nivel operativo-sustantivo de los GRD número 849, 515, 028, 137, 948, 641 y 700 en el IMSS38 para los eventos radioterapia a hueso, cirugía ósea, compresión medular, osteonecrosis de la mandíbula, reacción de fase aguda, hipocalcemia y toxicidad renal, respectivamente.
†Frecuencia de consultas según Body et al.3: 4.2 (radioterapia a hueso), 2.7 (cirugía ósea) y 4.1 (compresión medular), a un costo unitario a nivel operativo-sustantivo en el IMSS35de $1,417.46 pesos. ERE: eventos relacionados con el esqueleto; GRD: grupo relacionado con el diagnóstico; IMSS: Instituto Mexicano del Seguro Social; NA: no aplica.
Análisis de sensibilidad
Se llevaron a cabo análisis de sensibilidad de tipo determinístico (ASD) y probabilístico (ASP). La primera parte del ASD comprendió un análisis de sensibilidad para cuatro escenarios y la segunda consistió en un análisis univariante resumido en formato de diagrama de tornado. Cuando fue necesario, los valores mínimo y máximo se estimaron como los límites inferior y superior del intervalo de confianza. A los precios de denosumab y AZ se les aplicó una variación relativa de ± 5% con respecto al valor del caso base. En el resto de los costos, la variación relativa fue del 20%. El ASP refleja los resultados obtenidos tras generar mil simulaciones de Monte Carlo de segundo orden. La proporción de pacientes que tienen contraindicación para AZ se modeló mediante una distribución beta. Las RR de ERE se modelaron con una distribución log-normal. Las tasas de eventos se modelaron con una distribución gamma. El número de dosis por ciclo y los costos de adquisición de denosumab y AZ se modelaron con una distribución normal. La distribución normal también sirvió para modelar los parámetros que determinan la mortalidad (basada en una función gamma generalizada27). Los demás costos se modelaron mediante una distribución gamma.
Resultados
Caso base
Los resultados obtenidos para el caso base se muestran en la tabla 4. Como se puede apreciar, la atención de ERE representa, y por mucho, el mayor componente de los costos en ambas intervenciones. La diferencia entre el costo de adquisición de denosumab y el de AZ ($85,436) se compensa con la suma de los ahorros producidos por la reducción del 10.8% en el número total de ERE con denosumab frente al Mix AZ/No Trt ($79,617) y los ahorros generados al no requerir infusiones intravenosas para su administración ($7,342). Las diferencias en los otros dos rubros de gasto fueron menores, con una ligera ventaja para denosumab en el rubro de atención ordinaria debido a que no requiere de monitoreo de la función renal y una ligera ventaja a favor del Mix AZ/No Trt en el rubro de tratamiento de eventos adversos serios. El denosumab resultó dominante (es decir, con menos costos totales y menor número esperado de ERE con respecto al Mix AZ/No Trt).
Tabla 4 Resultados del caso base y análisis de sensibilidad de escenario. El símbolo Δ denota incremento en la comparación de denosumab vs. Mix AZ/No Trt.
| Valores descontados | Denosumab | Mix AZ/No Trt | Diferencia |
|---|---|---|---|
| Costo total por paciente | $795,156 | $797,650 | –$2,494 |
| Adquisición de TDH | $86,205 | $769 | $85,436 |
| Administración de TDH | $0 | $7,342 | –$7,342 |
| Manejo de rutina | $42,834 | $44,090 | –$1,256 |
| Atención de ERE | $663,676 | $743,292 | –$79,617 |
| Tratamiento de EA serios | $2,442 | $2,158 | $284 |
| Frecuencia de ERE | 6.472 | 7.252 | –0.781 |
| Descripción | Δ Costos | Δ ERE | RCEI |
| Caso base | –$2,494 | –0.781 | Dominante* |
| Variación, precio de denosumab | |||
| Incremento del 5% | $1,816 | –0.781 | $2,327 |
| Disminución del 5% | –$6,804 | –0.781 | Dominante* |
| Uso de análisis integrado† | –$4,508 | –0.800 | Dominante* |
| AZ aplicado cada 12 semanas | $2,722 | –0.781 | $3,488 |
*El denosumab resultó menos costoso y más efectivo (es decir, con menos ERE) que Mix AZ/No Trt.
†Se emplea una sola razón de riesgos para prevenir ERE con denosumab vs. AZ.32 AZ: ácido zoledrónico; EA: eventos adversos; ERE: eventos relacionados con el esqueleto; Mix AZ/No Trt: escenario mixto donde el 91.9% de los pacientes recibe AZ y el 8.1% restante no recibe tratamiento con TDH debido a que presenta enfermedad renal grave que implica contraindicación al uso de AZ; RCEI: razón de costo-efectividad incremental de denosumab vs. Mix AZ/No Trt; TDH: terapia dirigida al hueso.
Análisis de sensibilidad
La parte inferior de la tabla 4 presenta la comparación de los valores incrementales de costos y de ERE, así como la razón de costo-efectividad incremental (RCEI, si aplica) tanto para el caso base como para los cuatro escenarios evaluados durante el ASD. Manteniendo todo lo demás constante, un incremento del 5% en el precio de denosumab provocaría que este dejara de ser una intervención dominante, aunque la RCEI calculada, que indica el costo promedio por cada ERE evitado frente al Mix AZ/No Trt, fue de apenas de $2,327 pesos. Por otra parte, utilizar el análisis integrado de eficacia para denosumab permitiría mejorar sus resultados en relación con los del caso base. Si el AZ se administrara cada 12 semanas sin perder eficacia40, la RCEI de denosumab frente al Mix AZ/No Trt sería de $3,488 por ERE evitado.
El diagrama de tornado se muestra en la figura 1. Como se puede apreciar, la variable que aportó mayor incertidumbre a los resultados de costo-efectividad fue el factor de ajuste a mundo real para la ocurrencia de ERE. Las dos variables que le siguieron en la lista son las RR para ocurrencia de ERE con denosumab y sin tratamiento (ambas vs. AZ).
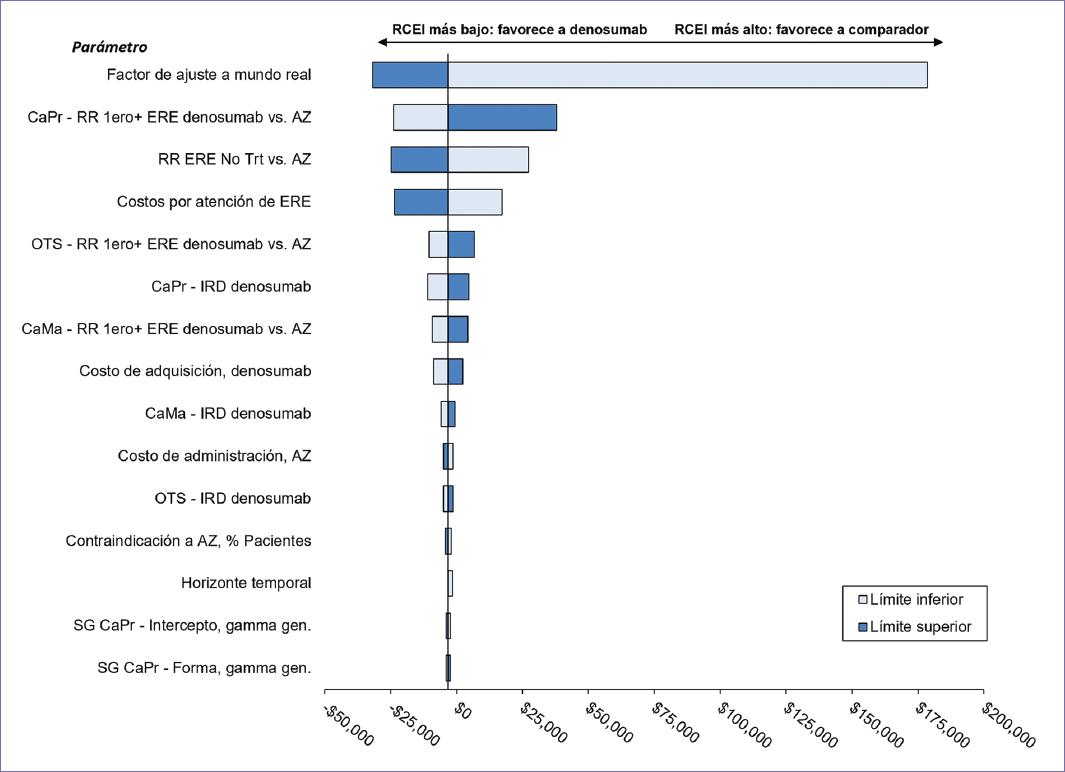
Figura 1 Diagrama de tornado: denosumab vs. Mix AZ/No Trt. AZ: ácido zoledrónico; CaMa: cáncer de mama; CaPr: cáncer de próstata; ERE: evento relacionado con el esqueleto; gen: generalizada: IRD: intensidad relativa de dosis; No Trt: sin tratamiento; OTS: otros tumores sólidos; RCEI: razón de costo-efectividad incremental; RR: razón de riesgos; SG: supervivencia global.
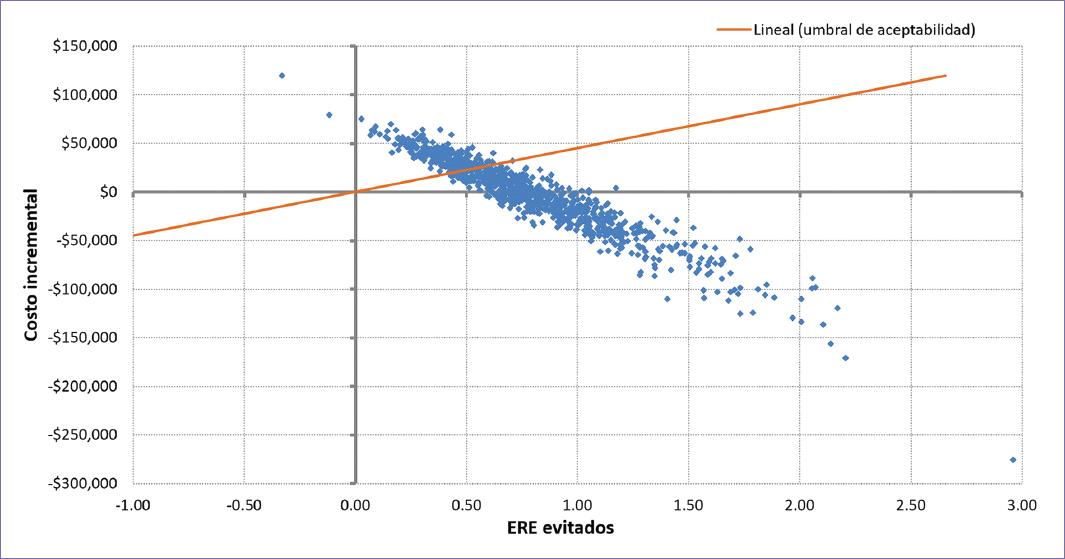
La figura 2 despliega el diagrama de dispersión de costo-efectividad incremental de denosumab vs. Mix AZ/No Trt. Casi la mitad (47.4%) de las simulaciones se ubicaron en el cuadrante IV del plano de costo y efectividad incrementales, estableciendo una situación de dominancia a favor de denosumab. Para un valor de disponibilidad a pagar de $45,000 pesos por ERE evitado, el denosumab resultó dominante o al menos costo-efectivo en el 74.7% de las simulaciones generadas como parte del ASP.
Discusión
El cáncer es una de las principales causas de muerte en México y en el mundo. Los pacientes con TS y metástasis óseas deben enfrentar el flagelo de la enfermedad avanzada en sus diversas manifestaciones, incluyendo un riesgo elevado de sufrir ERE. La prevención de las complicaciones óseas forma parte del tratamiento integral en este tipo de población. Los resultados del presente estudio sugieren que el denosumab representa una intervención dominante sobre el Mix AZ/No Trt, dando lugar a un ahorro neto de $2,494 pesos por paciente, en promedio. Si bien se trata de una cifra que podría considerarse modesta, el ahorro general en el IMSS puede llegar a ser considerable, dado el volumen amplio de pacientes que atiende.
Comparar los resultados del presente estudio con otros análisis publicados en la literatura resulta complicado debido a las diferencias en metodología y en los vectores de costos. No obstante, existen ciertos aspectos que vale la pena destacar. Uno de ellos es que los resultados farmacoeconómicos más favorables para denosumab se presentaron en el grupo de CaPr, situación consistente con lo publicado26-28. En ese sentido, es importante puntualizar que la condición de dominancia para denosumab solo aplica estrictamente a los pacientes con CaPr, en donde el ahorro neto a favor de denosumab alcanzó los $10,470 pesos, con una efectividad de 0.886 ERE evitados por paciente. En los subgrupos de CaMa y OTS, el denosumab resultó ligeramente más costoso y efectivo que el Mix AZ/No Trt, originando valores de RCEI de $21,723 y $14,042 pesos respectivamente. El valor bajo de estas últimas cantidades sugiere que el denosumab podría ser considerado costo-efectivo en esos subgrupos. Otra consistencia con lo reportado en la literatura26-28 es el hecho de que el mayor rubro de gasto correspondió a la atención de los ERE.
El estudio no está exento de limitaciones. Como en cualquier evaluación económica, fue necesario emplear ciertos supuestos. Por ejemplo, se asumió que no existen diferencias en mortalidad entre denosumab, AZ y No Trt. Si bien es cierto que en los estudios pivotales de TS no se identificaron diferencias estadísticamente significativas en mortalidad entre denosumab y AZ29-31, dado que los ERE se asocian con mayor riesgo de muerte, se puede argumentar que la expectativa de vida podría ser mejor con denosumab que contra AZ, pero sobre todo contra No Trt. Otra limitación tiene que ver con que en los cálculos de costos se empleó el precio de una formulación genérica de AZ, en tanto que en los ensayos clínicos se administró el medicamento de patente. Si el AZ genérico tuviera en realidad una menor efectividad con respecto al de marca comercial y/o si se asociara con un inadecuado perfil de eventos adversos, los resultados de evaluación económica aquí mostrados serían un tanto conservadores. Otro aspecto por tomar en consideración es que en los cálculos de costos para AZ se utilizó un esquema de administración por cada cuatro semanas, que se basa en los ensayos clínicos pivotales29-31. Dado que el AZ puede administrarse cada tres o cuatro semanas25, es pertinente señalar que si existieran pacientes recibiendo AZ en la modalidad de cada tres semanas, estos incurrirían en mayores costos a los aquí estimados tanto en los rubros de adquisición como de administración. Por otro lado, es importante recalcar que si los pacientes recibieran AZ con un intervalo de 12 semanas entre cada aplicación, los costos por concepto de adquisición y administración para dicho agente se reducirían a un tercio de los considerados en el caso base. En tal escenario, el uso de denosumab dejaría de ser dominante (es decir, menos costoso y con mayor efectividad) para convertirse en una intervención costo-efectiva, con un costo promedio incremental inferior a $3,500 pesos por ERE evitado frente al Mix AZ/No Trt.
Una última limitación es que el horizonte temporal definido para el análisis del caso base (15.33 años) impuso la necesidad de efectuar extrapolaciones más allá de la duración propia de los ensayos clínicos pivotales. Sin embargo, el análisis de sensibilidad mostró que el denosumab sigue siendo dominante incluso si el horizonte temporal se reduce a tres años.
Dentro de las áreas de oportunidad para investigaciones futuras se puede mencionar la necesidad de contar con información específica sobre preferencias por estados de salud en México para los ERE en población oncológica, que permita eventualmente desarrollar análisis de costo-utilidad confiables. De igual manera, sería deseable contar con mejor información sobre manejo ambulatorio post-ERE. Finalmente, es importante señalar que denosumab y AZ pertenecen a distintas clases de tratamiento antirresortivo y, por lo tanto, no son intercambiables desde un punto de vista terapéutico.
Conclusiones
El presente análisis demuestra que, en comparación con el Mix AZ/No Trt, el denosumab reduce el riesgo de experimentar ERE en pacientes con TS con metástasis ósea. Tras incorporar todos los rubros de gasto relevantes, en el caso base determinístico (el cual considera que el AZ se administra cada cuatro semanas) el denosumab representa una intervención dominante (más efectiva y con ahorros netos de costos) frente al Mix AZ/No Trt. Es importante señalar que en el escenario que evaluó la administración del AZ cada 12 semanas, el denosumab dejó de ser dominante, aunque se considera costo-efectivo (con una relación de costos y desenlaces en salud favorable). Por lo tanto, en general se concluye que el denosumab constituye una intervención dominante o al menos costo-efectiva en comparación al Mix AZ/No Trt. Esta condición prevaleció en el análisis por subgrupo y en los diferentes escenarios evaluados como parte del análisis de sensibilidad determinístico, así como en la amplia mayoría de las simulaciones generadas durante el análisis de sensibilidad probabilístico.











 nueva página del texto (beta)
nueva página del texto (beta)