Introducción
La aparición de una neoplasia primaria maligna múltiple es más frecuente en aquellos pacientes de edades más avanzadas; esta frecuencia es muy variable en la literatura, se estima entre el 0.7 y el 11.7%, esto depende de si nos basamos en autopsias, registros o bases de pacientes en centros oncológicos o estudios prospectivos1. Hablando del cáncer de pulmón, este es la causa principal de muerte relacionada con cáncer en el mundo; la frecuencia de los cánceres de pulmón sincrónicos o metacrónicos ha aumentado en los últimos años debido al desarrollo de técnicas de detección temprana como la tomografía computarizada y la tomografía por emisión de positrones, así como a los avances en los tratamientos oncológicos, lo que resulta en una mayor esperanza de vida de los pacientes y periodos más largos de supervivencia. La tasa promedio de desarrollar un nuevo cáncer primario de pulmón es aproximadamente del 1 al 6% por año2. Los tumores sincrónicos y metacrónicos pueden ser clasificados según el tiempo de aparición: sincrónico aquel ocurrido dentro de los seis meses posteriores al diagnóstico de la primera neoplasia y metacrónico aquellos que ocurrieron en un tiempo posterior a seis meses3.
Presentamos el caso de un paciente de sexo masculino con antecedente de haber sido tratado previamente por cáncer renal de células claras que posteriormente desarrollo cáncer pulmonar que requirió la colocación de un stent bronquial.
Caso clínico
Hombre de 66 años de edad, originario de Chiapas. Antecedentes heredofamiliares: un hermano con cáncer de próstata, otro hermano con tumor maligno de bronquios y pulmón. Antecedentes personales no patológicos: tabaquismo positivo desde los 16 años a razón de una cajetilla diaria (IT 16), con consumo de alcohol ocasional. Antecedentes patológicos quirúrgicos: colecistectomía a los 44 años, amigdalectomía a los 20 años, hernioplastia abdominal a los 25 años. Antecedente de paro cardiorrespiratorio que requirió reanimación cardiopulmonar a la edad de 46 años.
Antecedente de inicio con dolor tipo cólico renoureteral en fosa renal derecha con diaforesis, con hematuria al día siguiente y expulsión de lito de color claro, estrellado. Se realizó una tomografía abdominal, donde se encontró tumoración renal en polo inferior derecho con características de malignidad, de tamaño 120 x 80 mm, sin presencia de ganglios periféricos ni involucro vascular, motivo por el cual ingresó programado para nefrectomía laparoscópica radical derecha dos meses después de inicio de síntomas, con hallazgo de tumor renal a expensas del polo inferior, con tamaño total aproximado de 25 x 15 x 15 cm y diagnóstico histopatológico de cáncer renal de células claras Furhman 3 (pT3aNxMx), con invasión al seno renal con bordes quirúrgicos de arteria, vena y uréter negativos, sin tratamiento adyuvante y seguimientos cada tres a seis meses posteriores (Fig. 1).
Acude al área de urgencias siete años después por hemoptisis de un mes de evolución, que inicialmente se trató en medio privado sin mejoría. Se refiere transfusión sanguínea de tres paquetes globulares con reporte de hemoglobina (Hb) externa de 8.9 postransfusión; se realizó broncoscopia en medio externo con reporte de tumor endobronquial de lóbulo superior derecho de 5 cm parahiliar y toma de biopsia con reporte histopatológico de carcinoma epidermoide, en nuestro Servicio de Urgencias con adecuada coloración mucotegumentaria y adecuado estado de hidratación, sin compromiso cardiorrespiratorio; se solicitó tomografía de tórax (Fig. 2). Laboratorios al ingreso: leucocitos 8.4, Hb 9.6, hematocrito (Hto) 29.4, recuento de plaquetas 361, creatinina 1.26, Fa 80, glucosa 99, potasio 4.0, sodio 140, tiempo de protrombina 11.8, tiempo parcial de tromboplastina 43.9 e índice internacional normalizado 1.07.
El caso se comentó en la Unidad Funcional de Tórax, donde se consideró como segundo primario pulmonar metacrónico, carcinoma epidermoide etapa clínica (EC) IIIB, central que compromete bronquio fuente derecho a menos de dos centímetros de la tráquea, sin posibilidad de control quirúrgico ni con neumonectomía.
Valorado por Oncología Médica, se decide inicio de quimioterapia (QT) de inducción a base de carboplatino y paclitaxel por tres ciclos y dependiendo de la respuesta valorar la posibilidad de QT/radioterapia (RT).
Valorado por el Servicio de Radioterapia, se consideró candidato a recibir QT/RT concomitante.
Completó tres ciclos de carboplatino/paclitaxel, posteriormente se decidió iniciar tratamiento concomitante con carboplatino en monofármaco por estado funcional del paciente.
Completó por parte del Servicio de Radioterapia 66 Gy en 33 sesiones con muy buena tolerancia, y respuesta parcial por tomografía por emisión de positrones/tomografía computarizada (PET/CT), se consideró candidato a neumonectomía.
En el seguimiento posterior a dos meses valorado por el Servicio de Neumología, con sintomatología respiratoria a base de tos con expectoración blanquecina, se clasifica al paciente con neumonitis post-RT grado 2 (Fig. 3), por lo que se decide tratamiento con esteroide sistémico y esteroide/broncodilatador de acción prolongada (LABA) inhalado para reducir sintomatología.

Figura 3 Área en vidrio despulido lóbulo inferior derecho, datos en relación con el proceso inflamatorio.
Fue sometido a toracotomía posterolateral derecha, en la cual se procedió a exploración hiliar, identificándose actividad tumoral franca central con involucro de raíz de arteria pulmonar, bronquio principal, por lo que se decidió que el único procedimiento factible era neumonectomía en un paciente con factores de riesgo que podrían determinar un desenlace fatal (QT/RT concomitante previa), motivo por el que se decidió concluir el procedimiento con reporte de hallazgo de actividad tumoral dependiente de hilio con involucro de raíz de arteria pulmonar y bronquio principal con cambios posradioterapia.
Un mes posterior a toracotomía se valoró en Unidad Funcional de Tórax, donde se decidió brindar 2-3 ciclos con gemcitabina y valorar posibilidad de radioterapia corporal estereotáctica (SBRT).
Cinco meses posteriores al inicio de gemcitabina se documenta por PET/CT y radiografía de tórax atelectasia del lóbulo superior derecho (Fig. 4), por lo que se decidió interconsulta a Neumología para posible colocación de stent bronquial y valorar inicio de radiocirugía.

Figura 4 Radiografía de tórax con hemitórax derecho con disminución en expansión secundario a opacidad parahiliar derecha con broncograma aéreo, condiciona retracción de la tráquea y mediastino.
Posterior a colocación de stent bronquial (Figs. 5 y 6) es enviado a inicio de tratamiento con SBRT, donde recibió 30 Gy en 5 fracciones; en consulta de seguimiento el paciente refirió molestias secundarias a stent. Se documentó cambio en la coloración de las secreciones, por lo que se decidió tratar con antibiótico.
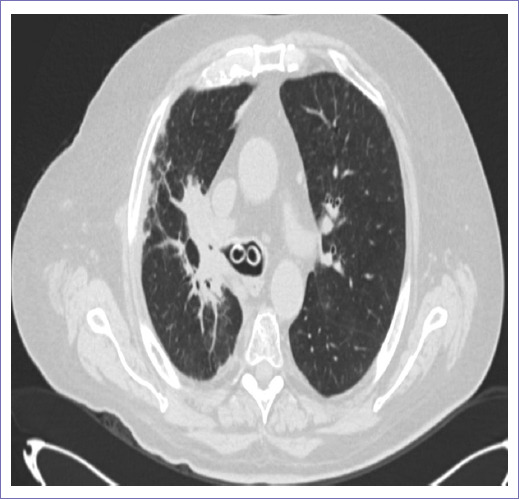
Figura 6 Presencia de stent en ambos bronquios principales, imagen sólida parahiliar derecha que condiciona disminución de luz de bronquio principal ipsilateral.
Se valoró y se decidió inicio de gemcitabina/platino posterior a control local por persistencia de enfermedad residual.
Por situación funcional y factores personales del paciente este decide continuar tratamiento en hospital local de su ciudad, motivo por el cual se pierde seguimiento del paciente.
Discusión
El cáncer pulmonar tuvo una incidencia de 2.2 millones de casos en 2017; año en el cual causó 1.9 millones de muertes y 40.9 millones de años de vida ajustado por discapacidad, de los cuales el 99% fueron de años de vida potenciales perdidos y un 1% de años vividos con discapacidad. Los hombres tienen más probabilidades de desarrollar cáncer pulmonar durante toda la vida que las mujeres (1 de cada 17 hombres en comparación con 1 de cada 43 mujeres). El cáncer pulmonar fue la causa mundial más común de muerte por cáncer y entre los años 2007 y 2017 los casos de cáncer pulmonar aumentaron un 37%; como factores relevantes, la edad cambiante contribuyó en un 19%, el crecimiento de la población en un 13% y los cambios en las tasas de incidencia específicas por edad un 5%4.
El cáncer renal es el doceavo cáncer más común en el mundo y el noveno más común en Europa5, las incidencias son mayores en países desarrollados como los de Norte América y Europa y más bajas en Asia y África6. Europa reportó aproximadamente 84,000 casos nuevos y 35,000 muertes por cáncer renal en 20127.
Las neoplasias primarias malignas múltiples (NPMM) son fenómenos poco frecuentes, su incidencia apenas alcanza un 0.99% para dos o más neoplasias distintas8. El término NPMM fue utilizado por primera vez en 1991 por Billroth9 y descrito por primera vez en la literatura por Warren en 193210.
En 1995 la Organización Mundial de la Salud adaptó la definición como aquellas neoplasias malignas de múltiples sitios primarios independientes, pueden surgir múltiples neoplasias en la forma de dos o más neoplasias primarias separadas que ocurren en distintos sitios, tumores múltiples de las mismas neoplasias, o en forma de una neoplasia que involucra múltiples sitios cuyo origen no puede ser determinado, estas también pueden surgir en la forma de dos o más neoplasias de diferentes morfologías que surgen en el mismo órgano11.
Los pacientes con neoplasias múltiples pueden dividirse en dos grandes grupos, aquellos con neoplasias sincrónicas, que se definen como la aparición de una segunda neoplasia maligna dentro de los primeros seis meses del desarrollo de la primera neoplasia, y aquellos con neoplasias metacrónicas, definidas como aquellas que se desarrollan en un periodo mayor de seis meses del desarrollo de la primera neoplasia12.
Se ha observado un aumento en la supervivencia de los pacientes con cáncer13. Dicho aumento es el resultado de los avances en QT y RT. El riesgo de cáncer esta influenciado por factores ambientales, la salud del individuo, su genética, predisposición y la terapia disponible14.
Los factores pronósticos para los pacientes una vez que fueron diagnosticados con cáncer son el tipo de cáncer, el estadio y las opciones de tratamiento. La supervivencia se ve influenciada por la detección temprana del cáncer y los avances en las distintas terapias disponibles. Esta situación influye indirectamente con la mayor ocurrencia y diagnóstico de NPMM, así como en una mayor esperanza de vida y un mejor monitoreo de los pacientes sobrevivientes, promoviendo así una mayor capacidad de detección de las NPMM15.
Es frecuente observar obstrucción maligna de la vía aérea en pacientes con cáncer pulmonar y se asocia con un impacto negativo en la supervivencia y la calidad de vida de los pacientes16. Los tratamientos oncológicos generalmente no resultan en una mejoría inmediata en los síntomas de los pacientes, es por esto que la broncoscopia terapéutica es un complemento necesario en el manejo de los pacientes en todas las etapas de la enfermedad17.
Las complicaciones relacionadas con la obstrucción maligna de la vía aérea son atelectasias, dificultad respiratoria o infecciones recurrentes (esto puede interferir con el óptimo tratamiento oncológico)18, la obstrucción maligna de la vía aérea es la principal indicación para realizar una broncoscopia terapéutica en el cáncer pulmonar (esta se realiza entre el 74 y el 100% de los pacientes en las series de casos grandes)19.
Conclusión
En conclusión, si bien la incidencia de neoplasias múltiples es relativamente baja, son más frecuentes en la población de pacientes que padecen cáncer en comparación con la incidencia de cánceres primarios en la población general; entre pacientes con neoplasias múltiples, la prevalencia de cáncer pulmonar es del 5.0%. Este cáncer se desarrolla con mayor frecuencia como un segundo tumor, los canceres sincrónicos se vuelven evidentes generalmente a edades más avanzadas.
El desarrollo tecnológico y el creciente conocimiento en el tratamiento del cáncer han contribuido a lograr una tasa de supervivencia a cinco años cercana al 66%20. El establecimiento de un seguimiento y la mejora de los métodos de examinación contribuye a la localización de otros tumores malignos primarios. Un estudio en pacientes que fueron sometidos a exploración de cuerpo completo con PET/CT mostró que en al menos el 1.2% de los pacientes con cáncer se detectó otra neoplasia primaria21.
La probabilidad de desarrollar neoplasias sincrónicas varia desde un 34.9 a un 41% y para neoplasias metacrónicas entre el 59 y el 66% en distintos artículos22.
Diversos metaanálisis de la literatura sugieren que la frecuencia de desarrollar un segundo tumor varía entre el 3 y el 5%, un tercer tumor aproximadamente en un 0.5% y un cuarto tumor en un 0.3%23.











 nova página do texto(beta)
nova página do texto(beta)





