Antecedentes
De acuerdo con la Global Initiative for Asthma (GINA), el asma se define por sus características clínicas, fisiológicas y patológicas como “una enfermedad inflamatoria crónica de la vía aérea, en la cual diversas células y elementos celulares desempeñan un papel importante. La inflamación crónica induce un aumento en la hiperreactividad de la vía aérea que provoca episodios recurrentes de disnea, sibilancias y tos, particularmente por la noche o la mañana. Estos episodios se asocian generalmente con obstrucción extensa y variable del flujo aéreo pulmonar, a menudo reversible espontáneamente o con tratamiento”1.
El asma es uno de los principales problemas de salud en el mundo; en las últimas 4 décadas se ha producido aumento en su prevalencia, morbilidad y mortalidad asociadas. Se calcula que aproximadamente 300 millones de personas en todo el orbe la padecen.
La frecuencia por sexo demuestra que es casi 2 veces mayor en los varones antes de los 14 años de edad y disminuye conforme la edad aumenta; en los adultos es mayor en las mujeres.2
Los factores de riesgo para el desarrollo de asma incluyen factores genéticos y ambientales, no obstante, se reconoce que si bien el antecedente familiar de asma es común, no es suficiente ni necesario para el desarrollo de la enfermedad.3
Obesidad en crisis asmáticas
La prevalencia de asma y obesidad ha aumentado en forma considerable y paralela en varios países durante las últimas 2 décadas. Los pacientes con obesidad que ingresan a la unidad de cuidados intensivos (UCI) por crisis asmática requieren mayor estancia hospitalaria en comparación con los pacientes con asma pero sin obesidad cuya gravedad del broncoespasmo al ingreso es similar, además de recibir un tratamiento más prolongado con oxígeno suplementario, betaagonistas y esteroides por vía intravenosa y requerir un periodo más largo para su recuperación.4
Mecanismos biológicos relacionados
La relación entre asma y obesidad no está bien establecida, pero existen factores posiblemente relacionados como la dieta y la actividad física, cambios mecánicos derivados de la obesidad, trastornos hormonales, activación de regiones genéticas específicas y alteraciones en el sistema inmunológico.
Influencia de la dieta y actividad física
Numerosos factores dietéticos tiene relación con la prevalencia del asma en niños y adultos; los antioxidantes (vitaminas A, C y E), riboflavina y piridoxina pueden tener un efecto benéfico al aumentar la función inmunológica, reducir los síntomas de asma y mejorar la función pulmonar. Se ha observado que los antioxidantes son la primera línea de defensa contra los radicales libres, capaces de dañar los componentes celulares y contribuir a la inflamación.
El consumo frecuente de frutas, verduras, pescados, mariscos, oleaginosas, queso y crema, al igual que la realización de actividad física han demostrado un efecto protector contra el desarrollo de sibilancias; por el contrario, el consumo frecuente de comida rápida y golosinas y el sedentarismo elevan la probabilidad de presentarlas. El efecto protector de las frutas y verduras se debe probablemente a su alto contenido de antioxidantes; las vitaminas E y C (abundante en el líquido extracelular pulmonar) representan una de las principales defensas del cuerpo contra la oxidación. De igual manera, el betacaroteno, precursor de la vitamina A, acumulado en las membranas tisulares, genera aniones superóxido, los cuales reaccionan con la peroxidación de los radicales libres.
En cuanto a las oleaginosas (nuez, almendra, cacahuate y avellana) se ha observado que aportan al organismo grasas de origen vegetal y son la principal fuente de vitamina E; además, interactúan con radicales libres solubles en lípidos de la membrana celular, con lo que mantienen la integridad de esta y confieren protección a la célula ante la presencia de compuestos tóxicos, metales pesados, drogas y radicales libres. De igual forma, inducen la proliferación de células de defensa y aumentan la respuesta celular ante algún daño o infección.5,6
Efectos de la obesidad en la mecánica respiratoria
Los efectos mecánicos de la obesidad sobre el aparato respiratorio parecen ser los más fáciles de explicar y comprender. La obesidad produce disminución de la capacidad residual funcional y del volumen corriente, cambios que reducen el estiramiento del músculo liso. La habilidad para responder al estrés fisiológico como el ejercicio se obstaculiza por el pequeño volumen corriente, lo que altera la contracción del músculo liso y empeora la función pulmonar.
Otro efecto mecánico de la obesidad, identificado principalmente en adultos, es el reflujo gastroesofágico, ya que cuando el ácido gástrico tiene contacto directo con la vía aérea origina broncoconstricción debido a la microaspiración o al reflejo vagal.7
López et al. demostraron que los pacientes con asma y obesidad no tienen un mayor riesgo de desarrollar broncoespasmo inducido por el ejercicio (BIE), comparados con sujetos con asma y sin obesidad (50 % y 38 %, respectivamente). Sin embargo, el porcentaje de disminución máxima del volumen espiratorio forzado en el primer segundo (VEF1 ) y el tiempo de recuperación fueron significativamente mayores en los primeros.8 Por lo anterior se deduce que el sobrepeso no aumenta la prevalencia de BIE, pero sí la severidad de este y retrasa la recuperación de los pacientes.
Existen informes y ensayos clínicos que demuestran que en pacientes con obesidad y asma, la pérdida de peso, ya sea por dieta o cirugía, mejora los síntomas y la función pulmonar, aumentando la capacidad vital forzada (CVF) y el VEF1; la pérdida de peso también disminuye la necesidad de medicamentos de rescate y la gravedad de las exacerbaciones, así como la morbilidad, mejorando el estado de salud en general.9,10
Influencia hormonal
Diversos estudios muestran que el efecto de la obesidad sobre el asma ocurre principalmente en las mujeres. La enzima aromatasa del tejido adiposo es responsable de convertir los andrógenos en estrógenos. Por otra parte, la obesidad se relaciona con mayor producción de estrógenos, lo cual se asocia con menarca precoz en mujeres y pubertad retardada en hombres.5,11 La asociación entre asma y obesidad parece ser más frecuente en mujeres que en hombres. Camargo et al. demostraron que las mujeres que ganan peso después de los 18 años de edad tienen un riesgo mayor de desarrollar asma.12
Los datos anteriores indican que las hormonas femeninas pudieran estar involucradas en la relación del asma con la obesidad. Dado que se ha descrito que la menarca se produce de forma temprana en las niñas con obesidad o sobrepeso, es razonable sugerir que la activación temprana de la hormona responsable de los procesos de iniciación de la pubertad está involucrada y estos mismos procesos podrían explicar el aumento en la incidencia de asma en las niñas prepuberales que aumentan de peso hasta llegar a la obesidad.
Participación de genes asociados en común
Existen diversos mecanismos mediante los cuales los genes pueden influir en el asma y la obesidad. Los estudios genéticos muestran la presencia de genes candidatos asociados con la obesidad y el asma. Además, existen genes de la obesidad en regiones cromosómicas que se han relacionado con asma, particularmente en los cromosomas 5q, 6p, 11q y 12q; la proximidad pudiera indicar mayor posibilidad para la herencia simultánea de estos dos rasgos. Más aún, los genes involucrados en la obesidad pueden codificar proteínas que influyen directamente sobre el estado del asma, como sucede con las citocinas.
El cromosoma 5 alberga los genes ADRB2 y NR3C1. El gen ADRB2 codifica para el receptor β2-adrenérgico, que tiene influencia en la actividad del sistema nervioso simpático. En la obesidad y síndrome metabólico participa en la regulación del balance energético mediante la termogénesis, efecto llevado a cabo principalmente por la estimulación de las catecolaminas a los receptores β2 y β3-adrenérgicos. Algunos polimorfismos en los genes de estos receptores han sido relacionados con alteraciones en la función de estos y, por lo tanto, con la modificación en la respuesta a las catecolaminas.13,14 Por otro lado, estos receptores son importantes para el control del tono de la vía aérea y se han encontrado polimorfismos asociados con la disminución del tiempo de respuesta al tratamiento con betaagonistas.15
Otro gen en esta área del cromosoma es NR3C1, que codifica para el receptor de glucocorticoides, involucrado en la modulación inflamatoria y respuesta al tratamiento del asma y la obesidad. Existen algunas modificaciones estructurales del gen; en este caso se ha descrito específicamente el polimorfismo rs56149945, que también se han relacionado con aumento en el índice de masa corporal (IMC) y la psicología alimentaria.16
En el cromosoma 6 se localizan los genes del sistema HLA, clases I y II, así como el del factor de necrosis tumoral alfa (TNF-α), cuyo gen (TNF) se encuentra ubicado en la banda cromosómica 6p21.3. Esta última es una potente citocina proinflamatoria secretada principalmente por macrófagos y se encuentra involucrada en diversos procesos biológicos (proliferación y diferenciación celular, coagulación, etcétera) y enfermedades (autoinmunes, resistencia a la insulina y neoplasias, entre otras) e inflamación de las vías aéreas, que repercute en la respuesta inmune e inflamatoria del asma y la obesidad. Los niveles séricos de esta citocina se han relacionado con el polimorfismo rs1800629 del gen TNF en pacientes con obesidad (razón de momios 2.4) y asma.17,18
En el brazo largo del cromosoma 11 (banda 11q13) se encuentran los genes codificantes para las proteínas UCP2-UCP3, que influyen en el metabolismo basal, regulación del peso corporal y homeostasis de la glucosa; la presencia de algunos haplotipos (rs591758, rs668514, rs647126, rs1800006) ha sido relacionada significativamente con mayor riesgo de desarrollar diabetes mellitus, principalmente en mujeres caucásicas con sobrepeso.19 Además, el brazo largo del cromosoma 12 contiene genes para citocinas inflamatorias relacionadas con el asma (IFNG, LTA4H, NOS1) y la obesidad (STAT6, IGF1) (Figura 1).20
Inflamación en asma y obesidad
La obesidad cursa con aumento de leptina en la circulación, que se correlaciona con el porcentaje de grasa corporal total, la cual puede estimular la producción de mediadores proinflamatorios a partir del tejido adiposo, como TNF-α, interleucina 6 (IL-6) e interferón gamma (INF-γ).21
Se ha propuesto que existe la posibilidad de que la leptina, relacionada con la estimulación en la producción de citocinas proinflamatorias, participe como un mecanismo regulador del asma.
El interés científico en la biología del tejido adiposo blanco (TAB) se ha incrementado a partir de la descripción de los efectos de la leptina y de la identificación de las adipocinas, un grupo de citocinas que promueven la presencia e incremento de la severidad de las enfermedades inflamatorias.
Actualmente se ha identificado que el TAB produce más de 50 factores con actividad similar a la de las citocinas. Las adipocinas utilizan mecanismos de acción endocrinos, paracrinos, autocrinos y yuxtacrinos e intervienen en una amplia variedad de procesos fisiológicos y patológicos, incluidas la inmunidad y la inflamación.
La obesidad se define como una enfermedad inflamatoria crónica de bajo grado que se asocia con inflamación sistémica originada principalmente por el tejido adiposo que secreta adipocinas, las cuales dirigen el movimiento de los leucocitos circulantes a los sitios de inflamación o lesión por quimiotaxis.
Se ha demostrado que la leptina es un factor quimiotáctico para los eosinófilos, que participan en la respuesta asmática tardía,22 además de activar la producción y secreción de mediadores inflamatorios como TNF-α, IL-6 y proteína C reactiva (PCR).23,24
El tejido adiposo de los pacientes con obesidad se caracteriza por infiltración de macrófagos (determinada por aumento de la expresión de ARNm de CD68, un marcador especifico de macrófagos) y producción de mediadores inflamatorios.25
La leptina es una hormona peptídica no glucosilada de 16 kDa, constituida por 146 aminoácidos, que se produce a partir de un precursor de 167 aminoácidos; los primeros 21 se separan dando lugar a la forma activa que posee una estructura terciaria en un conjunto de 4 hélices similar a las citocinas clase 1, codificada por el gen LEP que pertenece a la familia de citocinas clase 1.26 Es producida principalmente por los adipocitos y sus concentraciones séricas están relacionadas con la masa del TAB, disminuye la ingesta de comida, aumenta el consumo energético por medio de la inducción de factores anorexigénicos e influye en la modulación de monocitos, macrófagos, neutrófilos, basófilos, linfocitos y células dendríticas.27
Por lo tanto, la leptina se podría considerar como una hormona semejante a las citocinas con acciones pleiotrópicas, ejerce sus funciones biológicas tras la unión con sus receptores (OB-R), codificados por el gen LEPR de la superfamilia de citocinas clase 1.25 Los receptores para esta proteína se han identificado en diferentes tejidos, aunque sus concentraciones más altas se encuentran en el pulmón.28
La leptina muestra similitudes estructurales con la familia de las citocinas y su receptor (OB-R) es una proteína de membrana que pertenece a la familia gp130, clase 1 de la familia de citocinas, cuyos efectos neuroendocrinos (actúa sobre el hipotálamo como un indicador de saciedad e incrementa el metabolismo basal y el gasto energético) modifican la sensibilidad a la insulina en músculo e hígado. El gen LEP codifica para la leptina y en los humanos se ha localizado en el cromosoma 7 (q31.33); está constituido por 3 exones y 2 intrones (Figura 2).29
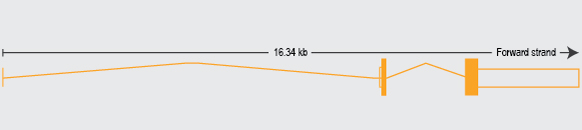
Figura 2 El gen LEP mide 20 Kb y contiene 3 exones y 2 intrones. Imagen esquemática del gen LEP, las cajas en color marrón representan los exones, la línea el intrón, la flecha indica el sentido de la transcripción. Fuente: http://www.ensembl.org
Se ha descrito una correlación entre las concentraciones elevadas de leptina y aumento en la expresión y liberación de INF-γ por las células periféricas mononucleares (respuesta Th1).30
Diversos factores pueden afectar los niveles séricos de la leptina: son relativamente bajos en la niñez pero aumentan gradualmente con la edad en ambos sexos y con el inicio de la pubertad se incrementan en las niñas y se reducen en los niños, de forma similar a lo que ocurre con el asma. También se ha registrado que permanecen constantes de las 10 a 18 horas del día, con incremento nocturno y concentraciones máximas entre las 22 y 2 horas del día,31 lo que podría asociarse con la presencia de las crisis asmáticas durante la noche o madrugada
Se ha demostrado asociación entre leptina, TNF-α, IL-6, IL-1 y PCR en los pacientes con obesidad.32 Además, IL-6 y TNF-α se han encontrado expresados en los adipocitos y se correlacionan con la grasa corporal total.
Si bien se conoce que en el asma las interleucinas IL-4 e IL-5 son mediadores importantes en la inflamación, existe escasa información acerca del papel de la leptina en esta enfermedad, en la cual también se ha demostrado incremento de la actividad de IL-1 asociado con la producción de IL-5 inducida por los linfocitos CD4.
En el asma las concentraciones séricas de TNF-α están aumentadas y con la exposición a los alérgenos se incrementan aún más. A su vez, el TNF-α aumenta el RNAm de IL-4; mientras que la producción de IL-4 disminuye la producción de TNF-α, también se incrementa la producción de IL-5 por las células epiteliales de los bronquios.
La producción de IL-6 se encuentra incrementada en el asma y se ha asociado con la estimulación de histamina, IL-4, TNF-α e IL-1; en modelos animales se ha demostrado que causa fibrosis subepitelial y puede ser un modulador clave en la remodelación de la vía aérea en el asma.33
La mayoría de los estudios sugieren que la obesidad aumenta la gravedad clínica del asma y disminuye la calidad de vida de los pacientes asmáticos. Los niveles elevados de la PCR en suero están asociados con el aumento en la gravedad del asma, por lo que se considera que la inflamación inducida por la obesidad puede contribuir a mayor gravedad de la enfermedad.34
Michelson et al. midieron los niveles séricos de PCR en pacientes con asma durante las exacerbaciones y remisión de la crisis: encontraron niveles elevados asociados con obesidad (p < 0.001) y severidad del asma, además de que existe descenso de los niveles de PCR más acentuado en los pacientes con IMC normal en comparación con los pacientes con obesidad, lo que sugiere que la gravedad de la crisis asmática aumenta a mayores niveles séricos de PCR.24
Mai et al. encontraron que en los pacientes con asma y sobrepeso, las concentraciones séricas de leptina eran del doble, en comparación con el grupo control de pacientes con asma pero sin sobrepeso. Además, el IFN-γ fue detectado con mayor frecuencia en los pacientes obesos en comparación con los que no tienen sobrepeso (61 y 12 %, respectivamente, p < 0.001).33,34
Conclusiones
La interacción entre asma y obesidad es compleja pues existen numerosos mecanismos que relacionan ambas patologías y pueden influir en la mejoría o exacerbación de los síntomas.
Cabe destacar la frecuente relación entre asma, obesidad y niveles de leptina sérica, principalmente en mujeres después de la pubertad; este aspecto es fundamental si se considera que las mujeres tienen mayor proporción de grasa corporal total en comparación con los varones, lo cual pudiera correlacionarse con el aumento en la incidencia del asma en las mujeres después de la pubertad.
Otro hecho que se debe tomar en consideración es el aumento de la gravedad de los broncoespasmos, el mayor requerimiento de medicamentos y la necesidad de atención hospitalaria prolongada en pacientes con mayor IMC, quizá por la sinergia que se produce entre los mecanismos proinflamatorios de ambas enfermedades.
El aumento en paralelo de la prevalencia de estas dos enfermedades en las últimas décadas probablemente pueda explicarse por la interacción y cercanía que tienen algunos genes relacionados con ambas patologías, que pudieran estar en alto desequilibrio de ligamiento (o segregándose juntos en una misma población).
Por lo anterior, es importante tener en cuenta la dieta, el peso y la actividad física en la evaluación y tratamiento de los pacientes en los que coexisten ambas patologías.
Resulta deseable que en futuras investigaciones en torno al asma se tome en consideración la participación de factores moleculares relacionados con la obesidad, como los marcadores genéticos de susceptibilidad o mayor gravedad, los entornos ambientales (sociales) desfavorables y la herencia, entre otros.











 nueva página del texto (beta)
nueva página del texto (beta)



