Introducción
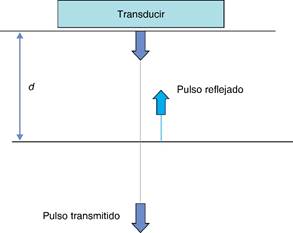
Cómo funciona el ultrasonido. El sonido es simplemente la transferencia de energía mecánica de una fuente vibratoria a través de un medio. El ultrasonido se define como sonido de una frecuencia por encima del rango audible humano, es decir, por encima de 20 kHz. Los cristales piezoeléctricos dentro de la cara del transductor tienen la propiedad de contraerse o expandirse cuando se aplica una tensión a través de ellos. Una capa delgada de un material piezoeléctrico sintético puede ser construida para vibrar a una frecuencia dentro del rango requerido. Esto actúa como una fuente de ultrasonido. Un impulso muy corto (aproximadamente 1 μs) es generado por el transductor y transmitido a los tejidos blandos. Después de la generación del «pulso», el transductor no recibe electricidad adicional durante un periodo de tiempo (aproximadamente 100-300 μs) y actúa como un «dispositivo de escucha» para detectar ecos de retorno generados dentro del medio de los tejidos blandos. A medida que la onda de ultrasonido de un ‘eco’ de retorno toca la superficie del transductor, los cristales vibran, provocando que generen una corriente eléctrica alterna. Esto se transmite de nuevo a la máquina de ultrasonido a través de los Cables conectados al transductor. La magnitud de la tensión de esta corriente se relaciona directamente con la cantidad de energía transportada por el eco de retorno y determinará el nivel de brillo mostrado para esta posición en el monitor. La máquina mide el tiempo que transcurre entre el pulso y el eco, y usando la velocidad conocida del sonido en los tejidos blandos (1540 m s-1) se puede calcular la distancia al objeto de eco. El ultrasonido de diagnóstico utiliza el principio de impulso eco para construir un sistema de dos dimensiones de las estructuras anatómicas (Figura 1).1
Los pulsos de sonido son disparados en secuencia desde múltiples cristales adyacentes a través de la cara del transductor. Éstos se utilizan para producir líneas de exploración contiguas a partir de las cuales se puede producir un «marco» de información de modo de brillo (modo B) que representa una sección transversal anatómica bidimensional. Este tipo de imágenes de ultrasonido se denomina «modo de brillo» («modo B» o «escala de grises») porque la intensidad de los ecos está representada por el brillo de la imagen de ultrasonido en esa ubicación (Figura 2).
Cuándo monitorizar el gasto cardiaco en el paciente crítico. Técnicas disponibles. El gasto cardiaco (GC) es considerado un evaluador de la función cardiaca global. Nos proporciona además información sobre la causa del choque y del fallo orgánico, por lo que representa un parámetro fundamental en la evaluación hemodinámica del paciente crítico. A pesar de todo, es necesario integrar el valor del GC con otras variables hemodinámicas (medidas de precarga, contractilidad, postcarga), signos biológicos y parámetros de oxigenación tisular para obtener una información completa que pueda guiar nuestras decisiones terapéuticas. Existe poca evidencia científica que apoye una monitorización sistemática del GC en los pacientes críticos. En muchas ocasiones, la situación de inestabilidad hemodinámica puede resolverse utilizando una valoración y monitorización más simple (exploración física, diuresis, presión arterial [PA], estimación de la precarga y parámetros de respuesta a volumen, etc.) sin necesidad de incrementar el grado de medidas o procedimientos. Sin embargo, algunos pacientes persisten con signos de hipoperfusión transcurridas las 3-6 primeras horas desde el inicio del tratamiento. En estos pacientes podría ser útil una monitorización más exhaustiva que pueda proporcionar información más detallada sobre la función cardiovascular y, por consiguiente, que permita entender el fracaso del tratamiento inicial y guiar de forma más adecuada las medidas de resucitación. Esta monitorización, que ha de incluir el GC, debería ser precoz si el paciente es refractario a las medidas iniciales.2-4
En la actualidad, disponemos de una gran variedad de métodos para monitorizar el GC con importantes diferencias entre ellos. La estimación del GC de la serie de «Puesta al día en monitorización hemodinámica» puede encontrar la información referente a los dispositivos disponibles.2 Estos dispositivos pueden ser clasificados en función del grado de invasividad. Según esta clasificación, disponemos de sistemas invasivos (CAP), semiinvasivos (termodilución transpulmonar, litiodilución, análisis del contorno de la onda de pulso, Doppler esofágico, etc.) y no invasivos (ecografía, biorreactancia, tecnología Doppler, etc.).4
Evidencia de la utilidad de la monitorización hemodinámica en el paciente crítico. La monitorización hemodinámica parte de la premisa de que la detección y el tratamiento de las alteraciones fisiopatológicas de los procesos de la enfermedad crítica deberían traducirse en un mejor pronóstico del paciente. A pesar de la lógica que se desprende de esta afirmación, el concepto «monitorización hemodinámica» ha estado sujeto a inacabables discusiones debido a la falta de trabajos que demuestren que la monitorización, per se, mejora el pronóstico de los pacientes. Dicho planteamiento podría ser equívoco, ya que el uso de determinadas variables, como las saturaciones venosas de oxígeno, en algoritmos de reanimación cardiovascular sí ha demostrado su impacto beneficioso sobre el pronóstico de diferentes patologías.2
Por otra parte, demostrar el valor pronóstico aislado de muchas variables hemodinámicas de las que disponemos va a resultar muy complejo. Éste sería el caso, por ejemplo, de la variabilidad de presión de pulso (VPP) y/o de variabilidad de volumen sistólico (VVS) como predictores de la respuesta a la administración de volumen en determinados pacientes. A pesar de su inegable sentido fisiológico, y de haber demostrado de forma concluyente su superioridad frente a las presiones de llenado cardiaco, la falta de trabajos aleatorizados demostrando específicamente que el uso aislado de una de estas variables dinámicas se asocia de forma directa a mejor pronóstico ha propiciado su exclusión de dichas variables en las diferentes recomendaciones y guías de manejo, manteniéndose, sin embargo, las ya mencionadas presiones de llenado cardiaco.
Por lo tanto, el impacto que la monitorización hemodinámica va a tener en nuestros pacientes no sólo dependerá de la fiabilidad de los sistemas utilizados, sino también del conocimiento de sus limitaciones, así como de la comprensión de las bases fisiológicas e interpretación de las variables obtenidas. La correcta utilización de estas variables, ya sea como objetivo o como herramienta en la toma de decisiones, será en última instancia la que determine el impacto beneficioso sobre la evolución del paciente. El razonamiento sería, pues, que la monitorización hemodinámica sólo se traducirá en una mejoría en el pronóstico cuando vaya asociada a un tratamiento que sí haya demostrado beneficio.5
Ecocardiografía en paciente crítico. Durante la última década, se ha incrementado significativamente el reconocimiento del ultrasonido y la ecocardiografía como herramienta para el manejo del paciente crítico. Aquellos pacientes que presentan diversos escenarios clínicos comunes pueden beneficiarse del uso de ecocardiografía. Dentro de los escenarios clínicos más frecuentes que se pueden beneficiar de la ecocardiografía se encuentran: la inestabilidad hemodinámica, hipoxemia inexplicable, posible embolismo pulmonar, daño o disección aórtica y posible endocarditis. Con frecuencia, la aplicación de la ecocardiografía produce un cambio directo en el manejo del paciente. En un estudio realizado a pacientes de cuidados intensivos, los cuales realizaron una ecocardiografía para los escenarios mencionados previamente, a 67% de los pacientes se les cambió o modificó el diagnóstico, 36% recibieron una modificación en el tratamiento, y 14% recibieron una intervención quirúrgica basados en los resultados de la ecocardiografía.6
A pesar de que se presentan dificultades en la adquisición de imágenes en paciente Unidad de Cuidados Intensivos (UCI), un estudio demostró que aproximadamente 97% de los pacientes obtuvieron un resultado que extrajo información valiosa.7 Los escenarios que pueden conducir a la adquisición de imágenes inadecuadas incluyen presencia de drenajes torácicos, empaquetamiento quirúrgico, niveles altos de presión positiva al final de la espiración o PEEP (> 15 cmH2O), incremento de peso superior al 10% comparado con el peso de ingreso, obesidad en general e hiperexpansión de tórax por enfermedad pulmonar obstructiva crónica (EPOC).8
La Red Mundial Interactiva Enfocada en Ultrasonido Crítico (WINFOCUS, por sus siglas en inglés) ha publicado un documento con su opinión y la acreditación de los médicos de cuidados intensivos. La sociedad cree que todos los médicos que atienden a pacientes de cuidados intensivos pueden beneficiarse de aprender y aplicar, por lo menos ecocardiografía básica.9
Métodos de estimación del gasto cardiaco por ecocardiografía. Los valores de normalidad del gasto cardiaco en el adulto sano en torno a 4-6.5 L/min (2.5 L/min por m2 de superficie corporal sería el índice cardiaco), en reposo. El volumen sistólico va a depender de variables como: 1) Precarga, 2) postcarga y 3) contractilidad miocárdica.
Las causas de hipotensión y choque se pueden separar en bajo gasto y alto gasto cardiaco con estado de baja postcarga. Debido a esto, el cálculo ecocardiográfico del gasto cardiaco puede ayudar a guiar el diagnóstico diferencial. Si el gasto cardiaco es bajo, entonces la causa más probable es hipovolemia o pobre contractilidad. Si el gasto cardiaco es normal o alto, un choque vasodilatador es la causa más probable. Se ha demostrado que la estimación no invasiva del gasto cardiaco en pacientes críticamente enfermos se correlaciona bien con otros estudios de estándar de oro.10
El uso de ecocardiograma en la Unidad de Cuidados Intensivos (UCI) ha demostrado que ofrece mejor información de la función miocárdica que el uso de los índices derivados del catéter en la arteria pulmonar. La ecocardiografía también permite la identificación de las anormalidades regionales del movimiento de las paredes cardiacas.10
Volumen sistólico en modo bidimensional y cálculo de gasto cardiaco
La forma más frecuente de conocer la función sistólica del ventrículo izquierdo (VI) es calculando la fracción de eyección del ventrículo izquierdo (FEVI), hay diferentes métodos, pero el que ofrece valores más exactos es calcular el volumen sistólico en modo bidimensional o también llamado Simpson modificado.
Simpson modificado: en este método se hacen múltiples cortes al VI en cuatro cámaras y dos cámaras en sístole y en diástole, y se promedian (VI en sístole y VI en diástole).
La obtención del gasto se realiza calculando el volumen eyectivo (volumen sistólico en modo bidimensional o también llamado Simpson modificado) y se multiplica por la frecuencia cardiaca (FC).11,12
Gasto cardiaco = FEVI (cm3) x FC
Medición del gasto cardiaco mediante ecocardiografía Doppler o ecuación de continuidad (ecuación de Bernoulli)
Fundamentos físicos: Ley de Doppler. La aplicación de ultrasonidos en el rango de 2-10 MHz con capacidad de interactuar con los tejidos humanos (en nuestro caso, su capacidad de reflexión sobre los eritrocitos en movimiento) constituye la base de todos los monitores que utilizan el efecto Doppler para medir el GC. La ley de Doppler expresa la relación matemática existente entre el cambio aparente que se produce en la frecuencia de una onda acústica cuando el emisor y/o el receptor se encuentran en movimiento relativo.
Existen diversos modos de estimar el gasto cardiaco mediante ecocardiografía, que se basan tanto en métodos volumétricos como en la tecnología Doppler en sus distintas modalidades (pulsado, continuo o Doppler color). De las diversas técnicas, la que presenta una mejor concordancia con las mediciones realizadas con la presión capilar pulmonar y es de uso más frecuente en la práctica clínica es la medición del gasto cardiaco por Doppler pulsado en el tracto de salida del ventrículo izquierdo (TSVI),13,14 determinando dos variables: el diámetro del TSVI para calcular el área de su sección (AS) y el espectro de velocidad del flujo (ITV) para calcular la distancia latido (DL).15,16
Objetivos de este estudio. Objetivo general: Comparar el gasto cardiaco por medio de ecocardiografía Doppler a través de la medición de volumen sistólico en modo bidimensional vs ecuación de continuidad en pacientes de las unidades de cuidados intensivos del Hospital General de Ecatepec «Las Américas».
Objetivos específicos: 1) Demostrar que el gasto cardiaco medido es similar por ambas técnicas. 2) Medir el gasto cardiaco en las principales patologías en la terapia intensiva. 3) Determinar el gasto cardiaco en pacientes con o sin soporte de aminas. 4) Determinar el gasto cardiaco en pacientes con y sin ventilación invasiva.
Material y métodos
Diseño del estudio: observacional, prospectivo, transversal y comparativo.
Criterios de inclusión: 1) Pacientes admitidos en el Hospital General de Ecatepec «Las Américas» en el Área de Terapia Intensiva y Terapia Neurointensiva en el periodo de tiempo comprendido del 1 de enero de 2018 al 31 de marzo de 2018. 2) Pacientes entre 18 a 90 años de edad. 3) Pacientes que aceptaron participar en el estudio previa firma de carta de consentimiento informado. 4) Pacientes en los que técnicamente fue realizable la ecocardiografía con la obtención de la ventana de eje largo paraesternal y eje apical cinco cámaras.
Criterios de exclusión: 1) Pacientes que no cumplieron los rangos de edad. 2) Pacientes que no aceptaron participar en el estudio previa firma de carta de consentimiento informado. 3) Pacientes en los que técnicamente fue imposible realizar la ecocardiografía con la obtención de la ventana de eje largo paraesternal y eje apical cinco cámaras.
Criterios de eliminación: Pacientes que en cualquier momento quisieron salir del estudio.
Variables. La conceptualización y operacionalidad de las variables se muestran en la Tabla 1.
Tabla 1: Conceptualización y operacionalidad de las variables.
| Variable | Definición conceptual | Definición operacional | Escala de medición | Indicador |
|---|---|---|---|---|
| Edad | Tiempo transcurrido desde el nacimiento hasta el momento del estudio en años | Se tomará la edad cumplida en años al momento del estudio | Cuantitativa discreta | Años |
| Sexo | Condición biológica y fisiológicas que distinguen al hombre de la mujer | Diferencia anatómica entre hombre y mujer | Cualitativa nominal | 1. Femenino |
| 2. Masculino | ||||
| Peso | Fuerza de gravitación universal que ejerce un cuerpo celeste sobre una masa | Se tomará el peso en kilogramos al momento del estudio | Cuantitativa continua | Kilogramos |
| Talla | Estatura o altura de las personas. Distancia que hay entre la planta de los pies a la parte más alta de la cabeza | Se tomará la talla en centímetros al momento del estudio | Cuantitativa continua | Centímetros |
| Diagnóstico | Patología por la cual el paciente se encuentra hospitalizado | Se tomará del expediente el diagnóstico principal por el cual el paciente fue ingresado al momento del estudio | Cuantitativa nominal | 1. Choque séptico |
| 2. Preeclampsia severa | ||||
| 3. Choque hipovolémico | ||||
| 4. Politraumatizado | ||||
| 5. Traumatismo craneoencefálico severo | ||||
| 6. ARDS/neumonía | ||||
| 7. Choque cardiogénico | ||||
| 8. Cetoacidosis diabética | ||||
| 9. Pancreatitis grave | ||||
| 10. Postoperado de LAPE abdominal | ||||
| Frecuencia cardiaca | Número de latidos por minuto del corazón de los pacientes participantes | Resultado numérico en latidos por minuto | Cuantitativa discreta | Latidos por minuto |
| Diámetro de anillo aórtico (DAAO) | Medida del diámetro a nivel del anillo aórtico a no más de 1 a 2 milímetros por arriba de la inserción de la válvula aórtica, obtenida en ecocardiografía en eje largo paraesternal | Resultado numérico en centímetros | Cuantitativa continua | Centímetros |
| Gasto cardiaco por volumen sistólico en modo bidimensional | Medida obtenida de la siguiente fórmula: (VS/frecuencia cardiaca) | Resultado numérico en litros por segundo | Cuantitativa continua | Litros por segundo |
| Promedio de la integral de velocidad tiempo del tracto de salida de ventrículo izquierdo | Promedio de 3 ciclos cardiacos de la integral obtenida por el software del ultrasonido SonoSite, después de hacer el trazado del espectro Doppler del flujo de sangre en sístole del tracto de salida del ventrículo izquierdo obtenida en ecocardiografía en eje apical 5 cámaras | Resultado numérico en centímetros | Cuantitativa continua | Centímetros |
| Gasto cardiaco medido por ecografía Doppler con aplicación de la ecuación de continuidad | Medida obtenida de la siguiente fórmula: (DAAo 0.785) (IVTTSVI) (FC)/1000 | Resultado numérico en litros por minuto | Cuantitativa continua | Litros/minuto |
Desarrollo del proyecto. Previa autorización del protocolo por el Comité de Ética y el Departamento de Enseñanza e Investigación del Hospital General Ecatepec «Las Américas», y una vez seleccionadas las pacientes que cumplieron con los criterios de inclusión del estudio, se les informó del tipo de investigación a realizar y se obtuvo carta de consentimiento informado, la cual fue firmada por su familiar.
Preparación: el paciente debe estar en decúbito supino, se retiran cables de monitoreo convencional que puedan hacer interferencia, posteriormente se coloca gel trasmisor de ultrasonido a nivel apical (punto localizado a nivel medio clavicular izquierdo entre el sexto y el octavo espacio intercostal) y nivel paraesternal (localizado a nivel paraesternal izquierdo entre el segundo y cuarto espacio intercostal), se coloca el transductor sectorial con la marca hacia la derecha para la ventana apical y hacia la izquierda para la ventana paraesternal.
1. Se procedió a obtener con el ultrasonido SonoSite, por medio del transductor sectorial de 3-5 MHz, el eje largo paraesternal y se realizó la medición del anillo aórtico, a nivel de éste o a no más de 1 a 2 mm por arriba de la intersección de la válvula aórtica. El trazo de medida se hizo perpendicular a las paredes del anillo, bajo el borde interno superior a borde interno inferior, obteniendo el resultado en centímetros.
2. Se procedió a obtener por medio de ultrasonido SonoSite el eje apical 5 cámaras. Se colocó el Doppler pulsado en dirección del tracto de salida del ventrículo izquierdo en la parte media, cuidando que la distancia entre éste y la válvula aórtica fuera menor a 30 mm. Se obtuvo el espectro Doppler de flujo de sangre que va hacia la válvula aórtica. Una vez obtenido este espectro, se hizo el trazado de tres ciclos cardiacos para que el software del ultrasonido obtuviera la medida de la integral de velocidad tiempo en cada uno, se tomó el promedio y se reportó en centímetros.
3. Se anotó la frecuencia cardiaca al momento de realizar el estudio ecocardiográfico.
4. Por medio de la medida del anillo aórtico, el promedio de la integral de velocidad tiempo y la frecuencia cardiaca, se obtuvo el gasto cardiaco aplicando la ecuación de continuidad, obteniendo el resultado en litros por minuto.
5. Con esta información se realizó el llenado de las hojas de recolección de datos.
6. Con las hojas de recolección de datos, posteriormente se realizaron cálculos de promedios, medias aritméticas y desviaciones estándar. Con estos datos se hicieron gráficas y tablas descriptivas, se sacó el coeficiente de correlación de Pearson, se consideró una r > 0.75 para inferir una aceptable correlación positiva entre las dos medidas.
Análisis estadístico. Los resultados fueron evaluados a través de estadística descriptiva para variables cualitativas, se emplearon medidas de tendencia central y dispersión, proporción y porcentaje.
Para las variables cuantitativas se utilizaron medidas de tendencia central: media, límite inferior y límite superior. Y de medida de dispersión: desviación estándar.
Se realizó una prueba de correlación para verificar que ambos métodos son equiparables mediante correlación de Pearson y correlación rho de Spearman.
Resultados
Fueron incluidos en el estudio un total de 56 pacientes. El promedio de edad fue 43 años (rango: 19 a 85 años, mediana 34 años, moda: 22 años).
La talla promedio fue 1.61 m (límites: 1.45-1.80 m), el peso promedio 68 kg (rango: 42-98 kg). La frecuencia cardiaca el promedio fue de 94 latidos por minuto (lpm) (límites: 70-128 lpm). La distribución por género fue 24 (43%) mujeres y 32 (57%) hombres.
La Tabla 2 muestra los diagnósticos de los pacientes. Los más frecuentes fueron choque séptico (18%) y trauma craneoencefálico (16%).
Tabla 2: Diagnósticos de los pacientes estudiados.
| Patologías | n | % |
|---|---|---|
| Choque séptico | 10 | 18 |
| Preeclapmsia severa | 5 | 9 |
| Choque hipovolémico | 3 | 5 |
| Politraumatizado | 6 | 11 |
| Trauma craneoencefálico severo | 9 | 16 |
| ADRS/neumonía | 4 | 7 |
| Choque carcinogénico | 4 | 7 |
| Cetoacidosis diabética | 5 | 9 |
| Pancreatitis grave | 4 | 7 |
| Postoperado de LAPE abdominal | 6 | 11 |
| Total | 56 | 100 |
Abreviaturas: SDRA = Síndrome de dificultad respiratoria aguda. LAPE = laparotomía exploradora.
De los 56 pacientes estudiados, sólo 21 (37%) tenían apoyo con vasopresor. Los restantes 35 (63%) no recibieron vasopresores.
En cuanto a ventilación mecánica, 30 (53%) recibieron este apoyo; la presión positiva al final de la expiración (PEEP) empleada en estos casos fue menor o igual a 8 mmHg en 23 (41%) pacientes y mayor de 8 mmHg en siete (12%). Los restantes 26 (47%) no recibieron ventilación mecánica.
Correlación entre los métodos de medición del gasto cardiaco. Se obtuvo un gasto cardiaco por volumen sistólico en modo bidimensional en promedio de 5.2 L/min (límites: 2.5 a 8.7 L/min, desviación estándar: 1.38). Mientras que con el método de gasto cardiaco medido por ecografía Doppler con aplicación de la ecuación de continuidad el promedio fue 6.0 L/min (rango: 3.2 a 9.8 L/min, desviación estándar: 1.49).
La correlación de Pearson mostró un coeficiente de 1 para el método de gasto cardiaco por volumen sistólico en modo bidimensional y un coeficiente de correlación de 0.856 para gasto cardiaco medido por ecografía Doppler con aplicación de la ecuación de continuidad. Esto indica una correlación lineal positiva, significativa en el nivel 0.01 (bilateral). Es decir, ambos métodos son parecidos.
Con la correlación rho de Spearman, se obtuvo un coeficiente de correlación 1 para gasto cardiaco por volumen sistólico en modo bidimensional y un coeficiente de correlación de 0.851 para gasto cardiaco medido por ecografía Doppler con aplicación de la ecuación de continuidad. Estos coeficientes señalan una correlación lineal positiva, significativa en el nivel 0.01. Es decir que ambos métodos son parecidos.
Discusión
Ante la disminución de la utilización del catéter de la arteria pulmonar debido a la controversia de no mejorar la mortalidad en los pacientes de las unidades de terapia intensiva, la colocación de dicho catéter ha caído en desuso; sin embargo, el gasto cardiaco medido por el catéter de Swan-Ganz sigue siendo el estándar de oro para la medición en tiempo real del gasto cardiaco. La medición de gasto cardiaco por médicos cardiólogos desde los años 60 comparada con la medición de gasto cardiaco mediante ecuación de continuidad, descrita desde los años 90 y publicada por WINFOCUS 2008, para la utilización en el paciente crítico,17,18 muestra que ambas se relacionan de forma estadísticamente significativa. La desventaja que existe es «el operador dependiente» ya que se necesita adiestramiento en la medición del flujo aórtico, pero en menor tiempo que el adiestramiento para medición de gasto cardiaco medido por volumen sistólico en modo bidimensional. Hasta el momento, ninguna de ellas cumple todas las características necesarias para ser considerada como excelente: no invasiva, continua, fiable, reproducible, cómoda tanto para el paciente como para el profesional y exacta. Por lo tanto, la utilización de cada una de ellas va a depender fundamentalmente de su disponibilidad y de los conocimientos o aptitudes del profesional.
El uso de la ecocardiografía ha demostrado que influye de manera significativa en el manejo del paciente con inestabilidad hemodinámica. En un estudio, el examen de FATE se utilizó para la optimización de la hemodinámica en 210 pacientes inestables. En 38% de los casos, los datos obtenidos apoyan la información ya disponible. En 37% hubo nuevos descubrimientos pertinentes, y en 25% se obtuvo información determinante que influyó o cambio el tratamiento del paciente. Los cambios más comunes instituidos después del examen de FATE fueron modificaciones de la terapia de volumen y apoyo inotrópico.17
Poelaert y colaboradores encontraron que de 64% de los pacientes con un catéter de Swan-Ganz en la Unidad de Cuidados Intensivos, 44% recibieron cambios terapéuticos tras un ecocardiograma; mientras que de los pacientes sin catéter de Swan-Ganz el ecocardiograma llevó a un cambio en el tratamiento en 41% de los casos. En resumen, se concluyó que el ecocardiograma produjo cambios en el tratamiento en un tercio de los pacientes graves, independientemente de que tuvieran insertado o no un catéter de Swan-Ganz. Por otra parte las presiones elevadas de pericardio y pleura pueden producir infrallenado fisiológico de los ventrículos y esto no puede ser diagnosticado con catéter de Swan-Ganz, pero es fácilmente identificado con el ecocardiograma.
A lo largo de los últimos años se han estudiado nuevos métodos que han llegado a reemplazar el uso del catéter de la arteria pulmonar para la determinación del gasto cardiaco.19 Estas nuevas tecnologías varían ampliamente entre ellas, de muy invasivas a menos invasivas y hasta no invasivas, proporcionan índices dinámicos de respuesta a los fluidos, otras permiten valorar variables de precarga volumétrica. Todas estas técnicas han sido valoradas y validadas mediante la comparación de sus resultados con el considerado estándar de oro, que aún hoy en día sigue siendo la termodilución intermitente de la arteria pulmonar.
Conclusiones
La medición del gasto cardiaco mediante volumen sistólico en modo bidimensional se relaciona de forma significativa con la medición de gasto cardiaco medido por ecografía Doppler con aplicación de ecuación de continuidad. Infravalorada por médicos cardiólogos, ambas son herramientas no invasivas; y la última puede ser reproducible, con la finalidad de continuar aplicándola a cabecera de paciente y mejorar la monitorización hemodinámica de los pacientes críticos. Sin lugar a dudas nuestro estudio adolece del hecho de que es un estudio con un número pequeño de pacientes.











 nova página do texto(beta)
nova página do texto(beta)