Introducción
La Medicina del Enfermo en Estado Crítico es una subespecialidad que en nuestros tiempos es esencial para el funcionamiento de los centros hospitalarios, ya que se encarga de manejar a los pacientes que ya no pueden seguir siendo tratados en áreas generales de hospitalizacion:1 los enfermos hospitalizados en los que no se tiene un pronóstico fatal inherente a su patología de base o a su estado de gravedad inicial, en los que, a pesar del manejo estándar para el proceso patológico original, han alcanzado un estado de pérdida de la homeostasis grave, que lleva a la presencia de la disfunción orgánica, que los hace requirentes de soporte externo para mantener la vida, siendo así pacientes candidatos al área de terapia intensiva; área especializada del hospital que tendrá que contar con la infraestructura y el personal especializado que pueda mantener esa función a costa de un soporte de vida. Este manejo tendrá el objetivo de dar tiempo al paciente y permitir, una vez que sea tratado el factor desencadenante, que la función orgánica se recupere o llevar al enfermo a un estado de homeostasis que le permita permanecer con vida, manejo que intenta evitar que la disfunción orgánica sea sumatoria a otros sistemas hasta llegar a la disfunción de múltiples órganos y la muerte del paciente.
Este estudio está enfocado en una pequeña parte del mundo tan vasto de la medicina crítica.
Enfocándonos ya en el tema a tratar de nuestro estudio, mencionamos que para la medicina crítica es esencial, por medio del monitoreo cardiovascular avanzado, determinar de manera fidedigna la causa por la que el enfermo desarrolló pérdida de la homeostasis. Además, una vez implementado el manejo específico de soporte, es muy importante poder monitorizar en tiempo real los cambios posteriores para tratar de llegar a metas preestablecidas.
Sin duda, poder determinar la hemodinamia del paciente da información de gran relevancia al médico de la terapia intensiva para poder tomar decisiones de vitalidad para sus pacientes.
La hemodinamia (del griego, αἷμα (haima) sangre y δύvαμις (dynamis) potencia) es el estudio del movimiento de la sangre a través del sistema vascular. Es difícil imaginar cómo serían los conceptos actuales de las enfermedades críticas sin los enormes conocimientos fisiológicos y anatómicos derivados de los últimos 60 años de estudio de ésta. André Cournand comentó al recibir el Premio Nobel en 1956, «el catéter cardiaco fue la llave en la cerradura». Al «girar esta llave», Cournand y cols. nos han llevado a una nueva era en la comprensión de la función cardiaca normal y la fisiopatología de las enfermedades críticas de los seres humanos. Hace tan sólo cuatro décadas, Swan y Ganz introdujeron a la práctica clínica un catéter terminado en un balón inflable en el que el flujo sanguíneo permite llevar la punta hasta la arteria pulmonar.
Hoy en día, la medición rutinaria de presiones, flujos y resistencias en las diferentes cámaras del corazón y lechos sistémico y pulmonar permite la objetivación del compromiso hemodinámico de diferentes condiciones fisiopatológicas y definir si el paciente se encuentra en estado de choque y qué tipo de choque es, logrando discernir entre un estado de choque hiperdinámico y uno hipodinámico.
El estado de choque hiperdinámico se refiere al hecho de que el paciente mantiene un gasto cardiaco dentro de parámetros normales o altos, pero que existe otra causa que hace que el gasto cardiaco sea insuficiente para alcanzar un aporte de oxígeno adecuado; situación que en la mayoría de las ocasiones se presenta por una pérdida de la función de la mecánica vascular, que hace que las resistencias vasculares sistémicas se encuentren por debajo de los límites de la normalidad, llevando al enfermo a un estado de vasodilatación importante. Estos mecanismos son específicos del estado de choque anafiláctico y del estado de choque séptico.2 En este último, además de los mecanismos ya referidos, también puede presentarse una disfunción mitocondrial y de la microcirculación, que llevan a una falla metabólica y a una disminución en el número de capilares para el intercambio y utilización de oxígeno.3
El estado de choque hipodinámico se refiere al hecho de que el paciente desarrolló esta patología debido a una disminución en el gasto cardiaco, situación que se presenta por una disminución en el volumen de eyección del ventrículo izquierdo, que puede ser secundaria a tres procesos: una disfunción de la bomba cardiaca, denominándose, si éste es el caso, como choque cardiogénico; a una disminución en el volumen intravascular, estado denominado como choque hipovolémico, y, por último, a una obstrucción al flujo de sangre del ventrículo derecho o a un proceso de compresión externa del corazón que no permite que haya un llenado cardiaco adecuado, ambas situaciones denominadas como estado de choque obstructivo.3
En este contexto, la monitorización cardiovascular avanzada con la medición del gasto cardiaco sería una medida más fidedigna para poder realizar esta clasificación de manera correcta. Se requiere, sin lugar a dudas, esta medida tanto como medida directa como para poder inferir las resistencias vasculares sistémicas. El hecho de que no se realice adecuadamente este diagnóstico diferencial puede llevar a errores en el manejo del paciente que resulten peligrosos.
Una vez que se realiza el diagnóstico específico de la causa del estado de choque, se tienen que implementar medidas terapéuticas para poder llevar al paciente a la remisión del proceso de hipoperfusión tisular. En este contexto, igualmente la medida del gasto cardiaco se convierte en una meta terapéutica a alcanzar.4,5
Gasto cardiaco, definición e historia
La medida del gasto cardiaco se refiere a la cantidad de sangre que sale de los ventrículos del corazón a la circulación mayor o menor, según sea el caso del ventrículo izquierdo o derecho, por unidad de tiempo (casi siempre referida en un minuto); por lo tanto, sus unidades de medición serán los litros por minuto (L/min), la fórmula ampliamente descrita en textos de la literatura médica se describe como sigue:4,5
GC = VEV × FC
GC = Gasto cardiaco
VEV = Volumen de eyección ventricular
(por latido cardiaco)
FC = Frecuencia cardiaca (latidos por minuto)
La técnica de medición de gasto cardiaco fue descrita por primera vez en 1870 por Adolf Fick,4,6 quien calculó el gasto cardiaco de un animal utilizando el consumo de oxígeno y las concentraciones de oxígeno en muestras de sangre arterial y venosa.4,7,8
GC = VO2/(CaO2 - CvO2)
GC = Gasto cardiaco
VO2 = Consumo de oxígeno
CaO2 = Contenido de oxígeno arterial
CvO2 = Contenido de oxígeno venoso
En 1897, Stewart describió experimentos con el principio de dilución de indicadores, inyectó cloruro de sodio en la circulación venosa central de animales y midió posteriormente su concentración en la arteria femoral.9 Hamilton modificó este principio para dar cuenta de las concentraciones variables de inyectado diluido en el tiempo, desarrollando una curva de concentración a través del tiempo para reflejar este fenomeno.7 Pudo demostrar, entonces, que el gasto cardiaco fue igual a la cantidad de colorante indicador (verde de indocianina) inyectado, dividido por la integral del área bajo la curva de dilución medida en el lado arterial, conocida hoy como la ecuación de Stewart-Hamilton.9
Flujo = (Ci Vi)/∫ C(t)dt
Ci = Concentración inicial del inyectado
Vi = Volumen inicial de inyección
∫ = Integral
C(t) = Concentración de inyectado diluido en el tiempo
dt = Área bajo la curva de la dilución
Basándose en el mismo concepto de la dilución de indicadores, Fegler introdujo la termodilución en 1954, inyectando una solución fría como indicador y midiendo los cambios en la temperatura sanguínea detectados distalmente.10 En 1970, Swan et al. desarrollaron lo que denominaron un catéter de lumen múltiple dirigido hacia la arteria pulmonar, por medio de un globo de flotación, denominado actualmente como catéter de Swan-Ganz o catéter arterial pulmonar (CAP).11 La introducción de este dispositivo permitió a los médicos medir el gasto cardiaco por termodilución.
Después de 50 años, este método todavía se considera el estándar de oro clínico para la medición del gasto cardiaco.4
En la actualidad, existe una variedad muy amplia de métodos tanto invasivos como no invasivos para poder realizar una medición del gasto cardiaco.4,5 Para fines de nuestro estudio nos enfocaremos en dos métodos no invasivos que describiremos de manera detenida.
Medición del gasto cardiaco por evaluación ecocardiográfica Doppler y utilización de la ecuación de continuidad
La medición del gasto cardiaco (GC) mediante el uso de dispositivos basados en la tecnología Doppler ha experimentado un crecimiento exponencial en los últimos años debido, fundamentalmente, a su no invasividad respecto al catéter arterial pulmonar y a la introducción, lenta, pero imparable, de la ecocardiografía en la unidad de cuidados intensivos como medio diagnóstico y como monitor hemodinámico.5
Fundamentos físicos
La aplicación de ultrasonidos en el rango de 2-10 MHz con capacidad de interactuar con los tejidos humanos (en nuestro caso, su capacidad de reflexión sobre los eritrocitos en movimiento) constituye la base física para la determinación ecocardiográfica del gasto cardiaco por medio de la utilización de la ecuación de continuidad, principio físico que de igual forma utiliza el monitor USCOM.5
La ley de Doppler expresa la relación matemática existente entre el cambio aparente que se produce en la frecuencia de una onda de ultrasonido cuando el emisor y/o el receptor se encuentran en movimiento relativo. La formulación matemática es la siguiente:5,12
Δf = (2ft(v/c))(cos Ꝋ)
Δf = Cambio de frecuencia.
ft = Frecuencia original transmitida
v = Velocidad relativa entre emisor y receptor
c = Velocidad del sonido en el medio (en los tejidos humanos blandos se toma como media
1.54 m/s)
cos Ꝋ = Coseno del ángulo de incidencia
entre emisor y receptor.
A nivel práctico, esta propiedad nos sirve para, mediante un transductor que es capaz de generar y detectar ultrasonidos, enviar un haz de ultrasonidos de ft conocida a nivel cardiovascular (tracto de salida del ventrículo izquierdo o derecho, aorta ascendente y descendente), que en parte chocarán contra los eritrocitos en movimiento y volverán a ser detectados a una frecuencia distinta con la que fueron enviados, con lo que podrá calcularse Δf. Si tenemos en cuenta que además conocemos el valor de c y el valor de cos Ꝋ es un valor fijo en algunos dispositivos y en otros puede calcularse (dadas las características matemáticas de la función coseno, se consideran clínicamente aceptables hasta 30-40o).5,12
La única variable que nos queda por conocer es v que podremos despejar:
v = Δf (c/2) ft cos Ꝋ
Dicha v es la velocidad de los eritrocitos en movimiento y, en consecuencia, la velocidad del flujo sanguíneo.5,12
Existen dos modos distintos de aplicar el efecto Doppler al estudio de la velocidad del flujo sanguíneo que nos proporcionarán informaciones distintas. Tanto si se usa el Doppler continúo como el pulsado, el análisis matemático mediante integración (cálculo del área bajo la curva) a lo largo de un ciclo cardiaco nos dará como resultado lo que se conoce como integral velocidad-tiempo (IVT) en centímetros. Esta medida representa la longitud de una columna de sangre que pasa por un punto determinado durante un ciclo cardiaco. Posteriormente, asumiendo que el punto donde calculamos el espectro de velocidad posee determinadas características geométricas, que habitualmente se asume como circular en el sistema cardiovascular (anillo aórtico), podremos calcular el área de su sección mediante su medición directa, asumiendo una geometría circular por medio de la siguiente fórmula:5,12-15
πr2
π = 3.1416
r = Radio del diámetro total medido
Con todas estas variables se podrá calcular a continuación el volumen sistólico y el gasto cardiaco con la ecuación de continuidad:5,12-15
GC = ((πr2)(IVT)(FC))/1000
GC = Gasto cardiaco en litros por minuto
π = 3.1416
r = Radio del área seccional
IVT = Integral de velocidad tiempo en centímetros
FC = Frecuencia cardiaca en latidos por minuto
Se puede, además, hacer una simplificación de la fórmula sustituyendo el valor de π de la siguiente manera:13-15
GC = ((π (D/2)2)(IVT)(FC))/1000
GC = ((D2π/22)(IVT)(FC))/1000
GC = (D2 (3.1416/4))(IVT)(FC))/1000
GC = ((D2 0.785) (IVT) (FC))/1000
Monitor ultrasónico de gasto cardiaco (USCOM)
Recientemente, se ha centrado mucho interés en los dispositivos de medición no invasiva de gasto cardiaco que utiliza tecnología Doppler. Para que un dispositivo de este tipo sea útil clínicamente debe ser preciso, claro y ser capaz de detectar cambios direccionales significativos, que reflejen la respuesta del corazón a una intervención, más comúnmente cambios en el volumen sistólico y gasto cardiaco.16,17 El monitor ultrasónico de gasto cardiaco (USCOM) es un dispositivo no invasivo de ultrasonido Doppler de onda continúa. Este dispositivo tiene una precisión medida por espectro Doppler de 2-3 Herz16,18 El transductor del dispositivo USCOM se coloca en el hueco supraesternal, para medir el gasto cardiaco de corazón izquierdo, o en la región precordial, para medir el gasto cardiaco de corazón derecho; es importante que el operador, por medio de la observación en la pantalla del dispositivo, dirija el transductor para obtener una imagen adecuada.19
El dispositivo detecta y grafica un espectro Doppler del flujo de la válvula pulmonar o aórtica. Para fines de nuestro estudio obtendremos la medición del gasto cardiaco del ventrículo izquierdo, por lo que nos enfocaremos en la obtención del espectro Doppler de flujo aórtico. Por medio del espectro obtenido, el monitor realiza la determinación de la integral de velocidad tiempo y de la frecuencia cardiaca por minuto. Para obtener de manera correcta el espectro Doppler, los fabricantes del monitor recomiendan realizar movimientos de manera sistematizada.15-19,20-29
De inicio, se requiere colocar el transductor en el hueco supraesternal, dibujando una línea paralela con respecto al esternón del paciente. Posteriormente, se realiza un movimiento de angulación dirigida hacia la cabeza del paciente, cuidando de no despegar por ningún motivo el transductor de la piel. Durante el proceso, el operador tiene que estar pendiente de la pantalla del monitor, observando las características del espectro Doppler dibujado. Inicialmente, se reconoce un perfil sistólico de baja velocidad y de duración sistólica corta. Este es el flujo de la aorta ascendente.19
Los movimientos de angulación deberán ser lentos para ir valorando al mismo tiempo las características del espectro Doppler en la pantalla del monitor. Al continuar inclinando el transductor, la velocidad del espectro aumentará a medida que el haz se alinea con la dirección del flujo aórtico, además, los lados del triángulo se volverán más rectos y tendrán más definición. El mejor ángulo de insonación será el que obtenga la mayor definición de ambos lados del espectro y la mayor velocidad de flujo. De principio probablemente la punta del triángulo del espectro será difusa y no bien definida. El siguiente paso es proceder a realizar movimientos de basculación del transductor entre las 4:00 y 8:00 horas en comparación con las manecillas de un reloj. Esto con el objetivo de mejorar la calidad de la imagen y así determinar una mejor área bajo la curva.19
El dispositivo cuenta con un software que puede también estimar por medio de la aplicación de ecuaciones de regresión indexadas a la altura del paciente, el diámetro de la sección transversal de la válvula aórtica.16,30 Una vez obtenidas estas tres mediciones, es capaz de calcular el gasto cardiaco con la fórmula de continuidad, ya referida con anterioridad, en el apartado de Doppler.13-15
EL monitor USCOM fue probado positivamente en estudios con catéteres de flujo en animales.16,31,32 Este monitor también ha sido comparado para su validación con el catéter de arteria pulmonar con resultados positivos.33 Dos estudios publicados recientemente por un grupo han sugerido que el USCOM en comparación con el monitor Doppler esofágico es capaz de realizar un seguimiento adecuado de los cambios en volumen sistólico después de intervenciones en los pacientes.34,35
Material y métodos
Se realizó un estudio tipo observacional, prospectivo, longitudinal y comparativo.
Definición de las variables
Promedio de la integral de velocidad-tiempo: cuantitativa. Definición operacional: promedio de tres ciclos cardiacos de la integral obtenida por el software del USCOM, después de hacer el trazado del espectro Doppler del flujo de sangre en sístole del tracto de salida del ventrículo izquierdo. Resultado: numérico en centímetros.
Frecuencia cardiaca: cuantitativa. Definición operacional: número de latidos por minuto del corazón de los pacientes participantes. Resultado: numérico en latidos por minuto.
Volumen sistólico: cuantitativa. Definición operacional: volumen de sangre que el corazón expulsa hacia la aorta durante el periodo de contracción (sístole).Resultado: numérico en mililitros.
Gasto cardiaco: cuantitativa. Definición operacional: medida del gasto cardiaco arrojada por la máquina de USCOM posterior a realizar la medición en hueco supraesternal de flujo aórtico y a agregar la edad, talla y peso de cada paciente al dispositivo. Resultado: numérico en litros/minuto.
Índice cardiaco: cuantitativo. Definición operacional: relación entre el volumen de sangre evacuado por el corazón cada minuto y los metros cuadrados de la superficie del cuerpo. Resultado: litros/minuto/m2.
Resistencias vasculares sistémicas: cuantitativo. Definición operacional: es la resistencia que ofrece el sistema vascular (excluida en este caso la circulación pulmonar) al flujo de sangre. Resultado: numérico en dinas/m2.
Variabilidad de volumen sistólico: cuantitativo. Definición operacional: fenómeno natural por el que la presión del pulso arterial baja durante la inspiración y sube durante la espiración debido a las variaciones en la presión intratorácica secundarias a la ventilación con presión negativa. Resultado: numérico en milímetros de mercurio.
Índice de inotropismo: numérico. Definición operacional: hace referencia al potencial y a la energía cinética suministrada para poder realizar un latido de VI. Resultado: numérico en W/m2.
Poder cinético (PKR): numérico. Definición operacional: cantidad de energía necesaria para poder desplazar un volumen en un área específica en una unidad de tiempo, manteniendo una adecuada relación flujo-presión.
Tamaño de la muestra: pacientes de entre 16 y 65 años que cumplieron con los estándares para poder donar sangre en un periodo del 01 de marzo de 2017 tomando la muestra hasta la fecha; sin embargo, el proyecto aún se encuentra en curso.
Muestra: no fue necesario realizar ningún tipo de muestra, ya que el universo de estudio pudo incluirse en su totalidad.
Criterios: fueron incluidos en el estudio todos los pacientes de entre 16 y 65 años, entre el periodo de 01 de marzo de 2017 hasta la fecha (sin embargo, el proyecto continua en curso), los cuales aceptaron participar, previa firma de consentimiento informado en el estudio.
Criterios de inclusión: Pacientes citados en el Banco de Sangre Estatal en el periodo comprendido desde el 01 de marzo del 2017 hasta la fecha, proyecto aún en curso. Pacientes de entre 16 y 65 años de edad. Pacientes que se encontraban sanos. Pacientes que aceptaron participar en el estudio, previa firma de carta de consentimiento informado. Pacientes en los que técnicamente fue realizable la medición de las variables con el monitor ultrasónico USCOM.
Criterios de exclusión (Anexo 1): Pacientes que no cumplieron los rangos de edad. Pacientes que no aceptaron participar en el estudio, previa firma de carta de consentimiento informado. Pacientes en los que técnicamente fue imposible realizar la medición técnica de las variables con el monitor ultrasónico USCOM.
Criterios de eliminación: Pacientes que en cualquier momento quisieron salir del estudio.
Resultados
Una vez realizado el estudio y aplicados los criterios de inclusión, exclusión y eliminación en la población estudiada, se logró recabar la información de un total de 120 pacientes.
En las Figuras 1 a 4 pueden observarse los diferentes cambios en los parámetros hemodinámicos que se detectaron al inicio y al término de la exanguinación. Vemos cómo se elevan de forma importante variables de postcarga, precarga e inotropismo, cambios, que se ven desde cifras de exanguinación aun menores a lo reportado en la literatura mundial (750 mL), por lo que los cambios en la hemodinamia son aun más tempranos. Las cifras en estos cambios son incluso menores de lo reportado y, sobre todo, el monitoreo con el sistema USCOM es efectivo, fácil de realizar y nos da amplia información precisa y eficaz para la toma de decisiones en bienestar de los pacientes.
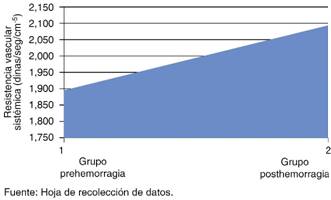
Figura 1: Se observan los cambios en la determinación de las resistencias vasculares por USCOM; vemos un aumento importante de las mismas al realizar el procedimiento de exanguiación en los pacientes en el Banco de Sangre.
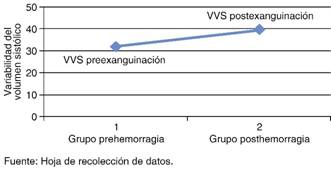
Figura 2: Se observa el cambio en los promedios al determinar la variabilidad de volumen sistólico; vemos un aumento en esta variable.
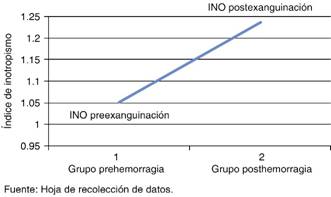
Figura 3: Se muestran los cambios en los promedios del índice de inotropismo antes y después de la hemorragia controlada; vemos como no hay aumento importante del mismo.
Discusión
En este estudio se decidió evaluar las diferentes variables hemodinámicas que determinan el USCOM al realizar una exanguinación, pretendiendo demostrar los diferentes cambios tempranos que puedan observarse con pérdidas hemáticas mínimas (450 mL). En las Tablas antes colocadas pueden verse dichos cambios en los diferentes parámetros hemodinámicos con predominio en la postcarga, los cuales sin duda se detectaron con frecuencia, independientemente de la edad, género o factores indirectos. Además de que proporcionan amplia información de los cambios que pueden darse en la hemodinamia de forma temprana, son de gran ayuda para evaluar a los pacientes, pues nos dan la pauta para mejorar de forma inicial su estado general sin necesidad de dar soporte hasta que se presente el estado de choque.
Conclusiones
Nuestro universo de estudio se compuso de pacientes que fueron aceptados y cumplieron los estándares para donar sangre en el Banco Estatal de Ecatepec. La distribución de género entre los pacientes fue principalmente en hombres.
Las medidas antropométricas de talla y peso en promedio refieren pacientes con complexión media que caen en el grupo de sobrepeso.
Nuestro objetivo principal es evaluar los diferentes cambios en las variables medidas con el monitor ultrasónico USCOM durante una hemorragia controlada (exanguinación de los pacientes en Banco de Sangre), logrando observar cuáles son los cambios que se presentan de forma temprana, considerando las variables para la precarga, postcarga o inotropismo, siendo esto lo más relevante que tomaremos en cuenta para tomar mejores decisiones que repercutan en el pronóstico de los pacientes.
En las terapias intensivas, actualmente ha disminuido el uso del estándar de oro clínico, lo que se explica tanto por su naturaleza invasiva como por el hecho de que no ha demostrado reducir la mortalidad. Por tal motivo, las actuales guías de práctica clínica para monitoreo hemodinámico sólo recomiendan este procedimiento para pacientes en estado de choque refractario y para pacientes con falla cardiaca derecha.
Las técnicas no invasivas de gasto cardiaco han cobrado importancia en los últimos años. En las guías de práctica clínica de monitoreo hemodinámico actuales se menciona a la ecocardiografía como la técnica inicial de elección tanto para la búsqueda del diagnóstico etiológico como para el seguimiento del monitoreo hemodinámico de los pacientes.
Sin duda, el monitor USCOM es una herramienta muy útil, fácil de realizar, no invasiva y con muchas opciones a favor para el monitoreo hemodinámico del paciente crítico, pero aún se necesita tener más evidencia al respecto de esta herramienta; sin embargo, en la bibliografía que utilizamos, los resultados fueron equiparables con el estándar de oro (catéter de flotación), por lo que consideramos que su uso es altamente recomendable.
En los resultados de este estudio puede verse claramente cómo las variables relacionadas con la postcarga (resistencias vasculares sistémicas) se ven aumentadas de forma más importante y más rápida, seguidas de las variables de precarga como la variabilidad de volumen sistólica, considerando que pueden observarse cambios importantes con la pérdida de pequeñas cantidades de sangre, cifras aun menores a las que se describen en la Tabla de hemorragia para estado de choque determinado por los cirujanos, en la que se indican cifras aproximadas de 750 mL, logrando incluso evaluar cambios con pérdidas de sólo 200 mL. Es aún más factible observar cambios tempranos en los pacientes con el monitoreo por USCOM, pues es un método sencillo de utilizar, rápido y que otorga parámetros inmediatos.
Sin lugar a dudas, nuestro estudio adolece, en primer lugar, del hecho de contar con un número pequeño de pacientes y, en segundo, de haber sido realizado por un solo investigador (en estudios de procedimientos dependientes del operador es de utilidad medir la variabilidad interobservador).
Situación por la que esta afirmación no puede generalizarse a todos los pacientes en áreas críticas de todas las partes del mundo; sin embargo, nuestro estudio da pauta para que en el futuro haya una planeación de estudios multicéntricos con mayor número de pacientes que puedan confirmar si la tendencia de estos datos estadísticos persiste y puede ser replicable.











 nueva página del texto (beta)
nueva página del texto (beta)




