Introducción
El paciente en estado crítico se caracteriza por un metabolismo de estrés catabólico en el que presenta una respuesta inflamatoria sistémica asociada a complicaciones de morbilidad infecciosa, disfunción orgánica múltiple y hospitalización prolongada. El metabolismo de estrés es una respuesta generalizada en la cual energía y sustratos son metabolizados para mantener la respuesta inflamatoria, la función inmunitaria y reparar tejidos. Esta movilización de energía y sustratos se genera a expensas de masa corporal magra. Lo anterior resulta en una rápida disminución de la masa corporal magra que excede la asociada a reposo en cama o en simple inanición.1 En el paciente crítico la mayor pérdida muscular (aproximadamente 17%) ocurre típicamente en los primeros 10 días de ingreso a la Unidad de Terapia Intensiva (UTI) y estas pérdidas se incrementan por la severidad de la enfermedad. La pérdida muscular puede ser atenuada o incluso revertida con un adecuado soporte nutricional.2,3
Por otra parte, es importante determinar el riesgo nutricional en todos los pacientes que ingresen a la UTI. Aquellos pacientes con alto riesgo nutricional son los que se beneficiarán de una terapia nutricional temprana y agresiva. El puntaje NUTRIC está diseñado para cuantificar el riesgo de desarrollo de eventos adversos que pueden modificarse con una terapia nutricional agresiva.4,5 Marcadores séricos tradicionales como albúmina, prealbúmina, transferrina y proteína unida a retinol se modifican debido a la respuesta aguda de la enfermedad por incremento de la permeabilidad vascular y alteraciones en la síntesis proteica y por tanto, no representan un estado nutricional del paciente en la UTI. Otros marcadores como calcitonia, proteína C reactiva, IL-1, el factor de necrosis tumoral, IL-6 y citrulina se encuentran bajo investigación para utilizarse como marcadores.3
El balance nitrogenado es un parámetro que se utiliza en forma rutinaria en la UTI para monitorizar el soporte nutricional. La meta ideal es un balance nitrogenado positivo, pero minimizar el déficit de nitrógeno en el enfermo crítico es probablemente más realista cuando se considera el hecho de que la proteólisis del musculoesquelético tal vez exceda la síntesis de proteínas relacionada con el metabolismo de estrés.6
El valor del ultrasonido como herramienta en la valoración nutricional tiene cada vez más aceptación a través de la medición del musculoesquelético a la cabecera del paciente. La medición de la pérdida del grosor muscular se efectúa mediante un transductor lineal con ondas de sonido de alta frecuencia (1-10 MHz).2 Estudios en pacientes críticos apoyan el uso del ultrasonido para valorar la masa corporal magra, además de evaluar los cambios de desgaste muscular secundarios a proteólisis y necrosis muscular evidenciados mediante biopsia de músculo.7,8
En un estudio prospectivo Puthucheary y cols. demuestran mediante medición del grosor del recto femoral con ultrasonido y análisis histopatológico que la pérdida muscular se amplifica dependiendo de la severidad de la enfermedad en la primera semana de ingreso a la UTI. Los pacientes con falla orgánica de más de dos sistemas tenían una pérdida de 16% contra 3% con una sola falla orgánica. Sin embargo, no establece una relación directa con el estado nutricional de los pacientes.9
La técnica con mayor aceptación en los estudios clínicos para determinar la masa corporal magra mediante ultrasonido es medir el grosor del grupo muscular a nivel de la cara anterior del muslo con el paciente en decúbito supino. Existe preocupación por posibles alteraciones en la medición debido a la presencia de edema en tejido celular subcutáneo, pero algunos estudios ya han confirmado que se tiene una buena aproximación de la pérdida muscular al hacer la medición con máxima compresión del trasductor.10,11 Varios estudios revelaron que el empleo del ultrasonido de músculo tiene una buena correlación con la masa corporal magra medida mediante tomografía computarizada (r = 0.77), por absorciometría con rayos X de doble energía (DXA) (r = 80) y resonancia magnética (RM) (r = 0.87).12-14 Esta técnica también ha demostrado una excelente confiabilidad en las mediciones intraobservador (coeficiente de correlación intraclases, ICC = 0.98 y coeficiente de variación, CV = 7%) e interobservador (ICC = 0.94, CV = 13%), incluso con personal sin experiencia previa en ultrasonografía.12,15
Por lo tanto, este estudio se llevó a cabo con el fin de evaluar el porcentaje de desgaste muscular (PDM) del músculo cuádriceps por ultrasonido en modo-B con el objetivo primario de buscar una relación en el cumplimiento de las metas nutricionales y el balance nitrogenado. Por otra parte, como objetivos secundarios evaluar la relación del PDM con el puntaje NUTRIC, horas de ventilación mecánica invasiva (VMI), tiempo de estancia en la Unidad de Terapia Intensiva (UTI) y mortalidad en la UTI.
Material y métodos
Estudio de tipo prospectivo con una intervención diagnóstica de bajo riesgo. Se llevó a cabo en el Hospital Español de México en un periodo comprendido del 1 de abril a 31 de agosto de 2016. Se contó con la aprobación del Comité de Ética en Investigación del hospital. Se reclutaron pacientes consecutivos que cumplieran con los siguientes criterios de inclusión: 1) edad ≥18 años, 2) ambos sexos, 3) pacientes que ingresen a la UTI con tiempo de estancia en terapia esperado mayor de siete días, 4) pacientes en los cuales se inicie terapia de soporte nutricional, ya sea por vía enteral o parenteral. Los criterios de exclusión fueron: 1) moribundos que no se espera que sobrevivan, 2) pacientes con amputación supracondílea en miembros pélvicos, 3) pacientes con una patología que altera el musculoesquelético: miopatías inflamatorias, rabdomiólisis, Miastenia gravis, síndrome compartimental y celulitis en región anterior de muslo.
En los pacientes que cumplieron con los criterios de inclusión se midió el grosor del músculo cuádriceps (GMC) en forma seriada del día uno al día siete. Se recolectaron datos de tipo demográfico, escalas de gravedad como SOFA y SAPS III. Se dio seguimiento nutricional de los primeros siete días de estancia en la UTI, el registro de kilocalorías (kcal), gramos de proteínas y gramos de nitrógeno administrados por día, además de balance nitrogenado al día dos, cuatro y siete con medición del nitrógeno en orina de 24 horas.
Posteriormente se dividieron dos grupos. El grupo 1 incluyó los pacientes que tuvieron desgaste muscular medido en porcentaje y el grupo 2 incluyó pacientes que no tuvieron desgaste muscular.
Descripción de la técnica de medición del GMC por ultrasonografía
Se realizó la medición del GMC mediante ultrasonografía en escala de grises con un transductor lineal con la técnica validada en pacientes críticos y descrita en el estudio de Gruther et al. con un coeficiente de variación de 1.3%.16 Esta medición incluye el músculo vasto interno y recto femoral. Se coloca al paciente en posición supina con las piernas relajadas y en extensión. Con el transductor a 90 grados del muslo y en máxima compresión se realizan dos mediciones a diferente altura del muslo en ambas piernas y luego se calcula la media de las 4 mediciones. La primera lectura se efectúa en el punto medio de una línea trazada de la espina iliaca anterosuperior (EIAS) al borde superior de la rótula. La segunda lectura a nivel de la unión del tercio medio con el tercio inferior de una línea trazada de la EIAS al borde superior de la rótula (Figuras 1 y 2).

Figura 1: Representa la primera lectura del grosor muscular con ultrasonido que se realiza en el punto medio de una línea que va de la EIAS al borde superior de la rótula.
Análisis estadístico
Las medidas de resumen y dispersión en las variables continuas con distribución normal fueron media y desviación estándar (s) y en las de distribución no normal fueron mediana y rango intercuartílico. Para las variables categóricas se muestra el número de pacientes (n) y porcentajes (%). Para comparar las variables cuantitativas se utilizó la prueba t de Student (t) o la prueba U de Mann-Whitney, según el caso. En las variables categóricas se usó la prueba Chi cuadrada (χ2) o el test exacto de Fisher. Aquellas variables que en el análisis univariado obtuvieron un valor de p α ≤ 0.2 se incluyeron en un análisis multivariado de regresión logística. Se determinó que una variable se asociaba de manera independiente cuando se obtenía el valor de p α ≤ 0.05. En los análisis de correlación se utilizó el coeficiente de correlación de Spearman. El análisis estadístico se hizo con el software de IBM SPSS Statistics 22.
Resultados
Se incluyó un total de 20 pacientes con mediada para edad de 75 (intervalo de confianza de 95% [IC 95%] 54.7-81). La mayor parte de la población fueron hombres con 75%. Con un índice de masa corporal (IMC) promedio de 28.2 ± 5 kg/m2. La media del puntaje de SOFA al ingreso fue de 4.9 ± 3.8, puntaje de SAPS III una mediada de 53 (IC 95%, 44-68.25) y mediada de puntaje NUTRIC de 3 (IC 95%, 2-4). El diagnóstico de ingreso más frecuente fue sepsis y choque séptico (30%). El tipo de nutrición inicial más frecuente fue la ruta enteral (65%). En el Cuadro I se describen las características clínicas y demográficas de la muestra.
Cuadro I: Descripción de las características demográficas de la población y análisis univariado de los grupos de estudio. Las variables continuas son representadas en medias y desviación estándar (± DE) y mediana con rango intercuartílico (IC 95%). Para variables categóricas se representan en números y porcentajes (n, %).

En la comparación por grupos, el grupo de pacientes con desgaste muscular representado por el PGM incluyó 11 pacientes y el grupo sin desgaste muscular incluyó 9. Se encontraron diferencias significativas entre los grupos en el día en que se logró la meta de nutrición establecida, en el grupo de pacientes con desgaste muscular fue más tardío en comparación con el grupo de pacientes sin desgaste muscular, 5 (IC 95%, 5-5.50) y 3 (IC 95%, 2.50-5) respectivamente con una p = 0.02.
En el análisis multivariado de regresión se incluyó el puntaje de SOFA, los gramos de proteína promedio administrados por día y el día en el que se lograron las metas de nutrición. Se observó una asociación entre la presencia de desgaste muscular y el día que se llegó a la meta nutricional con una razón de momios (RM) de 10.8 (IC 95%, 0.93-125.68) un valor de p = 0.05 (Cuadro II).
Cuadro II: Análisis multivariado de regresión logística para variables asociadas a desgaste muscular.

RM = Razón de momios.
En el análisis de correlación se utilizó el balance nitrogenado acumulado al día dos y cuatro y el balance global de siete días en relación con el PDM, pero no se detectó una relación lineal (Figuras 3, 4, 5 y 6). Por otra parte, se hizo un análisis de correlación para el puntaje de SOFA y el PDM final que demostró una correlación inversa casi perfecta, en la que conforme aumentaba el puntaje de SOFA disminuía el grosor muscular al día siete en proporción constante.
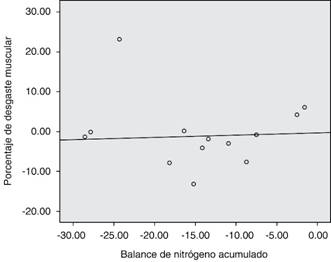
Figura 3: Gráfica de dispersión para correlación entre el balance nitrogenado acumulado al día dos y el porcentaje de desgaste muscular al día dos, con una r2= 0.004. En el análisis de correlación bivariada con una r = 0.33, valor de p 0.15.

Figura 4: Gráfica de dispersión para correlación entre el balance nitrogenado acumulado al día cuatro y el porcentaje de desgaste muscular al día cuatro, con valor de r2= 0.072. En el análisis de correlación bivariada con una r = 0.31, valor de p 0.17.
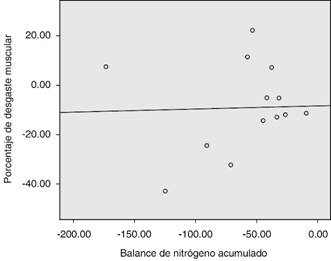
Figura 5: Gráfica de dispersión para correlación entre el balance nitrogenado acumulado al día siete y el porcentaje de desgaste muscular al día siete, valor de r2=0.001. En el análisis de correlación bivariada con una r = 0.07, con una p 0.73.
Discusión y conclusiones
Nuestro estudio reveló una asociación en pacientes con desgaste muscular y el retraso en alcanzar los objetivos nutricionales, lo cual se corroboró mediante el análisis multivariado de regresión en el que se observó una fuerte asociación; sin embargo, el intervalo de confianza es amplio y rebasa la unidad, una razón probable puede ser el tamaño de muestra pequeña. El resto de parámetros iniciales como la cantidad promedio de aporte de kcal por día, gramos de proteína por día y el balance nitrogenado global no tuvieron una significancia estadística que explicara el desgaste muscular en los pacientes de este estudio. Los análisis de correlación con los balances nitrogenados acumulados en diferentes días del seguimiento y el PDM no evidenciaron ninguna relación.
En el puntaje de SOFA no se encontró relación con el desgaste muscular, aunque el análisis univariado lo sugirió, posteriormente en el análisis multivariado no se obtuvo una significancia estadística. En cambio, en el análisis y gráficos de correlación se vio claramente una relación inversa con aumento del puntaje del SOFA y mayor pérdida muscular. Puthucheary y cols.8 ya habían observado una relación, a mayor número de fallas orgánicas aumenta el desgaste muscular, lo que podría explicarse como: cuanto más grave sea la enfermedad se genera un metabolismo catabólico y la proteólisis muscular es excedida.
Una limitante que hay que señalar en este estudio es el tamaño de la muestra que puede restringir las comparaciones. Es necesario un estudio con una muestra más grande que corrobore los hallazgos y busque asociaciones con las variables establecidas en la hipótesis, las cuales se obtuvieron con valores de límites de significancia.
En conclusión, la presente investigación reveló una posible asociación entre la presencia de desgaste muscular en el paciente crítico y el retraso en lograr las metas de nutrición, así como una relación inversa entre el valor de SOFA y el PDM. Lo anterior evidencia la importancia de identificar a los pacientes de alto riesgo de desnutrición, establecer y lograr en los tres primeros días los objetivos de la misma, sobre todo en pacientes con altos puntajes de SOFA, para limitar el desgaste muscular y posiblemente disminuir complicaciones. Asimismo, es esencial utilizar el ultrasonido muscular como herramienta complementaria en el seguimiento nutricional de los pacientes críticos.











 nova página do texto(beta)
nova página do texto(beta)




