Introducción
La hiperglucemia durante la enfermedad crítica es una respuesta evolutiva en gran manera conservada, la cual se cree que incrementa el flujo de glucosa a los órganos vitales (no insulinodependientes).1 Se sabe que el paciente críticamente enfermo suele presentarse a su ingreso con hiperglucemia o desarrollarla durante su estancia en la unidad de terapia intensiva (UTI); es llamada «hiperglucemia por estrés».2 Desde su inicio, el manejo glucémico en el individuo críticamente enfermo ha tenido una constante evolución, que ha ido desde la ausencia absoluta de manejo, discrepancias entre metas estrictas o liberales hasta el reconocimiento de los tres dominios del control glucémico, que son: 1) hipoglucemia, 2) hiperglucemia y 3) variabilidad glucémica.3 Dichos dominios nos ayudan a comprender la razón de las metas de la regulación glucémica, así como una perspectiva para el futuro en dichos protocolos. Cabe mencionar que no son los únicos dominios que pueden tener influencia en el manejo de la glucosa en esta población, y en el futuro la investigación deberá incluir más dominios para el mayor entendimiento de la hiperglucemia por estrés y sus consecuencias en los resultados clínicos.
La presencia de hipoglucemia se ha relacionado a un aumento en la mortalidad. Los estudios que exploran el uso de metas estrictas de glucemia han mostrado un incremento significativo en la incidencia de eventos de hipoglucemia, lo cual de forma indirecta los ha definido como potencialmente peligrosos.3,4 Debido a que las metas más liberales no han mostrado efecto negativo en resultados, pero sí una disminución en los eventos de hipoglucemia, las guías recientes abogan por no iniciar la administración de insulina a valores de glucosa sérica menores de 150 mg/dL, con una meta de control a menos de 180 mg/dL.3
Se ha investigado la relevancia del manejo glucémico previo a la enfermedad crítica, siendo que la hiperglucemia de novo se asocia a mayores riesgos.1 A su vez, es probable que los sujetos con historia de diabetes, algo recientemente llamado «hiperglucemia crónica», ya hayan desarrollado tolerancia a los niveles elevados de glucosa y, por ende, pudieran beneficiarse de metas más altas de glucemia.2 Se ha demostrado que en personas hospitalizadas con diabetes, la presencia de hiperglucemia logra atenuar los resultados en mortalidad, a diferencia de lo que ocurre con aquellos pacientes no diabéticos, que muestran mayor mortalidad asociada a hiperglucemia.3 El estado premórbido, en lo referente a la presencia de diabetes o no y más allá el control glucémico crónico previo, puede generar una respuesta diferente en relación con la disglucemia en el individuo críticamente enfermo. Se han mostrado diferencias en la mortalidad de los sujetos que presentan hiperglucemia dependiendo del estado premórbido: las personas no diabéticas se ven afectadas por mayor glucemia y variabilidad que aquellas diabéticas.3 Se ha generado controversia, pues en recientes estudios en pacientes críticos, una mayor hemoglobina glucosilada (HbA1c) se encuentra inversamente asociada con mortalidad, lo que sugiere a la hiperglucemia crónica como un factor protector en contra de la hiperglucemia aguda.1 Para sujetos con diabetes, el manejo glucémico previo a la admisión podría modular el impacto de la glucemia durante la enfermedad crítica. Las personas con hemoglobina glucosilada mayor muestran peores resultados a cifras de glucosa menores.4
A su vez, una variabilidad glucémica elevada ha sido asociada a mortalidad en diferentes estudios.4 La variabilidad glucémica puede ser un reflejo de disglucemia inducida por enfermedad severa, control glucémico inadecuado o ambas, lo que resulta en amplias fluctuaciones de la glucosa sérica.4 Modelos experimentales sugieren que las fluctuaciones en los niveles de glucosa sanguínea pueden incrementar el riesgo de estrés oxidativo inducido por hiperglucemia.5 Baithwaite define «variabilidad glucémica» como la propensión de un solo paciente a desarrollar excursiones repetidas de glucosa sanguínea sobre un periodo relativamente corto que excede la amplitud esperada en la fisiología normal.6 Permanece sin responder la interrogante sobre la mejoría en los resultados clínicos con una reducción de la variabilidad glucémica.2 No existe un estándar de oro para la medición de la variabilidad glucémica; diferentes estudios utilizan diferentes métricas, las cuales pueden ser complicadas de usar a pie de cama o en la práctica clínica, mostrando una asociación con mortalidad en individuos críticamente enfermos.3
Se propone que los protocolos de manejo glucémico tomen en cuenta las diferentes características del sujeto y tengan como meta reducir la incidencia de hipoglucemia y la variabilidad glucémica.2
Se ha recomendado en la publicación de protocolos de regulación glucémica incluir al menos una métrica de tendencia central, una de hipoglucemia y una de variabilidad glucémica.2
Es probable que una nueva era de control glucémico personalizado esté más cerca de lo que pensamos.4
No existe definición consensuada de variabilidad glucémica, tampoco de la métrica a utilizar en su medición.5
Material y métodos
En el presente trabajo proponemos una nueva forma de calcular la variabilidad glucémica tomando en cuenta el manejo en la glucosa previo mediante determinación de HbA1, considerando el componente premórbido (crónico), así como su relación con resultados clínicos como mortalidad o estancia hospitalaria. También se exploran las dos variables restantes según las recomendaciones para publicar artículos de control glucémico: hipoglucemia y medida de tendencia central. También se explora una métrica de variabilidad glucémica conocida, que toma en cuenta los valores de glucemia durante la estancia en la UTI (componente agudo).
Se trata de un estudio observacional prospectivo en el cual se incluyeron personas adultas (≥ 18 años de edad) ingresadas a la unidad de terapia intensiva en el periodo comprendido de marzo de 2014 a marzo de 2015, con una estancia ≥ 48 horas. Se excluyeron todos los reingresos, menores de edad (< 18 años), embarazadas, pacientes en cuidados paliativos, individuos que fallecieron o se dieron de alta antes de las 48 horas de estancia cumplidas y aquellos sujetos con cuidados paliativos u orden de no reanimación. Al ingreso de cada paciente se obtuvieron las variables demográficas: edad, sexo, peso, talla e índice de masa corporal. Se capturó el lugar de procedencia en dos categorías: urgencias o piso de hospitalización. Se obtuvo el Charlson Comorbidity Index (CCI) y las escalas Acute Physiology and Chronic Health Evaluation II (APACHE II) y Sequential Organ Failure Assessment (SOFA).
Al ingreso de todo paciente, como parte del paquete de rutina de análisis bioquímico, se hicieron determinaciones de hemoglobina glucosilada. Se siguieron todos los individuos hasta el momento del alta o defunción; se capturó dicho resultado y los días de estancia en la UTI, hospitalización y totales.
Los valores de glucosa capilar se registraron como máximo hasta el día siete del estudio.
El médico intensivista y el personal de enfermería a cargo de los sujetos se encontraban ciegos a este protocolo. Por ello, el equipo siguió el protocolo de control glucémico por tomas capilares (uso de «fingerstick») establecido en esta UTI.
Como medidas de tendencia central se usaron medias y medianas de glucosa dependiendo del tipo de distribución de los datos.
Como medida de tendencia central se obtuvo la media de glucemia por día mediante las mediciones de glucosa capilar.
Como medida de hipoglucemia se capturó el total de personas con al menos una glucosa en sangre ≤ 60 mg/dL.
Para el cálculo de una medida de variabilidad glucémica a partir de los valores de HbA1c, se obtuvo la glucemia promedio (GP), como lo describen Nathan y sus colaboradores, con la siguiente fórmula:7
1)GP = 28.7*HbA1c-46.7
Ésta muestra el promedio de glucemia en los previos tres meses predicho acorde a los niveles de HbA1c.
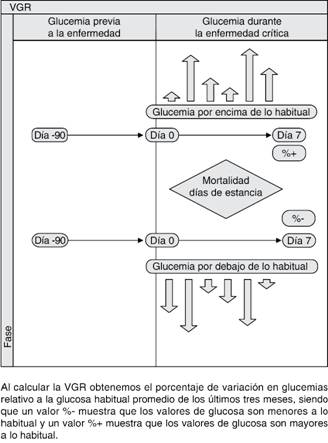
El promedio de las tomas de glucosa capilar por día fue obtenido y, posteriormente, se calculó lo que el equipo determinó como «variación glucémica relativa» (VGR), la cual pretende determinar el porcentaje de variación en la glucemia durante la enfermedad aguda en relación con la glucosa promedio de los tres meses previos, con la siguiente fórmula:
2) VGR(%)=((GP-GCP)/GP*100) x - 1
VG = Variación glucémica en porcentaje respecto a la glucosa promedio.
GP = Glucosa promedio derivada de la HbA1c.
GCP = Glucosa capilar promedio.
Se interpreta como se muestra en la Figura 1.
Otra medida de variabilidad calculada fue el coeficiente de variación por día y en total durante toda la estancia de cada paciente.
La población se dividió acorde a la media de HbA1c de esta misma, resultando en dos grupos: 1) HbA1c < 7% y 2) HbA1c ≥ 7%, así como en grupos en relación con la mortalidad.
Para el análisis estadístico se realizó la prueba de Kolmorogov-Smirnov para determinar la distribución de las variables continuas (normal o no normal); se presentan las variables con distribución normal mediante media y desviación estándar; de lo contrario (distribución no normal), como mediana y percentiles 25 y 75. Para la comparación de variables cuantitativas entre grupos se utilizaron las pruebas t de Student para muestras independientes o U de Mann Whitney; para la comparación de variables cualitativas se utilizó la prueba de χ2 o prueba exacta de Fisher.
Se consideró significativa toda p < 0.05.
Resultados
Las variables demográficas se muestran en el Cuadro I. No se encontró ninguna diferencia entre las variables demográficas. Las escalas de SOFA y APACHE II en ambos grupos no mostraron diferencia significativa. El CCI fue mayor en el grupo ≥ 7% y la estancia hospitalaria resultó significativamente mayor en este mismo grupo.
Cuadro I: Variables demográficas.
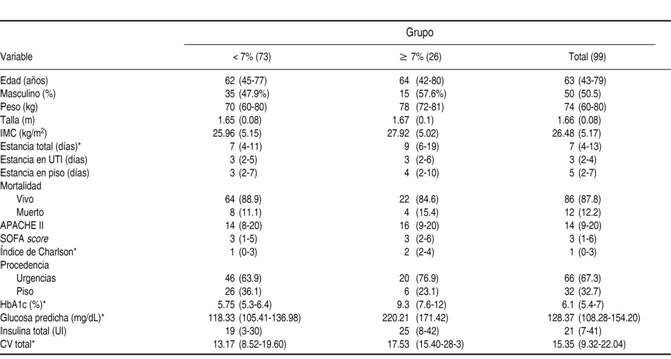
IMC = Índice de masa corporal, APACHE II = Acute Physiology and Chronic Health Evaluation, SOFA = Sequential Organ Failure Assessment,
HbA1c = Hemoglobina glucosilada, CV: Coeficiente de variación *= p < 0.05.
En cuanto a la mortalidad, no se encontró asociación entre los valores de HbA1c, glucosa promedio, insulina utilizada y VGR.
La cantidad de unidades de insulina no resultó diferente entre ambos grupos. Cabe mencionar que 25% de los individuos con HbA1c < 7% usaron insulina, lo mismo que 90% en el grupo ≥ 7% (p < 0.05). El porcentaje de sujetos con al menos un evento de hipoglucemia ≤ 60 mg/dL fue de 8.3 y 7.7% en los grupos < 7% y ≥ 7%, respectivamente, sin alcanzar diferencia significativa.
Como se muestra en la Figura 2, las metas de glucemia capilar se pudieron mantener la mayoría del tiempo en ambos grupos (< 180 mg/dL), siendo que los valores de glucemia capilar promedio fueron significativamente diferentes (p < 0.05) entre ambos grupos durante los siete días. Es decir, el grupo ≥ 7% mantuvo glucemias más altas en comparación con el grupo < 7%.
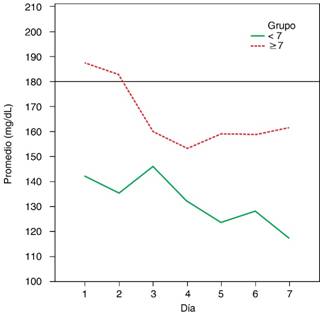
Figura 2: Cifras de glucosa capilar promedio por día. Las líneas horizontales delimitan un valor de glucosa capilar de 180 mg/dL. Las diferencias entre medianas se mantuvieron diferentes a una significancia estadística de p < 0.05 en todo momento.
La Figura 3 muestra la VGR de ambos grupos. Dichas cifras se mantuvieron significativamente diferentes durante los siete días, siendo que el grupo > 7% mostró valores de VGR positivos en todo momento; es decir, cifras menores de glucemia en comparación con los últimos tres meses. Por el contrario, el grupo < 7% mantuvo cifras de VGR positivas, lo que se tradujo como valores de glucemia mayores a los habituales durante los tres meses previos. El grupo ≥ 7% conservó dichas cifras negativas durante el periodo de estudio, mientras el grupo < 7% tendió a normalizarse a una VGR de 0%; es decir, valores de glucosa habituales.
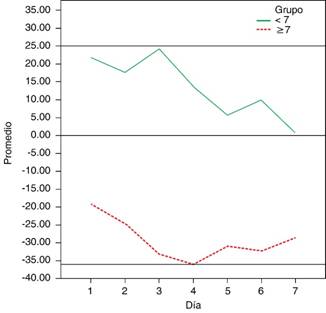
Figura 3: Variabilidad glucémica relativa. Las líneas horizontales delimitan los rangos de variación glucémica relativa en los puntos 25%, -36% y 0%. Las diferencias entre medianas se mantuvieron diferentes a una significancia estadística de p < 0.05 en todo momento.
En relación con el CV, sólo en el grupo < 7% se encontró diferencia significativa (p < 0.05), ya que el subgrupo de personas vivas mostró cifras menores 12.49 (8.2-8.75) en relación con los pacientes que fallecieron 27.49 (11.02-37.07).
Discusión
En el presente estudio se exploraron dos medidas de variabilidad glucémica en individuos críticamente enfermos. Aquella que toma en cuenta el control glucémico previo a la enfermedad crítica mostró una relación con la estancia hospitalaria; debido al diseño del protocolo, no fue posible saber las causas de la estancia más prolongada (pudiendo ser por complicaciones infecciosas o no infecciosas). De manera retrospectiva, se ha mostrado una asociación entre variabilidad glucémica (mediante métricas populares) e infecciones sólo en sujetos diabéticos; al mismo tiempo, las personas con requerimientos de infusión de insulina tendieron a mantenerse más tiempo en la UTI.8 Nuestra población de pacientes con HbA1c 90% requirió uso de insulina, en comparación con 25% del grupo contrario.
A su vez, la fórmula que toma en cuenta las cifras durante la etapa aguda mostró su asociación con mortalidad, pero únicamente en aquellos individuos con un manejo adecuado de la glucosa previo al ingreso (por HbA1c). Los demás componentes, tales como las medias de glucosa capilar y eventos de hipoglucemia, no mostraron diferencias o relaciones.
Se ha demostrado que una variabilidad glucémica definida como un CV > 20% se encuentra asociada a mortalidad con sujetos sin diabetes, pero cifras estrictas (80-110 mg/dL) de glucemia en personas con diabetes también son vinculadas a mayor mortalidad, en contraste con aquellos pacientes no diabéticos con las mismas metas o diabéticos con metas de 140-180 mg/dL.9 Esto concuerda con nuestro trabajo, ya que en los individuos con HbA1 < 7% (buen control glucémico previo), el CV de aquellos fallecidos fue de 27 y el mantener metas < 180 mg/dL, aunque no aumentó la mortalidad, mostró un efecto negativo en la estancia hospitalaria de los sujetos con HbA1c ≥ 7%. La VGR sostenidamente baja durante los primeros siete días mostró una complicación de magnitud crónica traducida en estancias prolongadas, mientras las excursiones «abruptas» en un periodo corto de tiempo mostraron su relevancia en resultados a corto plazo; es decir, mortalidad hospitalaria.
Se observó que aquellas personas con cifras de glucosa elevadas de manera crónica antes de la admisión podrían ser afectadas por un manejo de glucosa relativamente estricto, con cifras menores a las que están habituadas. Por el contrario aquellas con buen control se pueden ver afectadas por mantener fluctuaciones de mayor magnitud en la glucemia.
Este estudio reitera el hecho y la creciente evidencia que ha surgido sobre el manejo de la glucemia en el paciente crítico. Los nuevos protocolos deberán considerar de manera sistemática el estado premórbido del individuo y mantener un seguimiento durante la enfermedad aguda que evite excursiones de glucosa elevada (en ambos sentidos), previniendo los efectos deletéreos de la hipoglucemia y cambios abruptos causados por el manejo intensivo de dicha población, promoviendo que «una talla no se ajusta a todos». El uso de la HbA1c muestra un gran campo de investigación que podría ayudar a desarrollar protocolos de control glucémico individualizados.











 nueva página del texto (beta)
nueva página del texto (beta)