Introducción
Dentro del abordaje de los trastornos ácido-base, el método propuesto por Stewart en 1978 hace énfasis en la diferencia de iones fuertes y la concentración de ácidos débiles disociados para los trastornos metabólicos.1,2 El fundamento del abordaje de Stewart es el concepto de variables independientes y dependientes en la homeostasis ácido-base.3,4 Las variables independientes son aquellas que se alteran fuera del sistema sin afectar al resto, mientras que las variables dependientes son aquellas cuyos valores representan la reacción del sistema a un valor externo impuesto. Con base en lo anterior, la concentración de hidrogeniones y bicarbonato es dependiente de tres variables independientes: la diferencia de iones fuertes (SID), la presión parcial de dióxido de carbono (PCO2) y la concentración de ácidos totales débiles en una solución (ATOT). La diferencia de iones fuertes (SID) puede ser calculada como la diferencia entre los cationes totalmente disociados y los aniones totalmente disociados -principalmente albúmina, fosfato y, en la sangre total, hemoglobina-. La DIF puede ser calculada por la diferencia entre iones fuertes medidos; también es conocido como DIF «aparente» (SIDa); asimismo, puede ser calculado por la adición de bicarbonato y otros buffers, o DIF «efectivo» (SIDe). Ante la aparición de un anión anormal «no medido», aparecerá una brecha entre la diferencia de iones fuertes aparente y la efectiva; a esto se le denomina la «brecha de iones fuertes» (SIG). El valor normal de la brecha de iones fuertes, por lo tanto, debe ser cercana a 0 mEq/L y hasta cierto punto se considera análoga a la diferencia de brecha aniónica tradicional (ΔAG). De esta manera, se describen dos tipos de acidosis metabólica por el método de Stewart: una acidosis con SIDa bajo y brecha de iones fuertes alta, similar a una acidosis metabólica con brecha aniónica alta, y una acidosis con SIDa bajo y brecha de iones fuertes normal, similar a una acidosis metabólica con brecha aniónica normal.5 El método de Stewart para abordaje de desórdenes ácido-base aún no tiene un papel bien definido en el manejo de los pacientes críticamente enfermos.6 Utilizar este método para diagnóstico de desórdenes complejos del equilibrio ácido-base es comparable con el método tradicional, especialmente si se añade la influencia de la albúmina al cálculo de la brecha aniónica tradicional (brecha aniónica corregida o AGC).6-12 Por otro lado, la brecha de iones fuertes representa aniones fuertes no medibles, los cuales se acumulan en sepsis, lesión renal y falla orgánica múltiple, y su origen bioquímico no ha sido estudiado por completo. Su acumulación probablemente sea por aumento en la glicólisis, catabolismo proteico, disfunción mitocondrial y disminución en su depuración. Algunos candidatos potenciales incluyen los sulfatos, uratos, hidroxibutirato, succinato, piroglutamato, D-lactato e intermediarios del ciclo de Krebs, pero también componentes de medicamentos, nutrientes o coloides sintéticos.13,14 Además, se ha demostrado que la brecha de iones fuertes guarda una relación estrecha con marcadores de inflamación y mortalidad en algunas poblaciones de individuos críticamente enfermos.15,16 De esta manera, existe evidencia clínica contradictoria que apunta a que hay una relación entre la brecha de iones fuertes por el abordaje de Stewart y la mortalidad en ciertas poblaciones de pacientes críticos.17-30 Sin embargo, esta se ha medido sólo en un momento específico en el tiempo y no se han estudiado sus cambios a través del curso de la enfermedad o su comportamiento ante la reanimación hídrica.31 Por lo tanto, un marcador aún no explorado es la cinética de la brecha de iones fuertes en personas críticamente enfermas, análoga a la cinética de «depuración» del lactato, donde las mediciones seriadas de lactato son un predictor independiente de mortalidad ya establecido.32,33 El objetivo del estudio fue evaluar la cinética de la brecha de iones fuertes en relación con el resto de los parámetros clásicos del equilibrio ácido-base como predictora de mortalidad en sujetos con choque séptico.
Material y métodos
Se trata de un estudio retrospectivo observacional. Los exámenes diagnósticos utilizados en el protocolo forman parte del cuidado rutinario de los pacientes críticos, como lo marca la literatura actual, por lo que en este proyecto de investigación no se consideró el uso de un consentimiento informado. El trabajo se realizó en una unidad de cuidados intensivos adultos de 14 camas en un hospital privado de la ciudad de Monterrey, en Nuevo León. Al tratarse de una unidad abierta, los individuos representan una población heterogénea, incluyendo pacientes quirúrgicos y médicos. Desde su ingreso a la unidad de cuidados intensivos, las personas son manejadas bajo la discreción de un médico tratante externo especialista en medicina crítica, quien dicta el abordaje del sujeto.
La muestra del estudio fue por conveniencia y se incluyeron todos los pacientes admitidos a la terapia intensiva con diagnóstico de ingreso de choque séptico, de acuerdo a las guías.34 Se incluyeron individuos mayores de 18 años hospitalizados en la unidad de cuidados intensivos entre el primero de junio de 2014 y el 30 de junio de 2016, con una estancia mayor a 48 horas en la unidad, independientemente de las comorbilidades o pronóstico de la enfermedad de base. Se excluyeron personas que no contaran con la información completa en el expediente clínico, que no cursaran con una estancia de al menos 48 horas en la unidad, que contaran con un SOFA menor de un punto y un APACHE II menor de 8 puntos, así como mujeres embarazadas. Se registraron la variables demográficas de edad, género, comorbilidades, foco infeccioso, y los puntajes de SOFA y APACHE II, tiempo de estancia en la unidad de cuidados intensivos y mortalidad a 30 días o al egreso hospitalario. Se registraron los parámetros obtenidos de gasometrías sin hacer distinción entre muestras arteriales o venosas de pH, presión parcial de CO2 (PCO2), bicarbonato (HCO3), exceso de base (EB) y lactato al ingreso, a las 24 horas y a las 48 horas. Se extrajeron también las variables de la química sanguínea de sodio sérico (Na+), potasio sérico (K+), cloro sérico (Cl-), magnesio total (Mg++), calcio total (Ca++), fósforo (PO4 -), albúmina y creatinina al ingreso, a las 24 horas y a las 48 horas. De ser necesario, las unidades se convertían al Sistema Internacional de Unidades (unidades métricas). A partir de estos datos, se calcularon los parámetros de brecha aniónica tradicional (AG), brecha aniónica corregida para albúmina (AGC), diferencia de brecha aniónica (ΔAG), diferencia de iones fuertes aparente (SIDa), diferencia de iones fuertes efectiva (SIDe) y brecha de iones fuertes (SIG) de acuerdo a las fórmulas ya descritas en la literatura, a saber:1-5
AG = Na+ - (Cl- + HCO3 -)
AGC = AG + ([albúmina] × 2.5)
DAG = Brecha aniónica calculada - brecha aniónica esperada
SIDa = ([Na+] + [K+] + [Ca++] + [Mg++]) - ([Cl-] + [lactato])
SIDe = (1,000 × 2.46 × 10-11 × PCO2/10-pH) + [albúmina] × (0.123 × pH-0.631) + [fosfato] × (0.309 × pH-0.469)
SIG = DIFa-DIFe
A partir de estos parámetros, se evaluó la cinética de eliminación dentro de las 24 y 48 horas del lactato, AG, AGC, y SIG, que se expresa como porcentaje a partir de la fórmula:31
(7) Concentración inicial-concentración final/concentración final × 100
Dichos parámetros también se convirtieron en una variable nominal como una cinética mayor o menor de 70% a las 24 horas.31,33
De igual manera, se registró el tipo y cantidad de soluciones de reanimación utilizadas durante las primeras 12, 24 y 48 horas, el balance durante las primeras 12, 24 y 48 horas, así como sus totales acumulados. Se registró la administración de albúmina exógena, la administración de diuréticos, el uso de terapias de reemplazo renal en cualquiera de sus modalidades y el empleo de bicarbonato de sodio durante este tiempo.
Las variables de estudio se registraron y analizaron utilizando el software estadístico JMP® en su versión 12.1.0. Se analizó la distribución de cuentas y porcentajes para variables cualitativas, así como medias y desviaciones estándar para variables continuas. Para las diferencias en variables nominales, se utilizó χ2, mientras que para comparar variables numéricas, se empleó prueba de Mann-Whitney o Fisher, según aplicara, así como t de Student para las variables continuas. Se realizó un ajuste de bondad de modelo por regresión logística de las variables continuas en relación con la mortalidad utilizando el método de Hosmer-Lemeshow. A partir de esto, se evaluó la habilidad pronóstica de las variables continuas como área bajo la curva (AUC) de la curva característica operativa del receptor (ROC). También se realizó un análisis multivariante para evaluar posibles interacciones entre las diferentes variables. Para los objetivos de este estudio, se consideró una p de dos colas ≤ 0.05 como estadísticamente significativa.
Resultados
Se encontraron 99 pacientes con el diagnóstico de choque séptico que ingresaron a terapia intensiva en el periodo del estudio. Se excluyeron ocho individuos por no contar con un expediente clínico completo, lo que dio un total de 91 sujetos analizados. La edad promedio fue de 64.82 (± 18.49) años; 49 (54%) personas eran de género masculino y 42 (46%), de género femenino. El foco infeccioso más común fue abdominal, representando 35% de los casos, seguido del foco genitourinario, con 24%, y el pulmonar, con 20% del total. Las comorbilidades más comunes fueron la hipertensión arterial sistémica, que se presentó en 30 pacientes, la diabetes, en 26 individuos, la insuficiencia renal crónica, en 18 sujetos, y la enfermedad cerebrovascular, en 14 personas. Cabe mencionar que 15 pacientes se encontraron sin patologías previas. El SOFA promedio fue de 8 (± 3.5) y el APACHE II promedio fue de 19 (± 7.4). El tiempo promedio de estancia en la unidad de cuidados intensivos fue de 8.6 (± 6.7) días. De los 91 individuos analizados, 26 fallecieron dentro de la estancia hospitalaria o en los siguientes 30 días, para una mortalidad de 28.5% (Cuadro I).
Las variables asociadas a la mortalidad fueron el APACHE II, el sodio sérico a las 24 horas, el cloro sérico a las 24 horas, los niveles de creatinina a las 48 horas, los niveles de lactato a las 48 horas, la brecha aniónica tradicional a las 48 horas, la brecha aniónica corregida a las 48 horas, la diferencia de brecha aniónica a las 48 horas, la brecha de iones fuertes a las 48 horas, el balance acumulado, los días de estancia en la UCIA, el uso de diuréticos y un SOFA cardiovascular de 4 a las 48 horas (Cuadro II).
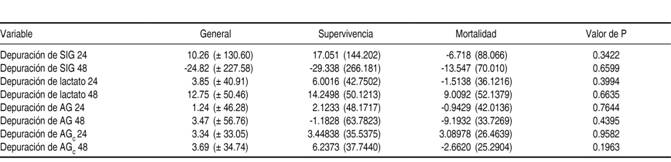
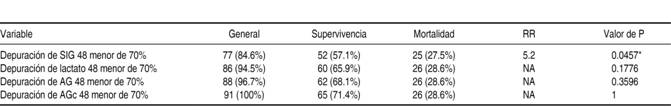
El pH, el exceso de base, el bicarbonato, la diferencia de iones fuertes aparente y la efectiva, así como el porcentaje de depuración tanto a las 24 como a las 48 horas de lactato, brecha de iones fuertes y brecha aniónica no se asociaron a mortalidad (Cuadro III). Una depuración menor de 70% a las 48 horas de brecha de iones fuertes se asoció a mortalidad con un riesgo relativo de 5.2 (p = 0.0457), lo cual no se observó con el resto de los cálculos de cinética de lactato, brecha aniónica, brecha aniónica corregida a las 24 o 48 horas, ni para la depuración de brecha de iones fuertes a las 24 horas (Cuadro IV). Cabe mencionar que la brecha de iones fuertes presentó un descenso del ingreso a las 48 horas de 7.51 a 6.39 (p = 0.0441) en la población en general; en las personas que fallecieron no se observó esta diferencia (8.65 versus 7.73; p = 0.1329), pero sí en aquellas que sobrevivieron (7.05 versus 5.85; p = 0.0456).
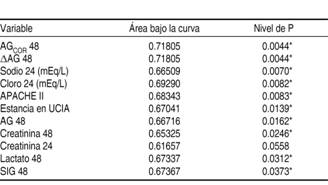
La mejor área bajo la curva característica operativa del receptor para predecir mortalidad por bondad de ajuste de modelo fue la de la brecha aniónica corregida a las 48 horas, con un área bajo la curva de 0.71805, seguida de la diferencia de brecha aniónica a las 48 horas, con un área bajo la curva de 0.71805, y el sodio sérico a las 24 horas, con un área bajo la curva de 0.66509 (Cuadro V y Figura 1).
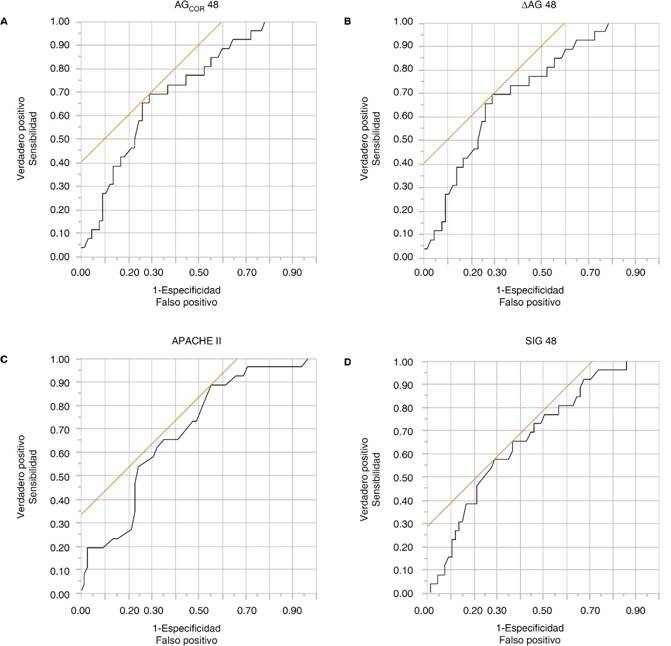
Figura 1: A. Área bajo la curva AGCOR 48, B. Área bajo la curva ΔAG 48, C. Área bajo la curva APACHE II y D. Área bajo la curva SIG 48.
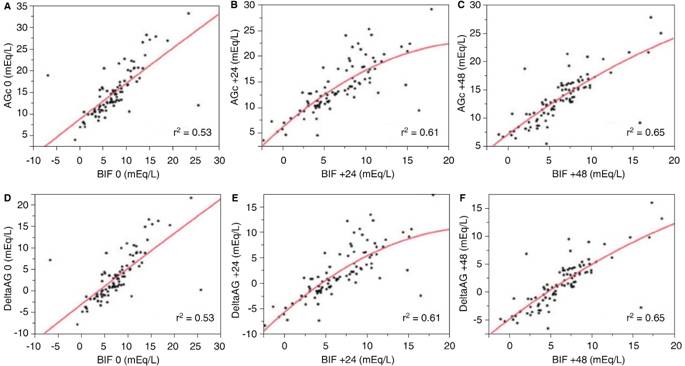
Asimismo, cabe mencionar que se encontró una relación entre los valores de diferencia de iones fuertes aparente a las 48 horas con el tipo de solución de 34.7 mEq/L con solución salina, versus 38.1 mEq/L con solución Hartmann (p = 0.0234), sin afectar los valores de sodio y cloro séricos. También se encontró una relación entre los niveles de brecha aniónica corregida a albúmina con la brecha de iones fuertes y de la diferencia de brecha aniónica con la brecha de iones fuertes tanto al ingreso como a las 24 y 48 horas (Figura 2).
Discusión y conclusiones
La utilidad clínica del método de Stewart para equilibrio ácido-base ha sido investigada en dos escenarios clínicos, ya sea para el abordaje diagnóstico de desórdenes ácido-base o como marcador pronóstico en el estado de choque,6 el cual fue el enfoque del presente trabajo. El estudio de la brecha de iones fuertes como marcador de mortalidad en pacientes críticos resulta interesante debido a dos procesos concomitantes: por una parte, funciona como marcador de daño celular, y por otra, como marcador de la respuesta inflamatoria. La brecha de iones fuertes representa aniones fuertes no medibles, los cuales se acumulan en sepsis, lesión renal y falla orgánica múltiple. Su origen bioquímico no ha sido estudiado por completo, pero su acumulación probablemente sea por aumento en la glicólisis, catabolismo proteico, disfunción mitocondrial y disminución en su depuración, y represente un marcador sustituto del daño celular que ocurre en los estados de choque.13,14 Algunos candidatos potenciales incluyen los sulfatos, uratos, hidroxibutirato, succinato, piroglutamato, D-lactato e intermediarios del ciclo de Krebs.
En 2004, Kaplan y Kellum17 demostraron en 282 pacientes de trauma con lesión vascular que la brecha de iones fuertes al ingreso a la unidad de urgencias era superior al resto de los parámetros de equilibrio ácido-base para predecir mortalidad a 28 días. El área bajo la curva ROC era de 0.911 para la brecha de iones fuertes, comparada con un área de 0.905 para el puntaje de severidad de la lesión clásico. Posteriormente, estos mismos investigadores analizaron una población no seleccionada de trauma y nuevamente demostraron que la brecha de iones fuertes al ingreso predecía fuertemente la mortalidad, incluso con un mejor desempeño que el lactato.18 Más tarde, Funk y colaboradores19 evaluaron los parámetros ácido-base al ingreso y las 12 horas en individuos que tuvieron retorno de la circulación espontánea tras un paro cardiorrespiratorio; ellos no sólo encontraron una relación positiva entre la brecha de iones fuertes y la mortalidad, sino también una relación con los desenlaces neurológicos a seis meses. En sujetos con hepatitis hipóxica,20 una brecha de iones fuertes elevada se asoció con mortalidad, mientras que en personas con falla renal aguda, la mortalidad se vinculó a una menor brecha de iones fuertes.21 En la población pediátrica, la brecha de iones fuertes también ha sido ligada a los desenlaces de los individuos. Se ha encontrado una relación entre ésta y la mortalidad en pacientes pediátricos críticamente enfermos no seleccionados,22 durante el postquirúrgico de cirugía cardiaca,23,24 y en aquellos con quemaduras extensas.25
No toda la evidencia clínica indica que la brecha de iones fuertes funciona como un marcador de mortalidad en sujetos críticos. Rocktaeschel y colaboradores,26 en una cohorte de 300 pacientes críticos no seleccionados, no demostraron habilidad de los parámetros ácido-base clásicos o por método de Stewart obtenidos al ingreso de predecir mortalidad. Martin,27 contrario a la evidencia de Kaplan y Kellum, no probó una habilidad pronóstica de la brecha de iones fuertes para mortalidad en enfermos de trauma, encontrando un área bajo la curva ROC de 0.54. Finalmente, el estudio más grande realizado a la fecha, con 6,878 pacientes críticos,28 tampoco encontró habilidad de la brecha de iones fuertes para diferenciar entre sobrevivientes y no sobrevivientes. La brecha de iones fuertes al ingreso de la UCIA demostró un área bajo la curva ROC de 0.631, comparada con 0.701 para las concentraciones de lactato, aunque al agregar dicho parámetro, sí mejoraba la habilidad pronóstica de otras herramientas de predicción como el MPM III. Estos resultados contradictorios podrían ser explicados por variaciones en los métodos de medición, incluyendo el tipo de equipo,29 las fórmulas utilizadas y la dependencia en el número extenso de variables que se requieren para los cálculos.6,29 También es posible que la disponibilidad creciente de las mediciones de lactato en escenarios clínicos y su inclusión dentro de la fórmula de la brecha de iones fuertes haya eliminado la necesidad de medir parámetros indirectos como la brecha de iones fuertes o la brecha aniónica clásica para su detección.6,30
En los estudios previamente mencionados, los parámetros del método de Stewart han sido medidos en un solo punto del tiempo, por lo general, al ingreso al departamento de urgencias o a terapia intensiva, sin consideración para los cambios potenciales que pueden ocurrir a través del tiempo. Sólo Noritomi ha seguido los cambios de la brecha de aniones fuertes a lo largo de varios días.31 En 60 individuos con choque séptico, demostró que los sobrevivientes presentaron una disminución en la brecha de iones fuertes a los cinco días, en contraste con aquellos sujetos que no sobrevivieron, aunque de una manera no estadísticamente significativa. El objetivo del estudio fue evaluar dichos cambios a través del tiempo como un análogo a la cinética del lactato, la cual ha demostrado su relación con mortalidad a lo largo de varias investigaciones y situaciones clínicas variadas.31
En este respecto, demostramos que la brecha de iones fuertes disminuyó a través del tiempo dentro de las primeras 48 horas tras el ingreso en la UCIA en mayor medida en las personas que sobrevivieron; sin embargo, en nuestro trabajo esto no fue mejor predictor de mortalidad que las variables clásicas del equilibrio ácido-base.











 nueva página del texto (beta)
nueva página del texto (beta)