Introducción
El Laringoespasmo (LEP) se define como el cierre sostenido de las cuerdas vocales. Se trata de un reflejo protector primitivo de la vía aérea (VA) que ocurre para salvaguardar la integridad de la VA, es decir, la VA se protege contra la aspiración pulmonar 1. El LEP también se define como, una respuesta exagerada de un reflejo de cierre o espasmo muscular glótico. Esencialmente es un reflejo protector que actúa para prevenir la entrada de algún material extraño al árbol traqueobronquial. La presencia de este reflejo puede resultar en un impedimento para respirar. En algunas situaciones el espasmo muscular se mantiene mientras el estímulo que lo causal persista, sin embargo una característica del LEP es que el cierre de la VA se mantiene, aún después de desaparecer el estímulo causal inicial. En cualquiera de las situaciones mencionadas anteriormente, nos enfrentamos a una pérdida parcial o total de la VA de causas múltiples.
El LEP puede resultar en una complicación severa para la vida, y es una causa importante de paro cardiaco en el paciente pediátrico, que incluye hipoxia severa (61%), bradicardia (6%), edema pulmonar obstructivo (4%), paro cardiaco (0.5), aspiración pulmonar (3%), arritmias y muerte. El 40% de las obstrucciones de la VA son secundarias a LEP. Es de suma importancia recordar que el 43% de las complicaciones por anestesia son de origen respiratorio 2.
El LEP es visto principalmente en el niño, la causa más frecuente de (LEP) es la manipulación de la VA superior, aunque sus casusas son multifactoriales. Su incidencia varía dependiendo del autor citado, Olsson and Hallen mencionan una incidencia del 1% en adultos y niños. La incidencia se duplica en niños lactantes y escolares y se triplica en menores de tres meses de edad. En niños con reactividad de la vía aérea o niños con asma, su incidencia aumenta hasta 10%, y se puede incrementar hasta 25% en pacientes que reciben cirugía de adenoamigdalectomía 3. La incidencia es la más alta en el niño entre uno y tres meses de edad. En los primeros nueve años de edad la incidencia de LEP es de 1.74%. Para los niños escolares es de 2.8%. De la misma forma hay una mayor incidencia de eventos adversos respiratorios en el niño obeso asmático, no así niños obesos sin asma 4.
Mecanismo de producción del LEP
En el LEP pueden estar involucrados, músculos laríngeos, cuerdas vocales verdaderas y falsas. La mayoría de los reflejos laríngeos son producidos por la estimulación de las fibras aferentes contenidas en la rama interna del nervio laríngeo superior. Estos reflejos controlan la contracción de los músculos laríngeos los cuales protegen la VA durante la deglución 5.
Fisiopatología
Las causas del LEP son múltiples, la presencia de estímulos locales, mecánicos, químicos o térmicos, que ascienden por el laríngeo superior vía fibras sensoriales del nervio del vago. Es decir que la sensibilidad de la región supraglótica está dada por el nervio laríngeo superior. Mientras que la inervación sensitiva por debajo de las cuerdas vocales, esta inervada por el nervio laríngeo inferior o recurrente. Existe una cantidad importante de receptores tanto en las cuerdas vocales como en la glotis y estructuras adyacentes. Pero la mayor densidad de receptores se encuentra en la entrada de la laringe, principalmente en la cara laríngea de la epiglotis.
La respuesta motora se da principalmente por la presencia de tres músculos laríngeos como el cricoaritenoides lateral, el tiroaritenoides (abductores de la glotis) y el cricoaritenoides (tensor de las cuerdas vocales). Todos inervados por el laríngeo inferior o recurrente, que es una rama del laríngeo superior. Es decir que los músculos laríngeos intrínsecos responsables de las curdas vocales falsas, son los músculos cricoaritenoideos, tiroaritenoideos y cricotiroideos.
Las cuerdas vocales verdaderas funcionan como válvulas unidireccionales, ofreciendo poca resistencia a las presiones ejercidas desde el interior del tórax a la VA, en estas condiciones la presión es de aproximadamente unos 30 mm Hg, pero la presión ejercida desde el exterior de la VA, entonces las cuerdas vocales pueden presentar una resistencia equivalente al 140 mm Hg o unos 190 cm H₂0 para el adulto. Lo anterior quiere decir que será más complicado vencer la resistencia de las cuerdas vocales con la presión que se ejerce través de la presión de oxígeno a través de la mascarilla facial.
No se conoce cuál es la presión en VA superior en el niño, pero las cuerdas vocales falsas por su ubicación superior, también actúan como compuertas, evitando el escape de aire del sistema respiratorio inferior, lo cual ofrece una resistencia efectiva equivalente a 30 mm Hg, lo que serviría para hacer más efectivo el reflejo de la tos.
Estudios recientes han mostrado que la forma de la VA no es la de un embudo, como se ha afirmado en los últimos 60 años, sino que tiene una forma más elíptica que redonda, por este motivo se ha cambiado la forma y el diseño de los tubos traqueales pediátricos con “globo” o tubos con “taponamiento”. Las publicaciones más actuales apoyan el uso de tubos con manguito con estas características, para la mayor parte de la población pediátrica, especialmente si el niño es conectado a un ventilador. Aun en los recién nacidos 6.
Factores de riesgo
Tradicionalmente los factores de riesgo para LEP pueden ser clasificados dentro de tres categorías. Relacionados con el paciente, relacionados con la anestesia y relacionados con la cirugía.
Factores relacionados con la anestesia.
El factor anestésico más importante se encuentra relacionado con el nivel de anestesia, una anestesia ligera o insuficiente, conlleva a una predisposición para desencadenar un LEP. La inducción y la extubación del paciente son el momento crítico, que conlleva a una anestesia ligera, y por lo tanto a presentar dolor durante esta fase de la anestesia, por ejemplo la anestesia con desflurano puede producir tos durante la recuperación de la anestesia, particularmente al retirar el tubo traqueal, ya que se puede correlacionar con un despertar más rápido y una percepción temprana de cuerpo extraño en la vía aérea. Lo mismo puede ocurrir por la presencia de secreciones o sangre alrededor de la laringe, factores descritos como estímulos fuertes que pueden terminar en un LEP. En anestesia pediátrica la técnica más frecuente para inducción anestésica, es mediante la inducción inhalada con alguno de los gases actuales. El halotano y sevoflurano son dos de los gases inhalados con una menor capacidad de pungencia para la vía aérea. No hay diferencia de LEP entre estos dos gases. Desflurano por el contrario muestra una pungencia muy alta, hasta el 50%, seguido de isoflurano y de enflurano. El halotano es el agente inhalado menos productor de irritación de la vía aérea, sin embrago este gas se encuentra prácticamente en desuso en anestesia pediátrica 7.
La ausencia de propiedades irritantes del halotano y del sevoflurano contrasta con las propiedades irritantes del desflurano y del isoflurano, particularmente en su relación con la inducción de la anestesia. El halotano y el sevoflurano pueden utilizarse para inducir anestesia general de forma gradual, aumentando la concentración inspirada en forma progresiva de cualquiera de los dos gases, con una incidencia baja de LEP.
La intubación de la tráquea es otro momento crítico para desarrollar un LEP. Tanto por la colocación de un tubo en la tráquea, como por las maniobras de la laringoscopia, en ambas situaciones se puede desencadenar en un fuerte estimulo, que puede termine en un LEP o broncoespasmo.
Por otra parte tenemos al propofol el cual actúa deprimiendo el reflejo laríngeo, produciendo una baja incidencia de LEP. El tiopental ha mostrado incrementar la incidencia de LEP, mientras que ketamina rara vez se ha asociado a esta complicación 8.
Los movimientos de la cabeza, la colocación de una sonda nasogástrica, o la irritación de las cuerdas vocales por sustancias como sangre, moco, vómito u otros líquidos, los catéteres de succión, la hoja del laringoscopio, y la intubación con el paciente despierto sin relajantes musculares, son otros factores que pueden desencadenar LEP.
La inexperiencia del anestesiólogo a la intubación traqueal, múltiples intentos de intubación traqueal y la colocación de una mascarilla laríngea (ML) en un plano anestésico insuficiente, son otras causas de LEP 9. La inserción de la ML provoca sustancialmente menos estimulación neurocirculatoria que la intubación traqueal durante la anestesia con gases inhalados.
Hay reportes contradictorios respecto a uso del midazolam, y sus efectos sobre el LEP, algunos reportes han mostrado incremento en la incidencia de LEP, sin embargo otros investigadores no han podido demostrar tal afirmación. Por el contrario midazolam con remifentanil ha mostrado una baja incidencia de LEP como en cirugía oftalmológica bajo anestesia general 10. El tiopental está asociada a una alta incidencia de LEP. Aunque no explica satisfactoriamente cuál es la causa 11. Ketamina está asociada al 0.4% de incidencia de LEP muy probablemente por un incremento en la producción de secreciones que actúan como factores irritantes de la VA o de las zonas adyacentes a la laringe 12.
Factores relacionados con el paciente
Dentro de los factores relacionados con el paciente, tenemos los siguientes. El más importante es la edad, entre más pequeño sea el niño, la incidencia de LEP es mayor. La incidencia de LEP seguida de anestesia general es inversamente relacionada con la edad. Probablemente esto se encuentra relacionado con la anatomía de las estructuras aéreas del neonato y el lactante. El hecho de encontrar una laringe uno o dos segmentos vertebrales más altos, es decir que la laringe tiene un posición cefálica, una epiglotis en forma de “omega”, rígida (larga, firme y angulada) e igualmente alta. Se dispone de un tiempo menor para la intubación de traqueal, por tener menor volumen de reserva disponibles de 0₂. Los recién nacidos (RN), los exprematuros y los menores de un año de edad, son más susceptibles a esta complicación.
Lo mismo ocurre frente a una infección de la VA superior, la cual se encuentra asociada a una sensibilización de las vías eferentes bronquiales que pueden durar hasta cuatro o seis semanas. Este tipo de niños deben recibir medicación anestésica preparatoria a base de esteroides. Una sola dosis para tratar de disminuir la posibilidad de LEP.
El Anestesiólogo deberá poner especial atención al riesgo asociado a hiperreactividad de la VA, especialmente si se trata de infección viral. El daño al epitelio respiratorio puede persistir varias semanas, los virus son responsables de incrementar entre dos y cinco veces más el LEP 13. Para otros autores la infección de la VA superior ha sido comparada con colocar un tubo en la tráquea muy ajustado, el cual puede incrementar hasta once veces la posibilidad de presentar un cuadro obstructivo respiratorio secundario. Se sugiere que en aquellos niños con antecedentes de infección de VA reciente en fase de curación, la VA debe manipularse de forma menos invasiva, por ejemplo la ML. Sin embargo los estudios son contradictorios ya que otros han encontrado mayor índice de presentación de LEP después de una infección de VA superior 14.
Un apartado importante son los niños fumadores pasivos en el hogar, incluyendo aquellos que son hiperrreactores de la VA y los asmáticos, a los cuales se le ha descrito hasta diez veces mayor la posibilidad de presentar un LEP, sin olvidar a los adolescentes fumadores, que también pueden ser hiperrreactores de la VA 15.
La apnea obstructiva del sueño, la obesidad y la VA complicada, la enfermedad por reflujo gastroesofágico, pacientes de ASA IV, es decir niños graves, son igualmente factibles de presentar LEP 16.
Factores relacionados con la cirugía
Hay una asociación muy estrecha entre LEP y tipo de cirugía. Dentro de los factores relacionados con la cirugía destacan, los procedimientos quirúrgicos de la VA superior, La amigdalectomía y la adenoamigdalectomía son los procedimientos quirúrgicos con una alta incidencia de desarrollar LEP. Se presenta entre el 21 a 27% de probabilidades de que surja esta complicación. Otros tipos de cirugía son la broncoscopia, y la endoscopía digestiva alta. La apendicetomía y la hipospadias o cirugía urológica inferior como la cistoscopia. Los procedimientos de la vía urinaria inferior requieren de un plano anestésico profundo y una adecuada anestesia intraoperatoria, ya que la manipulación uretral puede precipitar un LEP, esto es debido al reflejo de Breuer-Lockhart.
Las dilataciones cervicales, y trasplante de piel en niños, también están asociadas a LEP 17. La cirugía de tiroides relacionada con el traumatismo del nervio laríngeo superior, la extracción de las glándulas paratiroides es un motivo de hipocalcemia, puede producir LEP de repetición 18. Los pacientes con parálisis cerebral con frecuencia tienen problemas de deglución y de reflujo gastroesofágico, pobre reflejo de tos y una capacidad respiratoria disminuida, lo cual predispone a LEP, broncoespasmo y broncoaspiración.
Momento de la cirugía en donde se puede presentar el LEP
El LEP se puede presentar en cualquier momento de la anestesia, pero los dos momentos más frecuentes son; durante la intubación o durante la extubación de la VA, debido a un nivel ligero o superficial del plano anestésico, por lo tanto la manipulación de la VA es la causa más frecuente de LEP. La laringoscopia con el paciente despierto, sedado o con anestesia ligera o sin relajante muscular. La colocación de un tubo mayor para la edad y peso del niño, son causas frecuentes de LEP. Aplica mucha presión de aire al “neumotaponamiento” del tubo traqueal también es causa de LEP.
Sin embargo también puede presentarse durante el mantenimiento de la anestesia como resultado de una anestesia ligera o anestesia con dolor.
Manejo del LEP
El manejo del LEP puede dividirse en preventivo o curativo (Tabla 1).
Tabla 1 Clasificación del grado de LEP
| Tabla 1. Clasificación del grado de LEP | |
|---|---|
| I | Es el grado más común, menos riesgoso y no requiere de tratamiento. Es una reacción de protección normal. |
| II | Los músculos aritenoepiglóticos están en tensión y bloquean la visión de las cuerdas vocales. Es una reacción de protección más intensa y duradera. Cede llevando la mandíbula hacia delante. |
| III | Todos los músculos de la laringe y faringe están en tensión, requiere traccionar la laringe hacia la epiglotis, y en muchos casos se requiere la reintubación |
| IV | La epiglotis está atrapada en la porción superior de la laringe. Se requerir el uso de relajantes musculares para su resolución. |
| Tomado de: Hernández-Cortez E. Complicaciones de la anestesia general en el paciente pediátrico. En: Hernández-Cortez E, Editor. Complicaciones de la anestesia pediátrica. México: Editorial Prado; 2014. p. 63-81 | |
Prevención
Las medidas preventivas incluyen; el reconocimiento de todos aquellos factores de riesgo presentes, descritos en secciones anteriores, en este mismo escrito. En recién nacidos, lactantes y niños pequeños, los reflejos de la VA se estimulan en un grado mucho mayor durante la inducción de la anestesia con inhalados. Por lo tanto usar gases inhalados con una baja pungencia o “picor” o sensación de ardor en la garganta durante la inducción inhalada del niño.
La técnica de inhalación rápida requiere de bolos altos de gas acompañados con niveles igualmente altos de oxígeno, por lo que pueden producir irritación frecuente de la VA, acompañada de tos, y salivación, además de suprimir la respiración. La técnica de inducción de 6/6 descrita para algunos inhalados, particularmente en ausencia de medicación anestésica puede desencadenar en mayor incidencia LEP. Las técnicas de inducción con grandes bolos de inhalados y oxígeno con la finalidad de hacer una inducción rápida de menos de 40 segundos, puede resultar en LEP. En adultos no medicados, la irritación de la VA es mucho mayor con 2 MAC de desflurano que con 2 MAC de isoflurano o sevoflurano. Hay varias razones para afirmar que el mejor procedimiento de inducción es usar una inducción endovenosa con propofol, en lugar de una inducción inhalada. Es decir que en aquellos niños con antecedentes de asma o que son hiperreactores, la mejor forma de realizar la inducción anestésica es con inductores tipo propofol 19.
El pretratamiento con morfina o fentanilo parece que disminuye la incidencia de tos e irritación de la VA al menos en un 10% 20. Inductores endovenosos como propofol, produce una depresión del reflejo laríngeo 21. El uso de atropina es controversial, reduce la frecuencia de LEP por su efecto antisialogogo al reducir la cantidad de secreciones de la faringe. Sin embargo resulta molesto para el niño la sequedad de boca intensa, el aumento de la frecuencia cardiaca, y de la temperatura corporal, además del consumo mayor de oxigeno cardiaco, por lo tanto la administración de atropina solo están indicados en situaciones especiales, una de estas situaciones es el RN o el prematuro, el cual tiene una mayor actividad del tono parasimpático. El uso de relajantes musculares reduce el riesgo de LEP. Entre los medicamentos más usados y efectivos tenemos la aplicación de lidocaína 1 a 2 mg/kg, puede funcionar tanto preventivo como correctivo del LEP. Su aplicación antes de retirar el tubo traqueal ha sido investigada desde 1970, un reciente estudio bien conducido ha demostrado que la aplicación de lidocaína a 1.5 mg/kg, dos minutos antes de la extubación, reduce la incidencia de LEP y la tos, ya que la lidocaína actúa a nivel central e incrementa la profundidad anestésica. El LEP puede disminuir 30% vs 19% con respecto a los controles 22.
Recientemente Qi X y colaboradores realizaron un metaanalisis para demostrar la eficacia de la lidocaína tanto endovenosa como tópica. Demostraron que ambas son efectivas para prevenir el LEP durante la anestesia general en el niño 23.
La administración de sulfato de magnesio 15 mg/kg i.v, antes de la intubación de la tráquea, ha resultados en una disminución de la incidencia de LEP en niños postamigdalectomisados. El efecto protector del magnesio parece estar en relación principalmente con la relajación del musculo y al aumento en la profundidad anestésica, se requieren más estudios al respecto.
Desde luego que incluye remover cualquier posible causa desencadenante, como secreciones y sangre, hasta estar seguro de que la laringe se mantiene completamente limpia.
Técnica de “no Touch”
Tsui y colaboradores mostraron que utilizando la técnica de “no touch”, la incidencia de obstrucción de la VA disminuye. Básicamente es una técnica de extubación con el paciente despierto, la cual consiste en aspirar cualquier tipo de secreción aun con el paciente en un buen plano anestésico, después colocar al paciente en cualquiera de los decúbitos laterales, acto seguido descontinuar la anestesia, hasta que el paciente despierte por completo y entonces retirar el tubo traqueal en forma suave sin producir sobresaltos y sin estimular la laringe y solo ventilar con oxígeno al 100% con mascarilla facial 24. Esta maniobra sugiere que el tubo traqueal sea retirado mientras los pulmones sean inflados por presión positiva, lo cual disminuye la respuesta aductora de los músculos laríngeos y con ello reduce la incidencia de LEP. La medicación con alguna de las benzodiacepina oral, disminuye el reflejo de la vía aérea superior y por lo tanto disminuye la incidencia de LEP 25.
Tratamiento del LEP
En el manejo efectivo del LEP, se requiere primero de un diagnóstico correcto y de una rápida y agresiva intervención del anestesiólogo. Muchos autores recomiendan primero manipular la VA, luego retirar aquellos factores que actúen como irritantes y finalmente administrar agentes farmacológicos 26. El primer pasó en el manejo del LEP es el reconocimiento de aquellos pacientes que tienen factores de riesgo para LEP, tomar las precauciones más adecuadas, individualizando cada caso en particular.
El diagnóstico de certeza solo se puede realizar, si logramos visualizar la glotis o las cuerdas vocales cerradas, en la gran mayoría de los casos esto no es posible. Podemos inferir el diagnóstico por los dados clínicos que presente el paciente. El LEP se divide en parcial y completo, en el primer caso existe una cierta entrada de aire a los pulmones, y desde el punto de vista clínico es reconocido por la presencia de un estridor inspiratorio. En el caso del LEP completo no existe entrada de aire a los pulmones y existe ausencia de la respiración y de los sonidos de respiración.
El esfuerzo respiratorio Incluye estridor inspiratorio, el cual puede progresar a obstrucción completa en cuyo caso progresará a un esfuerzo respiratorio completo. El tórax presenta movimientos respiratorios inefectivos, que son movimientos paradójicos entre el abdomen y el tórax. Existe retracción supraesternal y/o supraclavicular con movimientos abdominal exagerados. Además de la desaturación de oxígeno con o sin bradicardia. En el caso de que se trate de un LEP completo hay silencio respiratorio. La capnografía mostrará una onda plana. Ausencia de movimiento en la bolsa de reinhalación. Después aparecen los signos generales, como desaturación, bradicardia, cianosis, y arritmias hasta terminar en paro cardiaco. Si la obstrucción de la VA no responde a la colocación de una cánula de Guedel. La posibilidad de regurgitación o la presencia de sangre en la laringe pueden estarán presente.
Manejo en fase de emergencia LEP
La primera maniobra para tratar de resolver el LEP, es la movilidad firme y vigorosa de la mandíbula hacia atrás con extensión de cuello y cabeza, es decir subluxar la articulación temporomandibular, también conocida como maniobra de Esmarch-Heiberg (35), es decir se trata del empuje de la mandíbula hacia arriba y hacia adelante con la cabeza ligeramente extendida para retraer la lengua de la parte posterior de la faringe, lo cual favorece la movilidad de la lengua hacia la parte anterior, lo que permite el pasaje laríngeo se abra. La colocación de una cánula de Guedel de un tamaño correcto para la edad del niño, puede ser suficiente, dependiendo del grado de LEP. Si la boca no es posible abrirla, se puede colocar una cánula nasal a través de la nariz, cuidadosamente colocada para no provocar sangrado nasal.
Simultáneamente la aplicación de CPAP con oxígeno al 100% vía mascarilla facial, en casos extremos pueden usarse a dos manos. Es muy importante tratar de no pasar demasiado aire al estómago, ya que este puede producir regurgitación y/o vómito, con la consiguiente posibilidad de broncoaspiración.
El propofol es el medicamento que rompe el LEP en el 77% de los casos, una pequeña dosis subhipnótica de entre 0.25 y 0.8 mg/kg es suficiente. Los efectos secundarios son relativamente benignos. Sin embargo el paciente puede estar en apnea, cianótico y bradicardico para cuando se aplique el propofol, lo cual puede aumentar la depresión cardiovascular. Propofol ofrece más ventajas que succinilcolina 27.
Si el LEP no se resuelve, la siguiente medida es la aplicación de succinilcolina. Es considerada como el estándar de oro para resolver esta complicación. Dosis muy bajas de succinilcolina como 0.1 mg/kg han sido reportadas para romper eficientemente el LEP, a esta dosis se preserva la ventilación durante situaciones de urgencia 28.
La administración de succinilcolina generalmente debe de ir acompañada de atropina. Para cuando administremos este medicamento, es muy posible que el niño, además de cianótico esté bradicardico, la succinilcolina es peligrosa, en un miocardio que está sufriendo por hipoxia y bradicardia y puede terminar por dañar el corazón. La atropina puede contrarrestar dicho efecto depresor de succinilcolina e hipoxia. La atropina también disminuye las secreciones faríngeas. Se recomienda que succinilcolina y atropina sean administrados antes de que la saturación de oxigeno se encuentre por debajo de 85% Si no es posible contar con una vía endovenosa permeable, entonces podemos utilizar una vía alterna, como por ejemplo la vía intramuscular intralingual o intraosea, la dosis intralingual es de por lo menos 2 mg/k. La vía intramuscular tiene la desventaja de que su absorción es irregular y se han reportado una mayor incidencia de arritmias, no se conoce la causa exacta. La dosis intramuscular de succinilcolina requiere de una dosis mayor hasta de 4 mg/k, su desventaja es que requiere de por lo menos un minuto para la ruptura total del LEP. En el caso de no contar con succinilcolina, se puede administrar un relajante muscular no despolarizante como el rocuronio, dosis de 1.2 mg por vía endovenosa es suficientes para romper rápidamente el LEP, el problema puede surgir cuando el niño no tiene una vía endovenosa permeable, para lo cual también puede usarse la vía intramuscular específicamente el musculo deltoides. Lynne y colaboradores demostraron que la dosis necesaria de rocuronio para tener una relajación completa al 100% de las cuerdas vocales, en niños menores de un año es de 1 mg/kg, en tan solo 2.5 minutos y de 1.8 mg/kg en niños mayores 29.
Otras drogas reportadas como efectivas en el tratamiento del LEP, son el alfentanilo y la meperidina, especialmente si el factor desencadenante del LEP es un estímulo muy doloroso. El doxapram a 1.5 mg/kg puede suprimir el LEP al incrementar la profundidad respiratoria. Nitroglicerina 4 μg/k, también ha sido reportada como efectiva, pero este fármaco actúa principalmente sobre la musculatura lisa y no sobre el musculo esquelético propio de las cuerdas vocales 30. El tratamiento definitivo para el LEP refractario es con bloqueo del nervio laríngeo superior con anestésicos locales 31.
Otras maniobras: La primera maniobra es hacer una presión gentil en la línea media del tórax, tratando de hacer una presión a la expulsión de aire atrapado en tórax y permitir la apertura de las cuerdas vocales que funcionan con apertura unidireccionalmente. Esta maniobra permite vencer una presión de las cuerdas vocales de tan solo 30 mm Hg, mientras que con la aplicación de CPAP con oxígeno al 100% vía mascarilla facial, tenemos que vencer una presión de más de 150 mm Hg (presión de adulto). Es decir que con esta maniobra se forza la apertura de la glotis al incrementar bruscamente la presión intratorácica, permitiendo la respiración o estimulando el reflejo vagal de Hering-Breuer. El 74% de los LEP fueron corregidos con esta maniobra en contra de un 34% a quienes se les aplico el tratamiento convencional en niños que recibieron cirugía de amígdalas 32.
La segunda maniobra es una maniobra con evidencia científica limitada respecto a su uso terapéutico. Se denomina maniobra de Larson. Es una técnica que primeramente fue descrita hace más de 40 años por Guadagni y más tarde retomada por Larson.
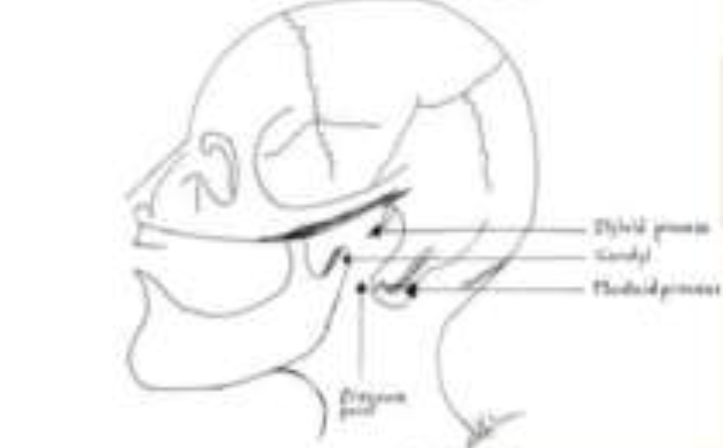
Se trata de una maniobra bilateral que consiste en hacer presión sobre las apófisis mastoides a nivel de los procesos estiloideos, entre la rama posterior de la mandíbula y el proceso mastoideo anterior, con una pequeña fuerza vigorosa dolorosa, que rompe el LEP por la presencia de dolor, que relaja las cuerdas vocales. Al mismo tiempo que se desplaza la mandíbula hacia adelante y arriba 33. (Figura 1)
El último paso para rescatar una vía aérea de urgencia es hacer una intubación traqueal, aun con las cuerdas vocales cerradas, produciendo un traumatismo en las mismas, pero rescatando la VA de urgencia. La última maniobra será la cricotirotomía o la traqueostomía, como maniobras de extrema urgencia.
Seguimiento después de un LEP
Cuando un paciente ha salido de un LEP severo, se recomienda dejarlo en observación por lo menos dos a tres horas, hasta estar seguros de que no presente una de las complicaciones más frecuentes, secundarias a un LEP severo. Es el edema agudo de pulmón por hipoxia severa. O edema pulmonar no cardiogénico. Se produce por la generación de presión negativa, al intentar respirar y enfrentarse con una glotis cerrada, promoviendo la trasudación de fluidos hacia el alveolo, además de que la hipoxia aumenta la estimulación simpática, causando vasoconstricción sistémica y pulmonar 34.
Conclusiones.
Lo más importante en el LEP es la prevención, la identificación de los factores de riesgo en aquellos pacientes susceptibles, podrá ayudarnos para evitar la obstrucción de la vía aérea, permitir todas aquellas maniobras que pueden contribuir a la prevención es prioritario. Si el LEP ya se ha instalado el tratamiento con propofol a dosis subhipnoticas ayudan a romper con el espasmo. La administración de relajantes musculares y la reintubación pueden ser medidas necesarias para resolver el problema, finalmente el nitroprusiato de sodio es una alternativa más que contribuye a relajar la musculatura bronquial y finalmente el bloqueo de los nervios laríngeos superiores puede ser una medida extrema. El edema pulmonar obstructivo es una complicación que se puede presentar en el periodo mediato a esta complicación.











 text new page (beta)
text new page (beta)