Introducción
La humanidad enfrenta, actualmente, grandes retos, desde la creciente aparición de casos de cáncer (Anjali Das et al. 2022), la progresiva demanda y contaminación del agua (Valadez-Renteria et al. 2023) hasta el calentamiento global de la tierra debido al incremento de los gases de efecto invernadero (Celaya et al. 2022) entre muchos otros. La síntesis de nanomateriales se observa como un campo que puede ayudar a mitigar los problemas antes mencionados. Sin embargo, en términos generales, la formación de estructuras nanométricas representa un reto y el poder controlar su morfología se ha vuelto tendencia. Si se busca el término “nanopartículas” en inglés, en alguna base de datos de artículos científicos como Scopus (www.scopus.com), se obtendrán más de 700,000 documentos, lo que dará idea al lector del gran interés de la comunidad científica en este tema. De estos, más de la mitad han sido publicados en los últimos 5 años; aunado a lo anterior, los documentos están centrados en 10 categorías, entre las que destacan ciencia de materiales, química, física y astronomía, ingeniería, ingeniería química, bioquímica, genética, farmacéutica, ciencias ambientales y medicina, entre otros. Sin embargo, no todos son de relevancia en nuestro caso, ya que este trabajo se enfoca en los materiales usados como soportes y catalizadores. Estos están principalmente centrados en los temas, ciencia de materiales, química, física, ingeniería, ingeniería química y ciencias ambientales. En su conjunto, estos representan el 82%, aproximadamente.
Típicamente, un soporte de catalizadores debe ser un sólido poroso inerte con propiedades como alta área superficial, para tener capacidad de carga de las fases activas. Una porosidad controlada, ya que es importante que éste facilite la difusión de los reactivos. Estabilidad térmica y química, para garantizar la estabilidad del catalizador, así como la actividad de las fases activas por el mayor tiempo posible. Baja toxicidad, disponibilidad y bajo costo (Satterfield 1991). De tal manera, la selección adecuada del soporte es de vital importancia en el desempeño y eficiencia del catalizador al ser aplicado en una reacción específica.
Entonces, la preparación de nanopartículas que sirvan como soportes es un campo que ha despertado un gran interés debido a las múltiples propiedades presentadas por las nanopartículas y la amplia variedad de aplicaciones en que se pueden usar. No obstante, por muchos años no se le dio gran importancia a la parte morfológica, puesto que las fases activas solo necesitaban soportes optimizados en sus propiedades de bulto. Esto ha cambiado con las propiedades encontradas en los nanomateriales. Y ahora, la parte morfológica y la estructura de un soporte se consideran parámetros importantes durante la preparación de un catalizador, al determinar, en cierto grado, la naturaleza del proceso catalítico al que será aplicado el material en cuestión. Esto se relaciona con la preferencia de los sitios catalíticos a ocupar ciertas posiciones específicas en un material, por ejemplo, en las esquinas, aristas, o sobre determinada familia de planos cristalográficos (Topsøe, Clausen, y Massoth 1996). De este modo, se han estudiado continuamente materiales que permitan modular estas características, y así tener control sobre la relación entre la estructura y la morfología, con la actividad catalítica.
La síntesis y preparación de nanomateriales presentados en la mayoría de los documentos se centra en nanopartículas de composiciones muy variadas. No obstante, de entre ellos destacan los trabajos relacionados con óxidos metálicos, pues estos se han usado históricamente como soportes y catalizadores para diversas aplicaciones (Martín et al. 2021). Destaca el óxido de aluminio mejor conocido como alúmina (Al2O3), uno de los más empleados industrialmente, al fungir como soporte de catalizadores para petroquímica (Trueba y Trasatti 2005). Este óxido tiene varias fases cristalográficas, la más utilizada es la fase gamma que se alcanza entre los 400 ºC y los 600 ºC, mientras que la más estable es la fase alfa, que se obtiene por arriba de los 1000 ºC. La fase gama tiene muy buenas propiedades mecánicas y alta área superficial, misma que puede ir hasta los 600 m2.g-1 dependiendo del método de síntesis (Satterfield, 1991). Normalmente, no presenta una forma específica, pues se considera amorfa, aunque para su uso industrial se fabrica en pellets de muy diversas formas. Otro de los materiales típicos es el óxido de titanio, mejor conocido como Titania (TiO2). Este óxido normalmente tiene una estructura cristalina tetragonal para los dos polimorfos más conocidos: la anatasa y el rutilo. Sin embargo, este óxido tampoco tiene una morfología definida que lo identifique. Más bien, es característico de la anatasa, su alineación en cadenas en zigzag a partir de los octaedros formados por un átomo de titanio y seis de oxígeno (Bagheri et al. 2014). Según Peláez y colaboradores, las estructuras de las fases de TiO2 se forman dependiendo de cómo se unan los octaedros que las conforman, es decir, que si los octaedros están unidos por los vértices se forma la fase anatasa (Figura 1a), mientras que al unirse a través de los bordes se forma la fase rutilo (Figura 1b). Finalmente, como se puede ver en la Figura 1c, si se unen los octaedros por medio de los vértices y los bordes tendremos la fase brookita (Pelaez et al. 2012). En la Figura 1 las esferas rojas representan oxígenos, mientras que el átomo de titanio se encuentra en el centro de todos ellos.
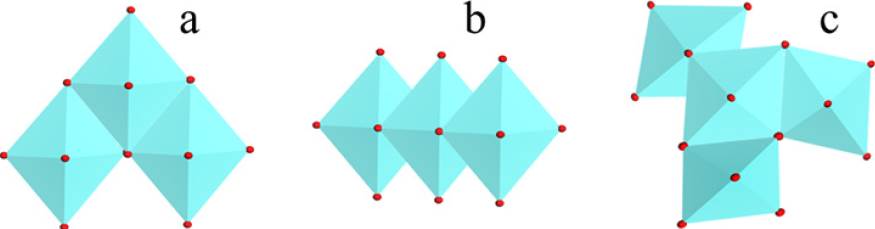
Fuente: Adaptado de Peláez et al. (2012).
Figura 1 Esquema representativo de octaedros TiO6 formando las fases a) anatasa, b) rutilo, y, c) brookita.
Otros materiales como el óxido de zinc, de zirconio, de cerio, de magnesio o de sílice son también muy utilizados. De entre estos, este último (el óxido de silicio) destaca, pues puede formar múltiples estructuras mesoporosas como la SBA-15 o las MCM, haciéndolo muy interesante como soporte (Figura 2).

Fuente: Elaboración de los autores.
Figura 2 Esquema de óxidos de silicio con estructura definida, SBA-15 (izquierda) y MCM-41 (derecha).
La síntesis de estos óxidos a escala nanométrica ha permitido modular sus propiedades electrónicas, mecánicas, magnéticas y de superficie (Kaur et al., 2022). Se encontró, por ejemplo, que las nanopartículas menores de 100 nm presentan típicamente un aumento en el área superficial específica, efectos de confinamiento cuántico (László et al., 2018) o enriquecimiento metálico superficial (Díaz de León et al., 2014). En las siguientes secciones discutiremos sobre la síntesis de nanopartículas de los óxidos más usados.
Síntesis y propiedades de nanopartículas de alúmina
Como se mencionó en el párrafo anterior, la obtención de nanopartículas de alúmina que puedan ser usadas como soporte abre un universo de posibilidades en las que se permita modular, por ejemplo, la interacción metal soporte, o lograr una amplia dispersión de las fases activas. Sin embargo, la síntesis de estos materiales tiene múltiples variables que tomar en cuenta, como el uso de agentes directores de estructura, temperatura, presión, metodología y precursores utilizados. No obstante, la posibilidad de preparar materiales con las características morfológicas deseadas es difícil y no existe un método de síntesis específico para lograrlo. Actualmente, la síntesis asistida por surfactantes es la más usada, debido a que ha demostrado un buen control de la morfología, forma y tamaño con su empleo, aunque las características obtenidas dependen mucho del método utilizado (Kaur et al., 2022). Un caso es la síntesis de alúmina por un método de autoensamblaje, empleando surfactantes como directores de estructura (Yuan et al., 2008). En este caso, se utilizaron distintos surfactantes y precursores de aluminio, lo cual permitió la obtención de materiales con propiedades texturales en función de los precursores y temperaturas de calcinación; áreas superficiales específicas entre 180 m2.g-1 y 480 m2.g-11 y volúmenes de poro de aproximadamente 0.80 cm3.g-1. En general, estos nanomateriales de alúmina presentaron una alta área superficial (> 200 cm3.g-1), con una red mesoporosa ordenada, lo cual es de interés para utilizarse como soporte (Fu et al., 2017) o catalizador. Liu y colaboradores estudiaron el efecto de la morfología de distintas alúminas mesoporosas ordenadas al servir como soporte de paladio en la oxidación catalítica de CO y C3H6, encontrando un aumento en la actividad y estabilidad térmica del catalizador comparado con alúmina comercial no nanométrica (F. Liu et al., 2015). Este material es estable hasta 1000 ºC, presentando una distribución estrecha de tamaño de poro y alta área superficial. Otro ejemplo es el trabajo de Dabbagh y colaboradores, donde reportan la formación de nanobastones de alúmina en presencia de alanina en medio acuoso a condiciones ambientales (Dabbagh et al. 2011). Sus nanobastones tenían diámetros de 6 a 8 nm y longitudes de 17 a 18 nm. Mientras que Díaz de León y colaboradores (Díaz de León et al., 2014) reportaron la síntesis de nanobastones de alúmina empleando surfactantes pluronics y usando 2-propanol como solvente a 0 ºC por 24 horas para formar un gel. Ellos encontraron que la morfología de los nanobastones obtenidos depende de la cadena del surfactante utilizado. La longitud promedio de los nanobastones fue de 26 nm para el pluronic L64 con cadena de 2900 g.mol-1, de 19 nm para el pluronic P123 de 5800 g.mol-1 y de 14.3 nm para el pluronic F68 de 8400 g.mol-1. En cuanto al diámetro de los nanobastones que obtuvieron, estos presentaron un comportamiento inverso, al ser mayor usando el pluronic F68 con 3.2 nm, seguido del P123 con 2.4 nm y de 1.9 nm para el L64. Los resultados de difracción de rayos X mostraron que la fase -Al2O era la que estaba presente en todos los nanomateriales. Usando este resultado realizamos el modelado de las estructuras nanométricas de los nanobastones dependiendo de su diámetro y longitud. Como se puede observar en la Figura 3, los nanobastones tienen el mismo arreglo cristalino y solo cambia la cantidad de átomos presentes en cada estructura. Para el caso de los nanobastones de Dabbagh y colaboradores (Dabbagh et al., 2011), se utilizaron 575 átomos totales, de los cuales 348 fueron oxígenos. Para el caso de los nanobastones más grandes de Díaz de León y colaboradores (2014), se usaron 1,454 átomos, de los cuales 912 fueron oxígenos (Figura.3).

Fuente: Elaboración de los autores.
Figura 3 Modelado de las nanoestructuras reportadas por Dabbagh et al. (2011) y Díaz de León et al. (2014). Los átomos indicadores de color no están a escala.
Más recientemente, por parte de nuestro grupo de investigación se reportó la preparación de nanoesferas huecas tipo erizo de Al2O3 por medio de una síntesis hidrotermal asistida por Triton X-100 como agente director de estructura (Mendoza-Núñez et al., 2022). La síntesis se realizó usando sulfato de aluminio (Al2(SO4 )3.18H2O) y urea (CO(NH2)2) como agente reductor y agua desionizada para disolver los reactivos a condiciones ambientales. Las muestras calcinadas a 500 ºC inicialmente mostraron por microscopía electronica de barrido (SEM por sus siglas en ingles) que la morfología se asemejaba a microesferas 3D huecas de 2.4 ± 0.6 micras. El análisis por microscopía electrónica de transmisión (TEM, por sus siglas en inglés) permitió observar claramente que sí eran microesferas huecas y parecían estar compuestas por nanocinturones y nanobastones superpuestos. Los nanocinturones asemejaban ser las bases para el crecimiento de los nanobastones, puesto que estos últimos presentaron tamaños más pequeños. Los nanobastones tuvieron en este caso un diámetro de 14 nm, pero longitudes mayores a los 100 nm. Por otra parte, Jiang y colaboradores (Jiang et al., 2022) utilizaron también el método hidrotermal, aunque en este caso los autores utilizaron nitrato de aluminio (Al(NO3 )30 9H2O) y fosfato de sodio (Na3PO4 2H2O) en solución acuosa. Ellos usaron la autoclave para verificar el efecto de la temperatura entre 160 ºC, 180 ºC y 200 ºC. Sus materiales no fueron calcinados, por lo cual sus nanopartículas resultaron de la fase bohemita. Ellos encontraron microestructuras que parecen cuerdas de hasta 3-4 nm y pequeños cúmulos laminares. Las cuerdas vistas en alta resolución resultaron estar formadas por nanocables, estas estructuras más pequeñas mostraron diámetros de entre 25 y 28 nm. Otro trabajo acerca de esferas de alúmina fue reportado por Demir Cakan y colaboradores, donde menciona que se utilizó el método hidrotermal pero esta vez asistido por glucosa y con diferentes concentraciones de ácido acrílico, molécula usada principalmente por su fácil polimerización (Demir-Cakan et al., 2022). La síntesis hidrotermal se realizó a 190 ºC por 16 horas. Las esferas micrométricas obtenidas con diámetros de hasta 4 micras resultaron estar formadas por estructuras esféricas más pequeñas. Cuando los autores aumentaron la concentración de ácido acrílico, las nanoesferas fueron más fácilmente detectables. En las imágenes que presentaron los autores se puede observar que su tamaño resultó cercano a los 50 nm en promedio.
Como se puede observar el método hidrotermal asistido por surfactantes ha generado interesantes resultados morfológicos. Sin embargo, en este punto cabría mencionar que algunos de los surfactantes no son fáciles de remover del nanomaterial final. Así, los procesos térmicos para estabilizar la estructura cristalina de las nanopartículas pueden llegar a sinterizar muy fácilmente las estructuras si estos son bruscos o se encuentran a temperaturas muy elevadas.
De tal manera, otros métodos como el de emulsión-hidrólisis (Shojaie-Bahaabad y Taheri-Nassaj, 2008), aerosol-hidrólisis (Ingebrethsen y Matijević, 1980) o plasma térmico (Ouyang et al., 2020) han mostrado ser eficientes para obtener nanopartículas esféricas. En particular, el método de plasma térmico hace uso de un sistema de alta frecuencia de 10 kW a 4 MHz, una antorcha de plasma controlada y un reactor cilíndrico que actúa también como cámara para colectar las nanoesferas formadas. Una vez que este sistema está estable se procede a enviar un flujo de aluminio y oxígeno a la cámara de plasma donde ocurre una reacción redox que produce las nanoesferas. Las nanopartículas obtenidas presentaron una distribución de diámetros centrada en los 60-70 nm. Sin embargo, de los trabajos mencionados anteriormente, en este es donde pudimos observar las nanoesferas más pequeñas.
Los nanomateriales de alúmina que hemos discutido hasta el momento tienen aplicaciones muy variadas dependiendo del campo en que se han especializado los autores. Particularmente, en nuestro grupo de investigación hemos usado nanobastones de alúmina como soportes de nanopartículas de óxidos de níquel y tungsteno (Díaz de León et al., 2014, 2015) sulfurados para realizar reacciones de hidrodesulfuración ultra profunda. El uso de los nanobastones en este caso tuvo excelentes resultados en cuanto a la dispersión (≈1) de las fases activas,1 ya que, si bien no presentaron porosidad, las fases activas resultaron más expuestas al flujo de los reactantes. Y aunque desafortunadamente no pudimos probar que disminuyen los efectos difusivos intrapartícula o extrapartícula, sí obtuvimos mejores propiedades catalíticas (≈50% más actividad) que un catalizador industrial contra el que se compararon (Díaz de León et al. 2015). En relación con esta aplicación, se ha reportado un efecto en la geometría de la fase activa dependiendo del plano en el que se sitúa sobre el soporte; la fase activa se sitúa de forma basal y tiene un ordenamiento preferencial en la dirección [001] cuando se encuentra en los planos (111) de la alúmina, mientras que de una interacción en los planos (100) se obtiene un crecimiento preferencial en la dirección [001] de la fase activa situada por los bordes del MoS2 en el soporte (Sakashita y Yoneda, 1999). Otro uso que les dimos fue como soporte para la inmovilización de cloroperoxidasa (CPO), enzima que funciona como catalizador en la reacción de oxidación de dibenzotiofeno (Juárez-Moreno et al., 2015). Cabe mencionar que en ambos casos las actividades observadas en sus respectivas reacciones se incrementaron considerablemente. Esto fue atribuido a la presencia de la nanoestructura y a un enriquecimiento de la superficie con aluminio, lo que propició que esta tenga un carácter más metálico y, por lo tanto, sus sitios de acidez Lewis se incrementen. Cabe mencionar que las propiedades de los nanobastones preparados con el método sol-gel suave asistido por surfactantes permite modular las propiedades texturales al calcinar las nanoestructuras a diferentes temperaturas. Pasando de 415 m2.g-1 calcinando a 500 ºC hasta 238 m2.g-1 calcinando a 700 ºC y hasta 170 m2.g-1 usando 900 ºC para este último tratamiento. El volumen de poro promedio formado por las redes entrelazadas de nanobastones pasó de 1.2 cm3.g-1 a 1.0 cm3.g-1 y a 0.8 cm3.g-1, respectivamente. Mientras que el tamaño de poros promedio se incrementó de 11.9 nm a 17.2 nm y hasta a 21.3 nm con el aumento respectivo de la temperatura de calcinación. De hecho, el material que resultó ser el mejor para poder inmovilizar la CPO y al mismo tiempo llevar a cabo la actividad catalítica fue el calcinado a 700 ºC. En el caso de las nanoesferas huecas formadas por los nanocinturones y nanobastones las utilizamos para la deshidratación catalítica de 2-propanol con excelentes resultados.
Estos trabajos muestran la importancia de la morfología en las propiedades generales de la alúmina; quisiéramos hacer énfasis en que un simple tratamiento térmico puede tener un efecto significativo en las propiedades texturales, morfológicas y por supuesto en la actividad catalítica (Juárez-Moreno et al., 2015). Como también lo demostraron Cheng y colaboradores, ellos observaron la formación de nanoplatos de alúmina al cambiar la temperatura de síntesis, lo cual generó un aumento en la acidez del material a diferencia del material sin tratamiento térmico (Jun-Cheng et al., 2006).
Como puede apreciarse, las propiedades de los nanomateriales de alúmina sintetizados por los diversos métodos mencionados en párrafos anteriores son muy variados, así como las propiedades texturales, morfológicas y estructurales obtenidas. Sin embargo, de manera general puede concluirse que los nanomateriales de Al2O3 obtenidos presentaron mejores propiedades que la alúmina de bulto sin morfología definida.
Por otra parte, cada vez existen más reportes de catalizadores preparados sobre nanoalúmina para muy diversas aplicaciones, por ejemplo, Shi y colaboradores reportaron el uso de nanopartículas de alúmina de diferentes tamaños para depositar 1% de Pd (Shi et al., 2023). Los autores tomaron alúminas de 10 nm, 20-50 nm, 50 nm y 1000-2000 nm para hacer las impregnaciones por llenado de poro, encontrando que la conversión de metano tenía una curva de actividad a menores temperaturas con los catalizadores soportados en la alúmina nano de 10 nm. Y que para llegar a la misma conversión debían aumentar de manera significativa la temperatura de reacción. Debido a este problema, los autores analizaron los catalizadores en condiciones de flujo continuo para probar su estabilidad a largo plazo, encontrando que la alúmina nano de 10 nm de tamaño promedio era la más estable de entre los materiales estudiados. Por su parte, Arul y colaboradores prepararon catalizadores de Co/Cu sobre nanoesferas de alúmina de 62 nm encontrando que el catalizador era térmicamente estable hasta 750 ºC para ser usado en la preparación de hidrocarburos lineales de cadena larga (Jayan, Dawn, y Vinoth Kumar, 2020). Asimismo, Khajeh y colaboradores informaron que un catalizador Ni soportado en nanoalúmina resultó con el mejor comportamiento catalítico en comparación con los catalizadores preparados sobre nanoceria y cliptilopita en el reformado seco de metano (Khajeh Talkhoncheh y Haghighi, 2015).
Síntesis y propiedades de nanopartículas de Titania
El óxido de titanio (TiO2) comúnmente se ocupa como base del color blanco en muchos tipos de pintura, papel, fibras sintéticas, alimentos y cosméticos (Haider, Jameel y Al-Hussaini, 2019). Sin embargo, de manera general, el TiO2 es un semiconductor tipo n con una banda de conducción de 3.2 eV, con excelentes propiedades electrónicas y ópticas, además tiene alta estabilidad física y química. Estas propiedades hacen que este óxido pueda utilizarse en muchos otros campos como en celdas solares, sensores, electroquímica y fotocatálisis. A partir de los años 70 el uso de este óxido se acrecentó como soporte para procesos catalíticos. Por ejemplo, Fujishima y Honda diseñaron un electrodo de TiO2 que aplicaron para la fotólisis del agua (Fujishima y Honda, 1972). Este electrodo se puso conectado con un electrodo de platino y se aplicó una carga externa. Al irradiar el electrodo de TiO2 se observó que la corriente fluía del electrodo de platino al de TiO2 a través del circuito externo. Esto reveló que la reacción de oxidación ocurría en este electrodo de TiO2 y que la reducción se llevaba a cabo en el de platino. Otro ejemplo es su empleo en equipos comerciales para el control de contaminantes del aire, usado como soporte para sistemas de reducción catalítica selectiva por Matsuda y Kato (1983). Cabe mencionar que los procesos catalíticos han sucedido históricamente sobre materiales con sitios específicos a escala nanométrica. Esto pasó desapercibido o no podía describirse por muchos años, es hasta los años 80 con la invención del microscopio de efecto túnel por Binning y Roher que fue posible observar átomos individuales. Esto permitió el desarrollo de la nanotecnología y el estudio de los materiales catalíticos a esta escala. Observar la morfología ha permitido correlacionar su desempeño en algún proceso catalítico con la forma de la nanopartícula. En la Titania destacan los trabajos en los que se puede sintetizar con forma de nanoesferas e incluso a estas alturas ya se encuentra a la venta de forma comercial (Titania degusa). Además de las nanoesferas, destacan algunas morfologías como lo son los nanobastones, nanotubos, nanovarillas y materiales mesoporosos/nanoporosos (Chen y Mao, 2006).
Entre los métodos de síntesis más estudiados para obtener nanomateriales de Titania se encuentran el sol-gel, hidrotermal, solvotermal y depósito de vapor químico (Chen y Mao, 2006). Donde pequeñas variaciones paramétricas nos permiten obtener morfologías diversas como se puede apreciar en la Figura 4. Por ejemplo, dentro de nuestro equipo de investigación se han obtenido nanobastones utilizando el método hidrotermal; a partículas micro y nanométricas de TiO2 se les añadió una solución de NaOH, la mezcla resultante fue colocada en una autoclave a 140 ºC por diferentes tiempos (Díaz de León et al., 2019). Esto permitió a Díaz de León y colaboradores observar la formación de nanohojas laminares 2D a 5 horas de tratamiento, coincidiendo con lo reportado por Zhang y colaboradores (Z. Zhang et al., 2010). A partir de las 15 horas de síntesis hidrotermal estas estructuras laminares se separan formando nanobastones de titanatos de sodio bien definidos con diámetros de 9 nm y longitudes cercanas a los 100 nm. Posteriormente, con tratamientos ácidos usando HCl y HNO3 a distintas concentraciones, se logró controlar el diámetro y longitud de los bastones. Partiendo de estructuras con longitudes de 107 ± 23 nm se pudieron obtener nanobastones de hasta 40 nm de largo, conservando su diámetro en no menos de 8.6 nm (Díaz de León et al., 2021). Sin embargo, previamente, Kasuga y colaboradores habían reportado que, con una síntesis hidrotermal parecida, pero a 110 ºC y limpiando los titanatos con HCl se obtenían nanotubos de Titania (Kasuga et al., 1999). Otro trabajo similar reportado por Sun y colaboradores menciona que los nanotubos obtenidos no son de TiO2 sino más bien de H2Ti3O7 (Sun y Li, 2003). En esta misma dirección, Ota y colaboradores reportaron que usando nanopartículas de TiO2 se pueden obtener los nanotubos sin la necesidad de un tratamiento hidrotermal (Ota et al., 2018). Los autores mencionan que solamente utilizando HCl sobre las nanopartículas y controlando el tiempo de contacto se pueden obtener los nanotubos con excelentes propiedades texturales.

Fuente: Elaboración de los autores.
Figura 4 Síntesis hidrotermal de nanomateriales de TiO2 con distintas morfologías.
Asimismo, variaciones en los precursores del titanio podrían ser significativos en cuanto a la morfología, debido a que si utilizamos isopropóxido de titanio podría dar como resultado la formación de nanohojuelas según lo reportado por Gopal y Basha (2018). No obstante, utilizando el isopropóxido en conjunto con solventes como alcohol isopropílico y N,N-dimetilformamida, en esa misma síntesis hidrotermal a 200 ºC durante 20 horas y con tratamientos térmicos de secado y calcinado, podemos obtener morfologías que asemejan flores (J. Wang et al., 2021).
Es bien conocido que este óxido puede funcionar como excelente soporte catalítico, pues las nanopartículas metálicas con la superficie presentan una buena interacción (Tauster et al., 1981). Se ha reportado también que esas interacciones inducen cambios en posición, dirección de crecimiento de las nanopartículas, en la actividad catalítica y que pueden además modificar la selectividad de las reacciones (Díaz De León et al., 2017 y 2018). Estudios recientes revelaron que para reacciones de oxidación de tolueno, xileno y benceno es mejor utilizar la fase rutilo debido probablemente a su alta estabilidad termodinámica y a que presenta una baja interacción metal soporte. Sin embargo, la gran mayoría de los catalizadores reportados en la literatura hacen uso de la fase anatasa (Bagheri et al., 2014). Normalmente, el comportamiento catalítico de un catalizador heterogéneo es determinado principalmente por el tamaño de partícula logrado. Por ejemplo, en el caso de nanopartículas de Au en donde la Titania ha demostrado ser un excelente soporte, según los reportes de Bamwenda y colaboradores (Bamwenda et al., 1997) para nanopartículas, y de Guo y colaboradores (Guo et al., 2023) para átomos solitarios. Ghampson y colaboradores también usaron este soporte para depositar Re-MoOx así como Re-Vox encontrando notable dispersión de las fases activas sobre nanopartículas de TiO2 (Ghampson et al., 2017). De hecho, Zhong y colaboradores reportaron un estudio sistemático del efecto de la morfología de este óxido, depositando Ru por un método fotoquímico a temperatura ambiente (Zhong et al., 2023). Los autores usaron nanoesferas, nanohojas, nanocinturones y nanoaglomerados de TiO2 en su fase anatasa, para depositar 5% en peso de Ru. Encontrando diferencias claras en la selectividad de la hidrodesoxigenación de guaiacol, con las nanohojas obtuvieron principalmente ciclohexanol, mientras que con los nanocinturones el producto principal fue metoxihexanol y, finalmente, con las nanopartículas se obtuvo ciclohexano, que es el producto totalmente hidrogenado.
Síntesis y propiedades de nanopartículas de otros óxidos
Otros de los óxidos metálicos utilizados en la catálisis es el dióxido de zirconio. Distintos estudios han analizado el efecto de la morfología de este material: desde materiales mesoestructurados, nanobastones o nanoestrellas. En el trabajo de Liu y colaboradores, se investiga el efecto de la morfología de soportes de ZrO2 en la reducción catalítica a bajas temperaturas de NO (Liu et al., 2019). Los materiales fueron sintetizados a partir del método de autoensamblaje inducido por evaporación y solvotermal, los cuales presentan estructuras definidas desde nanoesferas huecas, nanovarillas y nanoestrellas. Las principales diferencias de estos soportes se encuentran en las propiedades ácidas y texturales de los materiales, además, se muestra que las fases cristalinas expuestas en la superficie y en el bulto dependen de la morfología obtenida.
La conversión de CO2 y el posterior uso de carbón como fuente de energía son tecnologías de gran interés para combatir el continuo deterioro am biental. En esta dirección, la síntesis Fischer-Tropsch, la reacción de Sabatier al igual que la reacción de desplazamiento de gas de agua aparecen como una alternativa para recuperar y aprovechar el CO2. Estas reacciones suelen utilizar como catalizadores materiales de TiO2, SiO2, Al2O3, ZrO2 o CeO2 con metales nobles (Ru, Rh y Pd) o hierro como fases activas (Khdary et al., 2022). Además, diversos estudios muestran que este tipo de reacciones dependen de la morfología y estructura del catalizador. Por ejemplo, Yao y colaboradores estudiaron la hidrogenación de CO2 en una serie de materiales de FeOx, donde observan que la formación de nanovarillas tiene un efecto adverso, en comparación con catalizadores de nanopartículas (Yao et al., 2021). Por otra parte, Puga y Corma usaron nanopartículas de Ni-Fe bajo luz solar para la hidrogenación de CO2 (Puga y Corma, 2018). Los autores reportaron que el contacto entre las fases cristalinas de NiO y -Fe2O3 mejoró debido a su interacción cercana dentro de las nanopartículas, derivando en catalizadores eficaces para la generación de alcanos ligeros. Para el caso de la reacción de desplazamiento de vapor de agua, Romero-Nuñez y colaboradores prepararon catalizadores de Ni soportados en nanobastones de CeO2 dopados, encontrando una clara mejora de la selectividad a medida que existe dopaje de Ni en los nanobastones de ceria. Además, la presencia de Ni modificó favorablemente la selectividad inhibiendo la reacción de metanación y mejorando la estabilidad de los catalizadores (Romero-Núñez et al., 2018). Otro ejemplo del uso del óxido de cerio es en la oxidación de CO donde se reportó que las nanovarillas presentan una mejor actividad a comparación de las nanopartículas debido a una mayor exposición de los planos (110) (Mai et al., 2005).
Asimismo, Trovarelli y colaboradores mostraron que particularmente para el óxido de cerio (CeO2) es importante el control de la forma y el tamaño, ya que esto induce diferencias significativas en sus propiedades catalíticas. El control de la superficie del CeO2 afecta directamente la reactividad de los iones Ce+4/Ce3+ si se modifica la cantidad de oxígeno disponible para ser captado-liberado (oxygen storage capacity (OSC)). Este efecto también puede impactar directamente las interacciones metal-soporte y con esto modificar la dispersión de las nanopartículas depositadas. Los autores mencionan que el OSC se incrementa con la siguiente tendencia nanohojas > nanocubos > nanobastones > nanopoliedros. (Trovarelli y Llorca, 2017). Wu y colaboradores reportaron la oxidación de CO con nanobastones, nanocubos y octaedros, encontrando que los nanobastones fueron los más activos, seguidos por los nanocubos y al final los octaedros (Wu et al., 2012). Esto coincide con lo reportado por Zhou y colaboradores, quienes mostraron que los nanobastones presentan una mayor actividad durante la oxidación de CO en comparación con otras formas de nanopartículas. Lo anterior se debe a una mayor exposición de los planos reactivos (001) y (110) en las nanovarillas (Zhou et al., 2005). López-Rodríguez y colaboradores mostraron recientemente qué catalizadores bimetálicos de Cu-Pt tenían variaciones en su conversión de metanol al ser depositados en óxidos de cerio con diferentes morfologías nanométricas. Las nanopartículas impregnadas con 5% de Pt incrementaron su conversión a partir de 200 ºC. Asimismo, los nanopoliedros y los nanobastones a 250 ºC obtuvieron cerca del 45% de conversión, mientras que sobre los nanocubos solo se obtuvo cerca del 17%. Cuando se les impregnó % de Cu y 1% de Pt los nanopoliedros obtuvieron la mayor conversión a 250 ºC seguidos de los nanobastones y con la menor conversión los nanocubos (López-Rodríguez et al., 2022).
Adicionalmente, se ha reportado el uso de nanoestructuras de óxidos binarios como el bismuto de tungsteno, en reacciones fotocatalíticas. En el trabajo realizado por Zhang y colaboradores, se muestra la formación de estructuras de tipo flor conformadas por sub-bloques de nanoláminas de Bi2WO6 con actividad fotocatalítica superior a la del TiO2. Como explicación a este aumento de actividad, se atribuyó la facilidad de transporte a la estructura jerárquica presente en el material (Zhang et al., 2007).
Los óxidos de metales preciosos, como el RuO2 y IrO2, son utilizados en reacciones electrocatalíticas como la electrólisis de agua. Ambos sistemas cristalizan en la estructura del rutilo, y estudios se enfocan generalmente en la superficie (110), la cual es la más estable y expuesta de estos materiales. Sin embargo, algunos trabajos señalan sensibilidad estructural durante la reacción de evolución del oxígeno (OER), donde se espera una mayor actividad si la superficie expuesta corresponde a los planos (100) (Over, 2021), esto se atribuye a una mayor exposición de átomos coordinativamente insaturados de Ru e Ir sobre esta familia de planos.
Los métodos de síntesis pueden permitir el control de la forma de las partículas, como en el trabajo de Hankova y colaboradores, donde se presenta una metodología de deposición de nanopartículas de vanadio por un método físico utilizando un sistema compuesto de un magnetrón y una fuente de gas de agregación. En el trabajo se muestran las condiciones necesarias para llegar a obtener películas compuestas de nanopartículas o nanoesferas, dependiendo de la atmósfera y corriente utilizada (Hanková et al., 2022).
Nanopartículas de metales
A pesar de que la mayoría de los catalizadores en la industria tienen como componente principal un soporte inerte, como lo es en principio la alúmina. Antes de continuar cabe mencionar que, para ciertas reacciones, la alumina no es inerte y que incluso en catalizadores de hidroprocesamiento puede formar espinelas superficiales debido a la migración de las especies superficiales de Ni o Co, y, dependiendo de su acidez, llevar a cabo deshidrataciones o deshidrogenaciones (Laurenti et al., 2013; Phung et al., 2015; Busca, 2014). Debido a esto, diversos estudios se han enfocado en determinar las características, exclusivamente, de nanopartículas o nanoclústers metálicos que fungen como fases activas sin involucrar el efecto de su interacción con el óxido acarreador (Flytzani-Stephanopoulos, 2014). Lo anterior ha permiti do determinar y relacionar la actividad catalítica de estas nanoestructuras metálicas con su forma, tamaño y orientación, similar a lo comentado en secciones anteriores.
Comenzando por el platino, uno de los metales preciosos utilizados como fase activa en reacciones de electrocatálisis e hidrogenación. En el trabajo de Bratlie y colaboradores, se estudia la hidrogenación del benceno utilizando nanopartículas de Pt de forma cúbica y cuboctaédrica (Bratlie et al., 2007). Los resultados muestran un cambio evidente en la selectividad debido a una mayor exposición de los planos (111) en la superficie de los cuboctaedros, donde se promueve la producción de ciclohexano a diferencia de las estructuras cúbicas donde no existe la presencia de estos planos. El níquel también es un buen catalizador en reacciones de hidrogenación, y, al igual que el Pt, muestra una diferencia en la actividad catalítica durante la hidrogenación de glucosa. En el estudio de Fu y colaboradores, se sintetizan nanopartículas de forma esférica, varillas y cadenas de Ni, y se encuentra una mayor actividad para las partículas esféricas (Y. Fu et al., 2022). Referente a reacciones electrocatalíticas, se ha encontrado por estudios teóricos y experimentales que el Pt presenta sensibilidad en la forma de las nanopartículas durante la reducción de oxígeno, donde es necesario un efecto sinérgico entre las caras (100) y (111), donde la primera adsorbe fácilmente oxígeno, pero la reducción es ineficaz, en caso contrario, la cara (111) presenta una mejor reducción, pero una menor facilidad de adsorción de oxígeno. Por lo cual, además de presentar este efecto geométrico, la presencia de un menor tamaño de partícula promocionaría la proximidad entre las diferentes especies en la superficie (Komanicky et al., 2009).
Por otra parte, la Ag se utiliza como catalizador de oxidación de olefinas para la producción de productos como epóxidos o aldehídos en la industria; en el estudio de Xu y colaboradores se muestra la síntesis de nanocubos de Ag, estos exponen uno de los planos menos estables de este metal, el (100). Se encuentra que la actividad en la oxidación de estireno es hasta 4 veces mayor que al utilizar partículas cuasiesféricas (Xu et al., 2006).
De la misma forma, existen numerosos estudios de catalizadores de nanopartículas de Au soportados en CeO2 (Fu, Weber y Flytzani, 2001; Flytzani, 2014) en donde se pone de manifiesto que las nanoparticulas de Au coexisten con las de Ceria formando compositos. Fu y colaboradores encontraron que la adición de oro incrementa significativamente la reducibilidad de la nanoceria y que esta se correlaciona casi de manera lineal con la actividad catalitica (Q. Fu, Weber y Flytzani, 2001).
Asimismo, existen trabajos donde se muestra la síntesis de nanopartículas bimetálicas; Wang y colaboradores presentan un método para la síntesis de nanocápsulas de Pd-Au, los materiales presentaron familias de planos {730} y {221}. Estas caras fueron superiores en actividad catalítica para las reacciones de acoplamiento cruzado que las encontradas para nanocubos de Pd-Au (F. Wang et al., 2011). Los autores mencionan que este incremento de actividad se debe a que en estas caras se presentan múltiples defectos en forma de escalones salientes y pliegues.
Los trabajos presentados en esta sección muestran que la preparación de una nanopartícula metálica para su función como catalizador es muy versátil, y una simple variación en la metodología puede impactar en la actividad general del catalizador preparado debido a los efectos relacionados con la reactividad dependiente de su estructura y morfología (Figura 5).

Fuente: Elaboración de los autores.
Figura 5 Esquemas con relación de la estructura y reactividad catalítica de algunos trabajos mencionados: a) oxidación de CO sobre nanovarillas de CeO2; b) selectividad atribuida a la estructura de nanoestructuras de Pt durante la hidrogenación de benceno; c) reactividad en distintos planos durante la OER de RhO2 y IrO2, y, d) conversión de estireno en distintas nanoestructuras de Ag.
Perspectivas
Dado que la síntesis de nanomateriales ha probado ser un área efervescente en constante crecimiento y descubrimiento, el uso de nuevas técnicas para su obtención, más allá del tradicional método sol-gel o el hidrotermal, ha resultado ser una de las mejores opciones para controlar las propiedades de los materiales a escala nanométrica. Otras técnicas menos usadas también han dado buenos resultados al sintetizar nanopartículas, por ejemplo Son y colaboradores prepararon nanoesferas de Ag usando síntesis coloidal asistida por polivinilpirrolidona (Song et al., 2014). Patiño-Guillen y colaboradores reportaron la formación de nanoesferas de carbón por medio de la pirolisis de mezclas de tolueno-etanol (Patiño-Guillén et al., 2021). Afanasiev reportó la síntesis de nanoesferas huecas de MoS2 por medio de un proceso de metátesis seguido de sulfuración in situ (Afanasiev, 2018). Mientras que Safo y colabo radores reportaron la síntesis de nanocubos de Pt por medio del método de polioles usando etilenglicol (Safo et al., 2019).
Una de las técnicas que está cobrando relevancia es la síntesis de nanopartículas por medio de láseres pulsados. Esta presume ser la solución para un control preciso de la concentración, tamaño, cristalinidad, fases activas, defectos y, según Forzythe y colaboradores, de las propiedades electrónicas, ópticas, térmicas, mecánicas y catalíticas de los materiales obtenidos (Forsythe et al., 2021). Desde nuestro punto de vista, la mayor ventaja de esta técnica es que no se necesitan procesos largos de síntesis, reactivos costosos o el uso de surfactantes. Este método consiste en poner un objetivo metálico o un precursor soluble inmerso en un medio líquido y hacerle incidir un láser con propiedades específicas. Al momento en que el láser incide sobre la muestra se genera un plasma que está confinado por el líquido y que al mismo tiempo lo enfría. A través de este líquido es posible controlar las propiedades del nanomaterial resultante. Este proceso permite modificar la concentración de la solución manteniendo el tamaño de partícula, lo cual es especialmente interesante en el campo de la catálisis. No obstante, esta técnica no es del todo sencilla y su complejidad reside en controlar la longitud de onda del láser, la longitud del pulso, fluencia, potencia energética, velocidad de repetición y secuencia de los pulsos (Figura 6).

Fuente: Elaboración de los autores.
Figura 6 Representación esquemática de la obtención de nanopartículas a partir de un láser pulsado de nanosegundos.
Varios autores reportan que controlar los parámetros del láser permite un control preciso del tamaño de las nanopartículas, en especial la fluencia (Forsythe et al., 2021; Amendola y Meneghetti, 2013). Amendola y colaboradores reportaron que fluencias bajas producen tamaños de partícula pequeños, mientras que al aumentar la fluencia incrementa el tamaño de partícula obtenido (Amendola y Meneghetti, 2013). Los materiales sintetizados por múltiples autores han sido usados en electrocatálisis, fotocatálisis, fotoelectrocatálisis, oxidaciones selectivas, reducciones y en deshidrogenaciones (Forsythe et al., 2021). No obstante, nuevas aplicaciones son reportadas cada día, por ejemplo, en la fotoxidación de sulfametoxazol con materiales de anatasa-rutilo sintetizados con un láser de estado sólido (Zhang et al., 2023).
Conclusiones
Como puede apreciarse en este artículo, la síntesis de nanomateriales presenta múltiples variables para tener en cuenta, como el uso de agentes, directores de estructura, temperatura, metodología y precursores utilizados. Aunque no existe un método de síntesis específico para obtener nanomateriales de alúmina con las características morfológicas deseadas, actualmente la síntesis asistida por surfactantes es la más empleada debido a su buen control de la morfología, forma y tamaño. Sin embargo, las técnicas sol-gel e hidrotermal son las usadas para la síntesis de nanopartículas de Al2O3 aplicadas en catálisis. Las nanopartículas con formas definidas como los nanobastones, nanoesferas o nanoflores han permitido encontrar propiedades mejoradas en los catalizadores preparados con respecto a los materiales sin morfología definida. Para el caso de la Titania se han obtenido diversas morfologías como nanoesferas, nanobastones, nanotubos, usando métodos de síntesis como el sol-gel, hidrotermal, solvotermal y depósito de vapor químico. Estos nanomateriales, al igual que con la alúmina, se han usado como soportes y catalizadores. Estas nanopartículas han permitido encontrar un mayor número de sitios activos, al presentar más pliegues, defectos, escalones y bordes curveados que los materiales de bulto. Otros óxidos y nanopartículas aplicadas en catálisis han demostrado excelentes propiedades al tener morfología y tamaños nanométricas como el CeO2. En cuanto a perspectivas de métodos de síntesis sobresale la síntesis por medio de láseres pulsados, y se ofrece como una de las alternativas más atractivas de entre las técnicas nuevas reportadas, pues no hace empleo de agentes directores de estructura ni tiempos prolongados de síntesis.











 nueva página del texto (beta)
nueva página del texto (beta)


