I. Introducción
La energía como fuerza impulsora de la sociedad actual tiene en su forma de combustibles un punto especialmente incuestionable. Se sabe que gran parte de la energía, así como otros productos industriales, proviene de recursos fósiles como el petróleo, el gas natural y el carbón. La agricultura, por ejemplo, depende del trabajo mecánico, de la irrigación, pesticidas y fertilizantes. Estos últimos, a su vez, requieren para su obtención de recursos no renovables. Los recursos fósiles no renovables (petróleo, carbón y gas natural) representan actualmente hasta 81.4% del consumo total de las energías primarias (IEA, 2017).
La disponibilidad de los combustibles fósiles está descendiendo de manera acelerada en los últimos tiempos. Por lo anterior, se han presentado tres situaciones que han llevado a la humanidad a buscar alternativas a la energía de origen fósil: la disminución de las reservas de crudo convencional, el aumento en la demanda de energéticos y la preocupación por el medio ambiente.
En la actualidad se estima que el total de las reservas 2P (probables + probadas) mundiales es de alrededor de 1800-2200 (x109) barriles; pero existe cada vez un mayor temor respecto al agotamiento del crudo. La idea se deriva de las siguientes circunstancias: el crudo de mejor calidad y fácil de extraer (menos costoso) fue el primero en extraerse y consumirse (Ferrari, 2013). De lo cual deducimos que el crudo remanente es más difícil de extraer, por ejemplo, del tipo de arenas bituminosas o tipo shale. Además, el descubrimiento de nuevas reservas es cada vez más difícil. Asimismo, los nuevos pozos petroleros se hallan en áreas remotas difíciles de alcanzar, como lo son las aguas profundas, zonas subárticas, por mencionar algunas. Todo esto se traduce en una elevación del costo del crudo.
Existe un aumento continuo en el consumo. Entre 1990 y 2000 el alza en la demanda fue del 14% anual; pero las necesidades de combustibles en el sudoeste asiático y especialmente China no estaban contempladas en los pronósticos de esa época.
Finalmente, pero no menos importante, la preocupación por el medio ambiente, tema que se discutirá en la siguiente sección.
Las razones anteriores son suficientes motivos para pensar que actualmente la producción de combustibles de origen fósil no es sustentable y se vislumbra el punto1 en el que no será económicamente viable. Como ejemplo, la extracción de crudo de Estados Unidos presentaba en 1930 un EROI (barriles de petróleo equivalente producidos con respecto al invertido) de 100:1, disminuyendo en los años setenta a 30:1; para el año 2007, estos valores se reportaron entre 18:1 y 12:1 (Ferrari, 2013). Esto refleja las dificultades técnicas para extraer los crudos de los pozos.
Ciclo del carbono
La causa antropogénica (debida a actividades humanas) principal de las emisiones de CO2 a la atmósfera es la quema de combustibles para obtener energía. Debe considerarse el aumento de la población a nivel mundial y también las mejoras en el estilo de vida y comodidades que disfrutan los humanos como causa adicional del aumento en el consumo de energía. El alza de las emisiones de CO2 a la atmósfera está a su vez relacionada con el calentamiento global (CG) y el cambio climático. El CG tiene también otras contribuciones por la liberación de fuentes antropogénicas de gases de efecto invernadero (además del CO2, fluoro-carbones en aerosoles, solventes, vapor de agua, metano, óxido nitroso, etc.) y por procesos naturales (por ejemplo, la erupción de volcanes). El mecanismo del CG puede explicarse de la siguiente manera: la radiación del sol, llega a la Tierra y se adsorbe. La Tierra emite radiación térmica que es reflejada al espacio; pero, los gases de efecto invernadero adsorben esta radiación y la emiten en todas las direcciones y esto incluye cierta cantidad hacia la atmósfera de la Tierra, ocasionando que la temperatura promedio aumente en el planeta. El incremento también causa el derretimiento del hielo polar y crecimiento del nivel del mar. Por lo cual se debe evitar el aumento continuo de la concentración de los gases de efecto invernadero en la atmosfera. El reto se ha vuelto urgente en los últimos años (Mabee et al., 2005).
El sector transporte está identificado como el que presenta un mayor consumo del petróleo y el responsable de emitir la quinta parte de las emisiones globales de dióxido de carbono. Dadas las condiciones económicas actuales, el transporte de personas y mercancías es necesario. La perspectiva para la disminución de las emisiones vehiculares no es favorable, por el contrario, se estima que el número de automotores alcanzará más de 2 mil millones de vehículos para el 2050 (Rawat et al., 2013). Recuérdese que al mismo tiempo las reservas de crudo disminuyen y, ante esto, aumentar la eficiencia de los motores es solo un paliativo a corto plazo. Así las cosas, una solución recomendable es la producción de biocombustibles que ayudaría a reducir, y si es posible, evitar, nuestra dependencia con los combustibles fósiles. Se están investigando fuentes alternas para la producción de combustibles a fin de contrarrestar la generación de gases de efecto invernadero.
Consideraremos la definición básica de biocombustible como líquidos o gases cuya combustión genera energía. El sufijo bio se usa porque el combustible se obtiene a partir de fuentes biológicas como la biomasa. A su vez, se considera como biomasa toda materia de origen biológico; y se destaca la vegetal con lo que se involucra la fotosíntesis. La biomasa es, por lo tanto, renovable, sostenible, biodegradable, con un balance neutro en el ciclo de carbono y con la suma de todo lo anterior es respetuosa con el medio ambiente.
Explicaremos con más detalle el balance neutro en el ciclo de carbono, esto es básico para entender cómo van a ayudar los biocombustibles a reducir las emisiones de CO2. Analicemos para ello la Figura 1 donde se presenta el ciclo del carbono aplicado a la producción de biodiésel. Es conveniente aclarar que esquemas similares se aplicarían a cualquier biocombustible. El primer paso es la generación de biomasa; la fotosíntesis transforma la energía solar y CO2 en biomasa que contiene energía química. Esta energía está almacenada como lípidos, carbohidratos y proteínas. Si hablamos de la producción de biodiésel se incluye la extracción del aceite. El aceite se transforma a biodiésel con el proceso químico adecuado y en la combustión del biodiésel se genera CO2. De aquí cerramos el ciclo del carbono, ya que se emitirá el mismo dióxido de carbono que contiene la biomasa y que fue inicialmente consumido en la fotosíntesis de las plantas. El balance de carbono es neutro. En cambio, al usar combustibles fósiles liberamos CO2 que en el periodo de tiempo actual ya no se encontraba en la atmósfera.
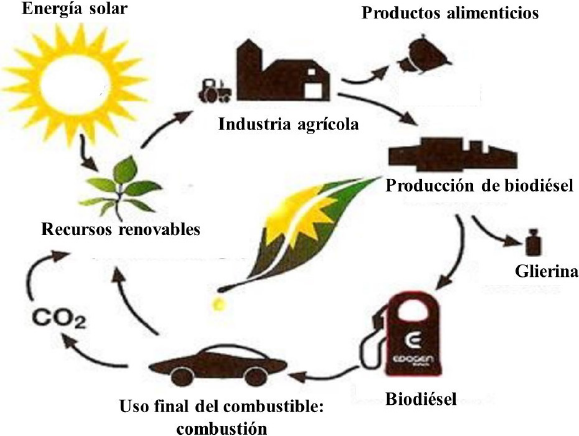
Fuente: Diagrama tomado de Primus (2015).
Figura 1 Ciclo del carbono del uso de biocombustibles, en específico biodiésel.
En cuanto al desarrollo de nuevos procesos para la producción de los biocombustibles se tienen dos componentes económicos importantes: los costos del proceso y los costos de la materia prima; como se verá líneas abajo, se están realizando grandes esfuerzos para reducir los costos de los procesos y hacerlos más eficientes. También se están buscando fuentes de materia prima más baratas.
Al reconocerse que la humanidad forma parte del ecosistema Tierra, en los últimos años ha aumentado su preocupación por el medio ambiente y esto ha puesto en el candelero el calentamiento global. En este último tema, los datos son alarmantes y nos indican que se deben tomar acciones para al menos evitar daños mayores y, en el mejor panorama, revertir los cambios causados por el uso excesivo e ineficiente de los combustibles. Así, la humanidad se enfrentará al dilema del negocio versus necesidad. Por el momento, producir los biocombustibles se considera caro y el punto de quiebre económico se encontrará cuando el costo del barril de petróleo alcance, aproximadamente 100 dólares.2 Hasta ese momento los biocombustibles se producirán con ayudas gubernamentales e incentivos fiscales.
Distintas generaciones de biocombustibles
Tomando una perspectiva histórica, la humanidad ha obtenido energía calorífica a partir de madera y carbón, entonces, los primeros combustibles fueron biocombustibles. La situación cambió con la revolución industrial y las necesidades de energía intensiva y trasporte se decantaron por combustibles de origen fósil, hablamos del etanol, queroseno y gasolina. En 1882, Rudolph Diesel recibió la patente por la creación de su máquina de combustión interna; curiosamente, dicho motor estaba proyectado para usar aceite vegetal. Es preciso mencionar que en 2008 la energía de biomasa fue la mayor fuente de energía renovable y representó el 10.4% del suministro total de energía primaria del mundo o el 77.4% del suministro mundial de energía renovable (Carlos y Ba Khang, 2008).
Para los biocombustibles una de las clasificaciones, y quizá la más utilizada, se apoya en ciertas consideraciones éticas. El primer biocombustible producido a escala industrial fue el etanol, generado principalmente con el proceso de fermentación. Después se descubrió que las grasas vegetales o animales pueden transesterificarse con relativa facilidad para obtener esteres de ácidos grasos (FAAE: fatty acid alkil esters), mismos que tienen propiedades físicoquímicas adecuadas para usarse como sustitutos del diésel. La industria de la extracción de aceites está plenamente establecida; así que se conocen los procedimientos para la obtención de aceites a partir de semillas oleaginosas. De ahí, la implementación de la producción de biodiésel a partir de excedentes locales de aceites se realizó fácilmente. Con estos procesos y por ser de los primeros en producirse el bioetanol y el biodiésel representan la primera generación de los biocombustibles. Sin embargo, esta manera de utilizar las grasas vegetales en la producción de biocombustibles causó una cierta incomodidad especialmente entre la comunidad científica. Rápidamente, surgió el debate sobre si es responsable este proceder, cuando existen diferentes comunidades humanas que padecen hambre. En el año 2005, el 30% de los aceites comestibles que se producían se destinaba a la producción de biodiésel. En especial destacaban los casos del aceite de soya (EUA) y aceite de palma (Tailandia). La alta demanda del biodiésel causó un rápido aumento de los precios de venta de los aceites. Estas acciones generaron la desviación de recursos alimentarios. Asociado a esto surgió la posibilidad e inconveniente de que tierra y agua fueran utilizados para estos cultivos y este problema sería más grave en países en desarrollo.
Considerando que la transesterificación solo requiere como alimentación moléculas orgánicas que correspondan a la descripción química de ácido graso, entonces pueden utilizarse diferentes insumos. Se pensó en el uso de semillas ricas en grasas no comestibles como la fuente para la producción del biodiésel. Esto llevo a los biocombustibles de segunda generación. Como ejemplo de las semillas no comestibles utilizadas en la producción de biodiésel se tienen: Jatropha curcas, Simmondsia chinensis (Jojoba), Pongammina pinnata (karanca), semilla de Nicotiana tabacum (tabaco), Recinus communis (ricino), entre otras. Otra opción investigada para la producción de biodiésel es el aceite de cocina usado, que tiene un costo menor que el aceite vegetal fresco. La producción de biodiésel de segunda generación es comparable a la basada en aceites comestibles en términos de rendimiento y calidad. Algunas ventajas que presenta el biodiésel de segunda generación respecto a la primera son (Atabani et al., 2013):
Los aceites utilizados como alimentación al proceso no compiten con los recursos agrícolas existentes; así, eliminan la competencia con las fuentes de alimentos y piensos. Esto es porque estos aceites no son adecuados como alimentos debido a la presencia de algunos componentes tóxicos.
La producción de aceite no comestible para biodiésel de segunda se considera más eficiente comparada con los aceites comestible porque:
b1. El cultivo de semillas oleaginosas para la producción de aceites no comestibles requiere menos tierras de cultivo y se puede utilizar como una mezcla de cultivos.
b2. La mayoría de los cultivos para aceites no comestibles son altamente resistentes a plagas y enfermedades.
b3. La adaptabilidad de las plantas para aceite no comestible a tierras marginales y zonas no agrícolas con baja fertilidad. Los cultivos de semillas para aceites no comestibles se pueden realizar en tierras pobres y gastadas o contaminadas que no son adecuadas para cultivos alimentarios. Además, existen especies con baja demanda de humedad. E, incluso, se pueden propagar a través de semillas o esquejes.
b4. El cultivo de plantas para aceites no comestibles tiene un enorme potencial para restaurar tierras degradadas, generar empleo rural y fijación de hasta 10 t/ha/año de CO2.
Además, la materia prima no comestible puede producir subproductos útiles durante el proceso de conversión, que pueden utilizarse en otros procesos químicos o quemarse para la generación de calor y energía. Por ejemplo, las tortas de semillas después de la extracción del aceite se pueden utilizar como fertilizantes para el enriquecimiento del suelo.
El analisis de la estructura de los ácidos grasos, conocimientos fundamentales de catálisis y el relativo éxito del biodiésel como sustituto del petrodiésel llevó a la idea de que se puede procesar el aceite para obtener compuestos con propiedades análogas al diésel de origen fósil. Con esta idea surgió la producción de diésel verde o diésel renovable. Es posible producir diésel verde con las mismas alimentaciones utilizadas para producir biodiésel.
Sin embargo, los análisis actuales muestran que la producción de biocombustibles no es económica en costos e inversión energética si se compara a uno de origen fósil, situación que no es sorprendente porque la industria de la refinación lleva bastantes más años plenamente establecida. Así, para el uso pleno y aceptación de biocombustibles se han detectado ciertas barreras técnicas que deben superarse antes de su éxito económico. También se vislumbra la posibilidad de que la producción de biodiésel no sea suficiente para cumplir la demanda en combustibles que existe hoy en día. Además, aunque se utilicen semillas no comestibles todavía existe la preocupación sobre el uso de suelo que podría destinarse al cultivo de vegetales comestibles o incluso problemas ecológicos por la utilización de toda la superficie arable, o más aún, por la disminución de las áreas forestales. De este modo, se empezaron a cultivar las microalgas, dando lugar a la tercera generación de biocombustibles. Las microalgas con un alto contenido de aceites tienen el potencial de producir un rendimiento de aceite de hasta 25 veces el de un cultivo tradicional, por ejemplo, el aceite de oliva. También tienen un mayor rendimiento de biomasa por m2, y pueden crecer en diferentes tipos de agua: residual, salada, fresca, entre otras.
Investigaciones para la producción de biocombustibles
Por todas las razones anteriores la comunidad científica está realizando investigaciones buscando la mejor manera de producir biocombustibles. Como ya se mencionó, Diesel creó su motor originalmente para trabajar con aceite vegetal. Quizá suene atemporal, pero a inicios del siglo pasado ya existía una porción de vehículos que podían trabajar con etanol, G. Eglof presenta el siguiente comentario:
Total consumption of power alcohol in Europe in 1937 amounted to 510,000 tons compared with 646,000 tons during 1936. The 510,000 tons of ethanol (some methanol) represented 4.3 per cent of the total 11,882,600 metric tons of motor fuel consumed during 1937 in Europe. It is estimated that the 510,000 tons of alcohol used in Europe cost the consumer and state in additional expenditures on the order of about $100,000,000 in subsidies, tax losses, and higher operating costs of vehicles. (Eglof, 1938).
Conviene aclarar que Eglof trabajaba para una industria petrolera, de tal forma que no sorprenden sus palabras negativas sobre el etanol. En el párrafo, incluso se muestra que el consumo de etanol como combustible estaba disminuyendo.
Nuestro estudio sobre el aporte de la ciencia de la catálisis a la producción de biocombustibles se ilustra en la Figura 2, donde se muestra el número de artículos publicados en el tema de biocombustibles utilizando la base de datos Scopus. Se emplearon las palabras clave indicadas y su incidencia únicamente en el título y resumen de los artículos. Dentro del tema de combustibles que pueden obtenerse con la biomasa, el alcohol es un caso especial. La humanidad lo ha producido desde la prehistoria y actualmente su uso principal no es como combustible. Una búsqueda de solo etanol arrojaría demasiados aciertos. Por eso se optó por presentar los resultados de etanol y combustible. Finalmente, del universo de datos de biocombustibles se extrajeron aquellos que incluyen biocombustibles y catálisis.
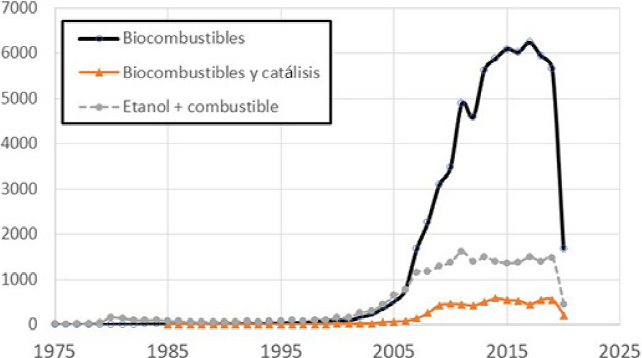
Fuente: Investigación propia utilizando la base de datos Scopus™ Elsevier.
Figura 2 Artículos publicados con las palabras clave o las palabras biocombustibles, etanol + combustible y, biocombustibles y catálisis entre los años 1972 e inicios de 2020.
Para el tema de biocombustibles, la primera mención de la palabra como tal se remonta a 1972. En años posteriores existió un ligero aumento en el número de publicaciones: en 1981 se publicaron un promedio de diez artículos anuales; en el año 2000 se alcanzaron 100 trabajos, y en 2007 un gran salto hasta 1,700 artículos anuales. A partir de ese año se muestra un aumento acelerado en las publicaciones consiguiéndose más de 6,000 artículos anuales en el tema. En 2015 se detiene el incremento en el número de artículos publicados; curiosamente, coincide con el arranque de la producción de crudo shale. Este punto ilustra claramente el efecto de la economía sobre la investigación. Al existir una fuente de energía barata cambian los apoyos gubernamentales y se olvidan las cuestiones ambientales, interés opuesto al de la sociedad en general. Esto indica que, en la situación actual, los temas económicos son más preponderantes que los temas de bienestar.
El caso especial del etanol ya se había mencionado. La manera industrial más común para la producción de etanol es la fermentación de azúcares simples. En esta revisión no hablaremos de este proceso, pero, por la magnitud de la demanda se requiere una fuente cuantiosa para producir combustibles. Requisito que cumplen los materiales lignocelulósicos de desecho en la agricultura y la industria maderera. Así, se abre una ventana de oportunidad para estudiar la producción de bioetanol a partir de materiales lignocelulósicos. En la Figura 3, se usaron como palabras clave etanol + catálisis. El tema presenta casi una tercera parte en la publicación total de artículos. En ese grupo se incluyen la obtención de etanol a partir de materiales lignocelulósicos, pero también el uso de bioetanol para producir otros combustibles. Este último tema tampoco se va a cubrir en este trabajo.
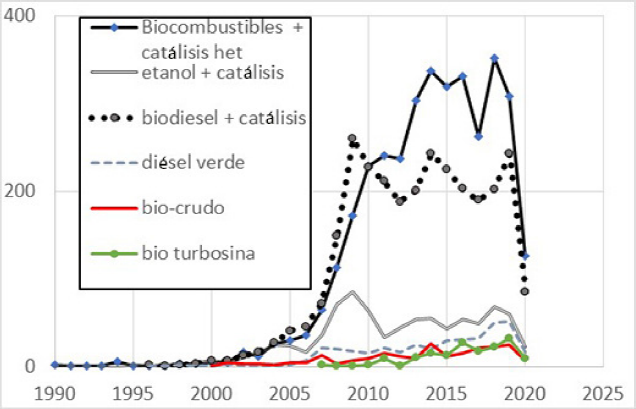
Fuente: Investigacion propia utilizando la base de datos Scopus™ Elsevier.
Figura 3 Artículos publicados con las palabras clave: biocombustibles y catálisis heterogénea, etanol y catálisis heterogénea, biodiésel y catálisis heterogénea, diésel verde y bio-crudo en el título o resumen entre los años 1990 e inicios de 2020.
Finalmente, se presentan los resultados de la búsqueda con las palabras biocombustible y catálisis heterogénea. En este tema se publicaron casi 4,000 artículos entre 1990 y 2020.3 El número de artículos por tema se presenta en la Figura 3. Inicialmente, casi cada artículo en biocombustibles y catálisis era en biodiésel, situación que se prolonga casi hasta el 2000. El estudio de producción de etanol a partir de materiales lignocelulósicos empieza a ser importante desde ese año, aunque arranca desde varios años antes. El biocrudo y la producción de diésel verde ya son notorias en 2005 y un caso similar se presenta para la bioturbosina, pero en 2010.
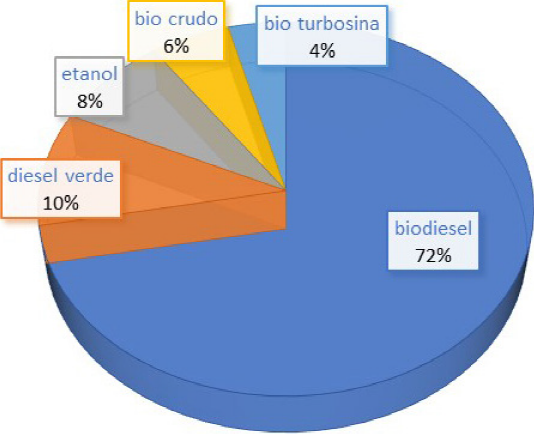
Con las diferentes contribuciones se presenta la Figura 4, donde se reporta la contribución en artículos publicados por tema de investigación al número de artículos totales. Es curioso que el porcentaje de publicaciones casi se presenta en el mismo orden de los años iniciales de publicación de cada tema.
Fuente: Investigacion propia utilizando la base de datos Scopus™ Elsevier.
Figura 4 Distribución en artículos publicados por tema de investigación en biocombustibles.
Este análisis estadístico nos ayuda a dilucidar el papel de la catálisis en la producción de biocombustibles, situación que se abordará con más detalle en cada una de las secciones siguientes de este trabajo. El caso inicial es el del etanol, gran parte de la producción industrial de este compuesto se realiza a partir de biomasa. Aquí la catálisis participa en la posibilidad de utilizar una alimentación totalmente distinta de la tradicional y ayuda a generar procesos nuevos, este caso se estudia en la sección II. En la sección III, se estudia el caso del biodiésel, aquí el proceso de producción con catalizadores homogéneos está plenamente establecido a nivel industrial y el papel de la catálisis es la mejora del proceso que se obtiene al usar un catalizador heterogéneo. En la parte IV se presentará el caso del diésel verde, no puede producirse diésel verde sin presencia de un catalizador. En la sección V se hablará de la bioturbosina, donde también es absolutamente necesaria la presencia de un catalizador. Finalmente, en la sección VI se describe el biocrudo y las aplicaciones que ha tenido hasta el momento. El biocrudo no es un combustible propiamente dicho, pero no puede negarse que de él se pueden producir combustibles.
II. Generación de bioetanol por procesos catalíticos
Producción de bioetanol
Una manera de utilizar el etanol es como un suplemento para combustible en mezclas con gasolina. La mayoría del bioetanol se obtiene con la fermentación de azúcares. El proceso se aplicó desde los años 70’s (Rubio-Arroyo et al., 2011). Esta fermentación se realiza mediante microrganismos. Se tiene registrado que en 2016 la producción mundial de bioetanol fue de 100.2 billones de litros, y su producción anual ha aumentado desde entonces, con una predicción de su consumo a 134.5 billones de litros para el 2024, siendo Brasil el mayor productor, seguido de EUA, la Unión Europea y China (Busic et al., 2018).
Existen diferentes materias primas para la producción de bioetanol (Figura 5), las fuentes son tan variadas como las cosechas productoras de azúcar, almidón o féculas; desde el azúcar de caña, remolacha, hasta material lignocelulósico proveniente de residuos agrícolas. Por el momento, el maíz y la caña de azúcar han sido las materias primas usuales en la tecnología de fermentación porque la producción y la obtención de azúcares ya está plenamente establecida y, por tanto, probada en comparación de otros procesos. En la producción de bioetanol el precio de la materia prima representa entre el 40-75% del costo total. Se estima que en Brasil el costo del bioetanol es de 0.20-0.30 USD/L empleando caña de azúcar, mientras que EU y la Unión Europea, es de 0.30-0.53 USD/L, empleando remolacha (Busic et al., 2018).
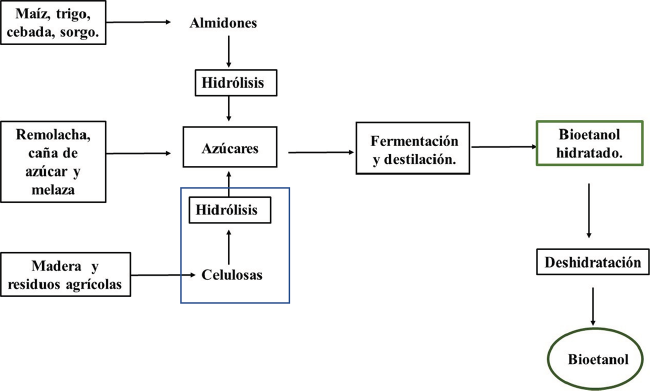
Fuente: Diagrama tomado de la página web www.renovetec.com
Figura 5 Proceso convencional de la producción de bioetanol a partir de diferentes materias primas.
Producción de bioetanol a partir de materiales lignocelulósicos
Por otro lado, existe una proyección al futuro que es la posibilidad para producir bioetanol a partir del uso de los residuos forestales y agrícolas formados principalmente de lignocelulosa. Esta es rica en carbohidratos complejos. Es obvio que el uso de esta alimentación permitiría una reducción en el costo de producción de bioetanol porque esta tendría un costo prácticamente nulo y además con disponibilidad muy amplia; adicionalmente, este suministro no competiría con las fuentes alimenticias.
Los materiales lignocelulósicos se utilizan en la naturaleza con fines estructurales. Por lo cual son más complejos y resistentes que los azúcares. Por esto, en su procesamiento se requiere un pretratamiento mediante molienda e hidrólisis, esta última generalmente por acidificación con H2SO4 para convertir la celulosa a glucosa. Después, la pasta resultante es neutralizada con agua y álcali. Como última etapa, la glucosa es convertida a bioetanol (Raman et al., 2017) mediante organismos fermentadores como Saccharomyces cerevisiae, Schizosaccharomyces pombe o Zymomonas mobilis (Suresh et al., 2019). El reto es disminuir los costos del proceso y es aquí donde pueden participar los catalizadores heterogéneos como, por ejemplo, al sustituir el ácido, evitando así la necesidad de una etapa para la neutralización.
Catalizadores heterogéneos empleados para la producción de bioetanol a partir de lignocelulosa
El enlace principal de la estructura lignocelulósica son enlaces del tipo C-O. Entonces, al inicio, la investigación se enfocó en el rompimiento de esos enlaces. Se busca despolimerizar la lignina y romper la celulosa a monómeros fermentables (Crews et al., 2014). Algunos ejemplos de los tipos de catalizador heterogéneos empleados en la hidrólisis de material lignocelulósicos o carbohidratos para producción de bioetanol se presentan en la Tabla 1.
Tabla 1 Catalizadores heterogéneos empleados en la hidrólisis de biomasa para obtención de azúcares fermentables o etanol de manera directa.
| Catalizador | Material procesado | Bibliografía | |
|---|---|---|---|
|
Catalizadores ácidos |
Zeolitas; H-beta (Si/Al=12), H-beta (75), H-mordenita (10) y HZSM5 (45) | Celulosa y almidón a 423 °K (150 °C) | Onda et al. (2008) |
| Amberlyst-15™ | Carbohidratos de extracto de macroalga Eucheuma cottonii a 393 K (120 °C) | Tan et al. (2013) | |
| Carbón amorfo con HSO3- , ácido niobico, NR-50, Amberlist-15™ y Nafión | β-1,4-glucano, celulosa y celulosa cristalina a 373 °K (100 °C) | Suganuma et al. (2010) | |
| HNbMoO6 | Sacarosa, celulosa y almidón a 403 °K (130 °C). | Takagaki et al. (2008) | |
|
Catalizadores enzimáticos |
Enzimas: celluclast 1.5L, Novozyme 188 y Novozyme A/S | Bagazo de caña de azúcar pretratado con SO2 y conservado con ácido láctico a 313 K (40 °C) por 96 hr. | Monavari et al. (2011) |
|
Catalizadores metálicos |
Catalizador Pt y Co NPs (nanopartículas) | Cáscara de maní triturada a temperatura ambiente en metil ter-butil éter | Crews et al. (2014) |
| Pd/Fe3O4 | Material celulósico para obtener en un solo paso alcoholes de C2-C3, a 240 °C por 12 horas | Gumina et al. (2019) |
Fuente: Elaboración de los autores.
Una forma de conseguir la ruptura de enlaces es con sitios ácidos. El sitio ácido fragmenta la estructura cristalina de la celulosa permitiendo la transformación de dicha estructura a compuestos fermentables (Figura 6). Como se observa en la tabla anterior, los tres primeros casos presentados son catalizadores con cierta acidez. De las zeolitas la HZSM5 (HMFI) se reconoce como una zeolita con características ácidas. Los cambios en acidez en las zeolitas beta se consiguieron alterando la relación Si/Al. La resina de intercambio iónico Amberlyst-15™ es una resina con propiedades ácidas. ¿Qué se puede decir del ácido niobico? En el caso del carbón se aumentó la acidez adicionando grupos sulfato. El molibdato de niobio, HNbMoO6, también tiene propiedades ácidas. El nafión está formado por alquenos perfluorados en resina modificada con ácido sulfónico, es decir, tiene características ácidas.
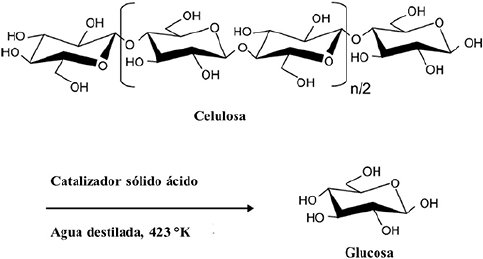
Fuente: Propuesta de reacción modificada del trabajo de Onda et al. (2008).
Figura 6 Conversión catalítica de celulosa a glucosa empleando catalizador ácido heterogéneo.
Es conocida la existencia en la naturaleza de enzimas capaces de metabolizar la celulosa. Actualmente se está investigando bastante sobre cómo soportar las enzimas, porque esto facilitaría grandemente la separación de la mezcla catalizador-productos de reacción. El segundo grupo de catalizadores es un ejemplo de estos esfuerzos, al ser enzimas soportadas.
Algunos metales en estado reducido también presentan actividad de ruptura de enlaces, entre ellos Pd, Pt, Ir y en menor grado Co y Ni. De tal forma, en la tercera clase de catalizadores mostrados en la Tabla 1, se incluye al catalizador de Pd/Fe3O2. También se han probado al Pt y Co con la adición de que en esa investigación se utilizó un método especial de preparación para obtener nanopartículas (NPs) de 5nm aumentando el área catalítica.
El segundo punto a considerar es el solvente. Por sus características ácido-base, se utiliza agua. La temperatura empleada para las pruebas de hidrólisis en presencia de catalizadores podría considerarse condición no severa. La razón para trabajar en condiciones no severas es como reporta Onda et al. (2008) evitar reacciones secundarias que causarían la degradación de la glucosa, que es el producto principal buscado.
Finalmente, se están probando rutas alternativas para la producción de alcoholes a partir de celulosa en una sola etapa, por caso, Gumina et al. (2019) aseguran haber logrado una selectividad del 51% de etanol a partir de celulosa. Esto significa la reducción del número de pasos del proceso y por consiguiente del costo total del mismo.
Resumiendo, las investigaciones en catálisis se centran en este momento en la utilización de los materiales lignocelulósicos, considerados de desecho, como alimentación, y en la posibilidad de crear un nuevo proceso que llevaría a la formación de alcoholes directamente a partir de celulosa. También se mencionó que es posible la fijación de las enzimas, lo que facilita la separación del catalizador, reduciendo los costos asociados con el proceso.
III. Biodiésel
El nombre diésel es un término genérico, y se refiere a cualquier combustible para un motor de encendido por compresión. Así, el término describe los combustibles fabricados comercialmente para los vehículos propulsados por el motor diésel. En la actualidad, el biodiésel es considerado como uno de los recursos alternativos promisorios para utilizar en los motores diésel. El biodiésel es renovable, biodegradable, amigable con el medio ambiente y no tóxico.
El biodiésel se puede obtener a partir de aceites vegetales o grasas animales, al consistir en los ésteres de los ácidos grasos que, a su vez, constituyen a los triglicéridos en aceites o grasas. En química a los componentes del biodiésel se les conoce como FAAE (faty acid alkil esters). Generalmente, se utiliza el metanol para la transesterificación y, entonces, los ésteres más relacionados con el biodiésel son los FAMEs (fatty acid methyl esters), también se produce glicerol, este último se vende como subproducto.
La industria de extracción de aceites está plenamente establecida, y así, la alimentación a procesos para la producción de biodiésel puede obtenerse con una relativa facilidad y a un costo relativamente bajo. Por otro lado, el biodiésel es un biocombustible que ya se obtiene industrialmente. En la Tabla 2, se presentan los constituyentes principales del diésel y el biodiésel y también sus propiedades químicas (Bacha et al., 2007).
Tabla 2 Comparación en las propiedades químicas entre el diésel fósil y el biodiésel.
| Propiedad | Unidades | Diésel | Biodiésel |
|---|---|---|---|
| Contenido de carbón | % | ~87 | ~77 |
| Contenido de hidrógeno | % | ~13 | ~12 |
| Contenido de oxígeno | % | - | ~11 |
| Azufre | ppm | 30-500 | - |
| Tipos de moléculas | Principalmente saturados, también naftenos, aromáticos, olefinas | Principalmente esteres >96.5, metanol o etanol, ácidos grasos | |
| Número de carbonos | 14-22 | 14-25 | |
|
Punto de
ebullición normal (TBP, true boiling point) |
°C | 180-260 | 250-450 |
|
Calor de
combustión (HHV, high heating value) |
KJ | 42 | ~37 |
Fuente: Elaboración de los autores.
Con la similitud de las características enumeradas en la tabla anterior, se ha aceptado ampliamente al biodiésel como un combustible de alta calidad para motores de encendido por compresión, es decir, motores diésel (Dunkan, 2003). El biodiésel también presenta un número de cetano alto, buenas propiedades de lubricidad, bajo contenido de poliaromáticos y se piensa que por su contenido de oxigenados se quema mejor. Pero, debe considerarse que el biodiésel tiene un menor contenido energético que el diésel convencional, presenta problemas de viscosidad a bajas temperaturas y si no se realiza una neutralización (del catalizador homogéneo) adecuada, causa problemas de corrosión. Dado que el biodiésel es un sustituto del diésel y ya se está comercializando y/o se planea su aplicación extensiva, existen reglamentaciones que el combustible debe cumplir y se presentan en la Tabla 3, basada en gran parte en el reporte de Ganduglia et al. (2009).
Tabla 3 Propiedades más importantes y su método de determinación que deben cumplir tanto el diésel como el biodiésel.
| Propiedad | Unidades | Descripción | Diésel | Biodiésel | ||
|---|---|---|---|---|---|---|
| Límites | Método de prueba |
Límites | Método de prueba |
|||
| Número cetano | Medida de la calidad de ignición. | 46 | ASTM D4737 | >47 | ASTM D816 | |
| Densidad | Kg/m3 | Medida de la energía por unidad de masa. | 820 | ASTM D1298 | 860 | ASTM D1298 |
| Viscosidad cinemática (40 °C) |
Mm2/s | Resistencia al flujo, la alta viscosidad crea hollín porque el combustible no se atomiza lo suficiente. | 2.0-4.5 | ASTM D445 | 1.9-6.0 | ASTM D445 |
| Flash point | °C | Temperatura a la cual se enciende el combustible si se expone a una flama o chispa. | 60-80 | ASTM D985 | >130 | ASTM D985 |
|
Cloud
point Punto de niebla |
°C | Temperatura a la cual los primeros cristales de parafinas aparecen. | -15-5 | ASTM D975 | -3 a -12 | ASTM D975 |
| Pour point | °C | La temperatura a la cual cierta cantidad de cera formada alcanza al combustible. | -35 a -15 | ASTM D975 | -15 a -16 | ASTM D975 |
|
Acid
number Número de acidez |
mg OH/g | Cantidad de ácidos carboxílicos presentes en el biodiésel. Indica el nivel de degradación del combustible. | - | - | 0.5 max. | ASTM D664 |
| Número de iodo | g I2/100 g | Índice de los enlaces insaturados en el combustible, tiene que ver con la estabilidad a la oxidación del combustible. | 120 | EN 14111 | ||
| Lubricidad | mm | Lubricidad es la habilidad de reducir la fricción entre superficies sólidas en movimiento relativo. | 0.460 | IP 450 | 520 | ASTM 6079 |
| Contenido de ésteres |
Medida de la pureza del biodiésel, disminución en el contenido de alcoholes, ácidos grasos etc. | - | - | 96.8 | EN 14103 | |
| Contenido de metanol |
masa/masa, % |
0.20.8 | EN 14110 | |||
| Contenido monogliceridos |
masa/masa, % |
EN 14105 | ||||
Fuente: Elaboración de los autores.
Usualmente el biodiésel se utiliza como una mezcla con el diésel convencional, se acostumbra presentar estas mezclas con la sigla B seguida del % en el contenido de biodiésel. Así el biodiésel puro sería B100, B30 es la mezcla con 30% de biodiésel. La mezcla más utilizada es la B5, que esta especificada en la norma europea EN 590 y la de América del Norte ASTM D6751.
Producción de biodiesel
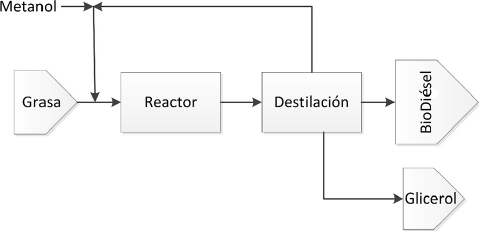
El proceso de transesterificación se puede llevar a cabo utilizando equipos simples y así el biodiésel puede ser fabricado a pequeña escala por los entusiastas del combustible. Estos entusiastas tienen la libertad de usar el biodiésel como quieren y esto incluye la posibilidad de dañar su propio vehículo. Sin embargo, para producir el combustible industrialmente se requieren condiciones más sofisticadas a fin de cumplir con los requisitos para los grandes volúmenes involucrados, obtener altos rendimientos y una producción diaria adecuada; pero lo más importante, cumplir con la calidad constante y consistente con los requerimientos de las normas ambientales, esto es, el biodiésel debe cumplir entre otras, con las pruebas enumeradas en la Tabla 3. Por el momento, el principal proceso industrial utilizado para la producción de biodiésel es la transesterificación en fase homogénea. Los catalizadores homogéneos más utilizados son ácidos o bases y destacan los hidróxidos de sodio y potasio, por su bajo costo. Sin embargo, se está investigando cómo obtener mejores catalizadores heterogéneos para mejorar la producción, si se logra, adicionalmente se aumentaría la facilidad de la recuperación del catalizador para su reutilización. El proceso industrial de transesterificación se presenta como diagrama de bloques en la Figura 7.
De acuerdo con Dunkan (2003) los pasos principales en la producción de biodiésel son:
Pretratamiento de la materia prima (aceite vegetal, grasas animales o sebo) para eliminar compuestos perjudiciales para las etapas del procesamiento posterior. El pretratamiento incluye: desgomado, desfosforización y deshidratación
Reaccion de transesterificación, donde los triglicéridos reaccionan con metanol para formar los ésteres metílicos crudos y el glicerol (ver Figura 8). Como todo proceso industrial se busca una alta conversión. En la producción de biodiésel hay dos pasos básicos: el proceso de reacción seguido de la separación del éster, el alcohol sin reaccionar y el glicerol. En la mayoría de los procesos de biodiésel la reacción-separación se lleva a cabo dos veces. La segunda separación es necesaria porque las condiciones de operación son cercanas al equilibrio termodinámico; para mejorar la conversión global del proceso es requisito la disminución de la concentración de glicerol y después de la separación se realiza una segunda etapa de reacción. La reacción también se acerca a la alta conversión mediante el uso de un exceso del reactivo metanol. Otra razón para la obtención de conversiones altas es que se requiere una alta pureza del FAME (> 96.4%). Concentraciones menores implican mayores niveles de monoglicéridos que causan problemas de procesamiento, entre ellos la formación de emulsiones y en el biodiésel problemas a baja temperatura como el alto punto de niebla.
Purificación de éster de metilo. Considerando que se trabaja una reacción homogénea, en esta etapa se elimina al catalizador, el exceso de metanol y glicerol. Inicialmente se separan el glicerol junto con el metanol. La presencia de glicerol causa problemas en el motor diésel, por eso debe separarse. Y el catalizador se elimina con un solvente de lavado, generalmente agua; por razones ambientales, la mezcla ácido (o álcali) - solvente de lavado debe neutralizarse.
Purificación de glicerol. El metanol se recupera y se recicla hacia el proceso de transesterificación. Otras impurezas, tales como parte de catalizador (proceso homogéneo), sebo y éster de metilo remanente, continúan en el glicerol y se deben eliminar para producir un glicerol de más alto grado de pureza.
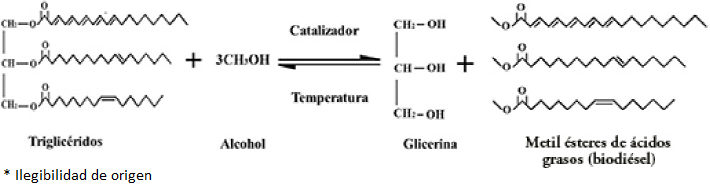
Fuente: Este esquema de reacción se tomó como ejemplo del trabajo de Kumar et al. (2019).
Figura 8 Reacción de transesterificación de los triglicéridos para la obtención de biodiésel.
Ahora nos referiremos a la transformación química para producir el biodiésel, esto es, la transesterificación.
Reacción de transesterificación
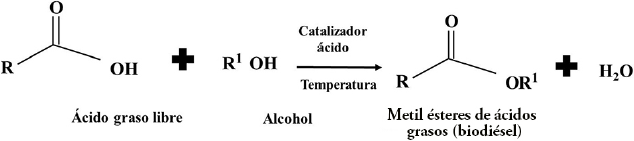
En la Figura 8 se presenta la reacción de transesterificación. De acuerdo con la estequiometría por cada mol de triglicéridos, se requieren 3 moles de alcohol (metanol); recuérdese que la estequiometría de la reacción es independiente del catalizador (homogéneo o heterogéneo) y de la temperatura (> 60 ºC). Los productos buscados son los metil ésteres de ácidos grasos (FAMEs) que constituyen el biodiésel, y glicerina (o glicerol) como subproducto. Si se tienen ácidos grasos libres también pueden reaccionar de acuerdo con la Figura 9.
Fuente: Elaboración de los autores.
Figura 9 Reacción de esterificación de ácidos grasos libres para producir biodiésel.
De una forma general, se presenta a continuación una descripción de los tipos de catalizadores empleados para la producción de biodiésel.
Catalizadores homogéneos
Los catalizadores homogéneos utilizados para la producción de biodiésel incluyen catalizadores ácidos: H2SO4, HNO3 o básicos: sosa o potasa, en solución acuosa concentrada. Todos ellos se eligieron por su relativamente bajo costo. Otro catalizador muy utilizado a nivel laboratorio es el metóxido de sodio; pero, su costo es muy elevado y no se utiliza a nivel industrial. Los catalizadores homogéneos tienen desventajas, entre ellas:
Algunos catalizadores son sensibles a la presencia de ácidos grasos libres.
El catalizador no se separa fácilmente del producto.
Entonces el catalizador no puede reusarse, considerando que es o un ácido o una base deben realizarse neutralizaciones y/o lavados sucesivos para removerlos del biodiésel crudo, se usa generalmente agua.
El excesivo uso de agua hace el proceso económicamente más caro y además antiecológico.
Aunque a veces se evada, es un requisito el tratar al agua. Esto aumenta nuevamente los costos.
Además, en el caso del uso de sosa se puede presentar una saponificación extensa
En cambio, el uso de un catalizador heterogéneo tiene las siguientes ventajas:
El catalizador puede utilizarse en un reactor de lecho fijo o ser recuperado por filtración o decantación.
Se elimina la necesidad de procesos de lavado y neutralización.
La pureza de los FAAEs (fatty acid alkil esters) producidos alcanza fácilmente las requeridas en las normas (> 96.5 %).
También se reduce la producción de agua contaminada y con ello la necesidad de los procesos de tratamiento de agua reduciendo entonces los costos económicos y ecológicos.
La presencia de ácidos grasos libres no afecta el desempeño del catalizador.
Todos estos puntos nos llevan a que el proceso que utiliza catalizadores heterogéneos podría ser económicamente más barato, aunque se utilice una mayor temperatura. El esquema de producción del biodiésel con un catalizador heterogéneo, idealmente se reduciría entonces al esquema de bloques en la Figura 10.
Catalizadores heterogéneos ácidos
De acuerdo con las investigaciones realizadas sobre la reacción y mecanismos de la transesterificación se han identificado dos tipos diferentes de catalizadores heterogéneos: ácidos y básicos. La catálisis heterogénea ácida puede realizar simultáneamente la esterificación de ácidos grasos libres (FFA: free fatty acids) y de los triglicéridos de ácidos grasos. El mecanismo de reacción es similar al del proceso catalizado homogéneamente (Bonelli et al., 2007). La reacción implica un ataque nucleofílico del ácido carboxílico adsorbido con el alcohol libre. La formación de un intermediario más electrofílico también se produce con ácidos de Lewis superficiales. El paso determinante de la rapidez de reacción depende de la fuerza del ácido. Pero, si la fuerza de los sitios ácidos es demasiado alta, la desorción del éster se reduce (Lotero et al., 2006).
Se han realizado muchos estudios sobre la esterificación con catalizadores ácidos heterogéneos y resinas ácidas. Se ha probado la actividad de varios catalizadores ácidos homogéneos o heterogéneos en la transesterificación de triacetina a 60 ºC. Se observó el orden de actividad siguiente: H2SO4 > Amberlyst-15 (resina ácida) > zirconia sulfatada > Nafión NR-50 (alquenos perfluorados en resina modificada con ácido sulfónico) > zirconia > ácido fosfórico soportado > zeolita B (López et al., 2005). Estos resultados confirman que la fuerza del sitio ácido es una variable importante. Además de la Amberlyst 15, Amberlyst BD20 y Nafión NR-50 (De Rezende 2008); Nafión SAC-13 (Mo et al., 2008); e incluso se ha reportado un proceso de demostración industrial; pero, debido a la baja actividad de los catalizadores heterogéneos ácidos se debe trabajar a temperaturas mayores a 170 ºC; esto reduce la utilidad de las resinas de intercambio iónico y obliga a la búsqueda de mejores catalizadores.
Catalizadores heterogéneos básicos
Los catalizadores básicos heterogéneos presentan las ventajas enumeradas por operar en fase heterogénea. Pero además se piensa que los catalizadores heterogéneos básicos tienen un futuro más promisorio porque se consideran más activos que los catalizadores ácidos y esto permitiría un menor tamaño del equipo de proceso (Zhang et al., 2010); todo lo cual conduce a una disminución de los costos y del impacto ambiental del proceso. El estudio de diferentes materiales con características básicas que se ha realizado es muy amplio y en la Tabla 4 se enlistan los catalizadores y su clasificación por grupos.
Tabla 4 Catalizadores heterogéneos básicos empleados en la producción de biodiésel.
| Tipo de catalizador | Ejemplos |
|---|---|
| Resinas de intercambio iónico. | Amberlyst A 26, A 27 |
| Óxidos de metales alcalinos. | K2O
(producido por el desperdicio de la quema de
cultivos) CaO, SrO, BaO |
| Carbonatos y bicarbonatos de metales alcalinos. | Na2CO3, NaHCO3, K2CO3, KHCO3 CaCO3 |
| Sales de metales alcalinos y ácidos carboxílicos. | Ca-laurato |
| Hidróxidos de metales alcalinos. | Ba(OH)2 |
| Óxidos y carbonatos de metales de transición. | Fe2O3 (+ Al2O3), Fe2O3, Fe3O4, FeOOH, NiO, Ni2O3, NiCO3, Ni(OH)2 Al2O3 |
| Sales de metales de transición y ácidos grasos. | Zn- y Mn-palmitatos y estearatos |
| Hidrotalcitas. | Li-Al, Zn-Mg-Al |
Fuente: Elaboración de los autores.
Resinas de intercambio iónico. Presentan el problema de la estabilidad a temperaturas mayores a 70 ºC, por lo que a menos que se consiga una mejora en la actividad, su aplicación industrial parece limitada.
Óxidos y carbonatos de metales alcalinos. Presentan una alta actividad, similar a los hidróxidos utilizados en fase homogénea (sosa o potasa). No obstante, los óxidos y carbonatos tienen problemas como: sensibilidad a la presencia de ácidos grasos libres, baja estabilidad en presencia de agua y con ella la posible lixiviación de los componentes. Evitar el agua en este proceso es difícil; así que la búsqueda de catalizadores heterogéneos básicos continúa.
Hidrotalcitas. Quizá, uno de los tipos de catalizadores más prometedores para la producción de biodiésel son las hidrotalcitas, cuya fórmula general es:
Donde M2+ and M3+ son cationes metálicos y An- un anión de compensación de carga por ejemplo CO3-, NO3-, etcétera.
Una de las ventajas de las hidrotalcitas es la facilidad para sintetizarlas y agregar distintos cationes metálicos con carga 2+ o 3+, permitiendo obtener compuestos con prácticamente cualquier composición que uno desee (Cavani et al., 1991). También es posible usar los productos calcinados de las hidrotalcitas. Estos productos son óxidos metálicos que tienen una alta área superficial, fuerte basicidad, estabilidad térmica y no se ven afectados por la presencia de agua (Serio et al., 2008; Coelho et al., 2017; Hájek et al., 2015; Deng et al., 2011; Trakarnpruk y Porntangjitlikit, 2008). Es relativamente fácil producir hidrotalcitas ternarias. Esto permite cambiar las propiedades catalíticas del material sustituyendo al Mg por otro metal con carga 2+. Sobre la actividad de hidrotalcitas ternarias en la transesterificación se han reportado varios trabajos, ver: Cabrera et al. (2017), Fan et al. (2016) y Hájek et al. (2017) que usaron los productos de calcinación de hidrotalcitas ternarias con Zn, Ca y Fe, respectivamente, obteniendo buenos resultados en la actividad de transesterificación.
Así que, en la producción de biodiésel, la catálisis presenta soluciones en los temas ecológicos pues reduce la cantidad de agua requerida, evita la contaminación de esta y la necesidad de un tratamiento de limpieza. Reduciendo así la complejidad del proceso y los costos. Adicionalmente, el uso de catalizador permite cambiar a un proceso continuo más fácilmente.
IV. Diésel verde
¿Por qué se habla de biodiésel y diésel verde? Como ya se mencionó el biodiésel está constituido por metil-esteres de ácidos grasos (FAMEs). Pero, la presencia de oxígeno en estos compuestos y en el biodiésel refinado tiene las siguientes desventajas:
Baja estabilidad química, no se puede almacenar mucho tiempo.
Un poder calorífico menor al diésel.
Resistencia al flujo causada por alta viscosidad en especial a bajas temperaturas.
Comercialmente estos problemas se evitan al máximo utilizando mezclas petrodiésel-biodiésel. En cambio, el diésel verde tiene una mayor semejanza química con el diésel convencional, porque está formado por cadenas alifáticas (parafinas) con un número de carbonos entre 14-25, dependiendo del aceite vegetal de origen. El diésel verde es totalmente compatible con el petrodiésel y su uso en el motor diésel no requiere ninguna modificación. Y, debido a que el diésel verde tiene un número de cetano alto se puede utilizar para mejorar al diésel fósil. Por su similitud química con el petrodiésel cumple también con las normas del petrodiésel (Tabla 3).
Lo primero que se tiene que destacar es que la producción de diésel verde solo se presenta en presencia de catalizador. Para convertir triglicéridos o ácidos grasos en un compuesto alifático se debe eliminar el oxígeno, lo cual requiere necesariamente de hidrógeno para formar agua y convertir el carbono terminal de ácido carboxílico (COOH) al grupo -CH3. Entonces estamos hablando de una hidrodesoxigenación (HDO, eliminación de oxígeno en presencia de hidrógeno). La HDO es una reacción incluida en el hidrotratamiento (HDT) proceso ampliamente utilizado en la limpieza de petrodiésel. En el procesamiento de cortes de crudo, si se utiliza el HDT es posible eliminar simultáneamente heteroátomos de: azufre, nitrógeno, oxígeno y metales. El HDT de cortes de petróleo se ha estudiado desde alrededor de 1930. Entonces, la tecnología del HDT puede utilizarse para la HDO de aceites vegetales o animales. Pero, existen ciertas diferencias respecto a los contenidos de heteroátomos entre aceites y petróleo. Una alimentación típica de crudo fósil contiene en promedio 94% en peso de carbón, hasta 1.8% de S y 0.1% de oxígeno y 0.1% de nitrógeno. En cambio, la alimentación a partir de aceites vegetales puede contener hasta un 50% de oxígeno (Yang et al., 2008).
Para eliminar al oxígeno, en realidad ocurren varios tipos de reacciones. El esquema de la Figura 11 presenta las posibles reacciones de manera simplificada. En la HDO se tienen hidrogenación, ruptura de los triglicéridos, descarboxilación, descarbonilación y desoxigenación. En la HDO, el primer paso es de hidrogenación, que causa la separación de los ácidos grasos del triglicérido. Posteriormente, los ácidos grasos sufren un proceso de descarboxilación, descarbonilación y desoxigenación, liberando CO2, CO y H2O, respectivamente. Además del propano, el resultado son parafinas con el mismo número de carbones que el ácido graso original (reacción de descarbonilación) o con el número de carbones menos uno (descarboxilación). A veces ocurren isomerizaciones, pero los productos tienen estructuras químicas iguales a los presentes en el petrodiésel, porque sigue predominando la cadena alifática larga.
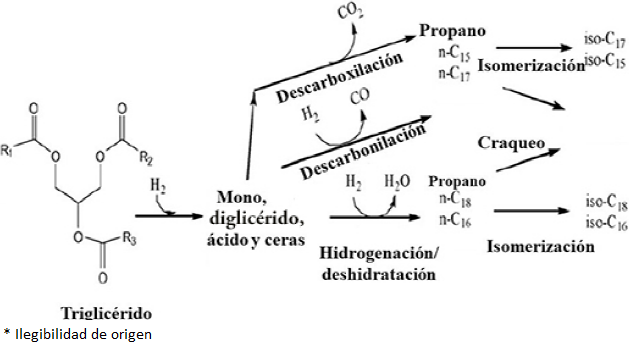
Fuente: Esquema de reacción adaptado de Huber et al. (2007).
Figura 11 Obtención de hidrocarburos alifáticos para combustibles a partir de aceite vegetal, empleando catalizador sólido NiMo/Al2O3 sulfurado.
En la Tabla 5 se presentan algunas investigaciones catalíticas sobre el procesamiento de diversos aceites para la obtención de diésel verde. Como se puede observar los catalizadores utilizados en la reacción son de dos clases: catalizadores metálicos, con actividad en hidrogenación, y catalizadores sulfurados NiMo o CoMo. El uso de estos últimos no es sorprendente porque los catalizadores sulfurados son los utilizados en los procesos de HDT del petróleo. Por esta razón este tipo de catalizadores ya ha sido bastante estudiado y se conocen los procedimientos adecuados de preparación. Como desventaja se tiene que los catalizadores sulfurados posiblemente adicionan azufre al diésel verde resultante.
Tabla 5 Tipos de catalizadores empleados en la producción de diésel verde.
| Tipo
de catalizador |
Ejemplos | Soportes | Alimentación | Condiciones de operación (°C, MPa), conversión alcanzada (%) |
Referencia |
|---|---|---|---|---|---|
| Sulfuros | CoMo | Al2O3, SiO2-Al2O3 |
Aceite de canola |
325-400, 3.10,99% | Afshar y Kaliaguine (2018) |
| NiMo | Al2O3 | Aceite de girasol |
310, 40, rendimiento 0.4 |
Liu C. et al. (2013) | |
| Metales nobles |
Pt, Pd | SAPO 11 | 375-380, Reactor continuo |
Srifa et al. (2015) | |
| Metales de transición |
Ni Co |
Al2O3, Materiales mesoporosos |
375-380 |
Kordulis et al. (2016) Srifa et al. (2015) |
Fuente: Elaboración de los autores.
Por otro lado, como se observa en la Figura 11, el esquema de reacción incluye varias hidrogenaciones, por lo cual los catalizadores de hidrogenación son útiles en este proceso. Se han utilizado metales reducidos como Pt, Pd, Ni y Co. Estos tienen, también, cierta actividad de ruptura de enlaces.
Como conclusión se prevé que por sus propiedades el diésel verde se aprovechará fácilmente como complemento de la producción de diésel y el único camino para producirlo es utilizando catalizadores.
V. Combustible alternativo para aviación: bioturbosina
La turbosina, jet fuel en inglés, se refiere al combustible cuyas propiedades como: contenido energético, viscosidad, densidad y composición química son aptas para ser empleados en aviones con motores de turbina de gas. La turbosina es una mezcla de hidrocarburos con una distribución en el número de carbonos de C6-C16, entonces, corresponde a las temperaturas de destilación en el intervalo de 150 ºC a 275 ºC; por lo que compete al queroseno. La turbosina está conformada por 20% de parafinas, 40% de isoparafinas, 20% de naftaleno y 20% aromáticos (Gutiérrez-Antonio et al., 2017). Dadas las cuestiones de seguridad este combustible debe cumplir con las propiedades mencionadas en la Tabla 6, existen dos estándares operacionales para Jet A (usada en EU norma principal ASTM D1655) y Jet A-1 (empleada alrededor del mundo).
Tabla 6 Propiedades físicas de los combustibles para turbina de avión.
| Propiedades físicas | Norma | Jet A-1 | Jet A |
|---|---|---|---|
| Punto de inflamabilidad (°C) | ASTM D2382 | 42.0 | 51.1 |
| Temperatura de autoignición (°C) | 210 | 210 | |
| Punto de congelación (°C) | -47 | -40 | |
| Densidad a 15 °C (kg/L) | ASTM D1655 | 0.775-0.840 | 0.775-0.840 |
| Viscosidad | ASTM D1655 | 8 mm2/s | |
| Flash point | ASTM D93 | 32 | |
| Energía específica (MJ/kg) | 43.2 | 43.0 | |
| Densidad energética (MJ/L) | 34.7 | 35.3 | |
| Cantidad máxima de agua | ASTM D7566 | 75 ppm | |
| Numero ácido total (KOH 1M) | ASTM D1655 | 0.1 mg KOH/g |
Fuente: https://bioresources.cnr.ncsu.edu/resources/chemical-composition-and-fuel-properties-of-alternative-jet-fuels/ consultada el 02/06/2020, 16:03.
En el mundo, el consumo de turbosina está entre 1.5-1.7 billones de barriles por año (Wang y Tao, 2016). Por otra parte, el sector de aviación contribuye con el 2%-6% del total de las emisiones antropogénicas de CO2 y el 10% del consumo de combustibles totales (Chiaramonti et al., 2014; Wang y Tao, 2016). Las proyecciones actuales indican que en 20 años aumentará al doble el tráfico aéreo lo que traerá como consecuencia que la demanda de combustible y emisiones se duplique (Gutiérrez-Antonio et al., 2017). De esta forma, la International Air Transport Association (IATA) estableció el objetivo de lograr un crecimiento neutral de carbono después del 2020 y reducir las emisiones en un 50% para el año 2050 (referenciado al 2005); para cumplir con este objetivo se prevé utilizar el mejoramiento tecnológico, pero sobre todo operacional adoptando la turbosina renovable (RJF: renowable jet fuel) (De Jong et al., 2017). El compromiso de la IATA ha sido un aliciente importante en el desarrollo y aplicación de este combustible. La bioturbosina producida a partir de biomasa permitirá la reducción de las emisiones de CO2. El RJF, turbosina renovable, bioturbosina, turbosina verde, queroseno parafínico sintético (SPK) o bio-queroseno, está constituido por hidrocarburos casi idénticos a la turbosina convencional. Este tipo de combustible siempre requiere del uso de catalizador en su producción. Existen diferentes rutas tecnológicas para producir RJF a partir de biomasa, como los que se pueden observar en la Figura 12, entre ellos están: el hidroprocesamiento de esteres de ácidos grasos, Fischer-Tropsch, licuefacción hidrotérmica, pirólisis, transformación de alcohol a turbosina y la transformación directa de azúcares a hidrocarburos (Wang y Tao, 2016; De Jong et al., 2017). La aplicación de los diferentes tipos de procesos y tecnologías puede variar en función del tipo de materia prima. Por ejemplo, en el hidrotratamiento, grasas y aceites vegetales pueden ser convertidos a bioturbosina a través de las reacciones de desoxigenación, isomerización/hidrocraqueo, donde siempre se utilizan catalizadores. La materia sólida orgánica, como biomasa lignocelulósica, puede asimismo ser convertida a gases, alcoholes o biocrudo y, después, estos productos mediante proceso bioquímicos y termoquímicos pueden ser convertidos a bioturbosina (Wang y Tao, 2016).
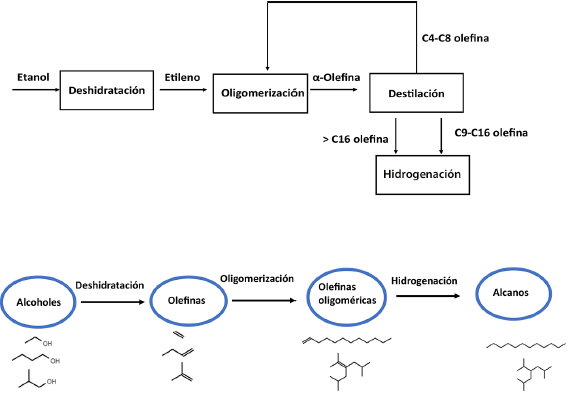
Fuente: Adaptado de A) Wang y Tao (2016); B) Díaz-Pérez y Serrano-Ruiz 2020.
Figura 12 Producción de bio-turbosina a partir de alcohol.
Transformación de alcoholes a bioturbosina (ATJ alcohol to jet)
El proceso en general involucra la deshidratación de alcoholes (etanol, butanol o isobutanol), oligomerización e hidrogenación para lograr producir hidrocarburos en el rango de la turbosina (Figura 12). Como ya se ha visto, la obtención del alcohol se puede producir vía hidrólisis-fermentación de material lignocelulósico y almidón. Como se observa en la Figura 12, se presenta el proceso de producción de hidrocarburos para turbosina a partir del alcohol como etanol (Figura 12A), del isobutanol y butanol (12B), en ambos casos las rutas son similares.
Con el compromiso expresado por la IATA, se han registrado (Gutiérrez-Antonio et al., 2017) experiencias exitosas de un vuelo con jets A-10 y F/A-18 Hornet fighter (US Navy) en los años 2012 y 2014 con RJF que se produjo en el proceso ATJ. Díaz-Pérez y Serrano Ruiz (2020) describen la empresa conjunta entre Gevo y BioChemtex, para convertir un bioalcohol, isobutanol, a bioturbosina. Gevo también está desarrollando un proyecto para incrementar la capacidad de una planta a 10,000,000 galones/año, para la distribución de RJF en Francia y gran parte de Europa.
Catalizadores en el proceso de producción de alcohol a turbosina
Con referencia a la Figura 12, la reacción de deshidratación puede realizarse empleando catalizadores ácidos como sílica-alumina, sílica-aluminofosfatos, zeolitas y hetero poliácidos. Dentro de esos catalizadores, el caso más prometedor ha sido con zeolita 0.5% La-2%P HZSM-5 que se reportó alcanza 100% de conversión, una alta selectividad a etileno con una velocidad espacial 1 h-1, a 250 ºC (Zhang et al., 2010; Wang y Tao, 2016). Respecto a la deshidratación de otros alcoholes se ha reportado la conversión de isobutanol a isobutileno (2-metilpropeno), con catalizador alúmina, siendo la mejor condición a 325 ºC, 0-60 psig, LHSV = 5 h-1 con 15% de agua (Taylor et al. 2010).
Con los hidrocarburos olefínicos y mediante reacciones de oligomerización puede obtenerse la bioturbosina. La oligomerización podría ocurrir sobre sitios ácidos y entonces los catalizadores propuestos son: resinas ácidas sulfónicas, zeolitas ácidas o sólidos ácidos fosfóricos bajo condiciones de temperatura de 100-300 ºC y de 0-70 bares. Wang y Tao (2016) reportaron catalizadores tipo Ziegler Natta (ZN) y fosfuro de cromo y zeolitas. Para catalizadores ZN, Diaz-Pérez y Serrano Ruiz (2020) reportan el uso de una sola etapa y el proceso INEOS (dos etapas) para producir oligómeros de etileno. Por su parte, Shell desarrolló un proceso con catalizadores homogéneos basados en Ni-P. Peters y Taylor (2011) reportaron la obtención de hidrocarburos olefínicos C8-C16 a partir de alcoholes C2-C6, principalmente isobutanol, con catalizadores (γ-alúmina, β zeolita, y resinas ácidas sulfónicas) a temperaturas de 250-350 ºC (0-7 bares). Según Gutiérrez-Antonio et al. (2017), los productos exceden los requerimientos D7566-10a. También se ha empleado la resina Amberlyst como catalizador para la producción de olefinas C8-C16 (C12 al 70%) a partir de la oligomerización de isobuteno (Díaz-Pérez y Serrano-Ruiz, 2020).
Trasformación de azúcares en turbosina
Por otro lado, la transformación directa de los azúcares o carbohidratos a bioturbosina y diésel, también se ha estudiado. Wang y Tao (2016) describen el proceso Virent BioForming (Figura 13), con el que se convierte biomasa a una mezcla de hidrocarburos de alto contenido energético. La biomasa es pretratada y separada a celulosa, hemicelulosa y lignina. Esta última se utiliza para la producción de calor. A partir de la celulosa y hemicelulosa se obtienen azúcares C5-C6 mediante enzimas e hidrólisis ácidas. Con la hidrogenación de los carbohidratos, estos son transformados a alcoholes y a compuestos oxigenados de cadena corta (hidrogenólisis). Después, dichos productos reaccionan con agua mediante un catalizador heterogéneo a temperaturas de 450-475 K y presiones de 10-90 bares, El proceso es conocido como reformado en fase acuosa (APR en inglés); en este proceso, las reacciones son: reformado para producción de hidrógeno (usado en el mismo proceso); deshidrogenación de alcoholes/hidrogenación de carbonilos; desoxigenación; hidrogenólisis y ciclación. Otros productos son dióxido de carbono, alcoholes, cetonas, aldehídos, alcanos, ácidos orgánicos, furanos e hidrocarburos ligeros C1-C4, utilizados para generar más calor.
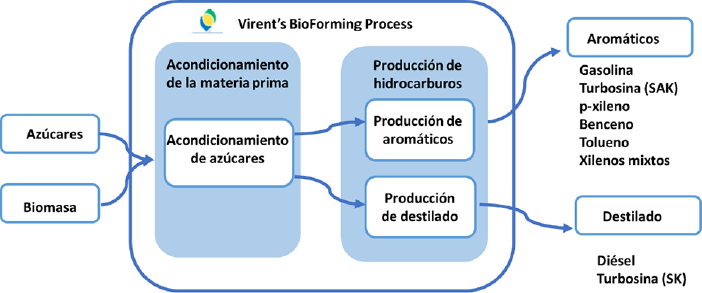
Fuente: Adaptado de la página web www.virent.com/technology/bioforming/
Figura 13 Producción de hidrocarburos para combustibles a partir de biomasa y azúcares.
Wang y Tao (2016) describen algunas rutas con potencial para producir hidrocarburos en el rango de turbosina usando los productos oxigenados del proceso APR. Por ejemplo, empleando catalizador zeolita ZSM-5 para mejorar la condensación ácida de hidrocarburos oxigenados convirtiéndolos a alcanos, isoalcanos y aromáticos. Posteriormente, mediante reacciones de deshidratación de oxigenados a alcanos, oligomerización de alquenos a alquenos pesados, craqueo, ciclación y deshidrogenación de alquenos pesados a aromáticos, isomerización e hidrogenación para la formación de alcanos. Finalmente, el producto es destilado y mezclado con turbosina. Otro ejemplo es la investigación de Kunkes et al. (2008) en un sistema de reactores en cascada; se reportó la conversión de carbohidratos a diferentes hidrocarburos (por ejemplo, bioturbosina). En el primer reactor, mediante catalizador Pt-Re/C, los azúcares son desoxigenados a 200 ºC obteniendo productos como cetonas, alcoholes y heterocíclicos. Posteriormente, algunos de los productos, como las cetonas fueron mejoradas para generar productos de C8-C12 para bioturbosina. También se han empleado catalizadores como Ru/Al2O3 (hidrogenación) y Pt/ SiO2-Al2O3 (hidrodesoxigenación) en azúcares C5, obtenidos de material lignocelulósico, para producir combustibles como diésel y bioturbosina (Olcay et al. 2013).
Transformación de aceites a bioturbosina (OTJ oil to jet fuel)
Los aceites vegetales o grasas animales también pueden utilizarse para generar bioturbosina. Los triglicéridos están conformados por ácidos grasos que contienen un número de carbonos desde 14 hasta 18, insaturados o saturados, así que una reacción clave es la ruptura de los enlaces. De acuerdo con Gutiérrez-Antonio et al. (2017), la bioturbosina se genera a partir de reacciones de hidrodesoxigenación, hidroisomerización e hidrocraqueo. Como se explica en la Figura 14, primero los triglicéridos son transformados empleando altas presiones y temperaturas en presencia de hidrógeno y un catalizador sólido a hidrocarburos de cadena lineal larga -ver producción de diésel verde en este articulo-. Como subproductos se obtienen agua, CO y CO2 por las reacciones de descarboxilación y descarbonilación. Como segunda etapa, los alcanos lineales son empleados para reacciones de craqueo e isomerización, produciendo cadenas en el rango C8 a C16. También se producen reacciones de isomerización que mejoran el producto. Otros productos son gases ligeros y naftas.
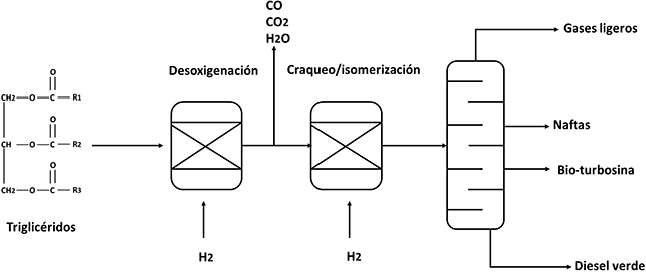
Fuente: Adaptado del trabajo de Gutiérrez-Antonio et al. (2017).
Figura 14 Proceso para obtención de bioturbosina a partir de triglicéridos.
Liu, G. et al. (2013) describen la experiencia de Syntroleum quien registró su proceso Bio-Synfining™, donde se produce RJF a partir de ácidos grasos y triglicéridos de grasas animales, aceite vegetal y algas. Después de la desoxigenación, las n-parafinas son hidrocraqueadas a parafinas ramificadas cortas. Idealmente, el producto está conformado por queroseno y naftas (principalmente n-parafinas). La planta de demostración de Bio-Synfining produjo 600 galones SPK (RJF) en el primer semestre del 2008 para la fuerza armada aérea de los EUA. También, los mismos autores, reportaron que Honeywell-UOP produjo bioturbosina a partir de aceite de palma, soya, camelina, jatropha y aceite de algas mediante el proceso de EcofiningTM SPK. Esta turbosina verde fue usada en mezclas del 50% en varios vuelos de aerolíneas comerciales en EUA. Chiaramonti et al. (2014) reportaron que en mayo del 2012 varias aerolíneas realizaron vuelos con bioturbosina proveída por compañías como NESTE, SkyNRG, Solazyme y ASA.
Existen diferentes catalizadores para la producción de bioturbosina que usan aceites vegetales. Se debe señalar que en este proceso hay dos etapas basadas en reacciones químicas diferentes: (hidro)desoxigenación y ruptura/isomerización con diferentes tipos de catalizadores cada una. Algunas veces se ha intentado utilizar la temperatura para facilitar la ruptura. Investigaciones recientes se centran en la producción en una sola etapa con catalizadores capaces de llevar a cabo los dos tipos de reacciones.
Catalizadores para la transformación de aceites a bioturbosina (OTJ Oil To jet fuel)
Respecto a la desoxigenación, Sinha et al. (2014) usaron reactores de micro canales y monolíticos recubiertos con catalizador Ni-Mo/γ-Al2O3 preparados por sol-gel para el hidroprocesamiento de aceite de jatropha. Ambos tipos de reactores presentaron alta selectividad a queroseno (6-20 veces) respecto a un reactor convencional, reactor de lecho de goteo. Liu et al. (2015) emplearon catalizadores Ni/SAPO-11, Ni2P/SAPO-11 y Ni/MCM-41 para hidrodesoxigenación de aceite de castor en un micro reactor de cama fija con flujo continuo a 300 ºC, 3 MPa y LHSV de 2h-1 y un flujo de H 2 de 160 mL/min. En esta experiencia fueron mayores los rendimientos molares de C17-C18 con Ni/SAPO-11. Además, dichos autores sintetizaron Ni/MCM-41-APTES (7.5 wt. %)-USY, donde APTE es (3 aminopropil)-trimetoxisiliano, permitiendo un rendimiento del 80.3% para C8-C15.
Los intentos de crear procesos con una etapa utilizan el concepto de realizar la oxigenación con una fase activa y la reacción de rompimiento con el soporte del catalizador. Por ejemplo, Cheng et al. (2014) emplearon dos zeolitas HY y HZSM-5 como soporte de Ni y Mo para la conversión del aceite de soya. Se observó que el uso Ni-Mo/HY incrementó la selectividad a alcanos en el rango de bioturbosina y tuvo un decremento en los aromáticos. El rendimiento aumentó a 49.1% cuando la temperatura se elevó de 330 a 390 ºC. Además, el aumento de la temperatura hasta 410 ºC propició el incremento de productos aromáticos (de 18.7% a 30%) disminuyendo la calidad de la bioturbosina. Por su parte, Verma et al. (2015) produjeron una mezcla de bioturbosina (40%), diésel (40%) e hidrocarburos ligeros del rango de la gasolina (20%) a partir del hidroprocesamiento del aceite de jatropha, con un rendimiento del 84%. Para esto, emplearon catalizadores NiMo y NiW soportados en mesoporos de SAPO-11 a las condiciones de 60-80 bar, 375-450 ºC y 1 h-1 en un reactor de cama fija con una reducción del consumo de hidrógeno.
VI. Ventajas de las microalgas en la producción de biocombustibles
Aunque los avances hasta aquí presentados son importantes, también se han realizado importantes progresos en los insumos que se utilizan para la producción de biocombustibles, en este punto destaca el uso de las microalgas.
En la producción de biocombustibles se ha llegado a la conclusión de que el mayor costo es la producción de los insumos. Por ejemplo, se estima que hasta un 85% del costo del biodiésel corresponde a la producción del aceite vegetal o grasa de la alimentación. Entonces existe una gran presión para una disminución en el costo de las materias primas, así como en los costos de proceso. Los biocombustibles de tercera generación utilizan microalgas como fuente de biomasa. Se han descrito a las microalgas como un conjunto heterogéneo de microrganismos fotosintéticos unicelulares procariontes (cianobacterias) y eucariontes. Se clasifican para fines biotecnológicos por el tipo de pigmentación, morfología y estructura celular (Garibay et al., 2009) siendo las más estudiadas las algas verdes y las diatomeas. Las ventajas de las microalgas son las siguientes:
Pueden cultivarse en estanques abiertos o sistemas cerrados (Figura 15), se puede pensar que no tienen demanda de tierras arables.
Son relativamente fáciles de cultivarse, con muy poca o ninguna atención, así es posible cultivar microalgas en agua salada o agua residual. En procesos de tratamiento de agua, son un subproducto que se ha probado que puede producir biocrudo (Nava Bravo et al., 2019).
El nivel de reproducción y crecimiento es muy alto. Se estima que la masa de microalgas en un cultivo se dobla cada 24 h.
Con lo anterior, las microalgas se pueden cosechar más de una vez por año.
Si se utiliza el agua de cultivo adecuada, son una fuente relativamente barata de nutrientes incluso para el ser humano.
Se tiene un potencial de producción hasta de 100 veces mayor que el rendimiento de las semillas por kilogramo de masa y el rendimiento de aceite se estima de 30-300 veces respecto a las semillas si se comparan por área de producción.
En las microalgas, los contenidos de lípidos pueden encontrarse entre 40-80% en peso en base seca y es posible ajustar el contenido de lípidos en las microalgas cambiando las condiciones de cultivo.
Recordando que el CO2, la luz solar y el agua son los insumos principales para el cultivo de microalgas. Estas últimas juegan un papel principal en el mantenimiento de sistema ecológico terrestre y tienen un papel importante en el control de la polución ambiental y renovación del oxígeno atmosférico.
Entre otras, las microalgas se han empleado en situaciones como:
La remoción de CO2 de instalaciones industriales (Wang et al., 2008).
No se requiere CO2 de una gran pureza para cultivar microalgas (Brennan y Owende, 2010).
El tratamiento de aguas. De hecho, los contaminantes del agua usuales como NH4+, NO3- y PO43- pueden ser utilizados eficazmente como nutrientes para el crecimiento de las microalgas.
Los compuestos de las microalgas, como son carbohidratos, lípidos y proteínas pueden ser empleadas para producir etanol, biodiésel, diésel verde bioturbosina, metano, o simplemente quemar la biomasa para la cogeneración de energía (electricidad y calor).

Fuente: Fotografías publicadas en la web.
Figura 15 Sistemas de cultivos abiertos o cerrados para microalgas.
Adicionalmente, se debe recordar que las microalgas es un grupo relativamente poco estudiado así que es muy posible que sean la fuente de algunos lípidos poco comunes u otro tipo de insumos de química fina.
Producción de biodiésel y diésel verde a partir de microalgas
Todo lo discutido anteriormente sobre los temas de biodiésel y diésel verde se puede aplicar en el caso de la obtención de aceite a partir de las microalgas. Es decir, una vez cosechada la microalga se puede extraer aceite y los triglicéridos, y estos se pueden procesar para obtener biodiésel o diésel verde. Durante el procesamiento se pueden utilizar los mismos tipos de catalizadores ya descritos en las secciones sobre biodiésel y diésel verde para su producción, puesto que la naturaleza de los triglicéridos es la misma.
El método convencional para la producción de biodiésel a partir de microalgas implica varias etapas; cultivo de microalgas, cosechado (centrifugación, sedimentación, etc.), secado, extracción de aceite, purificación (desgomado, desfosforización, deshidratación, etc.) y esterificación/transesterificación. Por el momento, estas etapas constituyen más del 70% del costo total de producción de biodiésel. En la actualidad se está investigando bastante sobre el cultivo de las microalgas y a veces es muy difícil conseguir la cantidad suficiente de microalgas para extraer el aceite.
En su constitución las microalgas tienen una amplia gama de compuestos que pueden clasificarse como lípidos, incluyendo lípidos polares, lípidos neutros, ésteres de cera, esteroles y compuestos como carotenoides, terpenos, tocoferoles, quininas y derivados de pirrol como clorofilas. Los lípidos polares participan en la estructura celular y contienen principalmente una gran cantidad de ácidos grasos insaturados (PUFAs: poli-unsaturated fatty acids). Los lípidos polares también pueden comportarse como intermediarios importantes en las vías de señalización celular (por ejemplo, esfingolípidos, lípidos de inositol, pro-conductos oxidativos, entre otros, y contribuir a reaccionar a los cambios en los parámetros ambientales. De todos esos biocompuestos nosotros estamos interesados en los lípidos de almacenamiento que son principalmente triglicéridos (TAG), con un alto contenido de ácidos grasos (Fas: fatty acids). En su periodo de vida, la mayoría de las microalgas acumulan muy pocos TAGs durante el crecimiento exponencial y la principal cantidad de TAGs puede acumularse durante la fase de crecimiento estacionaria (Sajjadi et al., 2018). En cuanto a la longitud de la cadena del ácido graso respectivo, la proporción que podemos encontrar es: C16 (7-41%) > C14(0.6-30%) > C18 (0.6-21%) >C17 (0.4-10%) e incluso algunas algas producen grandes cantidades de ácidos grasos de mayor peso molecular, por ejemplo: C22:6 (42%) usando Aurantiochytrium sp., C22:5 y C22:6 (39.4%) con Schizochytrium limacinum, o C20:5 (25%) Porphyridium cruentum. Los tipos principales de ácidos grasos que podemos encontrar en las microalgas son: palmitoleico (16:1), oleico (18:1), linoleico (18:2), linolénico (18:3) y ácidos grasos saturados como palmítico (16:0).
El uso de microalgas para la producción de biodiésel y/o diésel verde se ve como una de las situaciones más promisorias (Aransiola et al., 2014). Sin embargo, depende de dos factores económicos: la reducción del costo de producción del aceite y/o que el costo del crudo aumente. Aunque, claro si la preocupación por el ambiente se volviera real tendría una gran influencia. Es posible crear o modificar con ingeniería genética a las microalgas para tener un contenido de hasta 80% de lípidos. Otra situación que puede impulsar el desarrollo de biocombustibles es que el costo del crudo aumente. Chisti et al. (2007) estiman que la condición para el remplazo de crudo fósil como fuente de hidrocarburos se presentará cuando el costo del litro de aceite de alga respecto al precio por barril de crudo fósil sea:
Costo (aceite de alga/L) = 6.9*10-3 Costo (barril de crudo en dólares).
Producción de biocrudo a partir de microalgas
Si bien el enfoque para producir biodiésel y/o diésel verde parece promisorio, surge la pregunta ¿Y los otros compuestos biológicos (carbohidratos y proteínas) no se aprovechan? Con este enfoque se puede producir biocrudo usando microalgas.
En esta sección discutiremos la generación de biocrudo directamente de la biomasa micro-algal. El biocrudo si bien no es un combustible, con su procesamiento se generarán biocombustibles. Básicamente tenemos dos opciones: transformaciones biológicas y transformaciones termoquímicas (Figura 16).
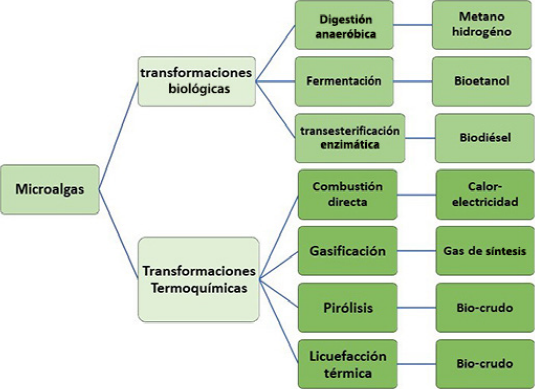
Fuente: Este esquema se realizó tomando como base el trabajo de Naik et al. (2010).
Figura 16 Procesos aplicados a las microalgas para la producción de biocombustibles.
Transformaciones biológicas para microalgas en la producción de biocombustibles
Si bien este trabajo se centra en la producción utilizando catalizadores, daremos una sucinta explicación de los procesos biológicos.
Digestión anaeróbica
En principio, se puede producir biogás con la digestión anaeróbica (DA) de cualquier biomasa. Con la DA la biomasa se puede trasformar en biogás. El biogás está formado por metano, CO2, agua y trazas de otros gases entre ellos H2S. En este proceso se puede utilizar material orgánico húmedo. El proceso DA tiene tres etapas secuenciales: hidrólisis, fermentación y metanogénesis. En la hidrólisis, los compuestos complejos se descomponen en azúcares solubles. Entonces, las bacterias fermentativas las convierten en alcoholes, ácido acético, ácidos grasos volátiles (VFA) y un gas que contiene H2 y CO2 y, finalmente, en la metanogénesis los compuestos orgánicos se metabolizan principalmente en CH4 (60-70%) y CO2 (30-40%) (Cantrell et al., 2008).
Fermentación
Se producen alcoholes con la fermentación de los carbohidratos, así es posible obtener bioetanol a partir de azúcares y almidones. La fermentación es parte de los procesos catabólicos que llevan a la degradación de compuestos orgánicos complejos a compuestos más simples. El proceso de fermentación también es anaeróbico y propio de ciertas bacterias y levaduras. Siendo una biomasa con azúcares en su constitución, también se pueden fermentar las microalgas
Transesterificación enzimática
La reacción de transesterificación se puede realizar con enzimas; especialmente del grupo de las lipasas. Trabajar con enzimas tiene la ventaja de que se utilizan temperaturas bajas, obviamente para no desnaturalizar las enzimas, pero estas condiciones de operación requieren tiempos largos de producción. Uno de los problemas iniciales en este tema fue que las enzimas se perdían con cada lote; pero en la actualidad ya hay enzimas soportadas.
Transformaciones termoquímicas para la producción de biocombustibles a partir de microalgas
Existen diferentes tipos de procesos térmicos para transformar la biomasa microalgal a biocrudo. Este producto es llamado así debido a su similitud al petróleo (Figura 17), y debe cumplir con requisitos asociados con el crudo, por ejemplo, en el contenido calórico (Sanna, 2014). De manera similar al crudo, el biocrudo se puede procesar para obtener productos con valor agregado alto o precursores para biocombustibles y diversos biocombustibles (Bello-Zakari, 2015; Vo et al., 2016; Markarfi Isa et al., 2018). A continuación, se describen estos procesos térmicos.
Fuente: Fuente: (A) tomado de Alonso-Ramírez et al. (2019); (B) tomado de Nava Bravo et al. (2019).
Figura 17 Corte de saturados de un crudo convencional (A) y, (B) bio-crudo producido a partir de licuefacción hidrotérmica de microalgas
Combustión directa
Se han estudiado las microalgas como posibles fuentes de energía por caso, las microalgas que crecen en el agua de drenaje (Hossain et al., 2019), y de lodos (Hossain y Morni, 2019). En estos casos, las microalgas fueron mezcladas con carbón sub-bituminoso para hacer briquetas y evaluar su poder calorífico. Sin embargo, el poder calorífico de las microalgas es bajo y se han buscado otras formas para aumentar el contenido energético en los biocombustibles.
Gasificación
La gasificación se define como el proceso donde materiales carbonosos se transforman en una mezcla gaseosa, llamada gas de síntesis o syngas. El syngas está formado por 45% de hidrógeno, 8% metano, CO y otros gases incluyendo CO2. Aunque el syngas tiene un poder calorífico reducido, puede utilizarse como combustible o como intermediario en la producción de otros químicos. Para producir syngas se tiene un sistema de reacciones complejo, cuyas reacciones principales son:
En cuanto al uso de biomasa para producir syngas se acostumbra realizar la oxidación parcial en presencia de oxígeno y existen dos procesos: catalítico y no catalítico. La temperatura de operación del proceso no catalítico es de alrededor de 1300 ºC, en cambio el catalítico trabaja a 900 ºC. Hirano et al. (1998) estudiaron la oxidación parcial de Spirulina sp. en el intervalo de temperaturas entre 850 y 1000 ºC. De esta forma, determinaron que la temperatura necesaria para generar el rendimiento máximo de metanol fue de 1000 ºC alcanzando un rendimiento 0.64 g de metanol/g de biomasa.
Otro uso del syngas es en la producción de gas sintético (GNS), metanol o alimentación para el proceso Fischer-Tropsch y generar hidrocarburos líquidos (Figura 18). El proceso Fischer-Tropsh trabaja a altas presiones, típicamente 25 bares, temperaturas mayores de 350 ºC y el catalizador más utilizado ha sido el óxido de zinc. Del proceso se obtienen hidrocarburos alifáticos en el rango de gasolinas, diésel o keroseno (Wang y Tao, 2016). Un ejemplo de este tipo de sistema de reacción se muestra en la Figura 18.
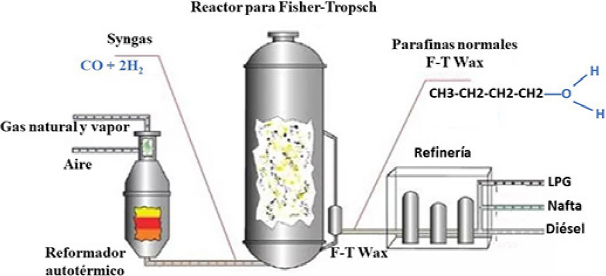
Fuente: Adaptada de la página web de ISI Andina (2020).
Figura 18 Ejemplo del tratamiento de syngas mediante Fischer-Tropsch.
Pirólisis para la producción de biocrudo
La pirólisis es un proceso que se realiza a alta temperatura (> 450 ºC) y en ausencia de aire. En esencia se generan compuestos de carbono más ligeros utilizando energía térmica que favorece la ruptura de los enlaces C-C o incluso enlaces C-heteroátomo (S, N, O, etc.). En estas condiciones el proceso bien puede realizarse en ausencia del catalizador. Por el momento y debido a la complejidad de los materiales orgánicos, se está trabajando en proponer esquemas de reacción y no se han propuesto mecanismos como tales (ver ejemplo en: Demirbas, 2000). En la experimentación se emplea la biomasa microalgal en un reactor de cama fija (Figura 19). Además, un gas acarreador inerte es usado para transportar los vapores de la pirólisis a los condensadores, de donde se obtiene el biocrudo. Cuando se emplea catalizador el único cambio es que se mezclan la biomasa y el catalizador. Utilizando un catalizador adecuado se puede reducir la temperatura de trabajo y considerando que las reacciones de ruptura de enlaces son importantes los catalizadores de elección poseen propiedades ácidas. Para procesar las microalgas, los catalizadores más usados por el momento son zeolitas como la HZSM-5, que, gracias a su estructura de poro y acidez, permite obtener productos con alto contenido de aromáticos, mejorando el poder calorífico en comparación de los procesos de pirólisis no catalíticos (Azizi et al., 2018). Así, adicionalmente al emplear catalizador se mejorará la calidad del biocrudo, por ejemplo, reducir el contenido de oxígeno, nitrógeno o azufre, según el tipo de biomasa que se procese.
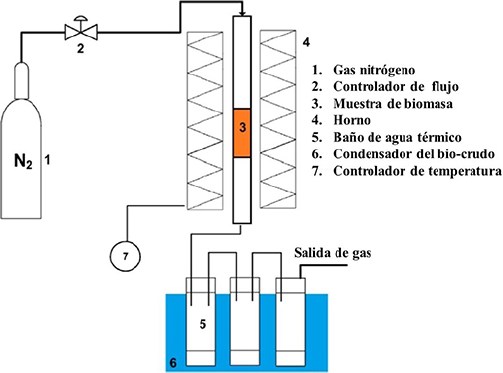
Fuente: Adaptada del trabajo de Azizi et al. (2018).
Figura 19 Sistema de pirólisis para la obtención de bio-crudo a partir de biomasa.
Otros catalizadores empleados han sido el Na2CO3 con microalgas Chlorella, produciendo bajo contenido de aromáticos a altas temperaturas (desde 450 y hasta 1100 ºC), y mayor calidad de biocrudo en comparación de un proceso no catalítico (Azizi et al., 2018; Babich et al., 2011). Además, se han probado óxidos metálicos (MgO y ZrO2) y ZYNa y como resultado se obtuvieron cetonas de cadena larga, mientras que el empleo ZYH promovió la formación de hidrocarburos aromáticos y nitrilos a partir de microalgas Schizochytrium limacinum (Azizi et al., 2018; Anand et al., 2017).
Obtención de biocrudo por licuefacción térmica
Para la obtención del biocrudo se mantiene la necesidad de reducir el peso molecular de los compuestos biológicos; por lo que en los primeros intentos se utilizan catalizadores con propiedades ácidas. El proceso de licuefacción es ideal para microalgas de bajo contenido de lípidos (Jena et al., 2011; Fortier et al., 2014). Los procesos de licuefacción emplean un solvente y se realizan en ausencia de oxígeno en un reactor de alta presión. El uso de solvente ayuda a operar a temperaturas más bajas comparadas con las utilizadas en el proceso de pirólisis. Los intervalos de trabajo están entre 200-600 ºC. La licuefacción se ha clasificado en dos tipos: cuando se utiliza un solvente cualquiera se le llama solvolísis; cuando se utiliza agua se tiene la licuefacción hidrotérmica (HTL en inglés). Respecto a la descripción de cómo ocurren las reacciones en este tema nos encontramos con bastantes problemas, entre ellos: a) la complejidad química de los biocompuestos que se están transformando; b) las reacciones complejas que tienen lugar durante la transformación de la biomasa en el biocrudo como producto. De este modo, en estas etapas iniciales de investigación se están planteando los esquemas de reacción. Un paso en este tema fue recientemente reportado (González-Gálvez et al., 2020). En este artículo se ha mostrado que la licuefacción puede procesar todos los tipos de biomoléculas: carbohidratos, lípidos y proteínas de las microalgas.
Dado que la HTL emplea agua, es posible evitar la etapa de secado de la biomasa. La HTL se realiza temperaturas de 230-400 ºC, a esas temperaturas es posible generar presiones en el intervalo de 5-40 MPa (García et al., 2012; Tian et al., 2014; Singh et al., 2015). Diversas investigaciones sugieren que varias de las reacciones presentes son catalizadas por la disociación del agua en H+ y OH- generados a alta temperatura (Cheng et al., 2017), es decir, se aprovechan las propiedades ácido-base del agua. Mediante HTL se pueden obtener rendimientos desde 5 a 30% de biocrudo. Además del biocrudo otros subproductos que se generan son gases y residuos sólidos, junto con el agua del medio de reacción rica en nutrientes. El agua producto del tratamiento en el proceso contiene carbono, nitrógeno y fósforo, provenientes de la biomasa, y es por tanto ideal para reutilizarse como medio de cultivo para las microalgas. Gollakota et al. (2018)) describen que esta agua puede ser tratada anaeróbicamente (de preferencia si es baja en contenido de fenoles y furfurales) o mediante gasificación catalítica para producir gas de síntesis rico en metano e hidrógeno. Adicionalmente, los residuos sólidos pueden contener nutrientes residuales y pueden ser empleados como bio-char o fertilizantes para suelo.
El biocrudo puede presentar cierto contenido de compuestos nitrogenados (pirrol, piridina, indol, quinolina, etc.), compuestos oxigenados con nitrógeno (derivados de la pirrolidona, piperidina, etc.), compuestos oxigenados (fenol, ácidos grasos, metil ésteres de ácidos grasos, alcoholes, etc.), hidrocarburos cíclicos (ciclohexano, ciclopentadecano, etc.), alifáticos (hexadeceno, hexadecano, heptadecano, pentadeceno, etc.), entre otros compuestos (Nava Bravo et al., 2019, González-Gálvez et al., 2020).
Las reacciones que ocurren en el proceso de licuefacción hidrotérmica HTL son: hidrólisis, deshidratación, descarboxilación, repolimerización, desaminación y reacciones de Maillard. Dichas reacciones son las encargadas de transformar lípidos, proteínas y carbohidratos de las microalgas a moléculas insolubles en agua, gases no condensables y carbón (Cheng et al., 2017). Estas reacciones se pueden observar en la Figura 20.
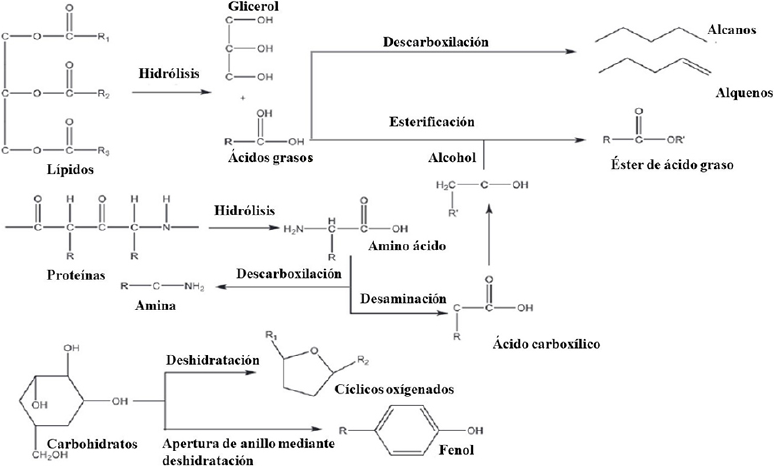
Fuente: Esquema de reacción modificado de Hu et al. (2019).
Figura 20 Reacciones del proceso HTL de las microalgas.
A temperaturas mayores de 373 ºC se producen las reacciones de gasificación, y entonces se habla de otro proceso denominado gasificación hidrotérmica (Cheng et al., 2017), resultando como producto gas sintético. Sin embargo, como es bien sabido, el biocrudo obtenido a partir de microalgas contiene tan alto contenido de heteroátomos (S, N y O) y alta viscosidad por lo cual es conveniente mejorar su calidad. De esta forma, una alternativa es emplear catalizadores que se encarguen de mejorar las propiedades del biocrudo.
Catalizadores empleados en el proceso HTL de biomasa microalgal
El uso de catalizadores tiene como uno de sus objetivos aumentar el rendimiento de biocrudo y mejorar la calidad de este producto. También, dependiendo del tipo de catalizador, se pueden lograr reacciones de desnitrogenación, desoxigenación, desulfuración y descarboxilación, para obtener un biocrudo con bajo contenido de nitrógeno, oxígeno, azufre y mejorar la producción de alifáticos, respectivamente. Dentro de los estudios realizados en este contexto, se han empleado aditivos homogéneos (como pretratamiento) y catalizadores heterogéneos (durante el proceso). A continuación, se dará una breve descripción de ellos.
Catalizadores homogéneos
Este tipo de catalizadores son solubles en agua a temperatura ambiente, Ross et al. (2010) utilizaron las sales alcalinas Na2CO3 y KOH, así como, ácidos orgánicos CH3COOH y HCOOH. Los autores determinaron que, de los catalizadores alcalinos, el Na2CO3 permite obtener desde 20.1% hasta 51.6% de rendimiento de biocrudo en las condiciones de reacción usadas: 280 ºC a 360 ºC con tiempos de reacción de 30 minutos hasta 60 minutos. El rendimiento de biocrudo presentó el siguiente orden Na2CO3> CH3COOH> KOH> HCOOH. Sin embargo, existen trabajos que confirman que los catalizadores alcalinos pueden inducir a la saponificación de los lípidos, aumentando los residuos sólidos (Xu et al., 2018).
Catalizadores heterogéneos
El empleo de catalizadores heterogéneos en la HTL presenta una ventaja competitiva con respecto a los homogéneos que es su recuperación para ser reusados, además, los catalizadores homogéneos (alcalinos y ácidos) presentan un efecto negativo en el pH de los productos líquidos y causan una fuerte corrosión en los equipos de reacción (Xu et al., 2018).
En años recientes en el proceso de HTL se están evaluando catalizadores con diferentes propiedades. Así, se probaron catalizadores con propiedades hidrogenantes: por ejemplo, Duan et al., (2011) probaron Pd/C, Pt/C, Ru/C, Ni/SiO2-Al2O3, CoMo/γ-Al2O3 (sulfurado). Los rendimientos obtenidos de biocrudo fueron de hasta 57% con el catalizador Pd/C. En forma general, los autores observaron que la fase gas estaba conformada por H2, CO2, CH4 y en menor proporción C2H4 y C2H6. En cambio, con Ni y Ru producían altos rendimientos de gas metano. También se han probado catalizadores con propiedades ácidas, los mismos autores utilizaron una zeolita y en este caso el gas presentó cantidades significativas de N2, mostrando que la zeolita es efectiva para reacciones de desnitrogenación. Por otro lado, el contenido de N, S y O decrece en el biocrudo en presencia de los catalizadores en comparación con el biocrudo producido sin catalizador. Mientras que en pruebas con hidrógeno (3,550 kPa H2) el contenido de heteroátomos fue insensible y presentó un ligero cambio en el contenido de dichos heteroátomos. Se ha reportado que el uso de HZSM-5 reduce el contenido final de azufre y nitrógeno en el biocrudo, aunque se utilicen microalgas con un alto contenido de proteínas, si se utiliza HTL (Nava Bravo et al., 2019) o se utiliza solvólisis (González-Gálvez et al., 2020). Otros trabajos reportan el uso de HZSM-5 modificada. Xu et al. (2014) trabajaron con Ce/HZSM-5 y HZSM-5 y mostraron que el catalizador con Ce presentó un efecto superior de craqueo catalítico de microalgas, alcanzando rendimientos a biocrudo de 49.87% (Ce/HZSM-5) comparado contra 34.02% (HZSM-5). Además, el uso de catalizador mostró un mayor efecto en la descomposición de la celulosa, hemicelulosa y proteínas de las microalgas. En un trabajo posterior los mismos autores (Xu et al., 2018) señalan que el catalizador Ce/HZSM-5 también es capaz de llevar a cabo las reacciones de desnitrogenación.
Transformación de biocrudo a bioturbosina
El biocrudo producido, sea por pirólisis o licuefacción hidrotérmica, puede ser empleado como materia prima para la obtención de biocombustibles, en este caso bioturbosina. Por ejemplo, Zhang et al. (2015) emplearon pirólisis de biomasa (Abeto de Douglas) mediante microondas y después realizó el mejoramiento del biocrudo pirolítico con hidrotratamiento, se reportó la producción de parafinas y aromáticos en el rango de turbosina. Se utilizaron como catalizadores ZSM-5 durante la pirólisis de la biomasa, y Níquel Raney para el hidrotratamiento. De esta forma, con la despolimerización de la biomasa a temperaturas de 375 ºC se obtuvieron aromáticos en el intervalo de C8-C15. En la etapa de hidrotratamiento del bio-aceite, se obtuvo una selectividad a parafinas (C8-C15) del 12.6% y de 19.4% para aromáticos. También se ha buscado el tratamiento de biomasa lignocelulósica y de una mezcla de material lignocelulósico y plástico (proporción 0.75) para la producción de cicloalcanos y alcanos en el rango de la turbosina, respectivamente (Zhang et al. 2015). En la producción de cicloalcanos y alcanos para turbosina, primero se obtuvieron aromáticos a partir de pirólisis con zeolita ZSM-5, posteriormente fueron hidrogenados a n-heptano para obtener los productos deseados (selectividad de 84.6%) con níquel Raney a 200 ºC y 2 horas de reacción a 500 psi con H2. Otro catalizador que se ha empleado para la hidrogenación de bio-aceite pirolítico ha sido Ni-Mo a 450 ºC. El bio-aceite pirolítico fue obtenido a 850 ºC de una mezcla de aserrín de eucalipto con desecho de aceite de soya y CaO. Con el proceso de hidrotratamiento, más del 60% de los compuestos oxigenados y nitrogenados fueron convertidos a hidrocarburos con propiedades similares al queroseno de aviación, entre ellas: punto de congelamiento, punto de inflamación, densidad, viscosidad y entalpía de combustión (Shah et al. 2019).
Conclusiones
De seguir por el camino actual se espera que la producción de combustibles fósiles disminuya y los problemas ecológicos aumenten. Inevitablemente se prevé un aumento en el uso de los combustibles aunado con el consiguiente aumento en las emisiones de CO2 a la atmósfera y se tendrán problemas a nivel mundial por el calentamiento global. Si sumamos la disminución de las reservas de combustibles fósiles, se vuelve necesario cambiar el paradigma de producción y consumo energético. Ante este panorama es muy importante seguir brindando apoyo al desarrollo tecnológico para la producción de energías limpias. Si bien, la completa aceptación del uso de biocombustibles ha generado polémicas a través del tiempo, en realidad la objeción más importante es económica. Así, algunas personas y gobiernos ven la producción de biocombustibles como una carga, pero, de cualquier manera, es deseable que en el futuro próximo esa percepción equivocada se evite. Para enfrentar esta resistencia, a través de los años, se han realizado arduos estudios respecto al abaratamiento de la producción de combustibles amigables con el medio ambiente.
Uno de los caminos más prometedores para alcanzar este fin es el uso, mejoramiento y síntesis de diversos catalizadores, los cuales pueden jugar un importante papel no solo para aumentar la conversión de la biomasa, sino, además, para mejorar las propiedades de los biocombustibles. En este trabajo se ha enumerado cómo el uso de catalizadores aporta desde diferentes ángulos en este tema. Para la producción de bioetanol se trabaja en la obtención de este utilizando una nueva alimentación, hasta hace poco tiempo considerada como desecho. En el biodiésel con un catalizador heterogéneo se simplifica el proceso con las ventajas económicas respectivas. En principio, el diésel verde es un mejor combustible que el biodiésel y no se puede producir sin catalizador. La producción de bioturbosina solo puede alcanzarse con catalizadores y, adicionalmente, estudiar las reacciones de oligomerización es importante. Para la producción de biocrudo el catalizador lleva a un descenso en la temperatura de reacción y mejora la calidad del producto. Para el biocrudo u otros combustibles dentro de las propiedades fisicoquímicas que se mejoran se tiene el aumento del contenido energético, disminución de viscosidad, densidad, contenido de nitrógeno, azufre, oxígeno, etc., según sea el caso.
Hoy en día, existen varios países que ya han apostado por la producción de fuentes de energía limpia a partir de diferentes tipos de biomasa. México no es una excepción, pero el país debe aprovechar el alto potencial para la generación de estos combustibles renovables. No obstante, la evolución del uso y producción de biocombustibles es lenta en el país comparándolo con otros países. Es necesario establecer más políticas públicas y energéticas que incentiven y puedan apoyar el desarrollo e investigación de este campo en nuestro país.











 nueva página del texto (beta)
nueva página del texto (beta)