Introducción
La fístula aortoentérica (FAE) es una patología poco frecuente, pero de riesgo vital, que consiste en la conexión anormal entre la aorta y el tracto gastrointestinal. Puede ser primaria si aparece de novo por compresión de un aneurisma, una neoplasia, radioterapia previa o infección, debido a factores mecánicos o inflamatorios, o secundaria a una prótesis vascular tras un procedimiento reconstructivo de aorta.
La fístula secundaria puede presentarse de dos formas: como comunicación anastomótica entre la luz aórtica y el intestino (fístula enteroprotésica verdadera), y menos frecuentemente como erosión aortoentérica (fístula enteroparaprotésica) a consecuencia del contacto directo de la prótesis vascular con el intestino.
El objetivo de este trabajo es destacar la importancia del diagnóstico precoz de la FAE y su manejo multidisciplinar.
Caso clínico
Mujer de 80 años con antecedentes de hipertensión, tabaquismo, enfermedad renal en estadio IIIb, intervenida de bypass aortobifemoral y posterior bypass femorofemoral por trombosis de rama derecha del injerto. Ingresó con diagnóstico de sepsis de probable origen abdominal, anemia y lumbalgia.
Se realizó gastroscopia por hemorragia digestiva (Fig. 1), visualizando en la tercera porción duodenal la presencia de un cuerpo extraño compatible con prótesis parcialmente emergente a la luz duodenal con coágulos adheridos, sin hemorragia activa. La angiografía por tomografía computarizada (angio-TC) (Fig. 2) reportó una ulceración por decúbito de la pared duodenal secundaria al material protésico del bypass aortobifemoral, probable hematoma o proceso infeccioso en el psoas derecho y ureterohidronefrosis derecha.
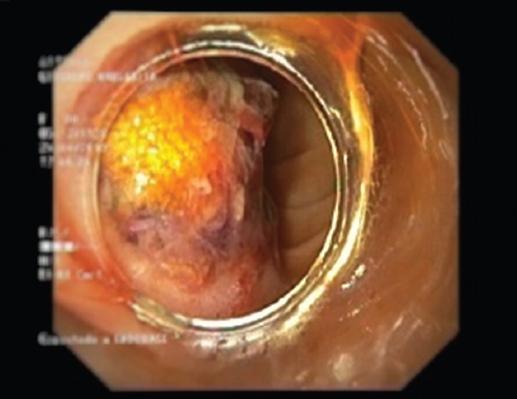
Figura 1 Gastroscopia: material amarillento compatible con prótesis emergente a la luz en la tercera porción duodenal.
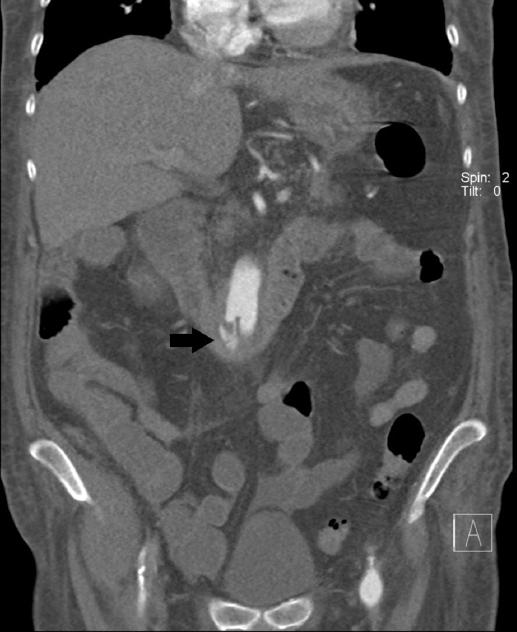
Figura 2 Angiografía por tomografía computarizada, corte coronal, que muestra extravasación de contraste de la luz aórtica al duodeno (flecha).
Con diagnóstico de fístula enteroparaprotésica, se programó intervención quirúrgica (Figs. 3 a 5) en la que se realizó bypass axilofemoral izquierdo, sección de aorta infrarrenal, sutura del muñón proximal y ligadura de la rama izquierda de la prótesis. En el procedimiento se objetivó perforación de la cara posterior de la tercera-cuarta porción duodenal secundaria a intrusión de la prótesis aórtica; se realizaron maniobra de Cattell-Braasch, sección duodenal, exclusión pilórica y reconstrucción en Y de Roux.
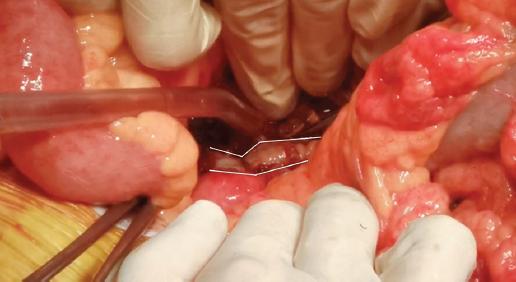
Figura 3 Intervención quirúrgica: prótesis aortobifemoral íntimamente adherida al duodeno (contorno blanco).

Figura 4 Intervención quirúrgica: mucosa duodenal (punta de flecha) y prótesis aortobifemoral (flecha).

Figura 5 Intervención quirúrgica: mucosa duodenal tras la liberación de adherencias a la prótesis aortobifemoral.
La paciente presentó como complicación posoperatoria (Clavien-Dindo IIIa) una colección abdominal que se solucionó mediante drenaje percutáneo y antibioticoterapia, siendo dada de alta el día 29 de posoperatorio.
Discusión
Concepto
La FAE es una patología infrecuente que se asocia a una alta morbimortalidad1-3. Se define como una conexión anormal entre la aorta y el tracto gastrointestinal, cuya localización más frecuente es el duodeno. Existen dos tipos: primaria y secundaria. La FAE primaria se produce de novo como resultado de la compresión de un aneurisma de aorta abdominal (AAA) contra el intestino, interviniendo en su fisiopatología factores mecánicos, inflamatorios e infecciosos4-6. La FAE secundaria, más común, se produce como consecuencia de una reconstrucción quirúrgica7,8, por erosión de material protésico aórtico sobre el intestino adyacente, pudiendo ocurrir también en procedimientos endovasculares9,10.
El AAA es el factor de riesgo más importante para desarrollar una FAE, bien como causa de fístula primaria o como reparación subsiguiente produciendo una fístula secundaria11. Las fístulas son más frecuentes en los varones, paralelamente a la incidencia de AAA y cirugía aórtica.
Manifestaciones clínicas
Su presentación clínica más frecuente es la hemorragia digestiva12 en pacientes con AAA, conocido o no, o cirugía vascular previa. Puede ser más o menos grave debido a la ruptura de la aorta a una porción de intestino íntimamente adherida, lo que puede dar lugar a una rápida exanguinación del paciente. Otras manifestaciones son malestar, pérdida de peso, sepsis, trombosis del injerto con isquemia de miembros inferiores o síntomas inespecíficos.
Diagnóstico
La tríada clásica descrita consiste en hemorragia, dolor abdominal y masa palpable. Sin embargo, en la práctica, el diagnóstico requiere una alta sospecha clínica y suele retrasarse, sobre todo si el aneurisma no es conocido, la etiología es otra (p. ej., aortitis) o es idiopática.
Los pacientes hemodinámicamente inestables con hemorragia masiva y AAA conocido (reparado o no) deben ser llevados directamente a quirófano para control del sangrado y reparación quirúrgica. En caso de sospecha de AAA por factores de riesgo, se requiere ecografía urgente para identificarlo, aunque no logrará visualizar la fístula.
Los pacientes hemodinámicamente estables con hemorragia digestiva aguda generalmente precisan una gastroscopia, aunque su sensibilidad para el diagnóstico de fístula es de solo un 50%13. Así, en casos de alta sospecha se debe realizar una angio-TC, y si esta es negativa, considerar una gastroscopia para visualizar el duodeno distal. El trombo y el material protésico impactado en esa localización no deben retirarse de inicio14.
En pacientes con sospecha de hemorragia digestiva y posible FAE se recomienda realizar una TC como prueba de elección no invasiva15,16, aunque las características radiológicas de la fístula y la infección periinjerto pueden ser difíciles de diferenciar y precisarán otros estudios complementarios. Los hallazgos radiológicos específicos en la TC que sugieren la presencia de FAE son gas ectópico adyacente o dentro de la aorta, engrosamiento focal de la pared intestinal, discontinuidad de la pared aórtica y extravasación de contraste a la luz intestinal17,18. Cualquier característica tomográfica de infección periinjerto debe plantear la posibilidad de una fístula secundaria.
Tratamiento
El tratamiento incluye resucitación inicial y soporte hemodinámico, antibioticoterapia y reparación aórtica, planteando la retirada del material protésico si lo hubiere. El tipo y el momento de la reparación deben ser individualizados, teniendo en cuenta la presentación clínica (gravedad de la hemorragia o infección), el tipo de fístula (primaria o secundaria), la comorbilidad del paciente, la anatomía aórtica, etc. Las opciones terapéuticas comprenden la reparación abierta y endovascular.
El manejo quirúrgico abierto incluye el control vascular, el desbridamiento del tejido necrótico e infectado (intestino y aorta), la restauración de la continuidad gastrointestinal y la revascularización (reparación local, reconstrucción in situ, extraanatómica, etc.)19.
Los métodos endovasculares, bien únicos o en combinación con la reparación abierta, incluyen la oclusión con balón de la aorta20, la embolización endovascular con coil21, plug endovascular22, pegamento de fibrina23 y la reparación con stent e injerto24. Estas técnicas suelen realizarse como medidas temporales para el control de la hemorragia y proporcionan un periodo ventana para resucitar al paciente y planificar el tratamiento definitivo25. En algunos casos, los procedimientos endovasculares se pueden emplear como tratamiento paliativo de pacientes con alto riesgo quirúrgico26. En presencia de infección sistémica, la reparación endovascular única condiciona infección recurrente27-29.
Conclusiones
La FAE es una patología poco frecuente que se asocia a una alta morbimortalidad. El pronóstico depende de la celeridad del diagnóstico, del estado basal del paciente, del grado de infección y de la porción aórtica afecta30. Así pues, el diagnóstico precoz y el tratamiento quirúrgico agresivo son los pilares fundamentales para lograr buenos resultados en pacientes con esta patología.











 nova página do texto(beta)
nova página do texto(beta)


