Introducción
El manejo de las fístulas es un reto para los cirujanos desde que se iniciaron las intervenciones quirúrgicas en el tracto gastrointestinal. Existen múltiples variantes de fístulas y diversos tratamientos. En la actualidad, el manejo conservador es de elección en las fístulas de bajo gasto, lo cual permite el cierre espontaneo, evitando intervenciones quirúrgicas. Cuando el tratamiento conservador falla o no es posible, por fístulas de alto gasto como las enteroatmosféricas, se deben buscar nuevas técnicas que permitan el manejo y el cierre de la fístula.
Las fístulas enteroatmosféricas son un subgrupo de las fístulas enterocutáneas que se caracterizan por ser superficiales, con alto gasto, rodeadas de vísceras o tejido de granulación, lo que causa mal control del gasto y lleva a malnutrición grave en periodos cortos debido a su alto gasto, alteraciones electrolíticas y sepsis1-3.
Si una fístula enteroatmosférica ocurre en el contexto de un abdomen abierto congelado se clasifica como Björck 4 y la mortalidad es del 42%, la cual se ha reducido gracias a los avances en técnicas quirúrgicas y cuidados intensivos4.
Una fístula enteroatmosférica puede generarse en un contexto de síndrome de intestino corto, lo cual empeora el pronóstico del paciente. El síndrome de intestino corto se define como la condición resultante de la resección quirúrgica o de una enfermedad congénita, con incapacidad para mantener el balance energético, hidroelectrolítico y de micronutrientes con una dieta normal, necesitando suplementación intravenosa o parenteral. Esta complicación se puede presentar en un 15% de los pacientes sometidos a resección intestinal, un 75% de los pacientes sometidos a resecciones masivas y un 25% de los pacientes sometidos a múltiples resecciones. Los pacientes con menos de 180 cm de intestino están en riesgo de sufrirlo5,6.
En este caso se hace énfasis en la necesidad de restaurar el tránsito intestinal, con manejo del gasto de la fístula enteroatmosférica mediante el uso de una endoprótesis intestinal como medida de salvamento7,8. Esta medida es controversial, ya que existen distintos resultados, pero puede ser un tratamiento de rescate en pacientes protocolizados, en los cuales no existe posibilidad de más resecciones o cirugías intestinales, por abdomen hostil, enfermedad adherencial grave o intestino corto9,10.
Describimos un manejo alternativo de una fístula enteroatmosférica en un paciente con abdomen abierto Björck 4, en el contexto de abdomen congelado y resección intestinal masiva. Se llevó a cabo una búsqueda detallada del uso de endoprótesis como medida de rescate, para ofrecer un procedimiento que pudiera favorecer el control y cierre temprano de la fístula, mediante colocación de endoprótesis intestinal. Se utilizaron los términos MeSH: enteroatmospheric fistula, intestinal stent, enterocutaneous fistula, intestinal endoprosthesis y hostile abdomen.
Caso clínico
Varón de 47 años, agricultor, originario de Oaxaca, quien fue referido de un hospital de segundo nivel con diagnóstico de obstrucción intestinal. Antecedentes personales: hipertenso de 15 años de evolución en tratamiento con antagonista de los receptores de la angiotensina II. Antecedentes quirúrgicos: apendicetomía de urgencia hace 15 años con resolución favorable y laparotomía exploradora hace 5 años por apuñalamiento, sin complicaciones.
Inicia su padecimiento el 15 de febrero de 2018 con dolor abdominal, vómito, náusea e incapacidad para evacuar. Dos días después acude a un hospital de segundo nivel, se le diagnostica obstrucción intestinal y se le realiza laparotomía exploradora, con hallazgos de necrosis de 10 cm de yeyuno, por lo que se realizan resección y anastomosis término-terminal. Con mala evolución, se opera al sexto día por obstrucción, pero solo se realiza laparotomía con toma de biopsia y se le envía a un hospital de tercer nivel para protocolo diagnóstico, inicio de nutrición parenteral total y manejo de la obstrucción intestinal. Es sometido a una nueva intervención el día 7 de marzo por salida de material intestinal en el tercio inferior de la herida quirúrgica, y se evidencian múltiples laceraciones en cuerda de violín en la pared antimesentérica del intestino, secundarias a una lesión traumática por el material utilizado (polipropileno) para el cierre de la aponeurosis en la cirugía previa, además de adherencias Zulkhe II-III. Se decide la resección en bloque del intestino dañado (Fig. 1), dejando únicamente un remanente de yeyuno a 40 cm desde el ángulo de Treitz y la totalidad del colon. Se realizó una anastomosis yeyuno-colónica con engrapadora GIA 80 mmHg y se cerró la cavidad abdominal. El manejo de la sepsis fue acorde a las guías actuales.
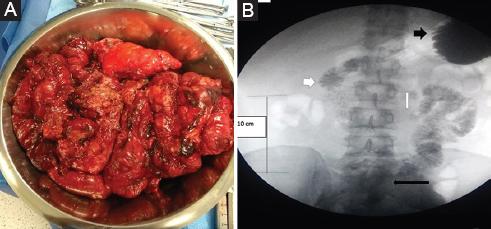
Figura 1 A: intestino resecado. B: medición del remanente de intestino, estómago (flecha negra corta), duodeno (flecha blanca corta), ángulo de Treitz (flecha blanca larga) y fuga de medio de contraste en el yeyuno (flecha negra larga).
En el tercer día posquirúrgico el paciente presenta fuga de material intestinal y es necesario intervenir quirúrgicamente, con los siguientes hallazgos: enfermedad adherencial grave Zulkhe IV, imposibilidad de disecar el yeyuno por adherencias firmes al sigmoides, y necrosis de la cara anterior del ciego. Se disecan los bordes necróticos, se remodela la anastomosis y se colocan drenajes en las caras anterior y posterior de la anastomosis. En el posoperatorio mediato se evidencia fuga, y debido a la imposibilidad de tratamiento quirúrgico se decide tratarla como fístula de alto gasto. Se inicia terapia antisecretora con omeprazol 80 mg al día en infusión y loperamida 16 mg/día, además de continuar con nutrición parenteral 2400 kcal/día y suplementación multivitamínica. Se realiza tránsito intestinal con medio de contraste hidrosoluble para determinar la cantidad de intestino remanente, siendo aproximadamente de 40 cm desde el ángulo de Treitz (Fig. 1). Además, se realiza estudio en colon por enema con medio hidrosoluble, verificando la permeabilidad del tracto inferior.
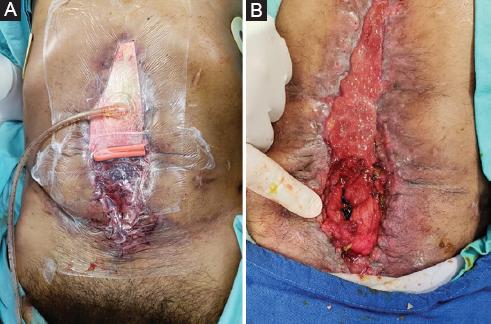
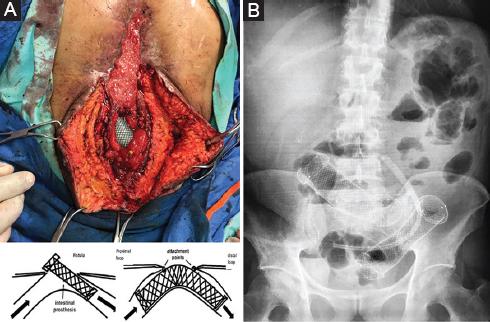
Se decide una tercera intervención en el hospital de tercer nivel, el 9 de abril, desmantelando la anastomosis previa, la cual presentaba dehiscencia de más del 70%. Se decide hemicolectomía derecha con la finalidad de prevenir fugas debido a la pobre irrigación del remanente de ciego y de colon ascendente. Se realiza anastomosis transverso-yeyuno. No es posible separar el yeyuno adherido al colon sigmoides (Fig. 2). Al cuarto día se produce fuga de la anastomosis por acodamiento en el colon sigmoides y aumento de la presión (Fig. 3). Para limitar la contaminación de la cavidad, se coloca un sistema de cierre asistido por presión (VAC) (Fig. 4), lo cual permite el cierre de la línea media de la herida en cuatro sesiones de VAC, dejando únicamente la dehiscencia de anastomosis como una fístula enteroatmosférica aislada. Debido a la condición del paciente (desnutrición, sepsis, desequilibrio hidroelectrolítico, abdomen hostil) no son posibles más cirugías, por alto riesgo de perforación y desvascularización. El aislamiento de la fístula ayudó a mejorar el estado hemodinámico y el control de la sepsis; sin embargo, las pérdidas entéricas eran elevadas, lo cual perpetuaba el desequilibrio hidroelectrolítico, la desnutrición y la malabsorción11-14.
Técnica quirúrgica de colocación de endoprotesis intestinal e indicaciones
En el contexto del paciente con fístula enterocutánea y síndrome de intestino corto se propone la colocación de una endoprótesis recubierta de 36 × 100 mm (nitinol) para restituir el tránsito intestinal desde el asa distal (yeyuno) a proximal (colon transverso), permitiendo el control de la fístula, la granulación desde los bordes intestinales y el cierre definitivo. La intervención se realizó el día 16 de mayo, colocando la endoprótesis a través de la línea media invaginando los dos segmentos del stent y fijándolo con puntos de sutura no absorbible. Mediante colonoscopia transoperatoria se colocó un segundo stent en el sigmoides para reducir la presión intraluminal y prevenir fugas9,10 (Fig. 5). Después de la colocación de los stents disminuyó el gasto de la fístula, de 1500 a 200 ml, en un periodo de 5 días. Se inició la alimentación enteral, coincidiendo con un incremento del gasto, el cual se estabilizó hasta 300 ml. El paciente continuó con nutrición parenteral total a razón de 30 kcal/kg al día (Fig. 6). Al noveno día posquirúrgico se decide el alta, sin evidencia de sepsis ni de desequilibrio hidroelectrolítico, y con control de la fístula.
Resultados
Se realizó seguimiento por consulta externa con el equipo multidisciplinario de manera mensual, evaluando el estado nutricional y la herida quirúrgica, que se encontraba cerrada en un 90% a los 6 meses de seguimiento, sin necesidad de nutrición parenteral total, solo suplementación multivitamínica y dieta sin oxalatos, y el gasto a través de la herida era de 50-150 ml (Fig. 7). El paciente se reincorporó de manera parcial a sus actividades diarias y se valía por sí mismo.
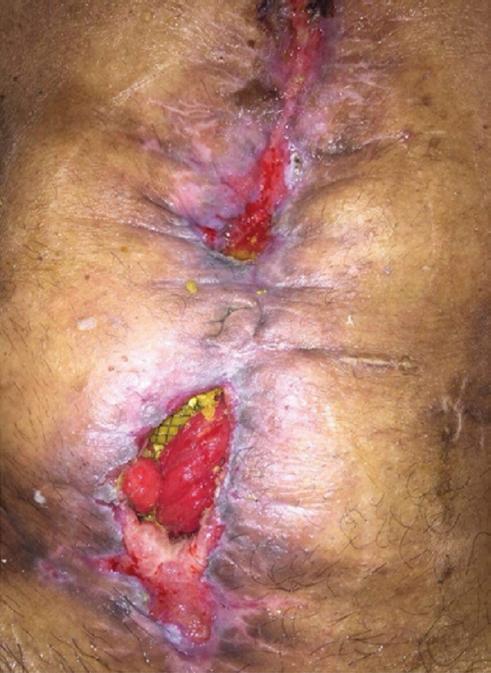
Figura 7 Fístula en proceso de cierre por segunda intención. Se observa el stent en el tercio medio.
El uso de la endoprótesis permitió el inicio temprano de la alimentación enteral, mejorando la calidad de vida y disminuyendo las complicaciones relacionadas con la nutrición parenteral total (daño hepático, esteatosis, síndrome colestásico, infecciones). La adaptación final del colon se alcanza a los 2 años. El paciente no presentó molestias abdominales en el sitio del stent.
Discusión
El uso de endoprótesis intestinales fue probado en fístulas colocutáneas relacionadas con estomas por Nikfarjam et al.9 en dos pacientes, permitiendo limitar la contaminación fecal en la herida y el cierre de la fístula. Puig et al.15, de la Clínica Mayo, utilizaron endoprótesis para el manejo de fístulas y estenosis en anastomosis de cirugía bariatrica, lo cual permitió la remisión de la sepsis, mejorando el estado nutricional antes de la corrección quirúrgica definitiva.
En 2016, Melich et al.10 reportaron el control endoscópico de fístulas enterocutáneas mediante la intususcepción de dos stents a través de la misma fístula, permitiendo su cierre con resultados aceptables. Xu et al.16 reportaron un caso de fístula enteroatmosférica manejado con un stent impreso en 3D, obteniendo una reducción drástica en el gasto de la fístula y una recuperación rápida.
El uso de prótesis intestinales para la restitución del tránsito intestinal en pacientes seleccionados con fístula enterocutánea es un procedimiento de salvamento que puede ofrecerse después de un estudio minucioso por un equipo multidisciplinario, y es efectivo para la restitución rápida del tránsito intestinal, en el contexto de abdomen hostil, sin posibilidad de movilización de segmentos intestinales, cirugías de elongación o resección intestinal, siendo necesario en pacientes en quienes debe maximizarse el remanente de intestino funcional.
La colocación de endoprótesis permite iniciar la vía enteral, mejora la salud general del paciente y disminuye los requerimientos de nutrición parenteral y las complicaciones de esta17.
Rebibo et al.18 explicaron el uso de endoprótesis cubierta como tratamiento de la fístula enteroatmosférica asociada a ileostomía, mediante una técnica combinada endoscópica y de cirugía abierta, permitiendo el cierre de las fístula. Sin embargo, se necesitan más series de casos y un mayor número de pacientes para evaluar el riesgo-beneficio de este tratamiento.
Las indicaciones y los beneficios del uso de endoprótesis se resumen en la tabla 1. Los riesgos, las complicaciones y las consideraciones se resumen en la tabla 28,9,15,16.
Tabla 1 Indicaciones y beneficios de las endoprótesis en las fístulas enterocutáneas
| Indicaciones | Beneficios |
|---|---|
| Fistulas colocutáneas relacionadas con estomas | Aislamiento de la herida, favorece la granulación y el cierre por segunda intención |
| Control de la materia fecal (disminución de la carga bacteriana), disminución de infecciones | Inicio de alimentación enteral temprana, disminuye la translocación bacteriana, mejora la salud del enterocito |
| Abdomen hostil o congelado, o incapacidad de movilizar los intestinos | Técnica simple, reproducible y bien tolerada (endoscopista entrenado y equipo multidisciplinario) |
| Necesidad de suplementación oral | Capacidad de recolocación en caso de migración o falla en la colocación |
| Restitución del tránsito intestinal |
Tabla 2 Riesgos, complicaciones y consideraciones del uso de endoprótesis enterocutáneas para el manejo de fístulas
| Riesgos y complicaciones | Consideraciones |
|---|---|
| Fibrosis del segmento intestinal en contacto con la endoprótesis | Requiere fijación al tejido subcutáneo y la piel |
| Necesidad de resección del intestino fibrosado | Necesidad de disminuir la consistencia de las heces con laxantes o fibra para reducir el riesgo de migración y expulsión |
| Puede actuar como cuerpo extraño y alterar la curación | Necesidad de protección de la piel, para promover la granulación y el cierre de la fístula |
| Necesidad de seguimiento mensual con colonoscopia para detectar complicaciones tempranas | Una vez que el defecto se cierra, la endoprótesis debe retirarse. Puede resecarse el segmento intestinal o quitar la fijación y observación hasta su expulsión |
| Se recomienda al menos 2 meses de observación antes de tratar el retiro |
Conclusiones
El uso de endoprótesis para el control del gasto de fístulas enteroatmosféricas es controversial; sin embargo, se puede considerar como medida de salvamento en pacientes seleccionados, sobre todo en aquellos con altas posibilidades de muerte a causa de la fisiopatología de la fístula. Esto hace de las endoprótesis intestinales una medida aceptable para pacientes con esta patología. Se necesitan más series de casos tratados de esta manera y con un protocolo formal capaz de reproducir la técnica y evaluar el riesgo-beneficio.











 text new page (beta)
text new page (beta)