Introducción
La impresión en tres dimensiones (3D) incluye un grupo de tecnologías por medio de las cuales es posible generar objetos tridimensionales a partir de información binaria. Se trata de uno de los avances tecnológicos más significativos de la era moderna al que el desarrollo actual otorga un acceso industrial y masivo.1,2
La European Commission la ha considerado una tecnología disruptiva, considerando por tal a una innovación que modifica abruptamente la forma en la que actúan los consumidores y cómo se desarrollan la industria y los negocios.3 En estos casos los procedimientos de práctica habitual son dejados de lado por reconocer que los atributos de las nuevas opciones son claramente superiores.
Las aplicaciones de esta técnica en el campo de la medicina incluyen el diagnóstico, planificación quirúrgica, creación de guías intraoperatorias, implantes personalizados, entrenamiento quirúrgico, impresión de ortesis y prótesis y la bioimpresión.2,4
La práctica de la ortopedia y traumatología también ha sido alcanzada por esta revolucionaria herramienta. La posibilidad de replicar la anatomía en forma tridimensional en dispositivos electrónicos y poder imprimirlos otorga una posibilidad enorme para comprender las lesiones a tratar y planificar los procedimientos a llevar a cabo. El habitual proceso de transformación de imágenes complementarias bidimensionales en una representación tridimensional en nuestros cerebros puede ahora ser plasmado en imágenes manipulables en el espacio virtual y aún ser impresas y así agregar no sólo su percepción visual, sino también táctil. Además, es posible crear guías y herramientas quirúrgicas adaptadas a las características de cada modelo. Éstos se pueden utilizar para calcular volúmenes y tomar medidas 3D precisas.
Las herramientas individualizadas permiten al cirujano simular cirugías, medir con precisión osteotomías correctivas, planificar correcciones de fracturas, calcular el volumen de aloinjertos requeridos y muchas otras aplicaciones.
El objetivo de esta revisión es ofrecer un acercamiento a esta tecnología y sus principios básicos.
Historia
El origen de la impresión en tres dimensiones puede remontarse al inicio del arte de la escultura en la Edad de Piedra. El ser humano, al desarrollarse en un ambiente tridimensional siempre ha intentado reflejar esta realidad en distintos materiales.
En 1859 François Willème desarrolla en Francia la primera tecnología de escaneo en 3D que denomina «fotoescultura». A partir de fotografías tomadas en 360 grados a una persona u objeto, con la ayuda de un pantógrafo se dibujaban las siluetas del modelo a la escala deseada y se recortaban perfiles que, al sumarse, componían la escultura en tres dimensiones.
En 1892, Joseph Blanther patenta en Estados Unidos un sistema de creación de mapas topográficos en 3D utilizando un método de estratificación de principios similares a las impresoras actuales. Casi un siglo después, Hideo Kodama propone en Japón la creación de prototipos 3D a partir de la inyección de fotopolímeros que solidifican por acción de la luz ultravioleta. Sin embargo, el creador de la primera impresora 3D fue Charles Hull en 1984 en los Estados Unidos. Es considerado el padre de la impresión 3D.4 En 1988 lanzó al mercado la primera impresora 3D llamada SLA-250.1
Paralelamente surgieron otros métodos de impresión. A partir de 2007 se liberaron las patentes y se produjo una verdadera explosión de interés con respecto al tema. Se desarrollaron impresoras de código abierto, de bajo costo y con capacidad de autorreplicarse.
Las primeras publicaciones que hacen referencia a la utilización de esta tecnología en el campo de la salud aparecieron a principios del siglo XXI.5,6
Hay una evolución en las publicaciones de 2009 a 2011, cuando la simple impresión para planificación preoperatoria da paso a la impresión de herramientas quirúrgicas y finalmente de los propios implantes.7
Conceptos básicos y definiciones
Se utilizan como sinónimos o equivalentes de impresión 3D los términos: prototipado rápido y manufactura aditiva.1 Se denomina aditiva por crear los objetos sumando capas.
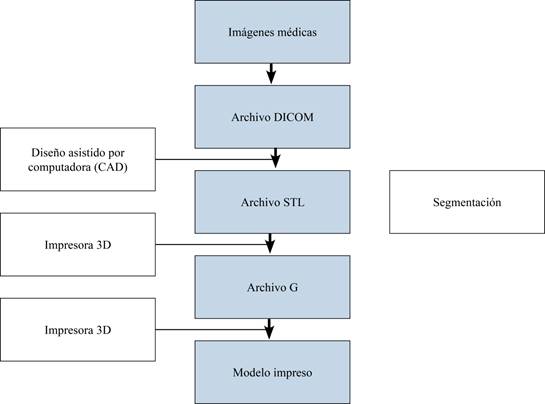
El proceso que termina en la creación de un modelo 3D tiene varias etapas (Figura 1).
1. Generación de las imágenes: el primer paso es la generación de las imágenes. Las mismas deberán cumplir requisitos mínimos de resolución y grosor de los cortes para poder ser procesadas. En el campo de la ortopedia y traumatología habitualmente se utilizan los estudios de tomografía computada, potencialmente también podrían utilizarse las imágenes de resonancia magnética, aunque tienen menos resolución.2
2. Transferencia de las imágenes: el siguiente paso del proceso es transferir la información de los archivos de imágenes médicas a nuestra computadora. Para lograr eso se utiliza el llamado lenguaje «DICOM». Éste es un protocolo estándar de comunicación entre sistemas de información y a la vez un formato de almacenamiento de imágenes médicas desarrollado por el American College of Radiology en asociación con la National Electrical Manufacturers Association de los Estados Unidos.
Este lenguaje permitió comunicar equipos heterogéneos entre sí mediante un protocolo común de trabajo, dando así un formato común de imágenes.
3. Procesamiento: a partir de la información obtenida en lenguaje «DICOM» es posible transformar las imágenes a un formato de archivo 3D. Éstos permiten almacenar en nuestras computadoras la información de las imágenes de manera que pueda ser leída y modificada por un programa de procesamiento 3D. La transformación y diseño de las imágenes se realiza con programas de diseño asistido por computadora. Éstos se conocen como CAD en inglés (computer aided design). Estos programas transforman el archivo original en STL. Un buen ejemplo de software CAD es el programa InVesalius® que puede ser descargado de manea gratuita de la red. Este tipo de programa permite transformar las imágenes en dos dimensiones de la tomografía computada, en un modelo tridimensional virtual, generando como resultado archivos STL que pueden ser impresos tridimensionalmente. El formato de archivo STL permite transferir el diseño asistido por computadora para ser impreso en 3D.1
El archivo STL no es el único, pero sí uno de los más usados por su simplicidad. STL corresponde a las siglas de Surface Tessellation Language (lenguaje de superficies de teselas) o también Standard Triangle Language (lenguaje estándar de triángulos). En el primer caso hace referencia a las teselas o mosaicos con los que se representa la superficie del objeto, en el segundo caso se refiere a la forma triangular de los mismos. El resultado es una malla de triángulos que permite definir la superficie y forma de un objeto. Cuanto de menor tamaño son los triángulos o teselas de esa malla, mayor será la resolución del objeto y mayor el peso del archivo.
Uno de los pasos esenciales del procesamiento de imágenes es la «segmentación», consiste en separar las estructuras anatómicas de interés de las estructuras circundantes y de cualquier otra imagen que no sea significativa. Por ejemplo, en el caso de una fractura de clavícula removeremos las partes blandas circundantes, omóplato, esternón y el húmero.
4. Postprocesamiento: el formato STL define la geometría de objetos, pero a diferencia de otros tipos de archivo no incluye detalles de color, textura o propiedades físicas. Es un formato adecuado para realizar un prototipado rápido, lo que es definido como el grupo de técnicas que permiten fabricar un modelo a escala. Si el objetivo es evaluar las imágenes en forma tridimensional en la computadora es suficiente, pero si se pretende imprimir el modelo en tres dimensiones o utilizarlo en una simulación de elementos finitos, será necesario realizar un paso adicional llamado «postprocesamiento».
Para este paso es necesario contar con otro programa, como por ejemplo el MeshMixer®, que también puede ser descargado gratuitamente de la red. Ha sido descripto como un cortaplumas suizo que contiene una serie de herramientas que permiten hacer el acabado final del modelo. Estas funciones incluyen la edición, reparación e incluso el análisis de la viabilidad de impresión del modelo.
Al final de esta etapa se podrán tomar medidas al modelo e incluso realizar cirugías virtuales como la planificación de osteotomías o la fijación de fracturas con osteosíntesis. Se podrán crear guías y herramientas específicas para cada caso. También se podrán realizar comparaciones con el lado contralateral sano cuando sean de utilidad.
5. Impresión: el paso final, cuando sea necesario, será la impresión del modelo. En este caso se tendrá una visión tridimensional más clara y se agregará la sensación táctil. Además, disponer del modelo impreso tiene una gran utilidad educativa y en la transmisión de información a los pacientes.
Si el modelo o las guías van a ser esterilizadas para su uso intraoperatorio, se deberá tener especial atención al tipo de material a utilizar y si éste tiene registro sanitario para ser usado en cirugía.
La impresora 3D interpreta las coordenadas proporcionadas digitalmente en el archivo STL y lo convierte en un archivo llamado G. Divide en una secuencia de cortes transversales horizontales en dos dimensiones de entre 25 a 100 μm, según la técnica utilizada. El objeto será impreso en capas consecutivas comenzando por la base, reconstruyéndolo a partir de una serie de capas de dos dimensiones. De esta manera se imprime una réplica exacta del objeto original.1
La calidad del software utilizado y de la impresora influirán en las características del producto final. La esterilización puede alterar las propiedades de los modelos pudiendo modificar el tamaño de una guía de corte impresa e influyendo en la posición de una osteotomía calculada en la computadora. Estos factores deben ser considerados y previstos.
Otra variable a tener en cuenta es el tiempo de impresión, que variará según el volumen y orientación del modelo y la resolución de la impresora.2 El volumen varía según el «relleno» que se defina para el objeto a imprimir.
Tipos de impresoras 3D
Existen dos tipos de tecnologías para crear un objeto: la sustractiva y la aditiva. En el primer caso, el material innecesario es extraído por la impresora remedando la labor de un escultor que trabaja sobre un bloque de piedra hasta obtener la escultura final. La tecnología aditiva, en cambio, se caracteriza por sumar capa sobre capa. El mecanismo más frecuentemente utilizado en la planificación operatoria es el aditivo por ser más barato y rápido (Tabla 1).
Tabla 1: Comparación de impresoras por estereolitografía y deposición fundida.
| Impresora | Calidad de impresión | Velocidad de impresión | Costo de impresión | Utilidad |
|---|---|---|---|---|
| Estereolitografía | Alta | Lenta | Alto | Producción en masa. Creación de moldes |
| Modelado por deposición fundida | Intermedia | Rápida | Bajo | Planificación preoperatoria |
Existen tres grandes mecanismos de funcionamiento de las impresoras aditivas:
1. Estereolitografía (SLA): primer método que se creó. Se aplica luz ultravioleta a una cubeta que contiene resina. La luz es controlada por una computadora y va polimerizando la superficie de la resina en la cubeta dando forma al objeto. Por medio de un pistón que desciende, se va exponiendo más resina a la luz y se van creando las distintas capas sucesivas.
2. Sinterización selectiva por láser (SSL): sinterizar implica fabricar objetos mediante el prensado de polvos u otras materias que previamente han sido calentadas sin llegar a la fusión. También se aplica una luz ultravioleta, pero en este caso actúa sobre un polvo, en lugar de hacerlo sobre resina líquida. Se produce una adición por capas solidificando al material.
3. Modelado por deposición fundida (MDF): en este caso el material utilizado es un filamento de plástico que pasa por una resistencia en una boquilla que lo calienta por encima de los 200 oC4 y lo funde para depositarlo sobre una plataforma móvil. Esta tecnología es más sencilla y accesible. Se puede hacer un símil en su forma de funcionar con una manga de repostería en la que el material es expulsado por la presión de las manos del operador y el movimiento de estas genera las formas. En este caso la impresora 3D tiene un extrusor y motores que van determinando la movilidad de éste y de la superficie sobre la que cae el material (cama), haciendo que la deposición del material genere la forma deseada en cada capa.
Aplicaciones en ortopedia y traumatología
La ortopedia y traumatología es uno de los campos de la medicina en los que mayor impacto ha tenido la planificación 3D, en especial en trauma y ortopedia oncológica.8,9
El análisis de la literatura ortopédica pone en evidencia un gran incremento en las publicaciones sobre el tema.8,10 El uso más común es en planificación preoperatoria seguido por el diseño de implantes y de guías personalizadas.8 Los materiales de impresión 3D más utilizados fueron titanio, acrilonitrilo butadieno estireno y ácido poliláctico.8
Las aplicaciones y ventajas más importantes de esta tecnología en el campo de la ortopedia y traumatología son:
1. Planificación preoperatoria: la planificación preoperatoria es un paso esencial en el proceso quirúrgico. La impresión 3D permite lograr un planeamiento preoperatorio con un grado de precisión que no es posible con instrumentos convencionales.11 Así en el caso de una fractura podremos planificar la reducción de ésta y trasladar las habilidades a la práctica quirúrgica (Figura 2).
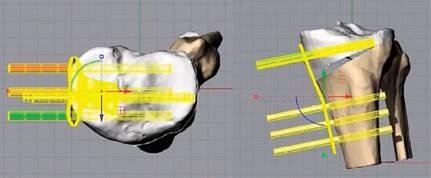
Figura 2: Utilización de planificación 3D para una osteotomía de rodilla. Posicionamiento de la placa y evaluación de posibles ingresos de tornillos.
Se ha demostrado la capacidad de la impresión 3D para representar distintos segmentos del esqueleto. La comparación de imágenes de tomografía computarizada (TC) de vértebras cervicales, torácicas y lumbares contra sus respectivos modelos impresos demostró una fuerte correlación anatómica.12
Izatt y colaboradores13 buscaron cuantificar las percepciones del cirujano sobre la utilidad de los biomodelos en comparación con las modalidades de visualización estándar para la planificación. Se incluyeron 26 casos consecutivos de deformidades y tumores raquídeos. Los cirujanos afirmaron que los detalles anatómicos eran más visibles en el biomodelo que en otras modalidades de imagen en 65% de los casos y visibles exclusivamente en el biomodelo en 11% de los casos. El uso de planificación preoperatoria 3D llevó a una diferente elección de materiales de osteosíntesis en 52% de los casos y del lugar de implante en 74% de los mismos.13
Se han demostrado también las ventajas de la planificación 3D en el tratamiento de tumores cervicales,14 artroplastías de rodilla15,16 y fracturas de extremo proximal de húmero,17 entre otras indicaciones de cirugía.
2. Guías y herramientas personalizadas: la planificación quirúrgica asistida por computadora, combinada con instrumentación específica para el paciente (IEP), es una nueva y poderosa tecnología que tiene el potencial de mejorar la precisión y eficacia de la cirugía ortopédica. Se pueden generar guías de corte, guías de implante de clavijas y dispositivos de alineación entre otras herramientas.4
La osteotomía correctiva mediante estas herramientas logró una corrección precisa y una buena recuperación funcional en la extremidad superior.18
La instrumentación específica de componentes glenoideos en la artroplastía reversa de hombro permite que sea ejecutada con mayor precisión.19
Cuando se utilizaron guías en reconstrucciones del escafoides carpiano las mismas fueron significativamente más anatómicas en comparación con las resultantes de la técnica a mano alzada.20
Buller21 utilizó guías específicas en huesos plásticos para simular el fresado y posicionamiento de componentes acetabulares en artroplastías totales de cadera. Logró 9 grados menos de variación en la orientación de los componentes, incluso en cirujanos de gran experiencia.
En lo que respecta a fracturas de pelvis, la técnica informada con más frecuencia utiliza dos modelos óseos impresos en 3D, uno del acetábulo fracturado y otro del contralateral sano. La réplica a gran escala de la fractura pélvica proporciona una impresión táctil precisa del volumen, tamaño y orientación de los fragmentos óseos. Con un conocimiento más profundo de la configuración de la fractura, se planifican la mejor técnica de reducción, el abordaje quirúrgico y las trayectorias óptimas de los tornillos.22 El modelo en espejo de la hemipelvis intacta opuesta es invaluable para premoldear las placas de osteosíntesis con precisión.23
En una serie de 11 osteotomías informadas por Gouin24 para la resección de tumores pélvicos, la colocación de guías personalizadas determinó una menor disección de tejidos blandos al momento de identificar el punto de la osteotomía.
También se reportaron buenos resultados en osteotomías de tibia,25 artroplastías de rodilla16 y la reconstrucción con aloinjertos en tumores de rodilla.26
3. Incremento de la precisión quirúrgica: Cabarcas y colaboradores27 demostraron en un estudio cadavérico aleatorizado que el uso de instrumental específico en artroplastías de hombro incrementó la precisión en la inserción del pin glenoideo en comparación con las guías estándar. En otro estudio, 46 pacientes con artrosis glenohumeral avanzada fueron asignados aleatoriamente a plantillas preoperatorias de tomografía computarizada tridimensional con instrumentación estándar o con instrumentación específica y se compararon con un grupo de 17 pacientes con imágenes bidimensionales e instrumentación estándar utilizados como control.28 Usando imágenes tridimensionales y plantillas con o sin instrumentación específica para el paciente, hubo una mejoría significativa en el posicionamiento del implante en comparación con imágenes bidimensionales e instrumentación estándar.28
Jacquot y colaboradores29 reportaron que la planificación preoperatoria 3D permitió un posicionamiento preciso del componente glenoideo con un método de implante a mano alzada mejorando ligeramente la posición del punto central, en pacientes con retroversión glenoidea severa.
También se han demostrado ventajas en el manejo de consolidaciones viciosas del miembro superior30,31,32,33,34,35,36 y el implante de tornillos pediculares para fijación cervical.37
Es muy importante tener en cuenta que las tecnologías de impresión 3D y navegación por computadora se pueden complementar fácilmente, ya que los modelos digitales 3D en formato STL se transfieren fácilmente entre sistemas. Chen38 reportó que la precisión en la fijación de implantes específicos en cirugía de reconstrucción de tumores pélvicos mejora de tres a cinco veces en comparación con la instalación de implantes sin navegación después de una osteotomía con planificación 3D.
4. Reducción de tiempo quirúrgico: una mejor comprensión de la lesión a tratar, el planeamiento preoperatorio y la posibilidad de contar con herramientas personalizadas redundarán en un acortamiento del tiempo quirúrgico.9,39,40,41,42,43,44,45,46,47,48
Se han reportado reducción de los tiempos de fijaciones cervicales,39,40 fracturas complejas de tibia,41,42 fracturas de calcáneo,43 fracturas de pelvis44 y húmero distal.48
Un estudio comparativo sobre fijación de tornillos pediculares lumbares no encontró diferencias significativas en la precisión de inserción de éstos, pero sí en la reducción del tiempo quirúrgico.45
5. Reducción de la exposición a rayos: se ha comprobado con el uso de planificación 3D en cirugías de muñeca y mano,34 inserción de tornillos pediculares a nivel cervical,40 fracturas complejas de tibia,41,42 fracturas de calcáneo43 y fracturas de pelvis.44
6. Reducción de pérdida de sangre: se ha reportado una reducción de pérdida sanguínea perioperatoria gracias a estas técnicas en cirugías de fracturas pelvianas,23,44 intertrocantéricas,47 de platillo tibial,41 de pilón tibial,42 de calcáneo43 y de húmero distal.48
7. Educación médica: los alcances de esta tecnología en formación médica son promisorios.49,50 Se han reportado buenos resultados con el uso de guías de perforación impresas en 3D en un entrenamiento cadavérico de residentes en laminoplastías expansivas.49
8. Información a pacientes: los pacientes y sus familiares han tenido un alto grado de satisfacción con el empleo de modelos 3D en la comunicación sobre fracturas de pilón tibial42 y fracturas trimaleolares de tobillo.51 También se ha utilizado con éxito en el proceso de consentimiento informado en artrodesis lumbares.45
9. Disminución de costos: si bien el uso de tecnología 3D implica gastos adicionales, se ha calculado que 10 minutos ahorrados en el quirófano equivalen en términos monetarios a una hora invertida en la preparación de un sistema de guiado.52
10. Diseño de implantes específicos: los implantes disponibles comercialmente no siempre coinciden con la anatomía del paciente. La impresión tridimensional fomenta el avance de la personalización quirúrgica.
Esta tecnología permite extraer parámetros de la geometría 3D de la anatomía ósea del paciente y luego crear un implante a medida. Un buen ejemplo es el diseño de implantes de cadera.53 También se ha demostrado su utilidad en defectos óseos complejos, deformidades y artrodesis de pie y tobillo.54
Placas de osteosíntesis impresas en 3D pueden corregir con éxito las deformidades del hallux valgus y permitir que los pacientes vuelvan a actividades más rápidamente.55
11. Bioimpresión: la «biofabricación» es el proceso por el cual se obtiene como resultado un producto con función biológica.56 En el ámbito de la medicina implica la producción automatizada de tejidos y órganos. Integrando tecnologías biológicas y de ingeniería, la construcción de estructuras biocompatibles ha facilitado el acceso a tejidos de trasplante autólogo. En el campo de la ortopedia y traumatología podría permitir a futuro la creación de tejidos para corregir pérdidas a consecuencia de traumas, resección de tejidos tumorales o defectos congénitos.
El rol de la impresión 3D sería el de crear «andamios» a partir de un biomaterial determinado a los que se podrían agregar moléculas biológicas como factores de crecimiento o antibióticos e incluso células extraídas del mismo paciente.57 Se está desarrollando, por ejemplo, la impresión 3D de discos intervertebrales.58
Limitaciones
Tenemos el privilegio de vivir el comienzo de una nueva era que tendrá un efecto equivalente al advenimiento de la radiología en el campo de nuestra profesión.4 Sin embargo, todavía existen múltiples limitaciones que impiden el uso generalizado de la impresión 3D en el entorno intraoperatorio. A medida que las aplicaciones ortopédicas de la impresión 3D continúan desarrollándose, es importante una evaluación crítica de las mismas.
Si bien el proceso está cada vez más optimizado y simplificado por los avances en software y automatización, es una técnica que requiere un entrenamiento adecuado. Se ha mencionado la necesidad de una curva de aprendizaje importante en el caso de los modelos de pie y tobillo.59
La mayoría de los datos hasta ahora provienen de estudios de baja calidad con inherentes sesgos vinculados con el entusiasmo por una técnica novedosa.60 En algunos procedimientos aún no se han podido demostrar ventajas significativas debido al tamaño limitado de las muestras. Se necesitan estudios de alto nivel de evidencia para evaluar los beneficios potenciales de la impresión 3D.8
La técnica demostró una alta precisión en la realización de osteotomías en cuña substractiva en los huesos del antebrazo. Sin embargo, para las osteotomías aditivas las correcciones finales fueron menos precisas.33
Aunque de gran utilidad, las guías personalizadas no pueden ayudar de manera confiable en la reducción de fracturas, que todavía es principalmente una técnica manual. En un estudio sobre fracturas de mano no se pudo demostrar su superioridad sobre las técnicas convencionales.61 En el caso de la inserción de tornillos intrapélvicos la relativa dificultad para alcanzar puntos de referencia óseos más profundos hace que el uso de guías personalizadas sea menos favorable en comparación con la navegación percutánea por computadora y la guía fluoroscópica.62 En la cirugía real, la colocación de las guías sobre el hueso suele requerir una exposición algo más amplia que en los estudios cadavéricos. En la mayoría de los casos, en el quirófano las estructuras de tejidos blandos bloquearán la visión al intentar verificar el ajuste óptimo de las guías.63 De la misma manera, la presencia de elementos nobles hará mucho más complicada su utilización in vivo.
Es evidente que se ahorra tiempo quirúrgico, pero el procesamiento de imágenes y la impresión pueden llevar varias horas previamente a la cirugía.46
Los costos adicionales que puede generar la impresión 3D son también motivo de preocupación, en especial en la salud pública. De todas maneras, los costos han disminuido drásticamente en los últimos años.64
A pesar del desafío de la viabilidad, se justifica un ensayo de gran magnitud para obtener conclusiones definitivas con respecto a las ventajas clínicas de esta tecnología avanzada pero también más cara.65 Mientras tanto, lo ideal es limitar el uso de esta tecnología a casos complejos que impliquen un difícil manejo quirúrgico (Figura 3).
Perspectivas en América Latina
La medicina ha incorporado una serie de herramientas que hace una generación hubieran sido impensables. Instrumentos como big data, las historias clínicas electrónicas, la inteligencia artificial, machine learning, deep learning y la planificación e impresión 3D permiten un mejor manejo y análisis de la información para desarrollar una atención de la salud personalizada y de precisión.
Acceder plenamente a la innovación tecnológica es un desafío para América Latina, si bien el acceso a la tecnología 3D se ha hecho más amplio en los últimos tiempos, la aplicación de ésta podrá variar de acuerdo con la disponibilidad en cada país de los programas que dependan de empresas comerciales de nuestra especialidad. La alternativa es respaldarse en los programas de acceso gratuito, involucrarse en todo el proceso desde la planificación a la impresión y crear redes que permitan la interacción de profesionales con distintos niveles de experiencia. Consideramos que la etapa de residencia es el momento clave para comenzar con la enseñanza y aplicación de la planificación 3D. Las impresoras 3D se autorreplican y su precio es cada vez más accesible.
No se trata sólo de un reto para los jóvenes, también dependerá de aquéllos que ocupan posiciones directivas y tienen la responsabilidad de enfrentar este desafío incorporando esta nueva tecnología a los programas educativos en todos sus niveles. De esta manera, América Latina no quedará afuera de esta revolución tecnológica que cambiará nuestra práctica asistencial irreversiblemente.











 nova página do texto(beta)
nova página do texto(beta)