INTRODUCCIÓN
La urea ha sido esencial para todos los cultivos por su alto contenido de nitrógeno (N: 46%). Este elemento es de vital importancia en el crecimiento y desarrollo de las plantas y necesario para obtener rendimientos adecuados (Fageria y Baligar 2005). Sin embargo, el nitrógeno (N) es un elemento inestable; que se puede perder por lixiviación y volatilización antes que la planta lo absorba, lo que reduce el potencial de rendimiento y calidad de los cultivos (Ortiz y Venialgo 2017, Guha et al. 2020). Asimismo, tiene un efecto contaminante, que se produce por la emisión de gases de efecto invernadero con la liberación del NO2, principal contaminante antropogénico de la fertilización nitrogenada (Tasca et al. 2017, Wu et al. 2018).
En años recientes, la investigación se ha centrado en mejorar la eficiencia del N en los campos agrícolas (Mukerabigwi et al. 2015). El uso de sistemas de liberación prolongada (SLIP) y controlada, se vienen desarrollando como una alternativa para evitar las pérdidas de N en el suelo (Azeem et al. 2014). Estos sistemas SLIP son formulaciones que contienen un nutrimento vegetal en forma tal que retrasa su disponibilidad para la planta después de la aplicación; o permite su liberación prolongada por un periodo de tiempo mayor que un fertilizante de rápida disposición como son nitrato y fosfato de amonio, entre otros. Por lo que el desarrollo de fertilizantes de urea encapsulada o recubierta con azufre, o urea con polímeros; de liberación ya sea lenta o prolongada, ha tenido buenos resultados en los campos agrícolas (Yamamoto et al. 2016).
El encapsulamiento o recubrimiento es un proceso en donde pequeñas partículas que contienen un agente activo son rodeadas por un recubrimiento para formar una cápsula. Ello permite la protección del agente activo contra agentes externos, además de proporcionar disminución en la tasa de liberación (Gamboa et al. 2011). La mayoría de los materiales encapsulantes son polímeros orgánicos obtenidos a base de subproductos agrícolas como: proteínas, almidón, celulosa y quitosano apropiados para su uso como encapsulamiento (Dima et al. 2015). Estos materiales son 100% naturales, biodegradables, de bajo costo y altamente disponibles; característica necesaria para evitar la contaminación del suelo y obtener un sistema de liberación a bajo costo (Blomfeldt et al. 2011).
El gluten de trigo (GT) es un polímero natural que posee dichas características y está compuesto por proteínas de bajo y alto peso molecular: gliadinas (28 000 - 35 000 Da) y glutaminas (70 000 hasta >10 millones de Da) (Scherf et al. 2016). Ambas proteínas han sido investigadas por su uso en la preparación de materiales encapsulantes a nanoescala y microescala, así como con alto potencial de aplicación en la agricultura (Castro-Enríquez et al. 2012, Barreras-Urbina et al. 2018). Por lo anterior, el objetivo del estudio fue caracterizar y analizar un sistema de liberación prolongada de urea en polvo como alternativa sustentable para utilizarse en la agricultura.
MATERIALES Y MÉTODOS
Diseño del SLIP de urea en polvo
Para la elaboración del SLIP se empleó gluten de trigo (GT) comercial de la marca Rockette® y urea (46%). El SLIP se elaboró de acuerdo con la metodología descrita por Fessi et al. (1989) y Barreras-Urbina et al. (2018) con modificaciones para aplicarse en polvo. Primero, se preparó urea 1 Molar (M) (60.06 g de urea en 1.0 L de agua destilada) de la cual se añadió 1.0 mL a 0.55 g de GT en polvo. Se mezcló con espátula y se amasó de forma manual hasta formar una pasta. Posteriormente se congeló a -50 oC en un ultracongelador y se liofilizó. La pasta liofilizada se maceró en un mortero hasta obtener un polvo homogéneo que se guardó a temperatura ambiente hasta su caracterización.
Microscopía electrónica de barrido
Se pesó 1.0 g del SLIP y se colocó en un equipo de microscopía electrónica de barrido JEOL 5410 LV operado a 20 kV, para observar las estructuras superficiales e internas, morfología, porosidad, tamaño de fibras, gránulos y poros.
Análisis de espectroscopia infrarroja por transformada de Fourier
Se analizaron muestras de 5.0 mg del SLIP en un equipo infrarrojo Perkin Elmer, modelo Spectrum Two. Las corridas se realizaron entre 4000 y 500 cm -1 con un accesorio de reflectancia total atenuada (ATR) con cristal de diamante. Se observaron las estructuras de los compuestos y puentes de enlaces de hidrógeno que se formaron entre los mismos.
Análisis termogravimétrico
Se pesaron 3.0 mg de SLIP y se analizaron en un equipo Perkin-Elmer TGA, Modelo Pyris 1, en una atmósfera de N con un caudal de 30 ○C por minuto hasta alcanzar los 600 ○C. Posteriormente, se midió la estabilidad térmica de los compuestos y la temperatura de degradación de los materiales utilizados en la elaboración del SLP.
Evaluación de la liberación prolongada de urea en agua
El polvo de SLIP se disolvió en un vaso de precipitado con 1.0 L de agua destilada, en pH 7, a 25 ○C con agitación magnética (IKA C-MAG HS7) a 110 rpm. La urea liberada se determinó a los siguientes tiempos: 0, 5, 10, 20, 25, 30 y 60 min, también a las 2, 4, 6, 8, 10, 12, 24, 36, y 48 h. En cada tiempo, se tomaron 10 µL del medio acuoso y se reemplazaron con otros 10 µL de agua destilada de acuerdo con Gulfam et al. (2012). En cada muestra se cuantificó la concentración de urea liberada en el medio con kit de Randox (Patton y Crouch 1977), en un equipo de espectrofotometría UV-vis, VARIAN modelo Cary 50.
El reactivo 1 (R1) se preparó añadiendo enzima ureasa (≤ 5000 U L -1) y el reactivo (R1b,) formado por los buffers fosfato (salicilato de sodio: 63.4 mmol L -1, nitroprusiato de sodio: 5.00 mmol L-1 y suero EDTA: 1.5 mmol L -1). Aleatoriamente, se prepararon tres viales: en el primero se agregaron 1000 µL de R1 que se utilizó como testigo, en el segundo 10 µL del patrón incluido en el kit más 1000 µL de la R1 que se mezclaron para formar la muestra estándar, y al tercero se le agregaron 10 µL de la muestra con 1000 µL de R1 y se mezclaron. Los tres viales se incubaron durante 5 min a 25 ○C y después se les añadieron 200 µL del reactivo R2 (Hipoclorito Sódico: 18 mmol L -1). Las tres muestras obtenidas se incubaron durante 10 min a 25 ○C. Finalmente, se midió la absorbancia por triplicado a cada muestra a longitud de onda de 695 nm.
Con las absorbancias y la curva de calibración de la urea obtenida, se determinó la concentración con las que se elaboró la curva de liberación en la que se determinó el punto máximo de difusión de la urea liberada en el tiempo. Los datos obtenidos se analizaron mediante estadística descriptiva.
RESULTADOS Y DISCUSIÓN
Se obtuvo un polvo homogéneo con tamaño de partículas de 2 mm aproximadamente, por lo que es viable para aplicarse como SLIP. El tamaño favorece la distribución uniforme en campo, lo que puede maximizar la eficiencia del uso del fertilizante, reducir el tiempo y la necesidad de energía de aplicación (Rodríguez-Félix et al. 2012, Dórame-Miranda et al. 2018). Las micrografías del GT comercial y del SLIP se muestran en la Figura 1. Para el SLIP se muestran ampliaciones de 350 y 750x, en las Figuras 1 b y 1c, respectivamente. En las micrografías SEM de la Figura 1a se observa una estructura aglomerada, no porosa y de superficie lisa, así como, la presencia de gránulos densos y compactos con estructuras irregulares. Éstos se componen de gránulos pequeños en su superficie, lo cual se debe a la interacción conformacional de las proteínas gluten, gluteninas y gliadinas (Robles-García et al. 2014). Con la Figura 1b, se observa la porosidad de su superficie, que varían de 18.8 µm a 187.8 µm de diámetro. Estas estructuras ofrecen ventajas, debido a que proporcionan la capacitad de liberar de forma lenta y adecuada el fertilizante (Shi et al. 2014, Hao et al. 2015), lo que aumenta la eficiencia del nitrógeno y corrobora su potencial de aplicación como SLIP en condiciones campo (Bruinink et al. 2015, Davidov-Pardo et al. 2015). Mientras que en las Figuras 1 b y 1c, no se observa la presencia de fibras.
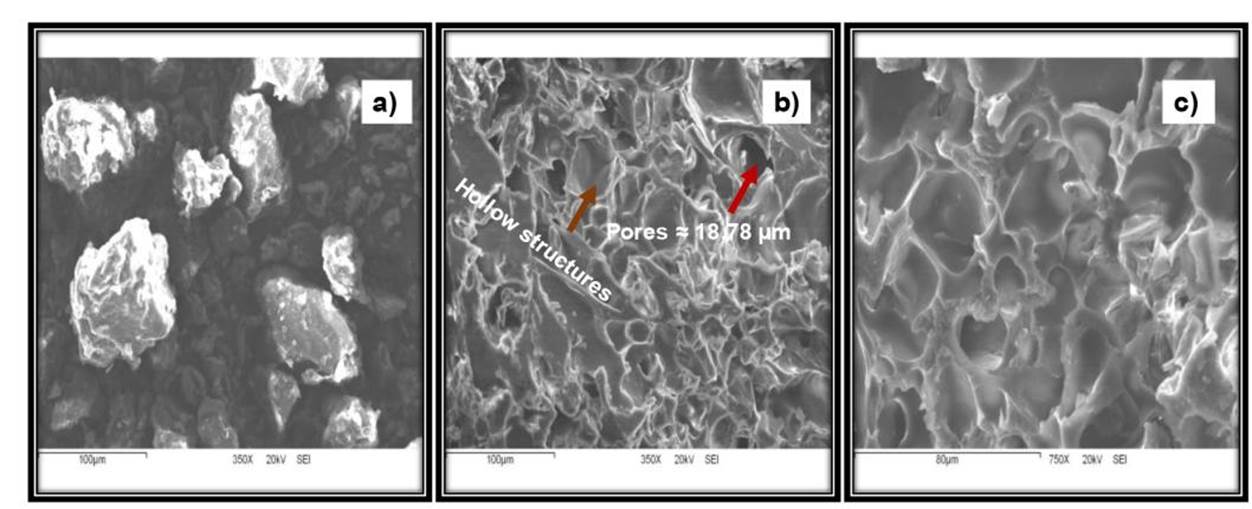
Figura 1 Micrografías SEM de los materiales evaluados: (a) polvo de gluten de trigo (wg), (b y c) superficie del polvo del SLIP.
La espectroscopia FT-IR (Figura 2), indica un espectro FT-IR del polvo de urea en la banda característica del estiramiento del enlace N-H de la amida primaria, la cual está compuesta por dos picos que corresponden a la vibración del enlace N-H de la amida primaria a 3 425 y 3 318 cm -1. Además, presenta una banda de intensidad media a 1 676 cm -1, que corresponde al grupo carbonilo (C = O). Para el polvo de gluten (5b), se observó una banda de media intensidad a 3292 cm -1 atribuida al estiramiento de los enlaces O-H de los aminoácidos presentes en las proteínas del gluten de trigo; con una banda de intensidad media de 2 925 cm -1, que corresponde al estiramiento del grupo - CH2 -. Asimismo, otras dos bandas de intensidades medias a 1 635 cm -1 asociada con la vibración de la banda frecuencia de la amina I; esta banda está relacionada con el estiramiento vibracional del grupo carbonilo C = O, que se observa traspalada detrás de la banda. La segunda banda de 1 520 cm -1 está relacionada con la frecuencia vibratoria de la banda de la amina II, que corresponde a la deformación del grupo N-H. En el polvo compuesto por gluten cargado con urea (5c), se observó la banda característica de una amida primaria en la misma región del espectro del polvo de urea, con intensidad media de 3 428 cm -1, lo que indica que la urea está presente en el producto elaborado. Además, se presenta una banda de intensidad media correspondiente al grupo carbonilo (C = O) de 1 671 cm -1, misma que también se observó en la urea y en el polvo de gluten. La descripción de estas bandas corresponde con los resultados reportados por Castro-Enríquez et al. (2012) y Barreras-Urbina et al. (2018), quienes evaluaron micropartículas de gluten cargadas con urea elaboradas con las técnicas de electrospray y nanoprecipitación. También, se observaron cambios en la posición de la banda de 5 cm -1 para la urea y de 41 cm -1 para las proteínas; lo que se puede atribuir a una posible interacción producida por los enlaces de hidrógeno entre el grupo amino de las proteínas y el grupo carbonilo de la urea y entre el grupo amino de la urea y el grupo carbonilo de las proteínas (Irissin-Mangata et al. 2001). Al respecto, Tapia-Hernández et al. (2018) reporta que hay una fuerte interacción del enlace formado por los puentes de hidrógeno de la urea y el gluten, lo que indica que las partículas de la urea se adhieren a las partículas del gluten, lo que permite que la urea no se libere de forma rápida una vez entre en contacto con el medio acuoso.
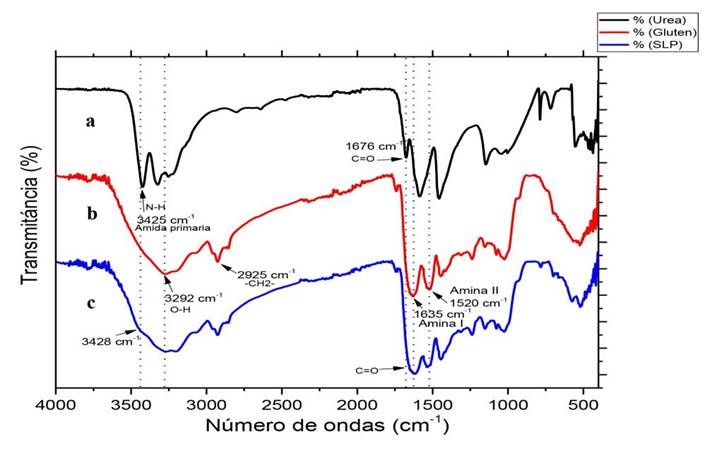
Figura 2 Análisis de los espectros de FT-IR de los materiales evaluados: a) urea, (b) polvo de gluten, (c) SLIP en polvo.
El análisis termogravimétrico (TGA) se muestra en la Figura 3. Mientras que en la Tabla 1 se muestran los porcentajes de pérdida de peso a diferentes temperaturas de la urea, gluten y polvo SLIP. La urea presento estabilidad a los 140 ○C y, a partir de ahí comenzó su degradación, presentando la mayor pérdida de peso (77%) a los 215 ○C y completándose su degradación a los 600 ○C. Al respecto, Mathrmool et al. (2014), reportan que la pérdida de peso de la urea está dada en tres etapas, la primera relacionada con la descomposición de la urea para producir ácido isociánico de amonio (HNCO), que va de los 140 a los 215 0C de temperatura, siendo la mayor pérdida de peso. Para luego evaporarse el amoniaco y el gas causado, debido a hidrólisis del HNCO, lo que corresponde a la segunda pérdida de peso que ocurre a partir de 215 a 308 0C. Para al final producir la reacción química de las materias primas, la cual se relaciona con la última pérdida de peso y la degradación total. En el presente estudio se observó que el GT y el SLIP comenzaron su degradación a los 100 ○C, lo que se atribuye a la primera pérdida a la humedad, lo cual pudo estar relacionado con el proceso de secado de estas muestras antes del análisis. El polvo de GT presentó la mayor pérdida de peso entre 24 y 100 0C, en general la mayor pérdida de peso de la urea fue del 7% y del SLIP de 5% en el mismo rango de temperaturas. También se observó que el polvo de gluten tuvo una pérdida de peso del 55% entre los 253 y 367 ○C, mientras que a los 600 ○C su degradación fue del 73%. Esta pérdida puede atribuirse a la descomposición de los carbohidratos y polisacáridos presentes en el compuesto (Li et al. 2006).
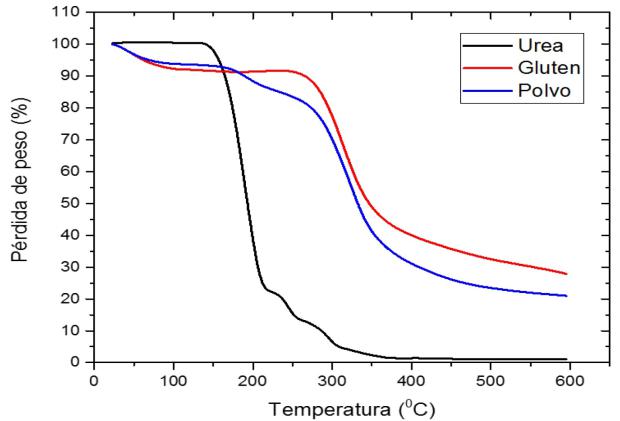
Figura 3: Análisis termogravimétrico (TGA) de los materiales evaluados: (a) urea, (b) polvo de gluten y (c) SLIP en polvo.
Tabla 1 Descripción de la estabilidad térmica (TGA) de los materiales evaluados: (a) urea, (b) polvo de gluten y (c) SLIP en polvo.
| Muestras | Análisis Termogravimétrico (TGA) | |
| Temperatura ○C | Pérdida de peso % | |
| 140 - 215 | 77 | |
| Urea | 215 - 254 | 85 |
| 254 - 308 | 95 | |
| 308 - 600 | 100 | |
| 24 - 100 | 7 | |
| Gluten | 246 - 367 | 55 |
| 367 - 600 | 73 | |
| 24 - 100 | 5 | |
| SLP | 100 - 204 | 15 |
| polvo | 204 - 358 | 63 |
| 358 - 600 | 79 | |
Para el SLIP, se observó estabilidad del peso en un 15%, al alcanzar temperaturas entre 100 y 204 ○C. Posteriormente, continuó su degradación hasta en un 63% del peso entre los 204 y 358 ○C, y se completa su degradación en un 79% a los 600 ○C. Por otra parte, el 27% del peso del polvo de gluten y el 21% del peso del polvo compuesto por gluten cargado con urea no se degradó. Para el sistema en polvo se observa que la urea comienza a degradarse de los 204 hasta los 600 ○C, en un 63% aproximadamente. Lo que difiere de lo reportado por Castro-Enríquez et al. (2012), quienes observaron una pérdida de peso del 19%, en temperaturas entre 117 y 207 oC; atribuyéndolo a la degradación de la urea. Mientras que en el presente estudio se observó que la urea comenzó su degradación a los 200 ○C, lo que indica mayor estabilidad del SLIP obtenido bajo altas temperaturas.
Para la cinética de liberación prolongada de urea en agua (Figura 4), se observa que la liberación de la urea ocurre durante los primeros 60 min, con liberación rápida de los 5 a los 10 min del 38% de la concentración original, lo que puede atribuirse a un efecto de estallido (Mulder et al. 2011). La liberación rápida puede deberse a las partículas de urea que quedaron desprendidas en el polvo, debido al proceso mecánico al que fue sometido, así como a las partículas de urea que se encuentran sobre la superficie de la matriz polimérica que son las primeras en liberarse al entrar en contacto con el medio acuoso. Para continuar con una tasa de liberación lenta durante el transcurso del tiempo. Resultados similares fueron obtenidos por Castro-Enríquez et al. (2012), quienes observaron una liberación rápida de la urea en los primeros 10 min en membranas de GT cargadas con urea con equilibrio de liberación a las 5 h con un 98% de urea liberada. La continuidad de la liberación (Figura 4b) indica una liberación lenta y gradual del fertilizante con respecto al tiempo, ocurriendo durante la primera hora una liberación lenta y gradual, para alcanzar el equilibrio de fusión en un 86.35% de liberación total a las 36 h Al respecto, Barreras-Urbina et al. (2018) con micropartículas de proteínas de trigo y gluten solubles en etanol, reportan una liberación aproximada del 50% de la urea durante la primera hora y el equilibrio de difusión a las 12 h con el 88% de la liberación total. Sobre lo mismo Bird et al. (2002) reportan que el equilibrio de difusión de la urea se alcanza cuando su concentración en el producto es igual a la concentración en el medio acuoso. En el presente estudio, el equilibrio de difusión de la urea se alcanzó a las 36 h, tiempo mayor a lo reportado, lo que podría proporcionar una característica favorable para la implementación de este sistema en condiciones de campo. Al respecto Azeem et al. (2014) reportan que un SLIP de urea recubierto con azufre y urea recubierta de cera, tuvieron una liberación lenta y prolongada de la urea con resultados relevantes en el rendimiento de los cultivos evaluados, y que las combinaciones de SLP de urea y urea convencional mejoran la eficiencia del N en los cultivos y disminuyen el costo de fertilización y manejo.
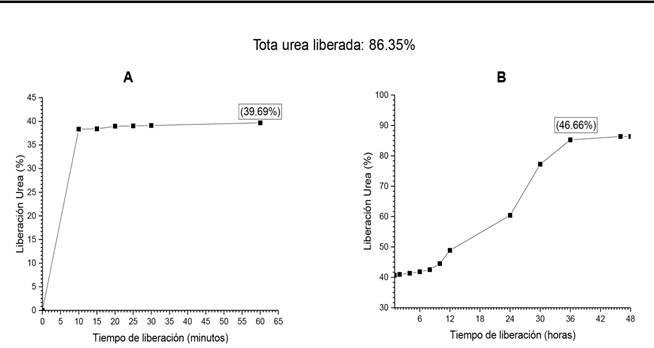
Figura 4 Cinética de liberación del SLIP en agua. A: Cinética de liberación en minutos y B: Cinética de liberación en horas.
Se sabe que el uso del SLIP está asociado con el mejoramiento de las condiciones de crecimiento de las plantas, la reducción del estrés y la toxicidad que resulta del exceso de abastecimiento de nutrientes en las zonas cercanas a la raíz de las plantas. Al respecto Trenkel (2010) reportan que al usar un SLIP se tiene la ventaja de reducir la toxicidad causada por las altas concentraciones de nutrientes. Lo permite la aplicación de fertilizante en mayor cantidad en una sola aplicación, lo que reduce la frecuencia de aplicación y disminuye las horas de trabajo. Así se disminuye el riesgo de contaminación ambiental y contribuye a la reducción de la emisión de gases a la atmósfera. Además de que aumenta la eficiencia en el uso de fertilizantes (Azeem et al. 2014). El SLIP de urea en polvo tiene características potenciales que pueden usarse como un sistema de liberación prolongada en el suelo, debido a su porosidad y las interacciones de enlace de hidrógeno formadas entre la urea y el gluten. Estas interacciones se confirmaron con las determinaciones de FT-IR y TGA que indican que el sistema de liberación es térmicamente estable a altas temperaturas. Además, la prueba de liberación de urea indicó su eficiencia como SLIP en el tiempo. Por lo que su aplicación en campo puede producir resultados satisfactorios en cuanto al desarrollo de los cultivos, ya que puede superar las expectativas en los rendimientos, mejorar la calidad del grano, reducir las pérdidas de nutrientes y prevenir los daños al medio ambiente.











 text new page (beta)
text new page (beta)



