Introducción
El cacao es un árbol originario de América, su fruto es la base para la elaboración de chocolate y sus derivados (Borrone et al. 2007). Esta especie se cultiva en los trópicos húmedos y es fuente importante de ingresos en los países en desarrollo (Lanaud et al. 2009). La propagación del cacao se realiza generalmente por la vía sexual o semillas (Minyaka et al. 2008). Por lo que el 70 % de los árboles de cacao cultivados en el mundo provienen de semilla sin selección previa (Eskes 2000). Aunque también, se propaga por métodos de reproducción asexual o vegetativa, por enraizamiento de estacas e injerto (Salvador et al. 2005).
En la actualidad, el empleo de la embriogénesis somática (ES) para la propagación clonal de plantas de cacao es de gran importancia (Yang y Zhang 2010). Este es un proceso en el que una estructura bipolar parecida a un embrión cigótico se desarrolla a partir de un tejido somático sin conexión vascular con el tejido original (Zahid et al. 2013). Las células atraviesan por una serie de cambios morfológicos y bioquímicos que dan como resultado la formación de embriones somáticos y la regeneración de nuevas plantas (Komamine et al. 2005). Los embriones somáticos (ESO) son parecidos a los embriones cigóticos y tienen también los mismos estados de desarrollo (Yang y Zhang 2010). Alternativamente, los ESO pueden ser utilizados como explantes para producir ESO adicionales a través de la embriogénesis somática secundaria (ESS) (Alejandro-Lázaro et al. 2015). La ESS puede ser repetida varias veces, por lo tanto, contribuye de forma significativa al incremento de la formación de embriones somáticos, especialmente en las plantas de baja capacidad embriogénica (Pérez-Núñez et al. 2006). La ESS también ha sido reportada para ayudar a retener la competencia embriogénica durante prolongados tiempos de cultivo en diferentes especies (Martinelli et al. 2001). Por otra parte, los embriones obtenidos a través de la ESS suelen ser más desarrollados que los obtenidos por embriogénesis somática primaria (Pérez-Núñez et al. 2006). Desde las primeras observaciones de la embriogénesis somática, su potencial ha sido mostrado y caracterizado en un amplio número de plantas dicotiledóneas y monocotiledóneas (Mathieu et al. 2006). Diversos estudios para el desarrollo de protocolos para la propagación clonal de cacao por cultivo de tejidos se han reportado (Alejandro-Lázaro et al. 2015), pero los resultados más relevantes se han obtenido por ES, con fuentes de explante de embriones cigóticos, estaminoides y pétalos, pero con baja eficiencia y bajas tasas de conversión a plántula (Urrea et al. 2011).
En la actualidad, se tienen avances en el desarrollo de sistemas de cultivo de tejidos de ES de cacao, lo que puede contribuir en el mejoramiento de las variedades (Maximova et al. 2008). Sin embargo, los resultados indican que muchos genotipos de cacao son recalcitrantes (Minyaka et al. 2008), por lo que se ve afectada la ES (Tan y Furtek 2003). Actualmente, dos limitaciones principales en la ES de cacao son la eficacia de producción de embrión dependiente del genotipo y la falta de desarrollo de cotiledones en los embriones somáticos, lo que provoca bajo porcentaje de conversión de planta (Maximova et al. 2014).
Los métodos utilizados para la propagación in vitro de plantas, presentan ventajas sobre los métodos tradicionales, como mínima superficie necesaria para mantener una gran cantidad de plantas, obtención de plantas libres de hongos, bacterias y/o virus, y la posibilidad de producir plantas todo el año (Albarrán et al. 2005). Debido a estas características, existen medios para cultivos in vitro en estado semisólido y líquido (Watt 2012). Los medios semisólidos son aquellos a los cuales se les agrega un agente gelificante, son los más utilizados en el establecimiento de explantes (Ziv 2005). Mientras que el medio líquido y el empleo de un sistema de inmersión temporal son adecuados para la producción y calidad de embriones somáticos (Albarrán et al. 2005). La inmersión periódica de los explantes en el medio de cultivo, beneficia al intercambio gaseoso dentro del recipiente y facilita la absorción de nutrientes (García-Gonzáles et al. 2010). Lo que se refleja en una mayor tasa de multiplicación y en un mejor desarrollo de los explantes (Albarrán et al. 2005). Por lo anterior el objetivo del presente estudio fue evaluar el sistema de inmersión temporal Rita® en el rendimiento de embriones somáticos secundarios de los 30 a los 180 d en dos ciclos de cultivo.
Materiales y métodos
Colecta y desinfección de botones florales
Se colectaron botones florales del genotipo híbrido INIFAP 1 entre las ocho y 10 h, los cuales se depositaron en frascos de Gerber que contenían agua bidestilada estéril. Para luego trasladarlos al laboratorio donde se desinfectaron en una campana de flujo laminar, con una solución de hipoclorito de sodio al 1 % durante 20 min. Para luego realizar tres lavados con agua destilada estéril, para posteriormente cultivarse las bases de los pétalos de las flores en cajas Petri.
Inducción de embriogénesis somática primaria
Se utilizó el medio de cultivo denominado Primary Callus Growth (PCG) suplementado con 5 μg de Thidiazuron y 200 μg de 2,4-D. Los cultivos se mantuvieron en obscuridad por 14 d a temperatura de 26 ± 1 °C. Para luego transferir los explantes a un medio de crecimiento de callos secundarios (SCG) y continuar con la formación de callo embriogénico en ED4 (Driver y Kuniyuki 1984). Para luego transferir a un medio EDL de desarrollo de embriones somáticos para la regeneración de plantas en medio PR (Li et al. 1998). Durante toda la etapa el cultivo se mantuvo en obscuridad y a temperatura de 26 ± 1 °C, renovando el medio de cultivo cada 14 d.
Inducción de embriogénesis somática secundaria a partir de cotiledones
Se usaron fragmentos de cotiledones de 5 mm2 procedentes de embriones somáticos primarios del híbrido INIFAP 1, generados después de cuatro meses de cultivo. Los fragmentos se cultivaron en un medio de regeneración de plantas PR (Figura 1) (Driver y Kuniyuki 1984). Suplementado con 30 gL−1 de sacarosa, 5 gL−1 de glucosa, 0.2 gL−1 de nitrato de potasio y 3 gL−1 de Gelrite como gelificante. El pH fue ajustado a 5.8 con hidróxido de sodio1 N.
Primer ciclo de embriogénesis somática secundaria
Se emplearon explantes del embrión somático tipo cotiledónar y fragmentos de cotiledón de 5 mm2. Los cuales se colocaron en un medio PR con fitohormonas para regenerar las plantas, desprovisto de fitohormonas. No se realizaron subcultivos durante el ciclo de cultivo. El experimento se estableció bajo un diseño experimental completamente al azar en arreglo factorial 3x2 con cinco repeticiones. Las variables estudiadas fueron el número de embriones somáticos formados y el porcentaje de oxidación. Los resultados se analizaron con un análisis de varianza y comparación de medias de Tukey (0.05). Los tratamientos evaluados se presentan en la Tabla 1.
Segundo ciclo de embriones somáticos secundarios
Un segundo experimento fue establecido para evaluar la capacidad de multiplicación de los embriones somáticos secundarios completos durante un segundo ciclo, partiendo de los embriones somáticos generados del experimento anterior. Solamente se utilizaron embriones somáticos procedentes del sistema Rita donde fueron cultivados. Los tratamientos en evaluación se presentan en la Tabla 1.
En este experimento se utilizó un solo tipo de explante: embrión somático tipo cotiledónar. El medio de cultivo utilizado fue PR (regeneración de plantas) desprovisto de fitohormonas. No se realizaron subcultivos a lo largo de 180 días de duración de este ciclo de cultivo.
El experimento se estableció bajo un diseño experimental completamente al azar con tres tratamientos (Tabla 1) con cinco repeticiones y cada repetición fue establecida con 10 explantes (embriones somáticos secundarios). Las variables en estudio fueron: número de embriones somáticos formados y porcentaje de oxidación de embriones somáticos. Los resultados fueron examinados por medio de un análisis de varianza y prueba de comparación de medias de Tukey (0.05).
Descripción del proceso histológico
El proceso histológico se realizó de acuerdo a Buffard-Morel et al. (1992) en muestras de fragmentos de cotiledón del sistema de inmersión automático a los 180 d. Se utilizó el estuche de Polysiences, Inc (USA) JB-4 a base de glicol metacrilato. Las muestras se fijaron en paraformaldehído al 4 % en amortiguador de fosfatos (pH = 7.2) por 24 h bajo presión negativa, posteriormente se deshidrataron en las concentraciones de etanol 30 % por 30 min, 50 % por 45 min, 70% por 45min, 90 % por 60 min, 95% por 60 min y 100 % por 60 min dos veces. Para la impregnación de los tejidos se utilizó 100 ml de solución A (monómero) y 900 mg del catalizador C (Bemzoil peróxido) por 24 h. Por último, se realizó la inclusión de las muestras en 25 mL de una solución A + C 25 mL, a la cual se le adicionó 1 mL de solución B (Polietilen glicol), para luego agregar al molde la solución conteniendo las muestras. A partir de los tejidos impregnados en resina, se obtuvieron cortes histológicos de 3 μm con un micrótomo Microm 325 (USA). La tinción se realizó con ácido periódico al 1 % por 5 min, para luego aplicar azul de metileno por 5 min, seguido de lavados con agua estéril. Posteriormente, se colocaron las muestras en una parrilla de calentamiento a 25 °C para su secado. Las secciones se observaron y fotografiaron con un microscopio Carl Zeiss (Alemania) con cámara digital acoplada.
Resultados
Primer ciclo de embriogénesis somática secundaria
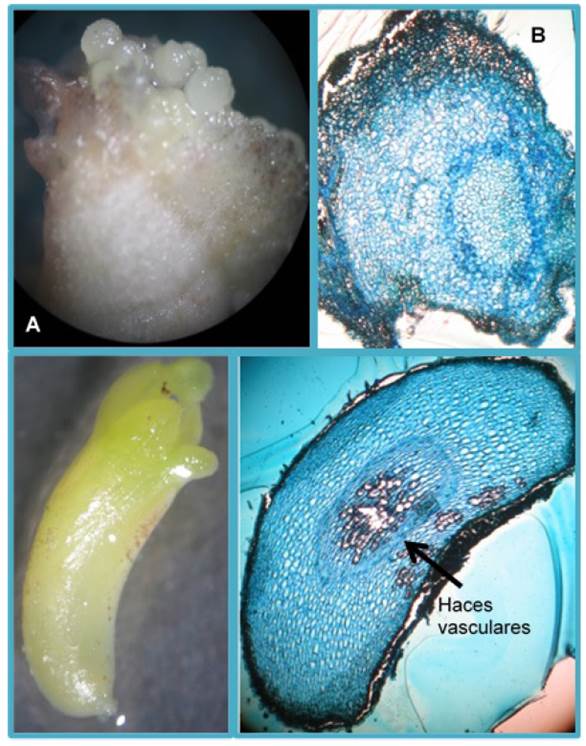
Después de los 30 d, todos los tratamientos fueron similares, mostrando escasa formación de embriones somáticos (ESO). Sin embargo, a los 120 d el tratamiento correspondiente a fragmentos de cotiledón fue estadísticamente superior al resto de los tratamientos con 26 ESO, mientras que con el tratamiento en recipiente Magenta sólo se obtuvieron ocho ESO. Al final del experimento, los cultivos en el sistema de inmersión temporal Rita® fueron estadísticamente superiores al testigo (Magenta®), en tanto que en el sistema Rita® se tuvieron 30 ESO generados con fragmentos de cotiledón y 29 ESO en cotiledones completos, produciéndose por explante en promedio tres ESO. Mientras que en el recipiente Magenta® se tuvieron cinco ESO de explantes de embriones somáticos completos y ocho ESO de fragmentos de cotiledón. Los resultados muestran que la producción de embriones fue mayor a los 180 d de cultivo en el sistema Rita®, mientras que en el recipiente Magenta la mayor producción de embriones se presentó a los 120 d de cultivo en fragmentos de cotiledón (Figura 1). En la Figura 2 se muestran los explantes utilizados y los embriones generados en el Sistema de Inmersión Temporal Rita®.
Porcentaje de oxidación
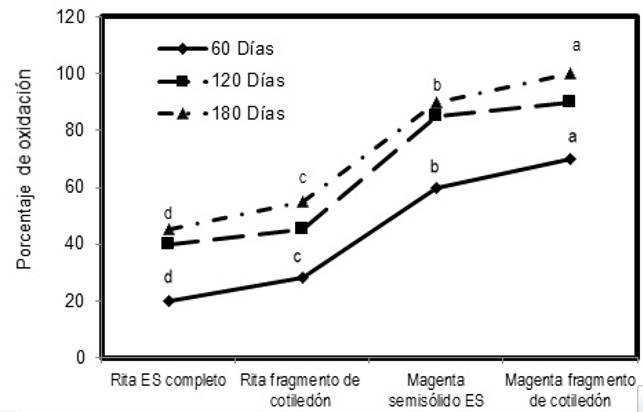
En los tratamientos, el porcentaje de oxidación incrementó con el tiempo, pero a los 180 d el sistema Rita® con embriones somáticos completos tuvo el menor porcentaje de oxidación con 45 %,mientras que el sistema Rita® con fragmentos de cotiledón presentó un 55 %, siendo estos tratamientos superiores estadísticamente a los tratamientos en medio semisólido en los recipientes Magenta®, los cuales tuvieron un 90 % de oxidación en embriones somáticos completos y 100 % en fragmentos de cotiledón (Figura 3).
Producción de embriones somáticos en un segundo ciclo
A los 30 d de cultivo se tuvieron embriones tipo globular, que se desarrollaron en el tejido superficial, apareciendo en mayor proporción en el sistema Rita® (Figura 4), con promedio de 0.84 ES a los 30 d. El mayor rendimiento de embriones somáticos secundarios se tuvo a los 180 d con promedio de 15 ES por recipiente. Este tratamiento superó estadísticamente al testigo en frascos tipo Gerber® y a los recipientes Magenta®.
En el testigo, la respuesta a la formación de embriones somáticos fue de 0.31 ES a los 30 d, obteniendose la máxima formación (1.7 ES) a los 90 d (Figura 4), con embriones de tipo globular que se observaron en pequeños grupos de color verde translúcidos. En el tratamiento Magenta®, se obtuvo la menor cantidad de embriones somáticos formados a los 30 d con 0.16 ES en promedio, incrementándose hasta alcanzar su mayor promedio a los 120 d con 1.73 ES (Figura 4), con embriones de tipo cotiledónar en menor tiempo que el resto de los tratamientos. Estos embriones tuvieron una coloración amarillenta a los 90 d de cultivo. En la Figura 5 se muestran embriones somáticos globulares y un embrión somático tipo torpedo y sus cortes histológicos.
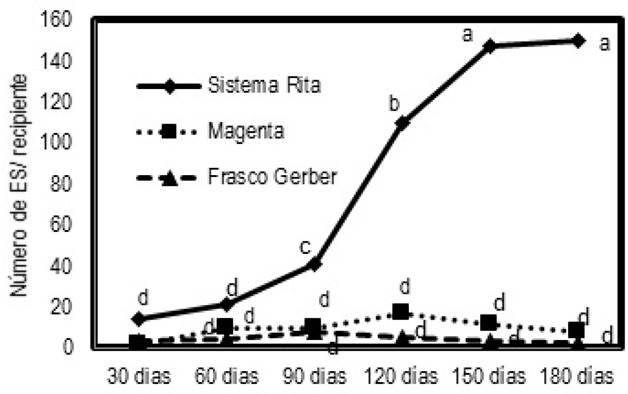
Figura 4. Número promedio de embriones somáticos secundarios cultivados en tres sistemas de cultivo. Valores con la misma letra son iguales estadísticamente (Tukey 0.05).
Porcentaje de oxidación
Todos los tratamientos presentaron diferentes porcentajes de oxidación a partir del primer mes de cultivo. El tratamiento en sistema Rita® mostró el porcentaje más bajo de oxidación durante todo el experimento (Tabla 2). A los 180 d de cultivo, el tratamiento Rita® presentó en 56 % de oxidación de tejido siendo superior estadísticamente a los tratamientos en recipiente Gerber y Magenta®. La aparición de pequeños puntos cafés fue un indicador del comienzo oxidativo. Los explantes establecidos en el tratamiento testigo se oxidaron por completo a los 150 d, mientras que en el recipiente Magenta® la oxidación total se presentó a los 120 d.
Discusión
El sistema de inmersión automático fue desarrollado para mejorar la propagación in vitro, de cultivos de importancia comercial (Watt 2012). En la presente investigación, los resultados mostraron que el uso de medio líquido en el sistema Rita® favoreció la producción de embriones somáticos, por lo que la baja producción de embriones somáticos secundarios en medios semisólidos está asociada al agotamiento de los nutrimentos (Ziv 2005). Por lo que los medios líquidos en el sistema de inmersión automático Rita® favorecen la producción de embriones somáticos debido a que el explante entra en mayor contacto con el medio, lo que facilita la absorción de nutrimentos (García-Gonzáles 2010). Adicionalmente, este sistema ha demostrado ser positivo en la producción y calidad de embriones somáticos de café (Albarrán et al. 2005), resultados similares se observaron en el presente estudio, con embriones somáticos secundarios independientes sin fusiones o malformaciones. Se observó que la exclusión de fitohormonas favorece la multiplicación y la sincronización de los embriones de forma independiente sin fusiones. Estos resultados son similares a los reportados por Alejandro-Lázaro et al. (2015) quienes indican que generaron ESS en cacao en un medio semisólido sin fitohormonas. La formación de ESS se pudo repetir en un segundo ciclo de cultivo, con disminución del porcentaje de oxidación en el sistema de inmersión automático Rita®. Al respecto Damiano et al. (2005) reportan que la disminución de la oxidación se debe a la renovación de la atmósfera dentro del recipiente, lo que permite reducir los niveles de contaminación y la hiperhidricidad de los tejidos. El uso de la ESS en cacao es una herramienta valiosa en la propagación de plantas de genotipos agronómicamente importantes (Maximova et al. 2008). Además de que los resultados obtenidos son superiores a lo reportado por Alejandro-Lázaro et al. (2015), incluso se logró la multiplicación de embriones somáticos en un segundo ciclo de cultivo, con estructuras como cotiledones, eje embrionario y haces vasculares. El potencial para usar embriones somáticos para la propagación a gran escala de genotipos élite de cacao puede representar un avance importante para la multiplicación de genotipos.
Conclusiones
El uso de medio líquido en sistema Rita® favoreció la producción de embriones somáticos de cacao. Los embriones somáticos secundarios obtenidos no presentaron fusiones o malformaciones recurrentes. La cual fue posible repetirla en un segundo ciclo de cultivo, demostrando la totipotencia de los embriones somáticos completos usados como explantes, al igual que los fragmentos de cotiledón y sobre todo la repetitividad del evento. El potencial de usar fragmentos de cotiledón procedentes de embriones somáticos primarios y embriones somáticos completos cultivados en un sistema de inmersión automático en medio de cultivo líquido, es un avance para la multiplicación de genotipos con caracteres deseables.











 nueva página del texto (beta)
nueva página del texto (beta)