Introducción
La demanda mundial de agroalimentos (productos agrícolas que han sufrido tratamientos industriales), ha ido en aumento durante las últimas dos décadas, con respecto al incremento de la población humana de acuerdo a la Organización de las Naciones Unidas para la Alimentación y la Agricultura (FAO, por sus siglas en inglés: Food and Agriculture Organization of the United Nations) (FAO, 2017). El consumidor actual de alimentos busca practicidad en su preparación, valor nutritivo, seguridad alimentaria, características sensorialespositivas, entre otros. Durante el procesamiento de estos alimentos se genera una gran cantidad de residuos agroindustriales que pueden ser de origen animal o vegetal. En general, estos residuos son una fuente de contaminación, por la gran cantidad que de ellos se genera, por ejemplo: a) en los productos vegetales, la cascarilla de arroz, la piel, semillas y tallos de uvas; y en los residuos de frutas como la papaya, el mango, la manzana, el plátano, por citar algunos, donde solo se aprovecha la pulpa, pero las cáscaras y semillas son desechadas y utilizadas en la mayoría de sus casos para abono; b) en productos generados por animales, los ejemplos más notables son el lactosuero, vísceras, sangre, pieles, entre otras, que en gran parte son desaprovechados y se convierten en contaminantes del medio ambiente, así como focos de infección (Schieber y col., 2001; Valdez-Vázquez y col., 2010).
Los residuos agroindustriales poseen un alto contenido de componentes bioactivos, por lo que constituyen una materia prima natural para la recuperación de compuestos fenólicos, aceites aromáticos, alcaloides, proteínas, fibra, carbohidratos, entre otros, que tienen su utilidad dentro de la industria alimentaria como aditivos por sus propiedades funcionales y nutraceúticas, así como también en las industrias cosméticas y farmaceúticas (Kowalska y col., 2017). Estas moléculas ejercen efectos farmacológicos en el organismo benéficos para la salud (Drago-Serrano y col., 2006).
En México, los residuos agroindustriales son de diferentes tipos y su cantidad depende de la zona de cultivo. Se ha estimado que 75.73 millones de T de materia seca se generaron a partir de 20 cultivos y que del total de esta biomasa, 60.13 millones de T correspondían a residuos de cultivos primarios como la paja de maíz, paja de sorgo, hojas de caña de azúcar y paja de trigo. Mientras que los residuos de cultivos secundarios originaron alrededor de 15.60 millones de T, donde los principales participantes fueron el bagazo de caña de azúcar, las mazorcas del maíz, el bagazo de maguey y la pulpa de café. Estos son solo algunos de los cultivos con mayor productividad en México, y su uso potencial principal es la producción de biocombustibles y como sustrato en fermentaciones (Valdez-Vázquez y col., 2010).
En el sureste de México, en el estado de Tabasco, uno de los residuos agroindustriales más rico en biomoléculas es la cascarilla de cacao, conocida también como testa, que constituye aproximadamente entre el 10 % a 16 % del total del grano tostado utilizado en la industria (Beckett, 2008). De acuerdo con la organización internacional del cacao (ICCO, por sus siglas en inglés: The International Cocoa Organization) (ICCO, 2015), en el 2014, se produjeron más de 4 millones de T de cacao alrededor del mundo. Tomando en consideración este volumen de producción, el porcentaje de cascarilla generado es de aproximadamente 680 000 T a 700 000 T (Okiyama y col., 2017). La cascarilla de cacao se enriquece en biomoléculas durante el proceso de poscosecha en las etapas de fermentación, secado y tostado, donde ocurren diversas reacciones bioquímicas dentro y fuera del grano, que dan lugar a la migración de diversos compuestos hacia la periferia del grano, donde quedan atrapados en la testa de la semilla (Schwan y col., 1995; Saltini y col., 2013; Aprotosoaie y col., 2016). La presencia del sabor amargo en las semillas de cacao se debe principalmente a la presencia de dos metilxantinas, la teobromina y cafeína; también se ha reportado que los compuestos polifenólicos contribuyen a notas amargas, pero usualmente su contribución es con la astringencia (Pickenhagen, 1975; Noor-Soffalina y col., 2009; Aprotosoaie y col., 2016). Las metilxantinas, son un grupo de alcaloides que poseen en su estructura un anillo característico de purina y radicales metil en distintas posiciones, son moléculas poco solubles y están contenidas principalmente en café, cacao, hierba mate y guaraná (Moratalla, 2008). En la cascarilla del grano de cacao, la teobromina constituye aproximadamente el 0.9 % y la cafeína el 0.3 %. Estas metilxantinas son capaces de alterar el sistema nervioso central de forma moderada, pero también relajan el músculo liso (bronquios), por lo tanto, ayudan en el tratamiento de enfermedades respiratorias, además son vasodilatadoras, mejorando así la circulación sanguínea, y se ha demostrado su efecto diurético (Arnaud, 2011).
En función de la importancia, el valor y la dificultad que tiene extraer compuestos bioactivos, la industria necesita hacer uso de tecnologías emergentes de extracción y de conservación, como la extracción por medio de microondas, ultrasonido o la extracción supercrítica, que son tecnologías que trabajan con campos electromagnéticos, ondas sonoras, tecnologías a altas presiones y temperaturas, las cuales mejoran el proceso de separación de biomoléculas desde la matriz natural (Putnik y col., 2017).
La extracción supercrítica se caracteriza por utilizar solventes químicamente inertes, como el dióxido de carbono (CO2), el cual, por sus características solvatantes, económicas y ecológicas, se ha convertido en el de mayor uso, además, es accesible y con alta efectividad (Hauthal, 2001; Herrero y col., 2010; Knez y col., 2014). En general, los fluidos supercríticos tienen la capacidad de penetrar en cualquier matriz sólida, debido a los cambios en sus características fisicoquímicas, por ejemplo, la viscosidad es mucho menor a la de un líquido, su densidad es cercana a los valores reportados para líquidos, por lo que los coeficientes de difusión de los solutos son mayores que un disolvente líquido. Por tanto, en la etapa supercrítica, los fluidos presentan las particularidades de un gas, pero también de un líquido (De-Melo y col., 2014; Sánchez-Camargo y col., 2014; Pardo-Castaño y col., 2015), lo que permite mayor solubilidad y una mejor extracción de compuestos, como polifenoles, ácidos grasos y alcaloides, entre otros, que previamente se han estudiado (Herrero y col., 2010; De-Melo y col., 2014; Sánchez-Camargo y col., 2014).
En la práctica, se efectúan dos técnicas de extracción supercrítica (Miller y col., 1993), la primera conocida como estática, donde se mantiene controlada la presión y temperatura por un determinado tiempo, para posteriormente realizar la extracción controlando el flujo de salida del extracto (en esta no hay flujo de fluido supercrítico). La segunda técnica conocida como dinámica, se realiza con un flujo constante de fluido supercrítico, y por lo regular tiene una fase estática de no más de 10 min para lograr que el fluido supercrítico penetre en la matriz de extracción y se puedan obtener mejores rendimientos de extracción (Fernández-Trujillo, 2008). Es importante controlar el flujo de salida en los equipos de extracción supercrítica, debido a que se ha observado un efecto del flujo sobre el rendimiento del extracto final (De-Melo y col., 2014).
El objetivo de la presente investigación fue evaluar la extracción de cafeína, teobromina y grasa del polvo de cascarilla de cacao con CO2 supercrítico, en función de la presión y temperatura.
Materiales y métodos
Materia prima
La cascarilla de cacao fue recolectada de un lote de aproximadamente 80 kg de una mezcla de cacao trinitario mexicano tostado. La procedencia del cacao fue de la comercializadora Intercambio Mexicano de Comercio (IMCO), S.A. de C.V., ubicada en la carretera CárdenasComalcalco S/N en el municipio de Cárdenas, Tabasco, México. Los granos de cacao que comercializa IMCO son una mezcla de cultivares de cacao de una región conocida con el nombre de la Chontalpa en el estado de Tabasco, México. El descascarillado de las muestras de cacao tostado se realizó de forma manual. La cascarilla se lavó con agua desionizada y se secó al sol. La muestra obtenida se llevó a molienda en un molino marca KRUPS (GX41001, México) y el tamaño de partícula se homogenizó a 0.841 mm, a través de un tamiz de malla No. 20 (Montinox, “Manufacturado por Montiel inoxidable, México”).
Extractor supercrítico SFE-150
Las extracciones se realizaron en un equipo de extracción supercrítica modelo SFT-150 SFE de la compañía (Supercritical Fluid Technologies, INC., Newark, Delaware, EUA) que cuenta con un intervalo de temperatura de operación máxima de 200 ºC, opera a una presión máxima de 10 000 psi, su caudal volumétrico varía de uno a a 330 mL/min (250 g/min) de CO2 líquido. Además, cuenta con cámaras de extracción para muestras de entre 100 mL y 2 000 mL, el aire seco se encuentra regulado a 0.75 psi por un compresor KAESER 7.5 C (Kaeser Compressoren SE, Carl-Kaeser_Str, 26, Germany), y el suministro de gas se llevó a cabo a través de un cilindro (Plaxair, Villahermosa, México) de CO2 gaseoso (Figura 1).
Extracción con CO2 supercrítico
Para la extracción de los compuestos solubles, de la cascarilla de cacao, se utilizaron 30 g de muestra, a los que se añadieron 20 mL de etanol absoluto; posteriormente, la mezcla fue colocada en la cámara de extracción del extractor supercrítico (Supercritical Fluid Technologies, INC., Newark, Delaware, EUA). Se propuso un diseño factorial 22 con 5 puntos centrales. Las condiciones de extracción se muestran en la Tabla 1.
Las extracciones se realizaron a flujo constante de 0.176 g de CO2 /min, con una fase estática o de remojo constante de 20 min (la fase estática conocida también como tiempo de remojo, permite que el CO2supercrítico penetre en la muestra de manera homogénea y así obtener una mayor recuperación de masa extraída) y una fase dinámica constante de 20 min (durante esta etapa es importante controlar el flujo de salida del CO2 , dado que puede haber diferencias significativas en la cantidad de masa extraída). La matriz de resultados obtenida a partir del diseño experimental se analizó en MATLAB R2014a, y el ajuste se llevó a cabo con una ecuación polinomial de primer orden con términos de interacción:
donde yi es la respuesta, x1 x2 las variables independientes o regresoras y su interacción, β0 es la ordenada al origen, β1 , β2 , β12, son los coeficientes de regresión lineales y de interacción respectivamente, que evalúan los efectos, εi es el error aleatorio con media cero, E(ε) = 0 y varianza V(ε) = σ2.
Determinación de grasa cruda por método Soxhlet
La extracción de grasa se realizó siguiendo la metodología propuesta por la norma mexicana NMX-F-615-NORMEX-2004. Para ello, se tomaron 2 g de polvo de cascarilla de cacao y se utilizó como solvente éter de petróleo, durante 8 h de extracción. El porcentaje de grasa se determinó de acuerdo a la fórmula:
donde P= Masa en gramos del matraz con grasa, p = Masa en gramos del matraz sin grasa y M= Masa en gramos de la muestra.
Cálculo de la razón residual y de remoción de cada variable
La razón de remoción y residual de cada variable, después de la extracción con CO2, se calculó de acuerdo a las siguientes ecuaciones (Kobori y col., 2013):
Y, X, significan la razón de remoción y residual, respectivamente. A y B expresan el contenido de la variables de respuesta antes y después de las extracción con CO2 supercrítico, respectivamente. Las cantidades Amo y Bm f representan el peso del polvo de cascarilla inicial en la unidad de extracción y el peso del polvo de cascarilla residual en la unidad de extracción, respectivamente. La proporción de cafeína y grasa cruda fueron establecidas como razón de remoción y la teobromina como la razón residual.
Rendimiento global
El rendimiento de la extracción (Rg ) fue estimado por la relación entre la masa total extraída (me ), después del proceso de extracción, por cada tratamiento del diseño experimental, con respecto a la masa inicial (mo ) en el contenedor de la unidad de extracción supercrítica y expresada en porcentaje:
Determinación de metilxantinas por espectroscopía de ultravioleta-visible
Los residuos de polvo de cascarilla de cacao en la unidad de extracción del equipo de extracción supercrítica se analizaron para cafeína y teobromina por espectroscopia UV-Vis. Para la extracción de teobromina y cafeína se utilizó una modificación de la técnica de Peralta-Jiménez y Cañizares-Macías (2013), donde 1 g de muestra se aforó con 100 mL de agua desionizada. Para la extracción de teobromina, la mezcla se colocó en baño ultrasónico (Elmasonic S40H, Germany) con una potencia fija de 340 W a 80 ºC durante 180 s; posteriormente, se agregaron 5 mL de reactivo Carrez 1, se dejó enfriar y se filtró. Al filtrado se le agregaron entre 3 g de NaHCO3 a 5 g de NaHCO3 y se filtró por segunda vez. El filtrado se aforó a 100 mL con agua desionizada y se tomaron 10 mL que se ajustaron a un pH entre 12.5 y 12.7, con NaOH (8 %). Para la extracción de cafeína se agregaron 10 mL de cloroformo y se realizó la extracción por ultrasonido (37 kHz de frecuencia) a 80 ºC por 30 s, después la mezcla se llevó a centrifugación (HERMLE Laboertechnik GmbH, Z 326, Germany) por 10 min a 1 474 xg.
En la extracción de metilxantinas a partir del extracto, 200 mL de extracto fueron aforados con NaOH (1 N) a 2 mL; la mezcla se llevó a ultrasonido (37 kHz de frecuencia) durante 180 s a 80 ºC. Posteriormente, se dejó enfriar y se centrifugó a 1 474 xg y - 5 ºC por 10 min, para separar la grasa del sobrenadante. A 1 mL de sobrenadante se le agregó 1 mL de cloroformo; la mezcla se llevó a ultrasonido por 30 s, para extraer la cafeína de la fase acuosa.
Al dar la teobromina y cafeína un pico máximo de absorbancia de 273 nm y 276 nm, respectivamente, y de acuerdo a lo reportado por Li y col. (1990) y Peralta-Jiménez y CañizaresMacías (2013), se eliminó de la muestra la mayor cantidad de interferencias con el uso de reactivo Carrez 1 (precipitación de proteínas, eliminación de turbidez y para destruir emulsiones) y se realizó la lectura para determinar la presencia de metilxantinas en los extractos.
Una vez obtenidas las fases acuosa y orgánica donde se solubilizaron teobromina y cafeína, respectivamente, se llevó a cabo la lectura en un espectrofotómetro (Thermo Fisher Scientific, G10S Uv-Vis, China). Para teobromina, una alícuota de la fase acuosa se diluyó en agua desionizada en una relación 1:25 y se tomó lectura a 273 nm. Para cafeína, una lícuota de la fase orgánica se diluyó en cloroformo en una relación 1:10 y se tomó lectura a 276 nm. Para teobromina y cafeína, se realizaron curvas estándares entre 0 mg a 50 mg en agua desionizada y cloroformo respectivamente.
Análisis estadístico
Se realizó un análisis de varianza (ANOVA) de las variables de estudio en el residuo (teobromina, cafeína y grasa), la razón residual (teobromina) y de remoción (grasa y cafeína), como función de la temperatura y presión, durante la extracción con CO2 supercrítico. Adicionalmente, la viabilidad del modelo se comprobó con el coeficiente de determinación R2.
Resultados y discusión
La cascarilla y el cotiledón del grano de cacao, son matrices de estudio complejas, tienen una composición química similar, que incluye una amplia gama de compuestos, como ácidos grasos, polifenoles, carbohidratos, proteínas y alcaloides, entre otras (Arlorio y col., 2005; Lecumberri y col., 2007; Martínez y col., 2012; Okiyama y col., 2017). El cotiledón es utilizado en la industria de transformación del chocolate, pero la cascarilla es un residuo con moléculas aprovechables en otras industrias, por su valor nutritivo, farmacéutico y cosmético (Okiyama y col., 2017). La extracción supercrítica de diferentes moléculas en la cascarilla constituye un elemento clave para el aprovechamiento, por lo que se tiene que considerar el residuo y los extractos. Una exploración inicial en esta investigación comenzó con el contenido de grasa y las metilxantinas presentes en el polvo de cascarilla de cacao. La cuantificación inicial a la cascarilla mostró una concentración de grasa de 80.00 mg/g (± 0.01), de teobromina de 15.85 mg/g (± 0.002) y cafeína de 0.80 (± 0.009) mg/g, respectivamente. En cuanto a los residuos y extractos (Tabla 2), durante el estudio de extracción con CO2 supercrítico, se observó que las concentraciones de teobromina fueron bajas en los extractos con respecto a la cascarilla residual, en donde se obtuvieron altas concentraciones, entre 14.98 (± 0.34) mg/g y 17.09 (± 0.53) mg/g, y un porcentaje de razón residual entre 90.39 % y 103.43 %. El método de extracción con CO2 resultó mejor para la extracción de cafeína, con porcentajes de remoción entre el 38.52 % y 78.38 %, con concentraciones en el residuo de entre 0.19 (± 0.02) mg/g y 0.54 (± 0.08) mg/g. A pesar de que las metilxantinas, cafeína y teobromina tienen estructuras químicas muy similares, la diferencia es por la presencia de un grupo sustituyente metil en la cafeína, lo que modifica las propiedades físicas y químicas. La diferencia principal de ambas moléculas se da en el punto de fusión y en la entalpía de fusión, que se incrementa casi en dos órdenes de magnitud (Li y Hartland, 1992; Johannsen y Brunner, 1994; Mohamed y col., 2002), esto provoca que la solubilidad de la teobromina en CO2 supercrítico sea menor que la de cafeína en casi dos órdenes de magnitud, y este comportamiento es similar en otros solventes líquidos (Johannsen y Brunner, 1994). En cuanto al contenido de grasa en el residuo, se removió hasta en un 94.54 %, disminuyendo en la cascarilla desde una concentración inicial de 80.00 (± 0.014) mg/g hasta 0.005 (± 0.000 1) mg/g, estos resultados indicaron que la extracción supercrítica es un método eficaz para separar grasa de matrices naturales, como la cascarilla de cacao, en menor tiempo y sin hacer uso de solventes contaminantes que dejan residuos en el extracto. Autores como Li y Harland (1992), Mohamed y col. (2002), Asep y col. (2008), Salajegheh y col. (2013), Asep y col. (2016), han reportado la dificultad para extraer grasa del grano de cacao con CO2 supercrítico solo, también hablan de la eficiencia de co-solventes como el etanol y el etano. Durante los experimentos, el polvo de cascarilla se reconstituyó con etanol absoluto antes de iniciar la extracción, este tratamiento de pre-extracción fue positivo, dado que mejoró la solubilidad de los compuestos durante la extracción supercrítica.
En función del rendimiento de extracción, se obtuvieron porcentajes de masa extraída entre 1.72 % a 9.61 % (Tabla 2), evaluando dos factores (temperatura y presión). Esto da posibilidades de proponer un diseño más complejo, donde sea posible hacer uso de variables como el tiempo, el flujo de CO2 , uso de co-solventes, o el empleo de un pretratamiento que pudiesen influir en la extracción de los compuestos solubles presentes en la cascarilla de cacao.
Durante la fase experimental de la extracción supercrítica de compuestos solubles en CO2 de la cascarilla de cacao, se apreció que la masa extraída en los experimentos estaba compuesta por una fase similar a la manteca de cacao en color y aroma.
Tabla 2. Concentración de teobromina, cafeína y grasa en el residuo, razón residual de teobromina y razón de remoción de cafeína y grasa.
Table 2. Concentration of theobromine, caffeine and fat in the residue, residual ratio of theobromine and ratio for removal of caffeine and fat.
| Variables naturales | Concentración en el residuo | Razón residual | Razón de remoción | ||||||
|---|---|---|---|---|---|---|---|---|---|
| Tratamiento | Temperatura (K) | Presión (psi) | Rendimiento (%) | Grasa (mg/g) | Teobromina (mg/g) | Cafeína (mg/g) | Teobromina (%) | Grasa (%) | Cafeína (%) |
| 1 | 318 | 4 000 | 9.44 | 0.018 | 15.82 | 0.19 | 90.39 | 79.32 | 78.38 |
| 2 | 318 | 4 000 | 8.33 | 0.014 | 16.31 | 0.24 | 94.30 | 84.25 | 72.15 |
| 3 | 318 | 4 000 | 9.61 | 0.012 | 15.90 | 0.26 | 90.67 | 86.10 | 69.92 |
| 4 | 318 | 4 000 | 9.57 | 0.017 | 16.21 | 0.54 | 92.48 | 81.17 | 38.52 |
| 5 | 318 | 4 000 | 9.07 | 0.021 | 16.34 | 0.25 | 93.72 | 76.22 | 71.72 |
| 6 | 333 | 6 000 | 5.72 | 0.033 | 16.31 | 0.34 | 96.98 | 61.31 | 59.77 |
| 7 | 333 | 2 000 | 1.72 | 0.011 | 14.98 | 0.34 | 92.86 | 87.10 | 58.06 |
| 8 | 303 | 2 000 | 4.04 | 0.014 | 17.09 | 0.50 | 103.43 | 83.55 | 40.31 |
| 9 | 303 | 6 000 | 8.63 | 0.005 | 16.26 | 0.23 | 93.71 | 94.54 | 73.89 |
Resultados del ANOVA
La Tabla 3 muestra que las variables: concentración en el residuo de teobromina y grasa fueron significativos (P ≤ 0.05), con efectos de forma lineal y no lineal por causa de interacción entre los mismos. La prueba de falta de ajuste reveló que el modelo seleccionado es confiable para describir los datos observados en el residuo de teobromina y grasa (P ≤ 0.05). Además, la viabilidad del modelo se comprobó con el coeficiente de determinación R2, de 0.89 y 0.90, respectivamente.
Table 3. Analysis of variance in the residue, residual and removal ratio.
| Variable | Modelo | Lineal | No lineal | Residual | Falta de ajuste | Error puro | Total | R2 | |
|---|---|---|---|---|---|---|---|---|---|
| Concentración en el residuo | Teobromina | 2.288 6* | 1.126 1* | 1.162 5* | 0.231 7 | 0.004 0 | 0.227 8 | 2.520 3 | 0.90 |
| Cafeína | 0.037 1 | 0.018 8 | 0.018 3 | 0.085 9 | 0.006 5 | 0.079 4 | 0.123 1 | 0.30 | |
| Grasa | 4.42 E-04 * | 1.98 E-04* | 2.43 E-04* | 5.00 E-05 | 1.92 E-06 | 4.80 E-05 | 4.92 E-04 | 0.89 | |
| Razón residual | Teobromina | 69.058 | 21.201 | 47.857 | 56.061 | 43.705* | 12.356 | 125.12 | 0.55 |
| Razón de remoción | Grasa | 613.26* | 275.1* | 338.16* | 61.489 | 0.101 31 | 61.388 | 674.75 | 0.90 |
| Cafeína | 568.72 | 314.66 | 254.05 | 1141.4 | 146.92 | 994.52 | 1710.2 | 0.33 |
* P ≤ 0.05
En cuanto a la cafeína en el residuo, no se encontró efecto significativo (P > 0.05), con respecto a los factores de estudio, lo que indica que otros factores pueden intervenir en el proceso y no fueron considerados dentro del modelo propuesto. El R2 para la cafeína en el residuo fue de 0.30, lo que mostró que no existe calidad de ajuste con el modelo propuesto, confirmando lo previamente establecido. La teobromina y la cafeína son moléculas que difieren en un grupo metil, sin embargo, la primera reportó una alta retención en la cascarilla (Tabla 2), debido a una menor solubilidad en el CO2 supercrítico, atribuido a la baja polaridad de esta metilxantina en compuestos como el CO2 y algunos otros líquidos, lo que dificultó su extracción bajo las condiciones propuestas en el estudio. A diferencia de la significancia que presentó la variable teobromina en la concentración del residuo, la razón residual registró falta de ajuste (P > 0.05) y un R2 de 0.55, lo que evidenció que el modelo propuesto no reproduce la conducta de esta variable.
En la razón de remoción de la grasa, los resultados del ANOVA indicaron que el modelo propuesto fue significativo (P ≤ 0.05) y un efecto de los factores de temperatura y presión de las condiciones de extracción con CO2 presentaron un comportamiento lineal y no lineal. El R2 fue de 0.90, lo que mostró que el modelo con efectos lineales y de interacción reproduce la conducta experimental, sin embargo, la prueba de falta de ajuste no fue significativa (P > 0.05), por lo que se revela que existen otras variables (tiempo de extracción, flujo de CO2, cosolvente) que están contribuyendo como factores importantes durante la extracción de la grasa. Durante la fase experimental, se observó que el tiempo de despresurización registró un papel importante para la colección de la grasa durante el proceso de extracción, por lo que debe ser considerada en posteriores estudios. La razón de remoción para cafeína presentó un R2 de 0.33 y falta de ajuste (P > 0.05).
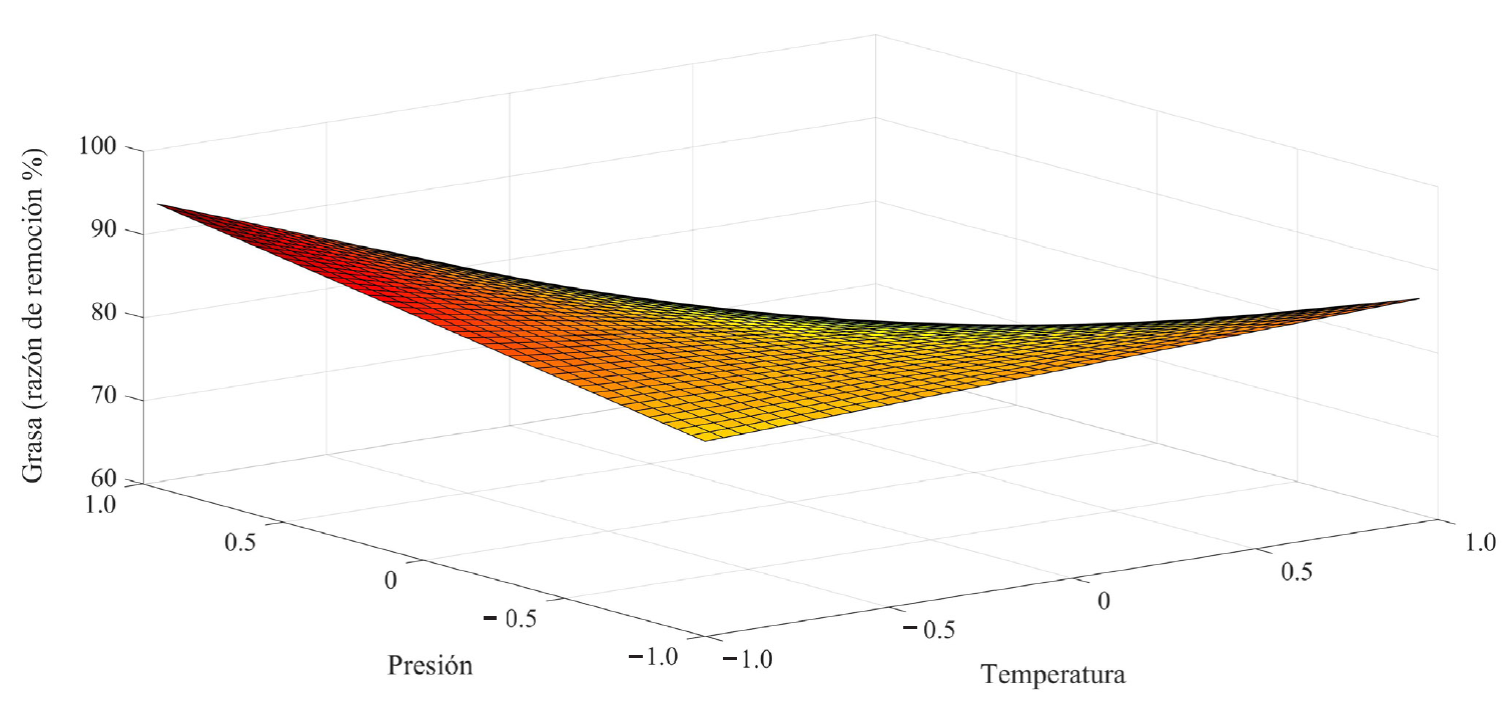
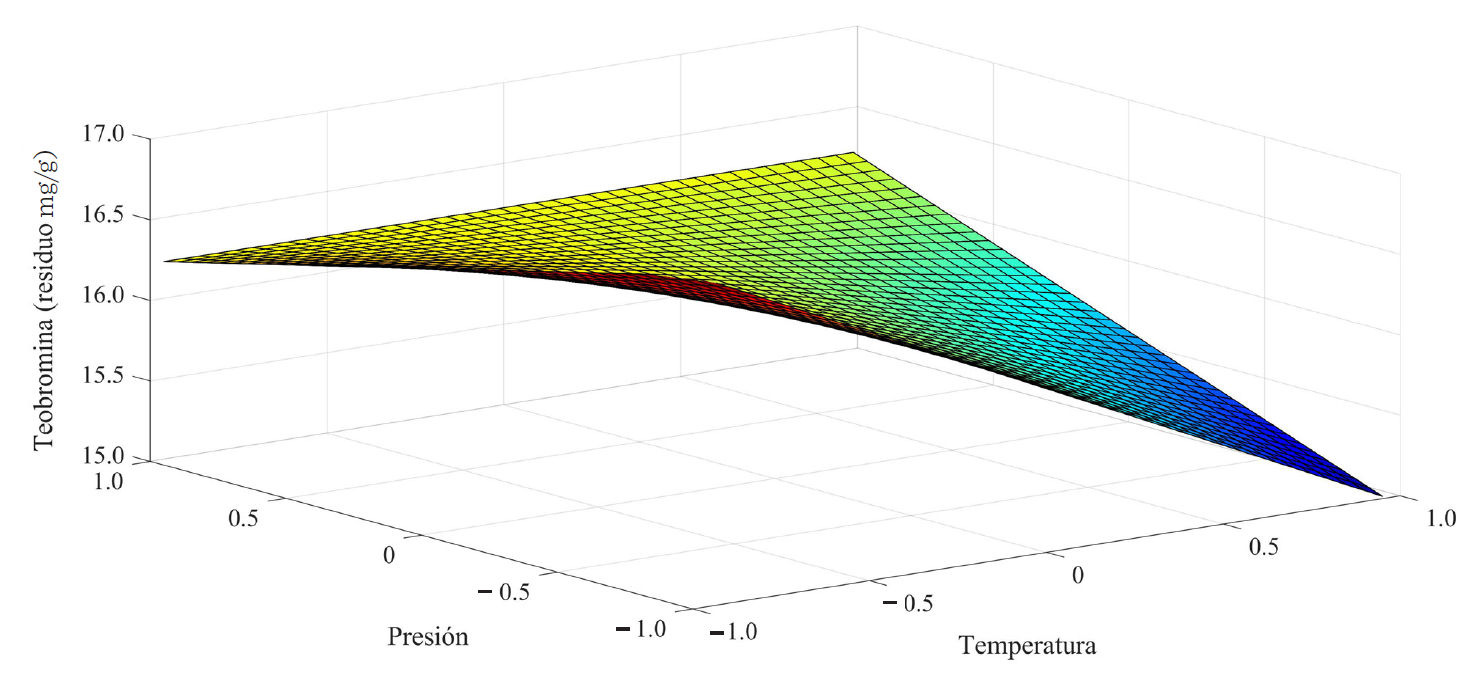
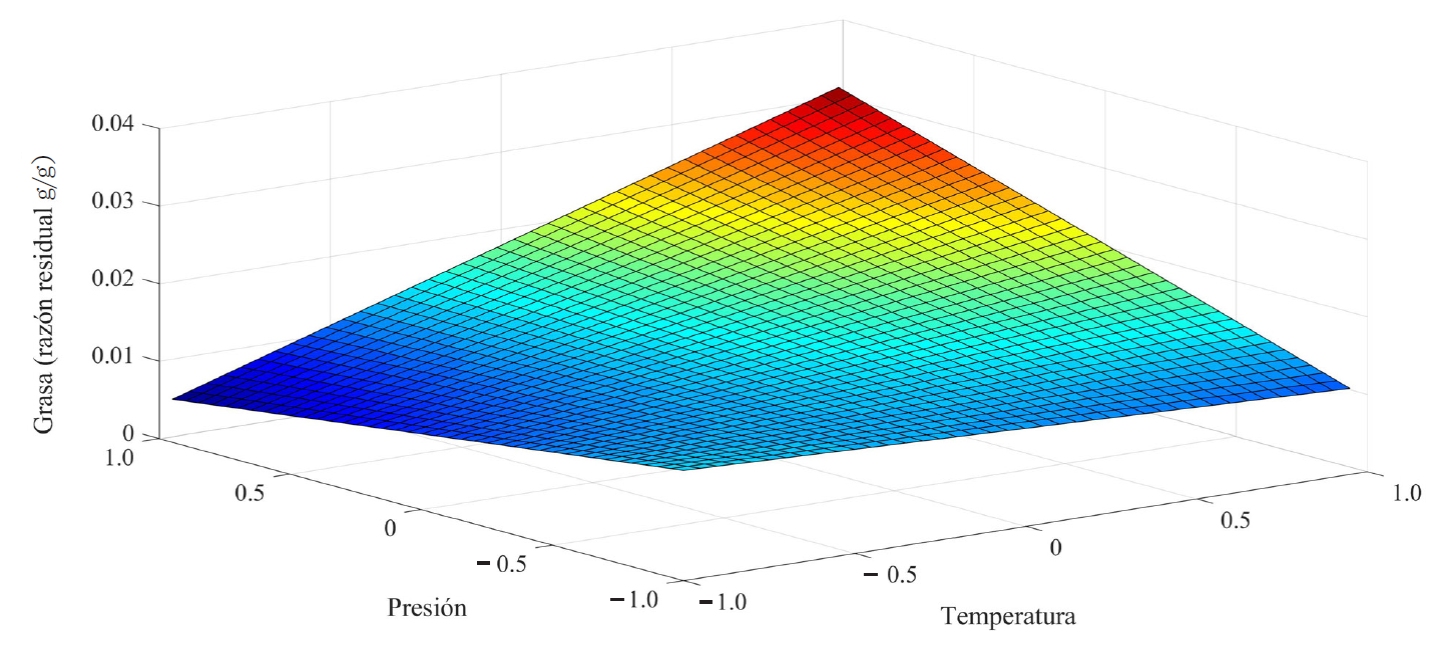
En la Tabla 4 se muestran los coeficientes de regresión del modelo propuesto para cada una de las variables de estudio. Los resultados evidenciaron que existen términos sin un efecto significativo con respecto a las variables que reportaron significancia (P ≤ 0.05) de acuerdo con el ANOVA. La teobromina en el residuo registró un efecto lineal negativo (β1) y un efecto de interacción (β12), en los términos significativos a P ≤ 0.05. Mientras que para la razón residual de grasa, los coeficientes de regresión indicaron un efecto lineal positivo y de interacción lineal positivo, mostrando que la concentración de grasa en el residuo se eleva como función de un incremento de las condiciones de temperatura y presión. Los cambios en la concentración de teobromina y grasa, en el residuo de polvo de cascarilla, se pueden observar en gráficos tridimensionales generados a partir del polinomio (Figura 2 y 3). En ambos casos son planos, con efectos de curvatura por la contribución del término de interacción. En el caso de la razón de remoción de la grasa, un efecto lineal negativo y de interacción se registró, lo que reveló que esta razón disminuyó como consecuencia del aumento de las variables operacionales antes mencionadas. La Figura 4 muestra la razón de remoción de grasa, como función de las variables de temperatura y presión. Kobori y col. (2013), señalaron que la extracción supercrítica es adecuada para extraer varios compuestos solubles en el polvo de granos de cacao, mientras otros compuestos presentes se pueden retener. Estos autores buscaron un valor agregado al cotiledón del cacao, en función de preservar los compuestos funcionales (polifenoles y teobromina) y eliminar la cafeína. En este estudio, los resultados evidenciaron que la extracción de grasa del polvo de cascarilla se llevó a cabo de forma eficiente, además que la cafeína se extrajo también de forma simultánea, con la retención de teobromina. Por lo que el residuo registrará características funcionales no sólo por la presencia de teobromina, sino también por la presencia de una amplia cantidad de biocompuestos aún observables, como serían los compuestos fenólicos y la fibra dietética, ya reportadas en este residuo por Okiyama y col. (2017).
Tabla 4. Coeficientes de regresión de las variables de respuesta en la concentración del residuo, razón residual y razón de remoción.
Table 4. Regression coefficients of the response variables in the concentration of the residue, residual and removal ratio.
| Variable | β 0 | β 1 | β 2 | β 12 | |
|---|---|---|---|---|---|
| Concentración en el residuo | Teobromina | 16.141 | - 0.515 65* | 0.125 | 0.539 1* |
| Cafeína | 0.324 56 | - 0.010 9 | - 0.067 7 | 0.067 7 | |
| Grasa | 0.015 96 | 0.006 2* | 0.003 35 | 0.007 8* | |
| Razón residual | Teobromina | 94.287 | - 1.827 | - 1.400 8 | 3.459 |
| Razón de remoción | Grasa | 81.511 | 7.422* | - 3.699 9 | - 9.194 5* |
| Cafeína | 62.529 | 0.905 85 | 8.823 | - 7.969 5 |
* P ≤ 0.05
Conclusiones
Las condiciones de temperatura y presión del proceso de extracción supercrítica con CO2 , en condiciones estáticas de operación, aplicadas a un lecho de polvo de cascarilla de cacao, permitieron extraer grasa y cafeína, además de retener en el residuo a la teobromina. Los efectos de las variables de temperatura y presión para la grasa, ya sea en el residuo o en la razón de remoción, pueden ser predichas a través de un polinomio de primer orden con efectos de interacción, no así para cafeína. Se requieren estudios adicionales, aplicando nuevamente condiciones de extracción supercrítica para ver el comportamiento del residuo sin el contenido de grasa, que llega a representar hasta el 8 % inicial.











 nova página do texto(beta)
nova página do texto(beta)