La palinología es una herramienta importante en el estudio de la flora, ya que, entre otros casos, aporta información útil en estudios taxonómicos. Por ejemplo, la morfología y micromorfología de las esporas de los helechos aportan caracteres como el tamaño, la forma y la ornamentación del perisporio, los cuales pueden ayudar a resolver problemas de delimitación taxonómica a nivel de familia, género y en algunos casos especie (Lellinger y Taylor, 1997). Adicionalmente, la información que los palinomorfos nos brindan puede ser empleada en estudios de tipo ecológico, fenológico y dispersión, como indicadores geológicos y paleoecológicos del registro fósil y en el campo forense (Harris, 1957; Vaughn et al., 1990).
Las Gleicheniaceae, por sus características anatómicas, morfológicas y por el registro fósil, se consideran dentro del grupo de los helechos leptosporangiados basales, apareciendo por primera vez durante el Cretácico, entre 144 y 65 millones de años atrás (Wallace et al., 1983; Thomas y Spicer, 1987; Gandolfo et al., 1997; Herendeen y Skog, 1998; Moran, 2004); comprende plantas cuyos rizomas son postrados con estela de tipo protostélico o solenostélico; láminas divididas pseudodicotómicamente (excepto en Stromatopteris Mett.); venación libre bifurcada; esporangios globoso con un anillo oblicuo y esporas tetraédricas o bilaterales (Smith et al., 2006).
De las 125 especies reconocidas actualmente en la familia (Smith et al., 2006), sólo Dicranopteris flexuosa (Schrad.) Underw., Diplopterygium bancroftii (Hook.) A. R. Sm., Gleichenella pectinata (Willd.) Ching, Sticherus bifidus (Willd.) Ching, S. brevipubis (Christ) A. R. Sm., S. palmatus (W. Schaffn. ex E. Fourn.) Copel. y S. underwoodianus (Maxon) Nakai, se encuentran en México (Smith et al., 2006).
La circunscripción de la familia Gleicheniaceae ha sido controvertida. Así por ejemplo, Christensen (1906) reconoce dos géneros: Gleichenia Sm. y Stromatopteris y divide a este último en tres subgéneros, posteriormente Underwood (1907) acepta además de los dos taxa anteriores a Dicranopteris Bernh. y Platyzoma R.Br., por su parte Christensen (1938) reconoce los cuatro géneros previos y adiciona a Sticherus C. Presl., Ching (1940) y Copeland (1947) siguen la propuesta de Christensen (1938), incluyendo además el primer autor a Gleichenella Ching y el segundo a Hicriopteris C.Presl., Nakai (1950) segrega a Platyzoma en su propia familia, Platyzomaceae, y Gleicheniaceae queda integrada por tres subfamilias y nueve géneros. Holttum (1957) divide al grupo en dos géneros: Dicranopteris y Gleichenia con dos y tres subgéneros respectivamente. Sin embargo, en las clasificaciones más recientes, Smith et al. (2006) y Christenhusz et al. (2011) reconocen para las Gleicheniaceae seis géneros a nivel mundial, Dicranopteris, Diplopterygium, Gleichenella, Gleichenia, Sticherus y Stromatopteris. La inclusión de este último género se ve apoyada por los estudios fitoquímicos realizados por Wallace et al. (1983) y Yusuf et al. (2003), en los que se demuestra la presencia de compuestos fenólicos (kaempferol y quercetina) en 16 especies de Gleicheniaceae incluyendo a Stromatopteris.
En lo que se refiere al estudio palinológico, son diversos los trabajos que incluyen información sobre la morfología de las esporas de alguna de las especies de la familia Gleicheniaceae (Erdtman y Sorsa, 1971; Lugardon, 1974; Tryon y Tryon, 1982; Kramer, 1990; Tryon y Lugardon, 1991; Palacios-Ríos, 1992;Velázquez-Montes, 2012), sin embargo los estudios realizados no abarcan la totalidad de las especies mexicanas. Es por esta razón que en el presente trabajo, utilizando microscopía electrónica de barrido (MEB), se describe la micromorfología de las esporas de las especies de Gleicheniaceae que crecen en México, describiéndose por primera vez las esporas de Sticherus brevipubis, S. palmatus y S. underwoodianus con base a fotomicrografías tomadas bajo MEB.
Materiales y métodos
Los ejemplares de respaldo y pinnas fértiles, fueron recolectados en distintas localidades de los estados de Oaxaca, Puebla y Veracruz (Tabla 1). Los especímenes se determinaron taxonómicamente con base en Mickel y Smith (2004) y se cotejaron con material de diferentes herbarios, entre ellos MEXU y UAMIZ, para corroborar su correcta determinación, una vez procesados se depositaron en la colección de los herbarios arriba mencionados. Las pinnas fértiles fueron colocadas en sobres de papel manila, los cuales fueron rotulados y colocados en estantes de tipo esqueleto durante una semana para propiciar la liberación de las esporas. Posteriormente se hizo pasar el contenido de los sobres por un tamiz con una malla de 74 µm de diámetro para eliminar restos de esporangios, pelos y/o escamas. Las esporas se depositaron en viales de plástico y se almacenaron bajo condiciones de refrigeración a 10 °C para conservarlas. Para las observaciones en el microscopio electrónico de barrido, se utilizaron pinceles de pocas cerdas con los que se espolvoreó una pequeña cantidad de esporas de cada especie sobre cinta de carbón de doble cara adherida a portamuestras de aluminio. Estas se cubrieron con una capa de oro-paladio utilizando una ionizadora Denton Vacuum Desk II. Una vez procesadas las muestras, fueron llevadas al Microscopio Electrónico de Barrido JEOL JSM-5310LV a 15 kv, donde se tomaron fotomicrografías de las esporas en vista proximal, distal, así como el acercamiento de la superficie de las esporas. Las imágenes digitales se obtuvieron con el sistema Orion-Jeol y fueron procesadas con el programa Adobe Photoshop CS5.
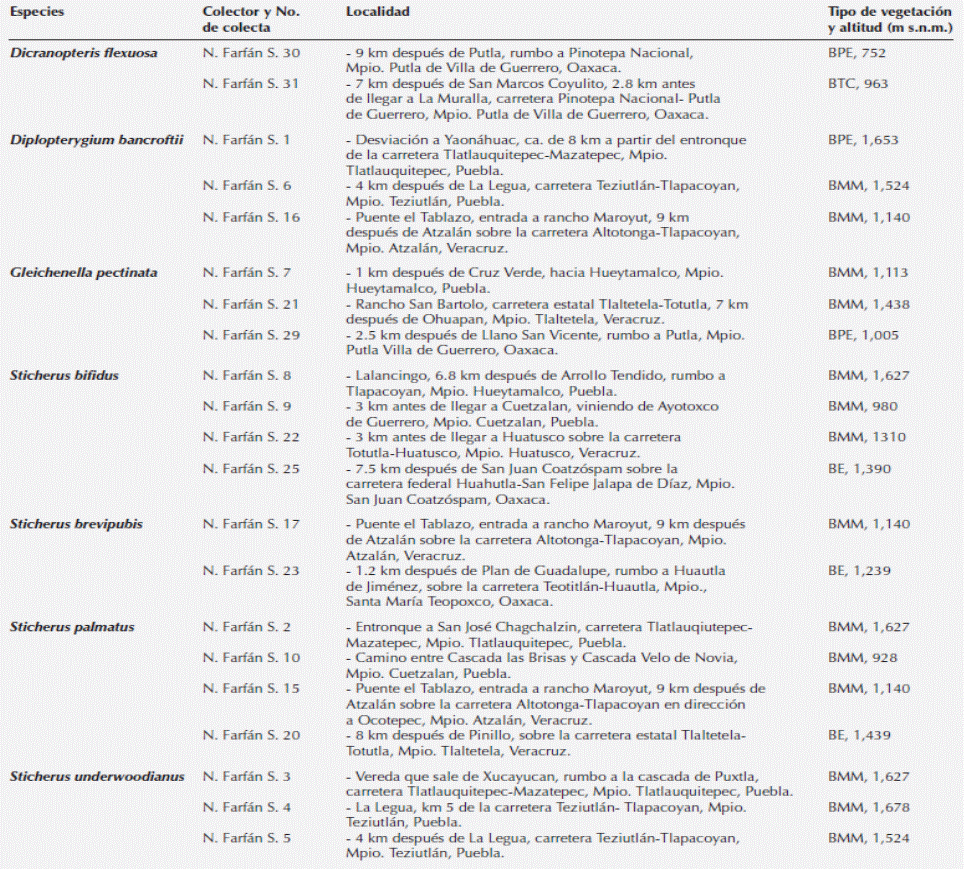
Tabla 1 Especies de la familia Gleicheniaceae recolectadas en varias localidades de México (BE = Bosque de encino, BPE = Bosque pino-encino, BMM = Bosque mesófilo de montaña, BTC = Bosque tropical caducifolio, con base en Rzedowski, 2006).
Adicionalmente se obtuvieron imágenes con un microscopio óptico Olympus modelo BX41 (MO), así mismo se seleccionaron al azar 25 esporas por especie, de las que se registró la coloración y se tomaron medidas, en el caso de las monoletes, de los ejes polar y ecuatorial y de las triletes sólo del eje ecuatorial, obteniéndose en cada caso el tamaño promedio.
Resultados
Todas las especies estudiadas son homospóricas, dos de ellas presentan esporas triletes y las cinco restantes monoletes. A continuación se describe la micromorfología, ornamentación y tamaño (mínimo, promedio, máximo y ± desviación estándar) de cada uno de los taxa de la familia Gleicheniaceae que crecen en México, ilustrando cada una de las especies con imágenes de las esporas obtenidas con el microscopio electrónico de Barrido (MEB) y con microscopio óptico (MO).
Dicranopteris flexuosa (Schrad.) Underw.
Esporas triletes; vista polar: forma subtriangular, contorno convexo-triangular, lados convexos, ángulos redondeados, lesura prominente > 3/4 del radio, torus presente; ornamentación isopolar: caras proximal y distal escábridas, elementos irregulares < 1 µm (Figura 1A-C); eje ecuatorial de 25 (32) 38 ± 3.7 µm; coloración amarillenta a simple vista y al MO (Figura 1D).
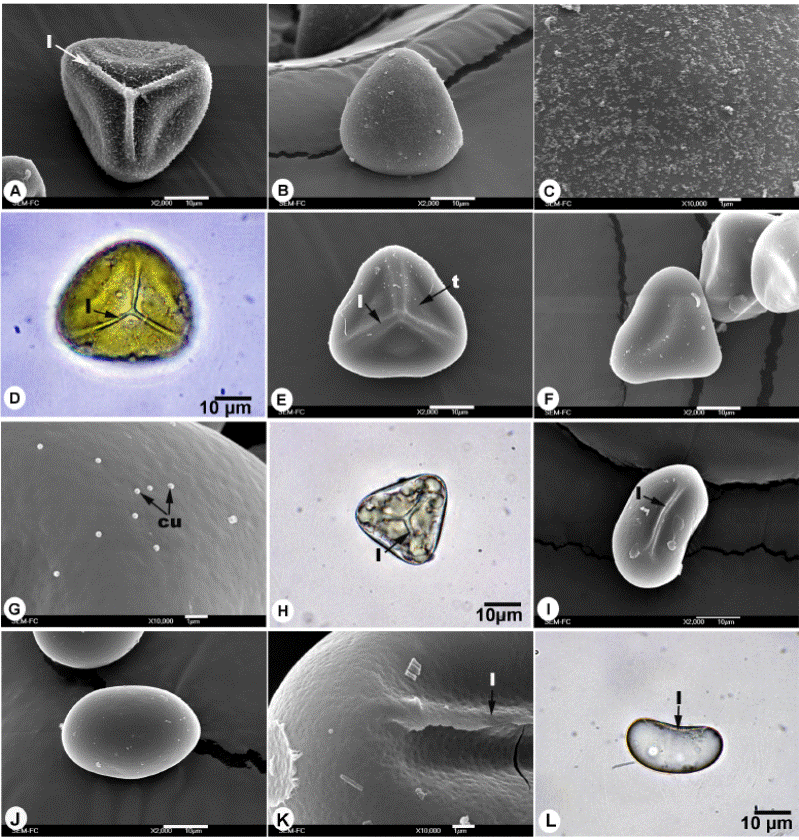
Figura 1 Esporas de Gleicheniaceae. A-D) Espora trilete de Dicranopteris flexuosa, A) Vista proximal, B) Vista distal, C) Acercamiento de superficie, D) Vista proximal en microscopía óptica. E-H) Espora trilete de Diplopterygium bancroftii, E) Vista proximal, F) Vista distal, G) Acercamiento de la superficie, F) vista proximal, H) vista proximal en microscopía óptica. I-L) Espora monolete de Gleichenella pectinata, I) Vista proximal, J) Vista distal. K) Acercamiento de la superficie. L) Vista ecuatorial en microscopía óptica. cu = cuerpos de Ubish, l = lesura, t = torus.
Diplopterygium bancroftii (Hook.) A. R. Sm.
Esporas triletes; vista polar: forma triangular, contorno triangular ligeramente cóncavo, lados rectos a ligeramente cóncavos, ángulos redondeados, lesura prominente > 3/4 del radio, zonas de contacto evidentemente deprimidas, formando lagunas triangulares; ornamentación isopolar: caras proximal y distal psiladas con escasos gránulos orbiculares denominados cuerpos de Ubish (MEB, Figura 1E-G); eje ecuatorial de 25 (31) 37 ± 3.2 µm; coloración amarillo pálido a simple vista, hialinas en MO (Figura 1H).
Gleichenella pectinata (Willd.) Ching
Esporas monoletes; vista polar: forma elipsoidal; vista ecuatorial: forma reniforme, polo proximal plano a cóncavo, polo distal convexo; lesura lineal prominente de menos de 1 µm de ancho y extendida 1/2 del eje ecuatorial; ornamentación isopolar: caras proximal y distal psilada (MO), nanofoveolada (MEB), foveolos < 0.5 µm con escasos cuerpos de Ubish (MEB, Figura 1I-K); eje ecuatorial de 28 (32) 38 ± 2.7 µm, eje polar de 13 (18) 23 ± 2.2 µm; coloración blanquecina a simple vista, hialinas al MO (Figura 1L).
Sticherus bifidus (Willd.) Ching
Esporas monoletes; vista polar: forma elipsoidal; vista ecuatorial: reniforme, polo proximal cóncavo, polo distal convexo; lesura lineal prominente de 1.5 a 2 µm de ancho, mayor a 1/2 el eje ecuatorial; ornamentación isopolar: caras proximal y distal nanofoveolada a perforada (MEB, Figura 2A-C) con escasos cuerpos de Ubish; eje ecuatorial de 33 (39) 45 ± 3.2 µm, eje polar de 15 (19) 25 ± 2.6 µm; coloración amarilla a simple vista, hialina a amarillo pálido en MO (Figura 2D).
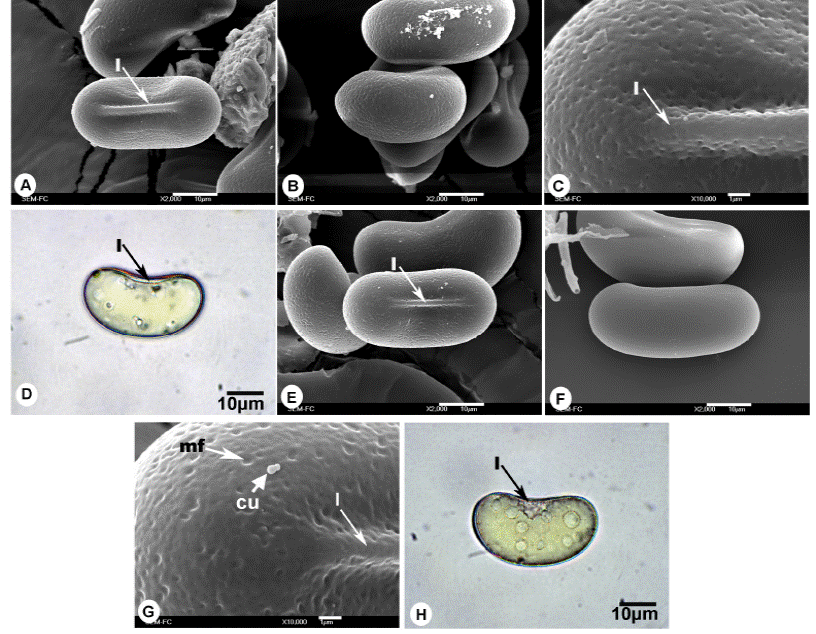
Figura. 2 Esporas de Gleicheniaceae. A-D. Espora monolete de Sticherus bifidus, A) Vista proximal, B) Vista distal, C) Acercamiento de la superficie, D) Vista ecuatorial en microscopía óptica. E-H) Espora monolete de Sticherus brevipubis, E) Vista proximal, F) Vista distal, G) Acercamiento de la superficie, H) Vista ecuatorial en microscopía óptica. cu = cuerpos de Ubish, l = lesura, mf = microfoveolas.
Sticherus brevipubis (Christ.) A. R. Sm.
Esporas monoletes; vista polar: elipsoidal; vista ecuatorial: reniforme, polo proximal cóncavo, polo distal convexo; lesura lineal prominente, de 1 a 1.5 µm, extendida de 1/3 a 1/2 del eje ecuatorial; ornamentación isopolar: caras proximal y distal microfoveolada a perforada (MEB, Figura 2F-G) con escasos cuerpos de Ubish; eje ecuatorial de 30 (38) 48 ± 4.9 µm, eje polar de 15 (19) 25 ± 2.6 µm; coloración pardo claro-amarillenta a simple vista, hialinas MO (Figura 2H).
Sticherus palmatus (W. Schaffn. ex E. Fourn.) Copel.
Esporas monoletes; vista polar: forma elipsoidal, lados rectos; vista ecuatorial: reniforme, polo proximal plano a ligeramente cóncavo, polo distal convexo; lesura lineal prominente > 3/4 del eje ecuatorial; ornamentación isopolar: caras proximal y distal nanofoveolado (MEB, Figuras 3A-C); eje ecuatorial de 30 (36) 43 ± 3.3 µm, eje polar de 13 (17) 20 ± 1.8 µm; coloración amarilla a simple vista, amarillo-pálido MO (Figura 3D).
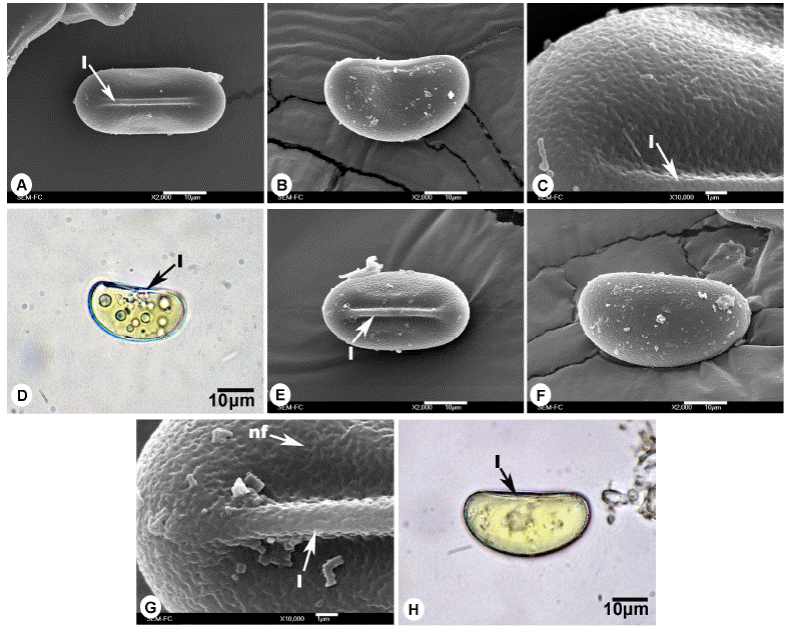
Figura 3 Esporas de Gleicheniaceae. A-D. Espora monolete de Sticherus palmatus, A) Vista proximal, B) Vista ecuatorial, C) Acercamiento de la superficie, D) Vista ecuatorial en microscopía óptica. E-H) Espora monolete de Sticherus underwoodianus, E) Vista proximal, F) Vista distal, G) Acercamiento de la superficie, H) Vista ecuatorial en microscopía óptica. l = lesura, nf = nanofoveolas.
Sticherus underwoodianus (Maxon) Nakai
Esporas monoletes; vista polar: forma elipsoidal, lados planos a convexos; vista ecuatorial: reniforme, polo proximal recto, polo distal convexo; lesura lineal prominente de 1.5 a 2 µm de ancho, mayor a 3/4 el eje ecuatorial; ornamentación isopolar: caras distal y proximal hamulada (rugulas irregulares) con nanofoveolos (MEB, Figura 3E-G); eje ecuatorial de 33 (40) 45 ± 3.0 µm, eje polar de 15 (20) 28 ± 2.9 µm; coloración blanquecina a amarillenta a simple vista, amarilla a hialina en MO (Figura 3H).
Discusión
Las observaciones de este trabajo coinciden con lo señalado en otros sobre la apertura de las esporas de especies de la familia (Erdtman y Sorsa, 1971; Lugardon, 1974; Tryon y Tryon, 1982; Kramer, 1990; Tryon y Lugardon, 1991; Palacios-Ríos, 1992; Velázquez-Montes, 2012), en el entendido de que las esporas en Dicranopteris flexuosa y Diplopterygium bancroftii son triletes; mientras que en Gleichenella pectinata, Sticherus bifidus, S. brevipubis, S. palmatus y S. underwoodianus son monoletes.
En cuanto al tamaño de las esporas triletes, las de Dicranopteris flexuosa y Diplopterygium bancroftii, presentan dimensiones similares con 32-31 µm de diámetro respectivamente; mientras que las esporas monoletes de Gleichenella pectinata fueron las más pequeñas con 32 µm de largo (vista ecuatorial) × 18 µm de ancho (vista polar) y las de Sticherus las más grandes con 36-49 µm en vista ecuatorial × 17-20 µm en vista polar.
En lo que se refiere a la ornamentación de las esporas, se encontró que las de Diplopterygium bancroftii, Gleichenella pectinata y las especies de Sticherus presentan cuerpos de Ubish en su superficie, mientras que las de Dicranopteris flexuosa son microgranuladas o escábridas (Tryon y Tryon, 1982; Kramer, 1990; Tryon y Lugardon, 1991) y no psiladas a ligeramente ruguladas como lo indica Velázquez-Montes (2012), lo anterior pueden deberse a las técnicas empleadas para examinar el material, ya que en el último trabajo citado las descripciones se realizaron con base a observaciones hechas con microscopio óptico, mientras que en los demás se utilizó microscopio electrónico de barrido.
Las esporas de Diplopterygium bancroftii presentan una superficie predominantemente psilada con cuerpos de Ubish dispersos lo cual concuerda con trabajos previos para esta especie (Lugardon, 1974; Tryon y Lugardon, 1991; Velázquez-Montes, 2012). Por su parte las de Gleichenella pectinata poseen una superficie predominantemente psilada a ligeramente nanofoveolada con escaso cuerpos de Ubish. La presencia de nanofoveolos y cuerpos de Ubish no habían sido reportada para esta especie en estudios previos (Erdtman y Sorsa, 1971; Tryon y Lugardon, 1991); en el caso de las esporas de Sticherus se observó que las de S. bifidus y S. palmatus tienen una superficie perforada o nanofoveolada coincidiendo con los reportes de Tryon y Tryon (1982) , Kramer (1990) y Tryon y Lugardon (1991) y no lisas como las describen Erdman y Sorsa (1971) para S. bifidus, mientras que las de S. brevipubis son perforadas y las de S. underwoodianus son perforadas o ruguladas.
Tomando en cuenta los resultados obtenidos en este trabajo, se considera que las Gleicheniaceae mexicanas pueden separarse a nivel genérico y en algunos casos a nivel específico, por la forma monolete o trilete, tipo de lesura, ornamentación del exosporio o perisporio y por el tamaño de sus esporas.
Cabe señalar que la micromorfología de las esporas de Sticherus brevipubis, S. palmatus y S. underwoodianus se describe por primera vez aquí, presentando imágenes de Microscopio Electrónico de Barrido que aportan información nueva y detallada respecto a la ornamentación de las esporas de Gleicheniaceae.
Las descripciones detalladas de la micromorfología de las esporas son útiles en los tratamientos taxonómicos de los helechos, ya que ayudan a distinguir géneros y en algunos casos especies como en el caso de las Gleicheniaceae mexicanas y para caracterizar a las familias. El tamaño y forma irregular también permiten distinguir grupos poliploides e híbridos (Brown, 1960). Finalmente el conocer con mayor detalle la micromorfología de las esporas de los helechos se aportan datos para realizar estudios de dispersión y lluvia de esporas (Gómez-Noguez et al., 2013) ya que nos ayuda a identificar las esporas recolectadas en el campo de manera más precisa.











 nova página do texto(beta)
nova página do texto(beta)


