Introducción
Los coronavirus son patógenos que afectan a animales y humanos, que ocasionan enfermedades neurológicas, respiratorias, intestinales y hepáticas; se conocen 6 coronavirus que causan enfermedades en los humanos, entre ellas el síndrome respiratorio agudo por coronavirus (SARS-CoV) que ocasionó epidemia en 2002 y el síndrome respiratorio del Medio Oriente (MERS-CoV) en 2012.1
Revisión de la literatura
Epidemiología
La pandemia por la que ahora atravesamos se originó en la provincia de Hubei en Wuhan, China, reportando el primer caso de neumonía el 12 de diciembre de 2019, ocasionando una epidemia, asociando los primeros casos a trabajadores o personas que habían visitado un mercado de mariscos y animales vivos. Del 18 al 29 de diciembre de 2019, se habían hospitalizado 5 pacientes con síndrome de distrés respiratorio agudo y uno de ellos había fallecido. Al 21 de enero de 2020, había 41 pacientes hospitalizados confirmados con infección por el nuevo coronavirus 2019 (COVID-19).
Los casos fueron ascendiendo, al 22 de enero de 2020 se reportaban 571 casos en 25 provincias de China, con 17 defunciones según lo reportado por la Comisión Nacional de Salud de China. El 30 de enero de 2020, se reportaban 7 734 casos, con 90 casos confirmados en países asiáticos fuera de China, así como, el primer caso en Estados Unidos. En febrero de 2020, la Organización Mundial de la Salud, le denominó COVID-19 y el Comité Internacional de Taxonomía de Virus (ICTV) como SARS-CoV-2.1-4
Para el 11 de marzo de 2020, la OMS declaró al síndrome respiratorio agudo SARS-CoV-2 como pandemia, con un total de 118,000 casos, 4 291 defunciones, afectando a un total de 114 países.5
En China, al 18 de marzo se habían reportado 13 415 casos confirmados y 120 defunciones, afectando a 30 provincias a pesar de las medidas masivas de salud pública que se implementaron a partir de la tercera semana de enero. El aislamiento domiciliario inicio en Wuhan el 23 de enero 2020, posteriormente aplicando estas medidas en las entidades contiguas hasta las megaciudades (como Beijing y Shanghái): distanciamiento social, uso de mascarilla facial obligatorio, cierre de escuelas, así como el cierre de servicios no esenciales. El 27 de enero 2020, ya se reportaba contagio comunitario fuera de Wuhan. En algunas provincias lograron retornar paulatinamente a las actividades cuando presentaron una disminución de casos hasta llegar a cero a finales de febrero 2020.
En Wuhan y la provincia de Hubei, el 16 de marzo 2020 se empezaron a levantar algunas de las restricciones; sin embargo, se espera un segundo brote de transmisión de COVID-19 debido a reintroducción del virus, principalmente por importación internacional proveniente de Europa y América y el retorno a actividades económicas normales, así como la interacción de personas.6 Hasta abril de 2020, se han reportado 83 402 casos positivos en China.
Al día 30 de abril de 2020, se han confirmado más de 3 000 000 casos en el mundo, afecta a 185 países, con más de 200 000 defunciones y aproximadamente 420 000 pacientes recuperados, presentando una mayor incidencia en Estados Unidos, seguido por España e Italia.7
En México, según la Secretaría de Salud del Gobierno de México y de acuerdo al Sistema Nacional de Vigilancia Epidemiológica (SINAVE) se han confirmado al 30 de abril de 2020: 19,224 casos positivos; con 5,912 casos activos; 15,520 casos sospechosos y 1,859 defunciones; realizando hasta el momento un total de 87,372 pruebas (ver imagen 1).8
Fisiopatología y diagnóstico
Los coronavirus son virus zoonóticos, de ARN. El SARS-CoV-2 en la secuenciación genómica se identificó como un betacoronavirus, dentro del subgénero de los coronavirus del murciélago (de los cuales son reservorios) y al responsable del SARS-CoV de la subfamilia de los Orthocoronavirinae. Los betacoronavirus causan infecciones en murciélagos, animales salvajes, así como en humanos. Dentro del análisis filogenético se reconocieron 130 cepas, de las cuales el tipo L se identificó como responsable del 70% de los casos en China (sobre todo en Wuhan) y el 30% a la cepa S.1,4,9
Acerca de la ruta de transmisión, no se sabe si hubo algún huésped intermediario, posteriormente desarrollándose la transmisión persona-persona mediante secreciones respiratorias o al contacto con superficies contaminadas con mucosas como ojos, nariz y/o boca. El primer paso para la entrada del virus es la unión al receptor en el hospedero, en este caso, en el epitelio respiratorio, el SARS-CoV-2 utiliza como receptor a la enzima convertidora de angiotensina II (ECA-II), permitiendo la unión de proteínas virales (proteínas S inicialmente) que intervienen con la respuesta inmune del huésped, seguido por la fusión a la membrana celular e iniciando su replicación. Algunos factores del huésped pueden hacerlo más susceptible a desarrollar un efecto inflamatorio persistente con una “tormenta de citocinas” desarrollando condiciones críticas como hipoxia, choque séptico, entre otras.1,2,4,9
El periodo de incubación es de 1-14 días, aunque la mayoría de los casos se reportan entre el cuarto al quinto día posexposición. De acuerdo a estudios de la población china, reportados en la Comisión de Control y Prevención de Enfermedades de China, el 81% de los casos son leves con un cuadro leve de neumonía o sin neumonía; el 14% como casos moderados con disnea e hipoxia, así como afección pulmonar mediante estudios de imagen; 5% estado grave con falla respiratoria, choque o disfunción multiorgánica. Asimismo, se han reportado casos asintomáticos. Los principales síntomas se enlistan en la Tabla 1.
Tabla 1 Síntomas más frecuentes
| Síntoma | Porcentaje |
|---|---|
| Fiebre | 99% |
| Fatiga | 70% |
| Tos seca | 59% |
| Anorexia | 40% |
| Mialgia | 35% |
| Disnea | 31% |
| Producción de esputo | 27% |
Fuente: Tabla modificada de la CDC de China.
Con una duración media de la sintomatología de 11.5 días. Las manifestaciones clínicas más graves son el síndrome de distrés respiratorio, choque séptico, acidosis metabólica refractaria al tratamiento médico, coagulopatías y falla orgánica múltiples. Éstas últimas son más frecuentes en pacientes con comorbilidades como enfermedades respiratorias crónicas, cardiovasculares, diabetes, hipertensión, enfermedad renal crónica y pacientes oncológicos.1,2,9,10
Otras manifestaciones neurológicas que se han reportado son anosmia, cefalea; respiratorias: rinorrea y odinofagia y gastrointestinales: náusea y diarrea. Ver figura 1.
El diagnóstico se realiza mediante una prueba de amplificación de ácido nucleico, como es la reacción en cadena de polimerasa transcriptasa reversa en tiempo real (PCR-RT) de exudado nasofaríngeo, orofaríngeo, aspirado broncoalveolar o de esputo. También se ha detectado en sangre y en heces. No se ha identificado en orina ni en líquido seminal.11 Por cuestiones de seguridad, no se encuentran indicados los cultivos. Las pruebas diagnósticas se deben de realizar bajo protocolos de control y prevención de infecciones.
Es importante que una prueba negativa no excluye el diagnóstico, ya que existen falsos negativos. En una persona con alta sospecha de COVID-19 se debe de considerar repetir la prueba por lo menos con un día de diferencia, sobre todo si la muestra inicial fue tomada de tracto respiratorio superior; se puede deber a poco material de muestra, haber realizado la prueba en etapa temprana o tardía de la enfermedad, manejo inadecuado del material o alguna circunstancia inherente a la prueba (ej. mutación del virus).12
Asimismo, se encuentran pruebas serológicas, de reciente desarrollo en Asia, Europa y Estados Unidos para la detección cualitativa de anticuerpos de inmunoglobulina G (IgG) e inmunoglobulina M (IgM) de SARS-CoV-2 en sangre y plasma, los cuales, hasta el 8 de abril 2020, aún no se encuentran validados por la Organización Mundial de la Salud. Por lo general, se pueden detectar los anticuerpos entre la segunda y tercera semana de iniciados los síntomas y la seroconversión ocurre primero para IgG que para IgM presentando mayor respuesta mientras más grave el cuadro clínico. Se propone, que dichas pruebas inmunológicas podrían también tener utilidad para detectar casos de COVID-19 cuando la prueba de ARN por PCR-TR resulte negativa y la sospecha sea alta.13,14
Durante el abordaje de la enfermedad crítica es importante la medición de la saturación de oxígeno, gasometría arterial para conocer el estado metabólico, perfil metabólico, marcadores de inflamación, tiempos de coagulación, troponina sérica, deshidrogenasa láctica y creatincinasa. Dentro de los estudios de laboratorio se han establecido factores de alto riesgo enlistados en la Tabla 2 los cuales nos hablan de un mal pronóstico en caso de que el paciente requiera apoyo ventilatorio mecánico invasivo.1,15
Tabla 2 Factores de mal pronóstico
| Leucocitosis |
| Leucopenia |
| Linfopenia |
| Elevación DHL |
| Elevación enzimas hepáticas |
| Elevación dímero D |
| Elevación PCR, procalcitonina, ferritina |
| Elevación protrombina y trombina |
| Elevación creatinin fosfocinasa |
| Lesión renal aguda |
En los estudios de imagen se prefieren el uso de radiografía de tórax y tomografía de tórax, esta última presenta una sensibilidad del 97% y una especificidad del 25%. Dentro los hallazgos tomográficos se describen los siguientes: 1) opacificaciones en patrón de vidrio despulido con o sin consolidaciones, 2) afección principalmente bilateral, con distribución periférica y basal, 3) engrosamiento pleural, 4) derrame pleural (ver Imagen 2 y 3).1,2,10,15
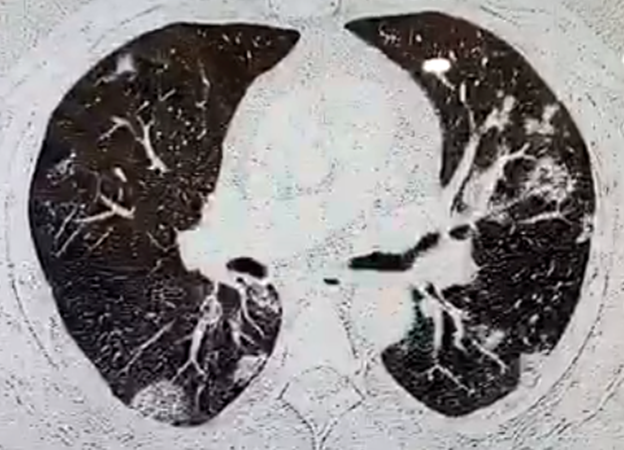
Imagen 2 Tomografía de tórax simple corte axial de paciente masculino de 45 años con evidencia de consolidaciones periféricas con patrón en vidrio despulido.
Tratamiento
Es importante mencionar que a la fecha no se ha aprobado ninguna terapéutica definitiva o específica para el tratamiento y control de la infección por COVID-19, ya que aún no hay ensayos clínicos aleatorizados que comprueben el beneficio sobre los pacientes afectados. Actualmente se encuentran más de 300 ensayos en estudio, por lo que en esta parte del artículo se citan dichos estudios con la intención de que sirva de base para el tratamiento de pacientes con diagnóstico de COVID-19 y a orientar las investigaciones posteriores hacia un tratamiento adecuado.
Al momento se han propuesto varias líneas de investigación para posibles terapéuticas. La primera es utilizar los antivirales de amplio espectro actuales en estudios estandarizados, la segunda consiste en investigación de compuestos químicos en las bases de datos para encontrar una terapéutica aplicable, y la tercera es basar la investigación en la genómica y fisiopatología de los distintos tipos de coronavirus a fin de encontrar un antiviral nuevo y funcional.16 Ante la ausencia de evidencia clínica, el manejo principal es el tratamiento de soporte.
Por lo anterior, la principal recomendación hasta el momento que los autores podemos realizar es que se evite el contagio a través de la prevención del contacto con enfermos o superficies contaminadas y confirmadas de COVID-19, mediante el estricto seguimiento de las recomendaciones de prevención de contagio de enfermedades virales del CDC “Discontinuation of Transmission-Based Precautions or Home Isolation”.17
Manejo clínico
Pacientes asintomáticos:
Son pacientes que se encuentran o que estuvieron en contacto con un probable caso positivo confirmado de COVID-19. El manejo de estos pacientes dependerá de las directrices gubernamentales de cada país, pero la recomendación científica es que debe ser aislado de humanos y animales y monitoreado de manera diaria por 14 días al menos.18
Enfermedad leve a moderada:
Son pacientes en quienes no se ha identificado neumonía o hipoxia, por lo que inicialmente no requerirán manejo hospitalario o dependiente de oxígeno. Esta decisión puede realizarse vía telefónica o a distancia por personal médico o paramédico debidamente entrenado, reduciendo así el contacto y exposición tanto de pacientes como del personal de la salud. La decisión dependerá de los factores de riesgo del paciente como edad, comorbilidades y capacidad de manejo y monitoreo en casa. Existe una alta probabilidad en pacientes de alto riesgo de progresión a enfermedad grave en los siguientes 7-10 días después del inicio de los síntomas, por lo que podría requerir atención hospitalaria e incluso de terapia intensiva.
El manejo de esta etapa de la enfermedad es únicamente sintomático con antipiréticos y se recomienda altamente el aislamiento del paciente de todo contacto con animales o humanos. Hasta el momento no se ha comprobado que ninguno de los medicamentos pueda empeorar o mejorar la evolución de los pacientes diagnosticados con COVID-19, por lo cual citamos que la Asociación Americana de Cardiología ha recomendado que se continúen los medicamentos antihipertensivos, antiarrítmicos, o que el paciente utilice para prevención o tratamiento de eventos isquémicos o falla cardíaca.17,18
Enfermedad grave:
Son pacientes con datos de neumonía grave o enfermedad severa que requieran manejo hospitalario de soporte para los cuales haremos mención de las terapias sugeridas o que actualmente se encuentren en estudio.18 En cuanto a los esteroides se menciona en un reporte de casos de pacientes con enfermedad severa en China, que no se puede demostrar el beneficio de estos al no ser un estudio controlado y ser únicamente observacional. Sin embargo, recomiendan que se debe limitar su uso a pacientes con enfermedad pulmonar obstructiva crónica, con exacerbación de la misma o que se encuentren en choque séptico, ya que se demostró en pacientes con influenza y otros tipos de coronavirus que los esteroides prolongan la replicación viral, aumentan el tiempo de ventilación mecánica y presentan mayor mortalidad.17,19
En esta etapa de la enfermedad se requerirá atención de terapia crítica de los pacientes en los cuales se deberá manejar los pacientes por individual y dar soporte para los distintos órganos y sistemas afectados como pueden ser neumonía, falla ventilatoria, sepsis y choque séptico, miocardiopatía y arritmias, falla renal, y otras complicaciones de la hospitalización prolongada incluyendo sobreinfecciones bacterianas, embolias, sangrado gastrointestinal y polineuropatías.17,18 Los manejos propuestos para el manejo hospitalario de pacientes con COVID-19 se encuentran en los anexos 1, 2 y 3.
Reinfección
En cuanto a la posibilidad de reinfección por SARS-CoV-2 después de haberse recuperado el Centro de Control de Enfermedades opina que “…el conteo de RNA viral disminuye con la resolución de los síntomas, y puede continuar de esta manera por semanas, sin embargo la detección de RNA durante la convalecencia no necesariamente indica la presencia de virus infecciosos viables, la recuperación clínica se ha relacionado más bien con la detección de anticuerpos IgM e IgG lo que es señal de que se ha desarrollado inmunidad”.17
Terapias en estudio
En cuanto a agentes antivirales el Remdesivir (GS-5734) es una droga intravenosa que se considera un antiviral de amplio espectro, que inhibe la replicación viral a través de la finalización prematura de la transcripción del RNA viral, dicho agente ha demostrado actividad contra el SARS CoV-2 in vitro y en vivo en contra de otros betacoronavirus.17,19
Otro antiviral que se encuentra en estudio es el Umifenovir, cuyo mecanismo de acción es inhibir la unión entre la proteína S y el ACE-II inhibiendo la fusión de la membrana del virus. Actualmente aprobado en China y en Rusia como profilaxis para la influenza, sin embargo, ensayos clínicos se están llevando a cabo para probar su eficacia contra el SARS-CoV-2.20
La Nitazoxanida es un agente antihelmíntico con actividad antiviral que in vitro ha demostrado actividad contra el MERS y SARS-CoV-2. Sin embargo, se requiere más evidencia acerca de su actividad antiviral, efectos inmunomoduladores, así como perfil de seguridad.20
Respecto a hidroxicloroquina y cloroquina el CDC opina que “se encuentran bajo investigación y en estudios clínicos de preexposición y postexposición como profilaxis ante la infección por SARS-CoV-2 y como tratamiento de pacientes con enfermedad leve, moderada y severa…”.17,19
Para continuar profundizando en este tema en caso de requerirlo para manejo clínico de algún paciente se sugiere al lector acudir a la página: https://clinicaltrials.gov/ y a revisar las guías interinas del CDC y la OMS ya que estas se actualizan constantemente.
Tromboprofilaxis
En este respecto se ha identificado que los pacientes diagnosticados con SARS-CoV-2 presentan distintas alteraciones en cuanto a la coagulación siendo las principales:21
Elevación en nivel plasmático del dímero D (DD)
Elevación del nivel plasmático de fibrinógeno (FIB)
Prolongación moderada del tiempo de protrombina (TP)
Trombocitosis moderada
Disminución moderada de la actividad de antitrombina (AT)
Estos factores son de mal pronóstico para el paciente que ingresa a Unidad de Terapia Intensiva de Adultos (UTIA), predisponiéndolo principalmente a tromboembolia venosa profunda, se refiere también que la insuficiencia cardiaca es en sí misma un factor de mal pronóstico para el paciente que ingresa a UTIA. Asimismo, se reportaron 3 casos en China de evento cerebrovascular isquémico (EVC) asociado a las mismas características de coagulopatía, sin establecer hasta el momento ninguna recomendación.17 Asimismo, recordar que la sepsis también es un factor de riesgo para presentar coagulación intravascular diseminada (CID).22
Por lo tanto, de acuerdo a la Sociedad Española de Anestesiología, Reanimación y Terapéutica del dolor se establecen las siguientes propuestas:21
Se recomienda mantener la anticoagulación en los pacientes que la precisen según sus indicaciones.
En los pacientes, con infección grave por Covid-19, ingresados al hospital, se recomienda la administración de tromboprofilaxis farmacológica, siendo de elección la heparina de bajo peso molecular, a las dosis habituales (3500-4000 UI/24h).
En los casos con antecedentes de trombocitopenia inducida por heparina (TIH), se sugiere plantear como alternativa la administración de fondaparinux (2.5 mg/24h sc) (fuera de indicación).
Ajuste de dichos medicamentos a función renal.
-
Específicamente respecto algunos medicamentos recomiendan:
◊ Ácido acetilsalicílico (AAS): se recomienda continuar el tratamiento con AAS en los casos indicados de prevención secundaria instaurados con anterioridad a haber contraído la enfermedad.
◊ Clopidogrel: no se recomienda su empleo en estos pacientes por la potencial disminución de su efecto al interaccionar con lopinavir/ritonavir. En caso necesario, valorar sustitución por Prasugrel.
◊ Ticagrelor: no se recomienda su empleo en estos pacientes por el potencial aumento de su efecto al interaccionar con lopinavir/ritonavir. En caso necesario, valorar su sustitución por Prasugrel.
◊ Prasugrel: se recomienda su empleo frente a clopidogrel o ticagrelor en los casos en los que sea necesaria la administración de un antiagregante tipo inhibidor del receptor P2Y12.
◊ Terapia dual: en los pacientes en los que se precise administrar una terapia dual (AAS + inhibidor de P2Y12) se sugiere como alternativa el mantenimiento de AAS junto a la administración de dosis terapéuticas de HBPM.
Además, respecto a fibrinolíticos se encuentra actualmente la recomendación de su uso con base en que se han reportado múltiples eventos isquémicos en pacientes con patología moderada y severa, dados por la presencia de trombos de fibrina en la microvasculatura pulmonar, siendo este uno de los factores para el desarrollo de síndrome de distrés respiratorio agudo, por lo que proponen el uso de alteplasa y posterior administración de heparina ya que se demostró en 3 pacientes en estado crítico con síndrome de distrés respiratorio agudo mejoría del ratio PaO2/FiO2 de un 11% a un 100%, mencionando que los cambios fueron transitorios y que se necesita más investigación al respecto de sangrado, interacciones medicamentosas y resultados a largo plazo en mayor número de pacientes.23,24
Se propone además el monitoreo de coagulopatías o índices que sugieran alteración de la coagulación en los pacientes detectados positivos, siendo la alteración de los factores de coagulación como dímero D, prolongación de protrombina, conteo plaquetario y fibrinógeno incluso indicativos de ingreso y monitoreo, aún en ausencia de otra sintomatología.25
Antecedente de vacunación con BCG
En este respecto podemos mencionar que a la fecha se encuentran disponibles en la literatura dos estudios titulados Reducing health care workers absenteeism in SARS-CoV-2 pandemic through bacillus Calmette-Guérin vaccination, a randomized controlled trial y BCG Vaccination to Protect Healthcare Workers Against COVID-19, ambos se encuentran en fase 3 pendientes de publicación y revisión por pares, mencionando que se encontrarán disponibles los resultados en 3-4 meses, refieren como conclusión al momento que la hipótesis de los mismos de que sea un factor protector contra el COVID-19 se encuentra basada en que los países sin vacunación sistemática con BCG están siendo más afectados por la pandemia de COVID-19, sin embargo, concluyen que hasta la fecha no se recomienda su uso fuera de las indicaciones establecidas para la prevención de la tuberculosis y debe limitarse al contexto de la investigación, ya que de lo contrario se podría comprometer la disponibilidad de la misma para los programas de vacunación de los recién nacidos en los países con alta incidencia de la infección y enfermedad tuberculosa.26,27
Conclusiones
Es importante que como urólogos nos encontremos actualizados e informados acerca de un tema de interés y relevancia a nivel mundial por ser parte del sistema de salud. Si bien no somos la especialidad de primer contacto, debemos estar informados para brindar el apoyo cuando sea necesario en las distintas áreas de nuestro sistema de salud. Debido a la falta de ensayos clínicos y evidencia científica no hay ningún tratamiento hasta el momento que haya probado su eficacia contra el COVID-19, por eso la constante búsqueda y propuesta de distintos tratamientos que pudieran beneficiar a los pacientes. Actualmente, se encuentran en desarrollo más de 300 ensayos clínicos para el tratamiento del COVID-19.











 nueva página del texto (beta)
nueva página del texto (beta)






