Antecedentes
Desde 1984 el cáncer de próstata (CPr) se encuentra como el cáncer más comúnmente diagnosticado en los hombres, siendo la estirpe diagnosticado en los hombres, siendo la estirpe adenocarcinoma la de mayor prevalencia.1 Cerca de 240 mil hombres se diagnostican con CPr anualmente en los Estados Unidos, y hasta el 80% de ellos se logran identifican en una etapa localizada.2 Aproximadamente 1 de cada 7 hombres se diagnosticarán con CPr a lo largo de su vida y cerca del 2.8% de los hombres morirán de dicha enfermedad.3 De acuerdo con las indicaciones de las guías de detección temprana del CPr de la National Comprehensive Cancer Network todos aquellos pacientes que presenten un APE mayor a 3 ng/ml o un tacto rectal con parámetros sospechosos de CPr deben de ser llevados a una biopsia de próstata.4 Siguiendo los parámetros estándar de la BPUST (patrón extendido de 12 tomas; 6 por lóbulo) se logra identificar entre un 20-40.7% de los cánceres en pacientes con un APE entre 3 y 10 ng/ml y hasta un 70% cuando el APE es mayor a 10 ng/ml.1 Después de una BPUST negativa en un paciente que continúe con sospecha clínica de CPr la Resonancia Magnética Multiparamétrica (RMm) es una herramienta útil en la detección de lesiones sospechosas en la próstata que hayan sido pasadas desapercibidas por el ultrasonido. Las biopsias de próstata guiada por ultrasonido transrectal con fusión de RMm (BPUT-RMm) logran aumentar en un 30% el diagnóstico de CPr de alto riesgo comparado con la técnica convencional de BPUST y en 17% los CPr de bajo riesgo.5 Presentamos la experiencia inicial con el uso del sistema Esaote para realizar una biopsia de próstata guiada por ultrasonido transrectal con fusión de RMm.
Presentación del caso
Paciente masculino de 63 años en seguimiento por un APE de 8.2 ng/ml que al tacto rectal no presenta datos sospechosos de malignidad. Se le había realizado una biopsia de próstata con ultrasonido transrectal identificando solamente hiperplasia fibromuscular y focos de prostatitis crónica. Se decide enviar una RMm de próstata en la que se identifica una zona hipointensa hacia segmento apical a nivel de la zona periférica lateral derecha que en difusión presenta restricción, midiendo 20 mm, clasificada como un PI-RADS 4. Se decide llevar al paciente a una BPUT-RMm con sistema Artemis. Se toman 6 fragmentos del sitio sospechoso con la técnica de fusión de imágenes y posteriormente, por un segundo urólogo, se realiza una biopsia extendida de 12 cilindros guiada solamente por ultrasonido transrectal.
Descripción del procedimiento
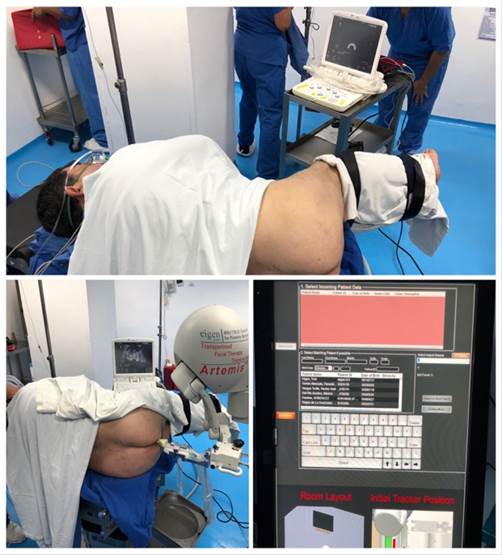
En nuestra institución utilizamos un equipo de biopsia con fusión de resonancia magnética Artemis (Figura 1) que cuenta con un magneto que crea un campo electromagnético en la dirección deseada e identifica la posición del localizador espacial adaptado a nuestro transductor transrectal. Se introduce el disco con la RMm de próstata en el panel de mando del ultrasonido para cargar las imágenes al sistema. Colocamos al paciente en una posición decúbito lateral con el soporte para el magneto de forma que el campo magnético se dirija hacia la zona genital del paciente.
Iniciamos realizando una revisión sistemática de la resonancia magnética en T2 y en la fase de difusión para identificar las lesiones sospechosas de malignidad según la clasificación de PI-RADS: hipointensa en T2, restricción a la difusión, irregularidad, dimensión, extensión fuera de la cápsula. Se realiza una selección de la imagen sospechosa con un marcador circunferencial que puede modificarse en diámetro para ajustarse a la lesión y el color para distinguir cuando se selecciona más de una lesión. Iniciamos con el ultrasonido transrectal de próstata utilizando un transductor transrectal de 12 Hz con un localizador adaptado a su base para identificar la posición espacial del transductor. Llevamos a cabo una revisión ultrasonográfica tradicional para identificar la anatomía prostática y estructuras vecinas. Colocamos, bajo técnica convencional, el anestésico de nuestra elección en el ángulo vesículo-prostático. Se activa en el sistema la opción de pantalla dividida, se observa a continuación la serie de la resonancia magnética seleccionada en la derecha y la imagen en vivo del ultrasonido en la izquierda. Localizamos por ultrasonido una imagen. Ajustamos la misma localización de la imagen por resonancia magnética y con ayuda del botón de empalme sobreponemos las imágenes para corroborar su similitud. En ese momento se presiona el botón “unión”. A partir de este momento el movimiento de nuestro transductor transrectal se traduce en un movimiento simultaneo de la resonancia gracias a la localización dentro del campo magnético del localizador adaptado al transductor. Pasamos al modo biopsia que nos ofrece imágenes de mayor dimensión y un plano de guía para dirigir el disparo. Además, en este modo la imagen sospechosa marcada en la resonancia aparece marcada también en la imagen por ultrasonido al realizar el rastreo. Iniciamos tomando la biopsia con una pistola de biopsias automática tipo Magnum con una aguja tipo trucut. Con esta pistola se tiene la opción de modular la longitud del cilindro de 10 mm o 12 mm. Se toman 4 biopsias de cada sitio sospechoso, en el ultrasonido se muestra con un círculo de color que aumenta de diámetro conforme nos acercamos al punto central de la lesión sospechosa. Con cada disparo se congela la imagen para identificar la punta de la aguja, y el sistema marca el trayecto de la aguja con el fin de no volver a biopsiar el mismo sitio en el siguiente disparo. Al finalizar las biopsias se retira el transductor y en caso de presentar sangrado se puede realizar una compresión digital gentil de la próstata por vía transrectal.
Resultados
Se realizó el procedimiento en 25 minutos, donde se logró identificar una lesión sospechosa de 20 mm. En el reporte histopatológico se identifica Adenocarcinoma de próstata Gleason 7(4+3) en 2 de los 4 cilindros guiados por fusión, en el 15 y 50% (Figura 2). El resto de los cortes se presenta negativo a CPr. El paciente no presentó complicaciones trans y post procedimiento, permitiendo que se realizara de manera ambulatoria.
Discusión
La BPUT-RMm ha surgido como una de las herramientas más prometedoras en el abordaje de los pacientes con sospecha de CPr y antecedente de evaluaciones negativas. Múltiples estudios se han llevado a cabo en este campo que han logrado demostrar superioridad a los procedimientos actuales, con un incremento en la probabilidad de identificar lesiones malignas.
Al analizar pacientes que contaban con una biopsia de próstata previa negativa, se identificó que hasta el 69% de ellos contaban con una lesión sospechosa por RMm.6 Incluso se lograron identificar prevalencias cerca del 95% cuando los pacientes presentaban una velocidad de APE >0.75 ng/ml/año y un APE mayor a 4 ng/ml.7 La prevalencia más baja identificada en un estudio fue de 65% en pacientes con BPUST previa negativa.8
Repetir una BPUST en pacientes que presentan una biopsia previa, disminuye las probabilidades de identificar un CPr de forma gradual. La probabilidad de identificar CPr en una primer, segunda, tercera o cuarta BPUST presenta un 17%,14%,11% y 9%, respectivamente.9 Por otro lado, el llevar a un paciente con una BPUST previa negativa a una guiada por fusión puede elevar la probabilidad de identificar un CPr hasta el 34%.10 Al no existir una relación entre el número de BPUST previas y la probabilidad de diagnóstico de CPr por medio de BPUT-RMm, se puede sospechar que este procedimiento ayuda a biopsiar sitios que previamente habían evadido el trayecto de la aguja.
Algunos especialistas suelen llevar a sus pacientes con BPUST previas negativas a una técnica de saturación con el fin de ampliar los sitios estudiados. Este tipo de técnica ha demostrado un incremento a 32.7% de probabilidad de identificar CPr en comparación con las biopsias de 12 o 14 cilindros. Sin embargo, con esta técnica hasta un 40.1% de los CPr diagnosticados suelen ser clínicamente insignificantivos.11 Con una técnica de fusión con RMm, se puede identificar entre un 39-59% de CPr, y en su mayoría,50-87%, llegan a ser clínicamente significativos.10,12
Un estudio realizado por Vourganti et al.,13 en pacientes con BPUST previas negativas, detecto CPr en el 37% de sus pacientes estudiados con lesiones sospechosas en la RMm. En su mayoría los pacientes se presentaron con tumores clínicamente significativos y menor número de pacientes con CPr insignificativos. Estos resultados nos arrojan, de forma indirecta, la probabilidad de que con las BPUTRMm se puede disminuir el sobre diagnóstico y sobre tratamiento que existe actualmente con las técnicas convencionales de BPUST. De igual forma se lograrían disminuir los efectos secundarios por las diferentes modalidades de tratamiento (radioterapia, cirugía, deprivación androgénica) en los pacientes que no requieren un tratamiento por presentar un cáncer que no aumenta su mortalidad a corto plazo.
Sin embargo, aún existe la duda de la cantidad de pacientes que no se someterán a biopsia de próstata por falta de una lesión sospechosa en la RMm y pudieran llegar a tener un CPr. Un análisis de dos estudios mostró que en el 23% de los pacientes que no presentaban una lesión sospechosa en la RMm se identificó CPr al someterlos a una técnica de BPUST.14,15 Al analizar ambas bases de datos, se identificaron 8 (2.3%) CPr clínicamente significativos que no hubieran sido diagnosticados si solo se hubiera estudiado a los pacientes con RMm.
Un estudio identifico que la BPUT-RMm presento un 30% de los cilindros positivos para CPr, mientras que solo el 7% de los cilindros de las BPUST aparecían positivos. 15-17
Con esta evidencia podemos concluir que la BPUT-RMm puede incrementar la probabilidad de identificar un CPr clínicamente significativo, con la necesidad de un menor número de cilindros obtenidos y presenta una mayor probabilidad de identificar CPr en los pacientes con biopsias negativas previas que una técnica convencional.
La ausencia de equipos ultrasonográficos con las características necesarias para realizar una BPUT-RMm y la falta de entrenamiento de los especialistas en México no ha permitido que se logre publica la experiencia y resultados en población mexicana. Hasta el momento, este es el primer reporte de experiencia en BPUT-RMm en un hospital mexicano del que tengamos conocimiento.











 nueva página del texto (beta)
nueva página del texto (beta)