Introducción
La presencia de productos farmacéuticos y de cuidado personal (PPCP) en diversos compartimientos ambientales se ha considerado como un problema ambiental de gran importancia (Al-Odaini, Zakaria, Yaziz, & Surif, 2010; Kosma, Lambropoulou, & Albanis, 2014). Desde la década de 1950 existe literatura, aunque limitada, que reporta productos farmacéuticos en el medio acuático (Watkinson, Murby, Kolpin, & Coztanzo, 2009). Sin embargo, sólo hasta principios de la década de 1990 el tema de los fármacos en el ambiente surgió con fuerza (Barceló & López, 2008); esto, porque hasta entonces fue posible determinar la presencia de estos microcontaminantes orgánicos en aguas residuales, superficiales y subterráneas en concentraciones muy bajas. Hoy por hoy se reportan desde los ng/l hasta los µg/l, aunque en algunos productos farmacéuticos se han detectado concentraciones > 1 000 µg/l en los efluentes de aguas residuales correspondientes a influentes de industrias farmacéuticas (Londoño & Peñuela, 2015a).
El compuesto ácido 2-(4-isobutil-fenil)propiónico es el primero de los fármacos anti-inflamatorios no esteroideos disponibles comercialmente como ibuprofeno (IBP) (Quero-Pastor, Garrido-Perez, Acevedo, & Quiroga, 2014). Es uno de los fármacos más importantes incluidos en la lista “Essential Drugs List” de la Organización Mundial de la Salud, que da lugar a su producción masiva en todo el mundo (Behera, Oh, & Park, 2011). En 1984 fue aprobado como un medicamento de venta libre y desde entonces las ventas sin formulación se han triplicado en América del Norte (Sabri, Hanna, & Yargeau, 2012). Sus propiedades fisicoquímicas favorecen su movilidad en ambientes acuáticos (Behera, Oh, & Park, 2011; Sabri, Hanna, & Yargeau, 2012), pues tienen alta polaridad y baja volatilidad (Zhang, Gersberg, Ng, & Tan, 2014). Debido a su amplio uso, sus residuos y metabolitos llegan por las aguas residuales a las plantas de tratamiento municipales o son vertidos directamente a los cuerpos de agua receptores (Osachoff et al., 2014).
Estos microcontaminantes pueden pasar a lo largo de las unidades convencionales de tratamiento de aguas residuales con diferente destino. Por ello se han hecho estudios con el fin de determinar su ocurrencia y destino (Reif, Suárez, Omil, & Lema, 2008). Varias clases de estos compuestos son vertidos a las aguas superficiales, subterráneas y aguas costeras (Parolini, Binelli, & Provini, 2011), lo cual evidencia que son descargados continuamente en medios acuáticos sin ninguna tipo restricción (Matamoros, Arias, Brix, & Bayona, 2007).
La presencia de fármacos en el medio receptor es preocupante debido a su naturaleza bioactiva y que aún en concentraciones ultra bajas pueden afectar negativamente a los organismos, incluyendo la vida silvestre y seres humanos (Osachoff et al., 2014). Una preocupación mayor es el hallazgo del ibuprofeno y otros fármacos, como diclofenaco y carbamacepina, en el agua potable (Barceló & López, 2008); tal condición indica que la exposición humana a estos residuos farmacéuticos puede producirse por el consumo directo de agua o por el consumo de organismos acuáticos, como los peces, que pueden acumular estos residuos (Cunningham, Binks, & Olson, 2009). No obstante, en los países latinoamericanos existe un gran vacío de información sobre la presencia de compuestos farmacéuticos en descargas de efluentes cloacales (Elorriaga, Marino, Carriquiriborde, & Ronco, 2012).
Se han realizado diferentes estudios con múltiples tratamientos, a fin de remover los fármacos de las aguas residuales y evitar que lleguen a los cuerpos de agua. Algunos de tales tratamientos son de tipo convencional, como lodos activados, oxidación prolongada, lechos bacterianos y biodiscos, obteniéndose rendimientos que oscilan entre 15 y 80%, según el tipo de tratamiento y fármaco (Cortacans, Hernández, Del Castillo, & Montes, 2006). También se han estudiado otras tecnologías para la remoción de residuos de fármacos, como los procesos de oxidación (ozonización, fotólisis y fotólisis heterogénea, fenton y fotofenton, sonólisis, oxidación electroquímica, entre otras); adsorción con carbón activado; ósmosis inversa; separación por membranas, y biorreactores de membrana, muchos de ellos usados para complementar los sistemas de tratamiento convencional (Parolini et al., 2011; Li, Zhu, Ng, & Tan, 2014; Osachoff et al., 2014). Sin embargo, la implementación a gran escala de estos procesos de tratamiento tienen un costo prohibitivo (Parolini et al., 2011; Li et al., 2014). Por tanto, la selección de tecnologías alternativas de alta eficiencia de remoción de productos farmacéuticos a bajo costo es de vital importancia, sobre todo en regiones con escasos recursos.
Los humedales artificiales son de bajo costo en la construcción, operación y mantenimiento, y están siendo estudiados para remover contaminantes farmacéuticos de las aguas residuales (Li et al., 2014), siendo su principal restricción la disponibilidad de espacio (Zhang et al., 2012). Así, este estudio tiene como objetivo evaluar el funcionamiento de humedales construidos de flujo subsuperficial horizontal a escala piloto para la remoción de ibuprofeno en aguas sintéticas, con el fin de considerar su uso en el tratamiento de aguas residuales con concentraciones significativas del contaminante.
Materiales y métodos
Montaje experimental
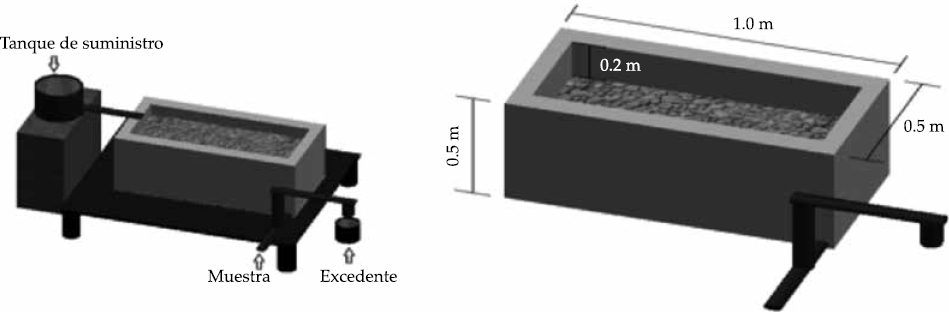
Los sistemas empleados durante la experimentación fueron tres humedales artificiales de flujo subsuperficial horizontal construidos en fibra de vidrio a escala piloto. El montaje experimental fue instalado en un espacio abierto, con una temperatura promedio de 24 °C, cubiertos con una capa plástica, a fin de evitar variaciones en las condiciones operacionales y una posible dilución del contaminante. Las dimensiones y el esquema del montaje se presentan en la figura 1. El medio de soporte empleado fue grava, con una granulometría entre 6 y 3 mm (1/4-1/8 pulgadas) para cada humedal, con una altura de 0.3 metros. Para los experimentos de dos humedales se plantó la especie Cyperus papyrus, conocida también con el nombre de papiro enano; un humedal se evaluó sin ninguna plantación, para evaluar la función que tienen las macrófitas en la remoción del IBP. La planta Cyperus papyrus se seleccionó para el estudio debido a que es una de las especies más usadas en sistemas de flujo subsuperficial en el trópico tanto en humedales naturales como construidos en Colombia (Agudelo, 2010).
Todos los humedales operaron con un tiempo de retención hidráulico de 3 d y un caudal influente de 15 cm3/min a flujo continuo (cuadro 1). El agua tratada fue un agua residual sintética dopada a tres concentraciones de IBP, aplicadas a las tres unidades experimentales en diferentes etapas, brindando un periodo de transición de 15 días entre una concentración y otra. En este periodo sólo se suministró a los humedales agua sintética sin presencia del fármaco, para eliminar residuos del contaminante en los humedales. El cuadro 1 presenta un resumen de la estrategia experimental empleada.
Preparación del agua residual sintética
La preparación del agua residual sintética se basó en la adición de glucosa para proporcionar los sustratos de carbono orgánico; y urea y fosfato para suministrar nitrógeno y fósforo, respectivamente, y así garantizar los principales nutrientes que requieren los microorganismos para su metabolismo (Agudelo, 2010). La composición del agua de alimentación presentó por cada 200 l lo siguiente: 28.8 g de glucosa industrial, 22.8 g de urea y 14.7 g de fosfato diamónico. Además, el agua residual fue dopada con las concentraciones de interés de ibuprofeno disuelto previamente en metanol.
Preparación de la disolución del fármaco
En las concentraciones C1 y C2 evaluadas en los humedales correspondientes a 2.7 y 0.2 mg/l se empleó ibuprofeno disódico en polvo; para la concentración C3 de 1.7 mg/l se utilizó el fármaco en forma comercial de la casa farmacéutica Genfar®, en su presentación de 600 mg.
El modo de aplicación fue a través de la preparación de soluciones concentradas. Con el ibuprofeno disódico se preparó una solución madre de 10 000 mg/l del fármaco en metanol grado HPLC y para la concentración C3 se preparó una solución de 6 000 mg/l en metanol grado HPLC a partir de pastillas comerciales, las cuales tuvieron un proceso previo de trituración. A partir de estas soluciones se contaminó el agua residual sintética de alimentación de los tres humedales.
Métodos analíticos
El pH, la conductividad, el oxígeno disuelto, la DQO y el COD se determinaron de acuerdo con las metodologías establecidas por el estándar de métodos (APHA, 2012).
El análisis del ibuprofeno se realizó con un cromatógrafo líquido de ultra resolución (UPLC) acoplado a un espectrómetro de masas Xevo TQD (triple cuadrupolo), equipado con una fuente de ionización por electrospray (ESI). La columna empleada fue una Acquity Uplc Beh C18, 2.1cm x 50 mm, 1.7 µm de tamaño de partícula, con un flujo de 0.3 ml/min. La temperatura de la columna se fijó en 40 °C y en el sistema de manejo de muestra se mantuvo a una temperatura de 10 °C; el volumen de inyección fue de 20 µl. Las condiciones del espectro de masas fueron las siguientes: temperatura de la fuente: 150 °C; temperatura de solvatación: 450 °C; flujo de gas de solvatación: 800 l/h; flujo de gas de cono: 50 l/h; ionización: ESI (-).
Se utilizó de fase móvil C: ácido fórmico al 0.01% en agua; fase móvil D: ácido fórmico al 0.01% en metanol (Aristizabal-Ciro, 2014). Se emplearon soluciones estándares: una de ibuprofeno de 100 µg/l y de 1 000 µg/l en agua, y una disolución estándar de ibuprofeno deuterado de 2 000 µg/l, que fueron empleados para el montaje de la curva, calibración y cuantificación. El límite de cuantificación (LC) del equipo es de 1 µg/l. Las muestras fueron centrifugadas en tubos falcón de 25 ml, a 5 000 rpm por 10 minutos; después se tomó 1 ml del sobrenadante en un vial ámbar de vidrio de 2 ml (certificados para LCMS). En caso de ser necesario, se realizó una dilución con agua ultrapura, para que la lectura estuviera en un rango de trabajo de 1 a 300 µg/l. Por último, se adicionaron 50 µl de la solución de 2 000 µg/l de ibuprofeno-deuterado como estándar interno previo a la inyección de la muestra en el UPLC.
Análisis microbiológico (conteo de heterótrofos)
Se evaluó la biomasa microbiana adherida al medio granular, conformada principalmente por microorganismos heterótrofos. La toma de las muestras se realizó a través de un piezómetro, que consistió en un tubo de PVC perforado, y dentro de éste se instalaron varios muestreadores de malla. Tales muestreadores de biopelícula son bolsas de malla que contienen el mismo material de soporte de los humedales en su interior. La cuantificación de los heterótrofos se realizó extrayendo 10 gramos de grava del muestreador de malla y se colocaron en un beaker previamente esterilizado; se adicionaron 90 ml de agua desionizada; la mezcla se agitó por 20 minutos a 290 rpm; después se realizaron diluciones sucesivas en tubos de ensayo hasta llegar a 10-5. Por último, se extrajo 1 ml del sobrenadante del tubo de ensayo y se colocó sobre una caja Petri, inmediatamente se agregó Plate Count Agar y se agitó; se dejó enfriar el agar y se incubó por 48 horas a 35 ± 0.5 °C; luego se hizo el conteo de las colonias en un estereomicroscopio.
Resultados y discusión
Montaje y puesta en marcha de los humedales superficiales
Los humedales, luego de ser instalados y plantados con papiro enano (en el caso de los humedales 2 y 3), tuvieron un periodo de aclimatación de 30 días, a fin de lograr un estado de maduración y permitir el desarrollo de la biopelícula en el material de soporte (Cardinal et al., 2014). Durante este periodo, los humedales se inocularon con 500 ml de biomasa floculenta obtenida del licor de mezcla del sistema de lodos activados de la PTAR domésticas de San Fernando, localizada en Medellín, Colombia. La biomasa se agregó al agua residual sintética que proporcionaba sólo la fuente de carbono y nutrientes. Luego de que los sistemas estuvieron acondicionados, se inició la experimentación con la aplicación de cargas de ibuprofeno.
Análisis en la remoción de IBP
• Experimento 1, a una concentración de 2.7 mg/l de IBP
Se preparó un agua residual dopada, con una concentración de 2.7 mg/l de IBP, con la cual se alimentaron los tres humedales al tiempo: dos plantados con macrófitas y uno sin plantar. Los resultados del comportamiento de remoción del contaminante se presentan en la figura 2.
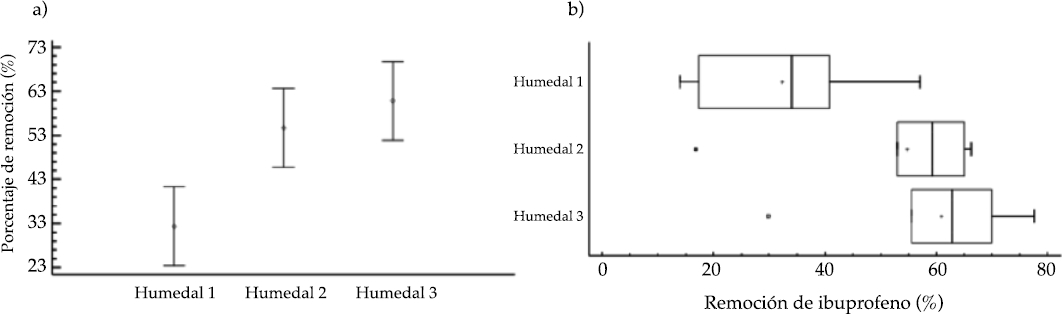
Figura 2 a) Análisis de remoción promedio de ibuprofeno; b) porcentajes de remoción de ibuprofeno para la concentración de 2.7 mg/l en cada humedal.
La comparación estadística de las medias (figura 2) permite identificar con un 95% de confianza que no existe una diferencia significativa en los porcentajes de remoción en los humedales 2 y 3 (con presencia macrófitas); mientras que la remoción del humedal 1 (sin presencia de macrófitas) sí presenta una diferencia significativa en los porcentajes de remoción del compuesto, en comparación con los dos humedales plantados. Esto permite concluir que durante el primer experimento, los humedales plantados presentaron porcentajes de remoción semejantes entre ellos, pero estadísticamente diferentes al porcentaje de remoción del humedal 1, en donde no se plantó la macrófita. La figura 2a muestra cómo los límites de confianza para la media del porcentaje de remoción de los humedales 2 y 3 presentan el mismo comportamiento, mientras que los resultados para el humedal 1 son diferentes.
Los humedales plantados presentaron mayores porcentajes de remoción de IBP que el humedal sin macrófitas. La figura 2b muestra que, en promedio, el humedal sin plantar obtuvo una remoción del 32% del IBP, mientras que los humedales 2 y 3 presentaron remociones promedio de 55 y 61%, respectivamente.
Aunque los mecanismos y las vías de eliminación farmacéutica aún no están claras, y para los objetivos de esta investigación no se contempló su estudio, se resalta con base en los aportes registrados en la literatura que la rizosfera de la planta actúa como un microcosmo, donde la actividad microbiana hace la degradación de compuestos químicos recalcitrantes (Bhatia & Goyal, 2014), los cuales pudieron tener influencia en la degradación del IBP. Según Fariya (2013), la biodegradación/biotransformación en los humedales ocurre mayormente en la rizosfera; asimismo, los exudados liberados por las raíces de las plantas son intensificadores de la actividad microbiana y pueden mejorar la biodisponibilidad de los productos farmacéuticos, actuando como agentes tensoactivos y transportadores. La captación activa de las plantas también afecta el destino de los contaminantes orgánicos emergentes (Zhang et al., 2012).
Se ha demostrado que las macrófitas ayudan a eliminar productos farmacéuticos con más eficiencia que los que carecen de ésta tanto a escala de laboratorio como a escala real (Cardinal et al., 2014), lo cual se evidenció con los resultados de esta investigación durante la primera concentración empleada del fármaco.
Otros investigadores han presentado diversas conclusiones, indicando que la concentración de los fármacos tiende a disminuir con rapidez en los sistemas de humedales, excepto en aquellos que se encuentran en la oscuridad, los cuales no presentaron remoción alguna; por otro lado, los reactores plantados han presentado una concentración mayor de fármacos que reactores sin plantas; se presume que este comportamiento se debió a la cobertura de las plantas, la cual bloqueaba la radiación solar y como consecuencia reducía la fotodegradación de los contaminantes (Zhang et al., 2014). Sin embargo, la fotodegradación no se considera un mecanismo importante a través del cual se eliminan los contaminantes en los humedales de flujo subsuperficial. Las posibles discrepancias entre los resultados presentados por Zhang et al. (2014) con los resultados de esta investigación pueden estar asociados con múltiples factores, como el TRH, la población de microorganismos existentes en el hábitat del humedal y en la rizófora de las plantas, las especies de macrófitas empleadas, la configuración del humedal y la fuente de carbono orgánico empleado como sustrato, entre otros. De igual manera, Collado et al. (2012), en pruebas de biodegradación del IBP, empleando concentraciones entre 10 y 1 000 µg/l no comprobaron remoción abiótica en el sistema que disminuyera la concentración del compuesto; con ello se demostró que la volatilización y fotodegradación no fueron un proceso importante para el destino del IBP (Londoño & Peñuela, 2015a).
Por otra parte, estudios de adsorción del IBP sobre la biomasa y/o el material orgánico han mostrado porcentajes de sorción inferiores al 0.5%; esto indicó que la sorción no es un mecanismo de eliminación de tal contaminante (Carballa, Omil, & Lema, 2007). Además, los valores de log kd del IBP varían entre 1.0 y 1.8, que son valores pequeños, para los cuales no ocurre sorción apreciable del fármaco en el material orgánico (Carballa, Finkb, Omil, Lema, & Ternes, 2008) (Londoño & Peñuela, 2015b). De acuerdo con lo anterior, se puede descartar que la sorción del IBP en el material del humedal haya sido un mecanismo importante para la remoción de este contaminante de la fase acuosa, y se presume que su remoción está asociada principalmente con la acción biológica ejercida por las plantas y microorganismos.
• Experimento 2, a una concentración de 0.2 mg/l de ibuprofeno
De acuerdo con el análisis estadístico para esta concentración del fármaco, se evidenció que la diferencia estadísticamente significativa se mantuvo entre los porcentajes de remoción del fármaco para el humedal sin macrófita y los humedales con macrófitas; sin embargo, las remociones presentadas por los humedales plantados fueron estadísticamente diferentes entre ellas. Se denota en la figura 3 que el humedal sin macrófita (humedal 1) tuvo el menor porcentaje de remoción, con un valor de 51%; seguido del humedal 2, con una remoción de 71%, y el de mayor porcentaje fue el humedal 3, con un valor de 84%.
Ambos sistemas plantados (humedales 2 y 3) no presentaron remociones estadísticamente iguales. Aunque en apariencia ambos humedales son semejantes, es realmente difícil que sean exactamente iguales, pues no contienen la misma cantidad de grava y el mismo tamaño; no están igualmente empacados y, por lo tanto, tienen flujos diferentes a través de la misma; además, la masa de las raíces de las plantas en ambos humedales no es la misma y por ende el ecosistema biológico tampoco, por lo cual el comportamiento de degradación en ambos no es exactamente igual. Además, durante la experimentación se observó un deterioro paulatino de las plantas, lo cual conllevó a una menor densidad de las mismas, que pudo haber afectado el normal desempeño del sistema.
• Experimento 3, a una concentración de 1.7 mg/l de ibuprofeno
En el análisis estadístico para la concentración 3 del fármaco (1.7 mg/l), el humedal 1 (sin macrófita) y el humedal 2 (con macrófita) no presentaron diferencia estadísticamente significativa en los porcentajes de remoción de ibuprofeno; ello permite indicar que la función de la planta no incidió de forma significativa en la remoción del fármaco. Los porcentajes de remoción del contaminante para los tres humedales fueron 74, 49 y 55%, respectivamente, para los humedales 1, 2 y 3.
Los resultados para este experimento muestran un comportamiento de remoción del fármaco contrario a lo evidenciado en los experimentos anteriores pese a la alta concentración del IBP. Esta condición puede estar relacionada con un mayor desarrollo y aclimatación de los microorganismos involucrados en el proceso de degradación de IBP debido al contacto previo con el compuesto. De igual manera, se manifestó un deterioro físico significativo en las plantas de los humedales en esta última etapa de experimentación, condición que pudo haber influenciado en la eficiencia de remoción del IBP; posiblemente se presentó algún efecto inhibidor de las poblaciones de microorganismos asociados con la rizosfera de las plantas, lo cual afectó su actividad y generó condiciones desfavorables que no permitieron el desempeño efectivo del sistema.
Por otra parte, los resultados de los tres experimentos reveló que para los humedales plantados, el comportamiento de remoción del IBP tuvo porcentajes de eliminación en un rango de 49 a 61% para las concentraciones altas del fármaco (2.7 y 1.7 mg/l); mientras que para la concentración más baja (0.2 mg/l), el porcentaje de remoción estuvo entre 71 y 84%. Esta condición puede indicar un efecto negativo de las altas cargas de IBP sobre el humedal; es posible que las altas concentraciones del fármaco generen un efecto inhibitorio sobre las poblaciones microbianas del sistema. Collado et al. (2012) mencionaron el efecto de la carga del compuesto sobre la tasa de degradación del contaminante y el efecto de la población microbiana, e indicaron que entre menor sea la carga del IBP y mayor sea la cantidad de biomasa activa, más eficiente es la remoción. Este planteamiento explica los bajos porcentajes de remoción obtenidos con el aumento en la carga del compuesto. De igual manera, se puede pensar que la carga evaluada tiene un efecto particular sobre las poblaciones de microorganismos del sistema en un momento determinado de la experimentación debido a su diferencia en concentración (Londoño & Peñuela, 2015a).
Análisis en la remoción del carbono orgánico disuelto (COD)
En el cuadro 2 se presentan los promedios del porcentaje de remoción de COD en los tres humedales. En las concentraciones 2 y 3, los porcentajes de remoción de COD en los tres humedales son mayores al 90%; sin embargo, en los humedales 1 y 2 para la concentración 1 se tuvo porcentajes de remoción de COD menores a 90%, que coincide con el primer experimento para cada humedal, lo cual indicaría que aún los humedales no estaban estabilizados o existió un efecto inhibidor por la mayor concentración del fármaco, afectando las poblaciones microbianas presentes en la biopelícula de la grava.
Cuadro 2 Porcentajes de remoción promedio de carbono orgánico disuelto con las tres concentraciones de ibuprofeno.
| Experimento | Humedal 1 (%±DS1) | Humedal 2 (%±DS1) | Humedal 3 (%±DS1) |
| C1 | 88±3 | 81±1 | 92±1 |
| C2 | 94±5 | 95±3 | 97±3 |
| C3 | 95±5 | 91±1 | 97±1 |
1 Desviación estándar.
En un estudio, cuya finalidad fue determinar la remoción del carbono orgánico disuelto, en humedales artificiales de flujo subsuperficial a escala piloto y plantados con Phragmites australis (carrizo o caña común) se reportó un promedio de 92.5% en la eficiencia de remoción del COD (Agudelo, Jaramillo, Peñuela, & Aguirre, 2010), indicando con base en este resultado que los porcentajes de remoción obtenidos en los tres experimentos del presente trabajo fueron altos, condición que mostró el buen estado de funcionamiento del sistema y una buena actividad de los microorganismos, pues los compuestos orgánicos disueltos son removidos por las poblaciones bacterianas presentes en la biopelícula formada sobre la grava y aquellas en la raíces y rizomas de las plantas (Agudelo et al., 2010; Choudhary, Kumar, & Sharma, 2011). También se pueden remover los compuestos orgánicos por adsorción y absorción (Choudhary et al., 2011) y, por lo tanto, la materia orgánica disuelta pudo haber sido removida mediante los mecanismos antes mencionados.
Análisis de heterótrofos
El periodo de aclimatación favoreció las condiciones de arranque de los humedales; esto permitió que la población microbiana aumentara (figura 4); de igual manera, la concentración inicial del ibuprofeno utilizada (2.7 mg/l) en un primer instante no afectó las poblaciones microbianas presentes en la grava, sin embargo, se evidencia un descenso al finalizar la etapa 1 y al iniciar la etapa 2 del segundo experimento (0.2 mg/l); durante este periodo, la concentración de heterótrofos se mantuvo del orden de 101; tal descenso aún mantuvo una buena población bacteriana y por la incertidumbre del método la reducción no es muy significativa (figura 4). Por último, el conteo de heterótrofos aumentó durante la tercera concentración (1.7 mg/l), donde posiblemente los microorganismos ya se habían adaptado a la presencia del fármaco.
Según la disminución del porcentaje de remoción del fármaco durante el tercer experimento, se pensaría que hubo un descenso en la población microbiana en el segundo humedal, sin embargo, ésta aumentó con respecto a los experimentos anteriores (figura 4); ello permite pensar que la población microbiana que se contabilizó en los muestreos de la grava (en el piezómetro) no es precisamente la misma que está presente en la rizosfera de las plantas, aunque estén en el mismo humedal, pues cada población está expuesta a condiciones ambientales diferentes; por ejemplo, con la muerte de algunas plantas, la población que se encontraba en la rizosfera pudo haber decaído, dado el cambio que se produjo a sus alrededores; no obstante, aquella población presente en la grava del sitio de muestreo, al no estar influenciado por las condiciones de las plantas, no presentó cambio alguno, por lo que no se vio perjudicada. Así, aunque haya aumentado el conteo de heterótrofos en la grava, esto no quiere decir que también haya aumentado el conteo en la rizosfera.
Conclusiones
El porcentaje de remoción del ibuprofeno en los tres humedales disminuyó conforme se aumentó la concentración del analito en el afluente. Los humedales plantados con papiro enano presentaron remociones de IBP entre 49 y 61% para las concentraciones altas del fármaco de 2.7 y 1.7 mg/l; mientras que para la concentración más baja de 0.2 mg/l, el porcentaje de remoción estuvo entre 71 y 84%. Los bajos porcentajes de remoción del IBP pueden estar asociados con la saturación en el sistema, un tiempo de retención insuficiente para que cada humedal pudiera asimilar el aumento en la carga de ibuprofeno o a un posible efecto inhibidor debido a la alta concentración del analito sobre las poblaciones microbianas del sistema. Por su parte, el humedal sin macrófitas presentó remociones del IBP en un rango de 32 y 74%, alcanzando la mayor degradación en la última etapa, con una concentración de 1.7 mg/l, condición atribuida a la posible aclimatación de los microorganismos al fármaco luego de estar un tiempo prolongado en contacto con el mismo. Por último, se evidencia que la presencia de macrófitas en los humedales favorece la remoción de IBP para las condiciones evaluadas en este estudio, al igual que las altas concentraciones del fármaco pueden generar efectos negativos sobre la composición del sistema biológico.











 nueva página del texto (beta)
nueva página del texto (beta)