Introducción
Los humedales naturales se han utilizado como receptores de aguas residuales desde la antigüedad. El siglo XX trajo el desarrollo de humedales construidos por el hombre, diseñados para optimar los procesos que se producen de manera natural en la vegetación del humedal, el sedimento o sustrato, y los microorganismos asociados, con el fin de mejorar la eficiencia del sistema en la depuración de agua. Esta tecnología comenzó a usarse en la década de 1970 y debido a su eficiencia, bajo costo de instalación y mantenimiento, su empleo se ha incrementado desde entonces. Los humedales construidos han sido ampliamente estudiados (Maine, Suñé, Hadad, Sánchez, & Bonetto, 2006, 2007; Maine, Hadad, Sánchez, Caffaratti, & Bonetto, 2009; Kadlec & Wallace, 2009; Vymazal, 2011; Zhang et al., 2014). Sin embargo, la mayoría de las investigaciones se han hecho para la depuración de efluentes domiciliarios para pequeñas comunidades, viviendas uni-familiares y hoteles, así como para aguas de escorrentía, donde los contaminantes a eliminar son fósforo (P) y nitrógeno (N). Hay cientos de estos humedales funcionando, en especial en países como Alemania, Francia, Reino Unido, España, Italia, Dinamarca, Australia y Estados Unidos. En Latinoamérica, en países como México, Colombia, Perú y Bolivia, tal tecnología ha encontrado una importante implementación para depuración de efluentes sanitarios de pequeños poblados, complejos turísticos, campus universitarios, etc. (García, Paredes, & Cubillos, 2013; Rivas-Hernández, Barceló-Quintal, & Moeller-Chávez, 2014). En Argentina, el uso de humedales construidos para tratamiento de efluentes es aún limitado, a pesar de que las condiciones para su implementación son ideales (gran disponibilidad de terrenos marginales de bajo costo, clima templado con inviernos poco rigurosos y suma disponibilidad de macrófitas adaptadas al clima).
De acuerdo con la experiencia de diferentes especialistas expuestas en las últimas conferencias internacionales de humedales construidos, en Argentina, como en otros países de América latina, existen empresas que se dedican a la construcción de humedales sin el estudio previo necesario y sin monitoreos posteriores para su control y optimación. Esto trae como consecuencia un funcionamiento inadecuado de los sistemas o que queden fuera de operación, generando la idea de que dicha tecnología no es eficiente. Por esto es importante llevar a cabo estudios previos específicos para cada caso y monitoreos de los sistemas a lo largo del tiempo; no sólo para comprender los mecanismos de depuración sino también para optimar el funcionamiento del sistema.
Los humedales funcionan de manera eficiente también para tratar efluentes industriales (Dunbabin & Bowmer, 1992; Chen, Kao, Yeh, Chien, & Chao, 2006; Khan, Ahmad, Shah, Re-hman, & Khaliq, 2009; Kadlec & Wallace, 2009). Dos industrias metalúrgicas de la zona en estudio realizan el tratamiento final de sus efluentes empleando humedales construidos. Como los volúmenes a tratar y la composición química de los efluentes es diferente, los humedales construidos presentan diferentes características de diseño. El objetivo de este trabajo fue comparar la eficiencia de los dos humedales construidos (HC1 y HC2) y determinar si los contaminantes son retenidos por el sedimento o por la plantas, conocimientos clave para llevar a cabo un correcto manejo de los humedales.
Metodología
Descripción de los humedales
Los dos humedales estudiados son de flujo superficial. Se construyeron para el tratamiento final de los efluentes de dos industrias metalúrgicas. Tanto en el HC1 como el HC2, el efluente sanitario de las industrias se trata junto con el efluente industrial. Antes de ingresar a los humedales, ambos efluentes reciben tratamiento primario previo. En trabajos en invernadero, se corroboró la hipótesis de que el enriquecimiento del efluente con nutrientes podría mejorar la tolerancia de las plantas a los metales (Hadad, Maine, Natale, & Bonetto, 2007), por lo que se decidió tratar en ambas industrias el efluente sanitario junto con el efluente industrial.
El HC1 está en operación desde hace 12 años, sus dimensiones son 50 m de largo por 40 m de ancho y 0.3-0.6 m de profundidad. Un tabique central obliga al efluente a recorrer el doble de distancia, logrando una relación largo:ancho de 5:1, que favorece la hidráulica del sistema. Se impermeabilizó con seis capas de bentonita compactada (lográndose una conductividad hidráulica de 10-7 m/s). Sobre la misma se colocó 1 m de tierra, donde se arraigaron las plantas. Inicialmente, se trasplantaron varias especies comunes de la zona, siendo Eichhornia crassipes y Typha domingensis las de mayor cobertura. Se tratan 100 000 l/día (efluente industrial de alto pH y salinidad, que contiene Fe, Cr, Ni y Zn con el efluente sanitario). El tiempo de residencia es entre 7 y 12 días. Después de atravesar el humedal, el efluente es conducido por un canal hacia una laguna de 1.5 ha, localizada en el mismo predio (Figura 1).

Figura 1 Fotografía de satélite donde se observa el humedal construido 1 (HC1), la laguna (a) e instalaciones de la empresa (b).
El HC2 se encuentra en operación desde hace cinco años, sus dimensiones son 7 m x 20 m y 0.5 m de profundidad (relación largo:ancho 3:1). Se impermeabilizó con una geomembrana de polietileno de alta densidad (PAD) de 1.5 mm de espesor. Sobre la misma se colocó una capa de tierra de aproximadamente 1.50 m, que sirve como sustrato de las plantas enraizadas. De acuerdo con la experiencia con el HC1, la especie seleccionada para este humedal fue Typha domingensis. Se trasplantaron ejemplares que crecen en la laguna existente en el predio de la empresa, lo que garantiza que las plantas se adapten al lugar. Las plantas se podaron a una altura aproximada de 30 cm, conservando los rizomas y se plantaron con una densidad de 3 plantas por m2. Para favorecer el desarrollo de las plantas en la zona más profunda y aumentar el recorrido del efluente a través del humedal, se construyeron taludes de 0.50 m de ancho, transversales al sentido de circulación del agua, sobre los cuales se plantaron los vegetales. El nivel de agua sobre ellos es de 0.30 a 0.40 m. En las otras zonas, la profundidad se encuentra entre 0.5 y 0.7 m. El humedal funcionó con efluente sanitario (previo tratamiento primario), efluente pluvial y efluente del circuito de enfriamiento durante un año. Luego comenzó a volcarse además el efluente industrial. El efluente industrial (que proviene de los efluentes del baño de cromado) y el efluente sanitario reciben tratamiento primario y son conducidos junto con el efluente del circuito de enfriamiento y el desagüe pluvial a una cámara ecualizadora, para luego ingresar al humedal. El volumen diario que ingresa al humedal es de unos 10 m3. El tiempo de residencia mínimo es de siete días; al cabo de ese lapso, el efluente, ya depurado, abandona el humedal por un canal de salida en forma de cascada, para volcar en una pileta de hormigón de 4 m x 2 m, con una profundidad de 40 cm. En este lugar se toman las muestras del efluente tratado para monitorear el sistema. El efluente tratado abandona la pileta a través de un salto de agua por rebase, llegando por un canal a una laguna adyacente en el mismo predio (Figura 2).
Muestreos y determinaciones analíticas
Se realizaron cada mes muestreos del efluente, sedimentos y vegetales, en las zonas de entrada y salida de ambos humedales. Se determinó su eficiencia a partir de las concentraciones del efluente de entrada y salida.
Las determinaciones analíticas en agua se llevaron a cabo de acuerdo con APHA (1998). La conductividad del agua se midió con conductómetro YSI, modelo 33, y el pH con un pHmetro Orion. El oxígeno disuelto (OD) se midió utilizando un oxímetro Hanna HI 91-46. El fósforo Total (PT), fósforo reactivo soluble (PRS) y nitrito se determinaron mediante técnicas colorimétri-cas, utilizando un espectrofotómetro UV-VIS Perkin Elmer Lambda 20. La concentración de nitrato y amonio en agua se determinó por po-tenciometría, utilizando un electrodo Orion Ion plus 93-07 y Orion 9512 BN, respectivamente. La determinación de demanda química de oxígeno (DQO) se realizó por el método de reflujo abierto y la demanda bioquímica de oxígeno (DBO5) por el test de cinco días. La determinación de alcalinidad y dureza se hizo por titulometría y la de sulfato por turbidimetría. Las determinaciones de Fe, Cr, Ni y Zn en agua se realizaron por espectrofotometría de absorción atómica (por llama o atomización electrotérmica, de acuerdo con la concentración de la muestra, Perkin Elmer AAnalyst 200).
En sedimentos y macrófitas (hojas y raíces) se determinaron las concentraciones de fósforo (P), y los metales cromo (Cr), níquel (Ni) y zinc (Zn). Las determinaciones se realizaron por es-pectrofotometría de absorción atómica, previa digestión con mezcla ácida de HCl:HNO3:HClO4 (5:3:2). En las mismas digestiones se determinó el PT mediante la técnica colorimétrica de Murphy y Riley (1962). Para evaluar la cantidad y forma química en la que estos contaminantes se acumulan en el sedimento, se realizó además el fraccionamiento químico de Cr, Ni y Zn, con base en el método de Tessier, Campbell y Bisson (1979). Este método se basa en sucesivas extracciones con soluciones ácidas, alcalinas o complejantes de forma secuencial, a fin de disolver las sales y óxidos, y extraer sus metales asociados.
Se utilizó el test T de a pares para comprobar si existía diferencia estadística entre las concentraciones de la entrada y la salida del humedal (p < 0.05).
Resultados y discusión
La Figura 3a muestra la cobertura de las macrófitas en el HC1 desde que comenzó a funcionar. Como se observa, Eichhornia crassipes se desarrolló con rapidez y fue la dominante, llegando a cubrir alrededor de 80% de la superficie del agua durante dos años, pero luego su cobertura comenzó a bajar. En octubre de 2005, se disminuyó el nivel de agua del humedal y se agregaron taludes de sedimento perpendiculares al sentido de circulación de la corriente, para favorecer el desarrollo de la especie enraizada Typha domingensis. Desde entonces, la misma aumentó su cobertura, convirtiéndose en la dominante durante los últimos 10 años. Su cobertura media fue de 80%. Las mermas en su cobertura se deben a que son podadas de forma periódica para favorecer su crecimiento. Durante los años 2009 y 2011, se observa una marcada disminución de la cobertura debido a que las plantas del humedal sufrieron una depredación por carpinchos (Hydrochoerus hydrochaeris). El humedal se presentaba como una " laguna con escasa vegetación, ya que la parte aérea de la vegetación había sido depredada por estos animales. Sin embargo, las raíces y rizomas de las plantas emergentes no habían sido dañadas (Maine et al., 2013), y las plantas se recuperaron luego de la colocación de un cerco perimetral que impidió el acceso de los animales al humedal.

Figura 3 Cobertura vegetal registrada a lo largo de los periodos estudiados en los HC1 (a) y HC2 (b).
La cobertura de Typha domingensis en el HC2 se muestra en la Figura 3b. Puede observarse que la misma llegó a 90% después de unos pocos meses. La disminución de cobertura que puede apreciarse durante los primeros meses de 2012 se debió a un volcado accidental de efluente sin el adecuado tratamiento. Sin embargo, se registró una rápida recuperación de las plantas. Es de resaltar que el ambiente se preservó debido a que los contaminantes quedaron retenidos en el humedal, cumpliendo una de las funciones para las que se le construyó. Como se expuso, ambos humedales sufrieron disminuciones en su cobertura de plantas debido a diferentes eventos, pero pudieron recuperarse demostrando la robustez de estos sistemas.
Ambos humedales funcionaron de modo eficiente, presentando altos porcentajes de remoción de contaminantes, disminuyendo no sólo los valores medios sino la variabilidad de los mismos, a pesar de la alta heterogeneidad del efluente de entrada (Cuadros 1 y 2). Si bien el pH de ambos efluentes fue diferente a la entrada, los valores a la salida no fueron significativamente diferentes. El efluente presentó menores valores de OD y mayores valores de conductividad en el HC1 que en el HC2. En el HC1, las concentraciones de nitrato y nitrito disminuyeron de manera satisfactoria, mientras que el amonio, PRS y PT presentaron bajos porcentajes de remoción, probablemente debido a las bajas concentraciones de OD. Las condiciones aeróbicas favorecen la retención de P a los sedimentos. En cuanto al amonio, las bajas concentraciones de oxígeno desfavorecen el proceso de nitrificación. Mientras que en el HC2, el amonio presentó la mayor remoción, el nitrito aumentó a la salida del humedal, debido al proceso de nitrificación en condiciones aeróbicas. Sin embargo, es de destacar que las concentraciones de nitrito medidas son bajas y se encuentran dentro de los valores exigidos por la legislación vigente (Ley 11220/94, Resolución 1089, Provincia de Santa Fe, Argentina). En general, en sistemas acuáticos, el amonio es removido por sedimentación, nitrificación, absorción por las plantas o volatilización. Por otra parte, la disminución de NO3- se debe de modo fundamental al proceso de desnitrificación y absorción por las plantas (Saunders & Kalff, 2001). Este proceso necesita energía, la cual se obtiene de la oxidación de la materia orgánica presente en las zonas anaeróbicas del sedimento. Las macrófitas pueden mejorar las condiciones de desnitrificación, pues suministran C orgánico, el cual puede ser usado de manera directa por las bacterias desnitrificantes o estimular la desnitrificación de forma indirecta, contribuyendo a disminuir el potencial redox (Weisner, Eriksson, Granéli, & Leonardson, 1994). DQO y DBO mostraron valores significativamente menores a la salida que a la entrada del humedal. Se observó además una importante disminución de sulfato, que es utilizado en los tratamientos primarios, por lo que ingresa a los humedales en altas concentraciones. En el efluente de entrada, las concentraciones de Cr y Zn fueron significativamente más altas en el HC2, y la de Fe y Ni en el HC1. En ambos humedales, la remoción de estos metales fue satisfactoria.
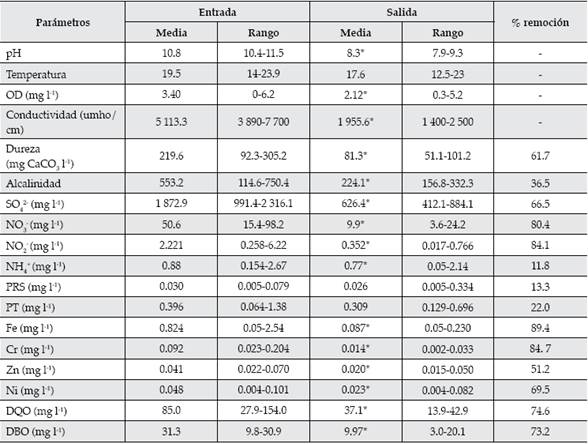
Cuadro 1 Concentraciones medias de los parámetros medidos en el efluente de entrada y salida del HC1. (*) indica diferencia estadísticamente significativa entre el valor del parámetro medido antes y después de atravesar el humedal.
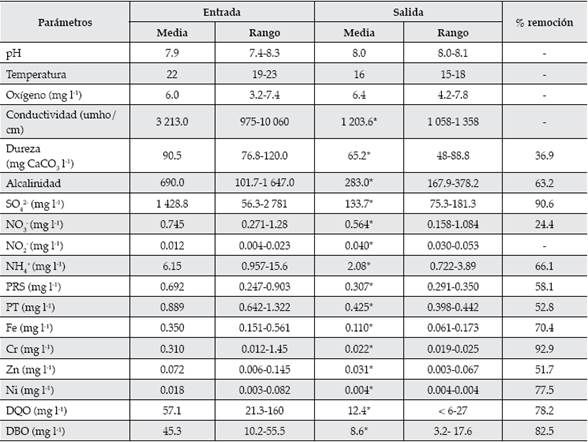
Cuadro 2 Concentraciones medias de los parámetros medidos en el efluente de entrada y salida del HC2. (*) indica diferencia estadísticamente significativa entre el valor del parámetro medido antes y después de atravesar el humedal.
Typha domingensis fue eficiente en la retención de metales, en especial en su zona radicular, lo que demuestra su capacidad de fitoestabilización (Cuadro 3). Esto es deseable, pues los metales quedan inmovilizados en el sedimento de los humedales. Las concentraciones de metales y P en tejidos fueron significativamente mayores en las plantas de la zona de entrada que en las de salida en ambos humedales, debido a que el efluente se va depurando a medida que circula. Tanto en la zona de entrada como en la de salida de HC2, la concentración de Cr en raíces de Typha domingensis presentó elevados valores. Esto se debió a que se produjo un volcado con altas concentraciones de Cr. En el HCl, a pesar del mayor tiempo de operación, las concentraciones de Cr en tejidos fueron significativamente menores.
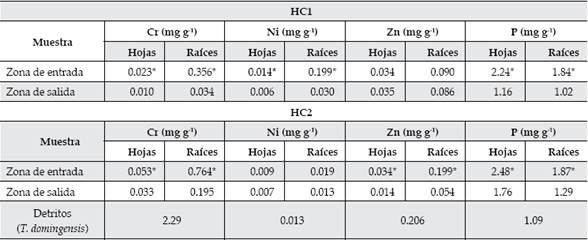
Cuadro 3 Concentración de P, Cr, Ni y Zn en tejidos de Typha domingensis. (*) indica diferencia estadísticamente significativa entre la concentración en los tejidos vegetales de la zona de entrada y la zona de salida.
La concentración de Ni en tejidos fue mayor en el HC1 debido a la presencia de este metal en el efluente tratado. Las concentraciones de Zn en las plantas de la entrada del HC2 mostraron mayores concentraciones que las del HC1, debido a que la concentración de Zn en el efluente fue mayor. Es importante resaltar que las macrófitas emergentes, además de acumular contaminantes en sus tejidos, influyen en los ciclos biogeoquímicos del sedimento a través de efectos en el potencial redox, debido a su capacidad para transportar oxígeno desde la raíz a la zona rizosférica (Barko, Gunnison, & Carpenter, 1991; Sorrell & Boon, 1992). De manera cuantitativa, esta capa oxigenada puede visualizarse por el color rojo asociado con las formas oxidadas del hierro en la superficie de las raíces y el sedimento circundante.
En la zona de entrada del HC2 se acumularon detritos de Typha domingensis, en los que se encontraron altas concentraciones de metales retenidos. Estos detritos están conformados fundamentalmente por hojas secas que quedan luego del invierno, lo cual es parte del ciclo anual de las macrófitas. Las macrófitas no sólo sorben contaminantes cuando están vivas. Schneider y Rubio (1999) demostraron a escala de laboratorio que la biomasa seca de tres macrófitas flotantes (Potamogeton lucens, Sal-vinia herzogii y Eichhornia crassipes) resultaron excelentes biosorbedores de metales pesados. Miretzky, Saralegui y Fernandez-Cirelli (2006) reportaron similares resultados cuando trabajaron con biomasa no viva de Spirodela intermedia, Lemna minor y Pistia stratiotes utilizando una solución multimetal (Cu2+, Pb2+, Cd2+, Ni2+ y Zn2+). Esto sería una importante ventaja para el manejo de humedales construidos, porque cuando las plantas mueren, como su degradación es lenta (Hammerly, Leguizamon, Maine, & Schiver, 1989), siguen reteniendo metales dentro del humedal, tal como se determinó de forma experimental. Estos detritos pueden ser removidos con facilidad del humedal para su disposición final, en caso de que fuera necesario.
Si bien las plantas retienen metales en sus tejidos, teniendo en cuenta no sólo la concentración sino también la masa, el sedimento fue el principal acumulador tanto de P como de metales. La sorción por el sedimento es el principal mecanismo de acumulación de contaminantes a largo plazo (Machemer, Reynolds, Laudon, & Wildeman, 1993; Wood & Shelley, 1999; Maine et al., 2009). En ambos humedales, el sedimento de la zona de entrada presentó concentraciones de Cr, Ni, Zn y P significativamente mayores que el sedimento de la zona de salida (Cuadro 4).
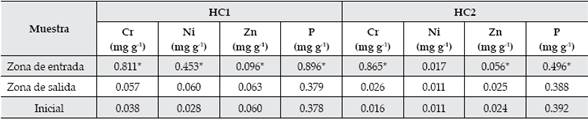
Cuadro 4 Concentración de P, Cr, Ni y Zn en sedimentos al final del periodo estudiado. (*) indica diferencia estadísticamente significativa entre la concentración en sedimento respecto a los valores iniciales.
Las concentraciones de la zona de salida no mostraron diferencias significativas con las concentraciones medidas al inicio del estudio, lo cual indicaría que los contaminantes fueron retenidos por el sedimento de la zona de entrada. Las concentraciones de Cr del sedimento de la zona de entrada de ambos humedales no mostraron diferencias significativas, a pesar del distinto tiempo de operación. El Ni se acumuló a la entrada del HC1, lo que no se observó en el sedimento del HC2, debido a que el efluente no contiene Ni. En el caso del Zn, el HC1 mostró las mayores concentraciones tanto en el sedimento de la zona de entrada como en el de salida. Sin embargo, el sedimento puede liberar los contaminantes si las condiciones ambientales cambian (Boström, Ahlgren, & Bell, 1985). A fin de determinar la perdurabilidad de la retención de contaminantes en los sedimentos de los humedales, se realizó una extracción se-cuencial que permite evaluar a qué compuestos químicos del sedimento se encuentran retenidos los contaminantes. En ambos humedales el Cr se acumuló en forma significativamente superior en la fracción de óxidos de Fe-Mn y en la materia orgánica (Cuadro 5).
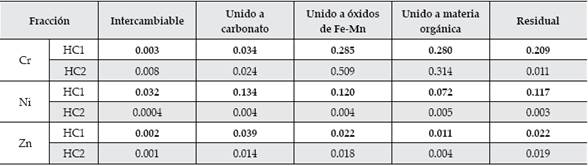
Cuadro 5 Fraccionamiento de Cr, Ni y Zn realizado en sedimentos al final del periodo estudiado en el HC1 y el HC2.
La materia orgánica tiene la capacidad de complejar y adsorber cationes debido a la presencia de grupos negativamente cargados (Laveuf & Cornu, 2009). El bajo Eh reduce el Cr(VI) a Cr(III), el cual precipita como Cr(OH) n (mayormente Cr(OH)3) (Guo, Delaune, & Patrick, 1997) o coprecipita con óxidos de Fe y Mn. La baja concentración de Ni en las distintas fracciones del sedimento del HC2 corrobora las bajas concentraciones de este metal en el efluente, indicando que no hubo acumulación en sedimento.
El Ni en el HC1, al igual que el Zn en ambos humedales, se acumularon en forma significativamente superior unidos a carbonatos, unidos a óxidos de Fe-Mn y en la fracción residual. La precipitación de carbonato está termodiná-micamente favorecida, y el Ni y el Zn pueden coprecipitar con el mismo. Los óxidos de Fe-Mn representan sumideros de metales pesados. La fracción residual significa formas litogénicas de unión fuerte de los metales, como en las estructuras cristalinas de las arcillas (Di Luca et al., 2011).
La secuencia de la extracción puede verse como una escala inversa de disponibilidad relativa de los metales. La fracción intercambiable de los tres metales, que es la más lábil y biodisponible, presentó en todos los casos una concentración significativamente menor a las demás. Por otra parte, es poco probable que los metales puedan liberarse al agua de las otras dos fracciones más lábiles (unidas a carbonatos y a óxidos de Fe-Mn), pues los efluentes proveen las condiciones (alto pH, alcalinidad, Fe, Ca y concentraciones iónicas) para que el sedimento continúe reteniendo Cr, Ni y Zn.
Conclusiones
En ambos HCs, las eficiencias de remoción de contaminantes fueron satisfactorias, ya que los HCs disminuyeron no sólo el valor medio, permitiendo cumplir con la ley 11220/94 de la Provincia de Santa Fe, Argentina, sino también la variabilidad de la concentración de los contaminantes de los efluentes, a pesar de la alta heterogeneidad del efluente de entrada.
Los metales y el P fueron removidos eficientemente en ambos humedales, quedando retenidos en la zona de entrada tanto en sedimento como en tejido vegetal.
Typha domingensis fue tolerante a los efluentes y eficiente en la retención de metales.
Los detritos de Typha domingensis acumularon altas concentraciones de metales. Estos detritos pueden ser removidos con facilidad para su disposición final.
Los humedales estudiados serían altamente eficientes en cuanto a la retención de los tres metales, pues se encuentran unidos a fracciones que no los liberarán al agua mientras las condiciones químicas y ambientales del sistema se mantengan.











 nueva página del texto (beta)
nueva página del texto (beta)



