En México, las cabras representan una fuente importante de proteínas1,2. Por ejemplo, el censo nacional de 2011 estimó una población de 9 millones de cabras3. El manejo de cabras es una práctica particularmente extendida en el estado de Puebla4,5, pero está menos desarrollada en Oaxaca6. La Reserva de la Biosfera Tehuacán-Cuicatlán (RBTC) en los estados de Puebla y Oaxaca en el centro de México se caracteriza por una alta biodiversidad de especies y endemismo7. Dentro del valle de Tehuacán-Cuicatlán, se estima que hay alrededor de 5,000 caprinocultores8, que practican principalmente la agricultura de subsistencia9. Las cabras han estado presentes desde su introducción durante el período colonial y actualmente la caprinocultura representa una de las principales actividades productivas en muchas poblaciones en y alrededor de la RBTC4. Al igual que en otras regiones áridas y semiáridas2,3, el sistema extensivo es la práctica principal en la RBTC. Este sistema consiste en dirigir los rebaños a lo largo de rutas fijas o migratorias para navegar en las colinas, los bordes de las carreteras y las áreas ribereñas4.
Partiendo de que la RBTC es un área natural protegida, es importante evaluar la influencia de las cabras en la estructura de la vegetación2,10,11 e identificar posibles interacciones competitivas con ungulados silvestres como el venado de cola blanca Odocoileus virginianus12. En este contexto, este estudio analiza la similitud en la planta consumida por los rebaños de cabras en el paisaje de la región de Cañada, Oaxaca, mediante el uso de métodos de agrupamiento de aglomerados jerárquicos. Para determinar las similitudes entre los rebaños en términos de las especies de plantas consumidas, en este estudio se utilizaron métodos de agrupamiento jerárquico aglomerado a través de análisis de grupos multivariados13. El objetivo del agrupamiento es reconocer los subconjuntos discontinuos en un entorno que a veces es discreto y, en la mayoría de los casos, se percibe como continuo en la ecología14. Específicamente, la agrupación consiste en dividir la colección de objetos en estudio. Para este propósito, se han empleado varios índices de similitud, como por ejemplo Sørensen, Jaccard y Morisita, para calcular la similitud o disimilitud entre los objetos de colección por pares. Los métodos de agrupación, como por ejemplo, vinculación simple, vinculación completa, aglomeración media y varianza mínima de Ward, se utilizan para aglomerar objetos en base a la distancia de pares dadas las similitudes o diferencias, dependiendo de cada caso13. Para interpretar y comparar los resultados de agrupamiento jerárquico, se calcularon las distancias de correlación cofenética para cada agrupamiento. Brevemente, el índice cofenético entre dos objetos en un dendograma es la distancia a la que los objetos se convierten en miembros del mismo grupo. La interpretación de este índice es similar al coeficiente de correlación r de Pearson14. Por lo tanto, para probar la hipótesis del presente estudio, se aplicaron métodos de agrupamiento jerárquico.
El estudio se realizó en la región de la Cañada en Oaxaca, dentro de la Reserva de la Biosfera Tehuacán-Cuicatlán (RBTC) en México. La RBTC se ubica en el extremo sureste del estado de Puebla y noreste de Oaxaca, entre los 17 ° 39 '- 18 ° 53' N y los 96 ° 55 '- 97 ° 44' O. Tiene 490,187 ha de superficie y la altitud varía entre los 600 y los 2,950 msnm. La temperatura media anual va de 18 a 22 °C, mientras que la precipitación anual varía entre 250 y 500 mm15. Los principales tipos de vegetación en la región son: matorral crasicaule dominado por cactus columnares del género Neobuxbaumia (8 % del territorio de reserva) y matorral rosetófilo (10 %), principalmente en el parte norte de la RBTC; mientras que el bosque seco tropical (29 %) domina principalmente en la región de Cañada; bosque de robles y pinos en las montañas altas (21 %); así como otros tipos de vegetación (10 %). El uso de la tierra es principalmente para la agricultura, ganadería y silvicultura (22 %)15.
El estudio se llevó acabo en ocho localidades: Coxcatlán, en el estado de Puebla, y Casa Blanca, Teotitlán, Toxpalan, Los Cues, Tecomavaca, Cuicatlán y Chicozapotes, en el estado de Oaxaca (Figura 1). En cada lugar, se siguió al mismo rebaño una vez durante la temporada de lluvias (de septiembre a noviembre de 2012) y una vez más en la estación seca (de abril a junio de 2013). La selección de estos rebaños dependió del interés de los criadores de cabras en participar en el estudio. Tradicionalmente, el sistema extensivo consiste en mover el rebaño diariamente a sitios de alimentación a lo largo de rutas predefinidas. Además, el tamaño de la bandada y el tiempo total de alimentación depende de la experiencia del propietario, entre otros factores6. En los sitios de estudio, el tamaño medio del rebaño y el tiempo de forraje fueron 70 cabras y 4.2 h, respectivamente.
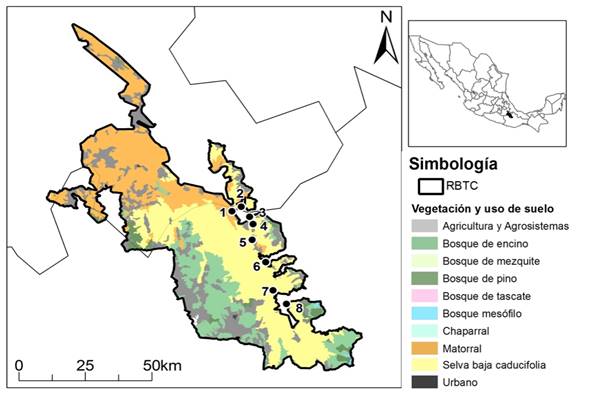
Figura 1 Localización geográfica de los sitios de estudio en La Cañada dentro de la Reserva de Biosfera Tehuacán-Cuicatlán, México. Sitios: Casa Blanca (1), Coxcatlán (2), Teotitlán (3), Toxpalan (4), Los Cues (5), Tecomavaca (6), Cuicatlán (7) y Chicozapotes (8)
Para determinar las principales plantas consumidas por las cabras, se observó directamente a los animales durante el pastoreo17. La selección de estos rebaños dependió del interés de los pastores en participar en el estudio. En el sitio de estudio, los criadores de cabras mueven sus animales para pastorear fuera de las aldeas casi todos los días. Por lo tanto, las cabras están acostumbradas a la presencia de personas, lo que elimina la posibilidad de sesgos durante la observación de las actividades de pastoreo18. Cada 20 min, se seleccionó un animal focal diferente y se registró el número de plantas de cada especie consumida durante un período de 10 min. Para cada rebaño, se registró el número de especies de plantas consumidas por el rebaño durante las estaciones lluviosa y seca18,19. El número de animales focales varió en función del tiempo de recorrido del rebaño muestreado (n= 57 y 58 cabras para las estaciones lluviosas y secas, respectivamente). Simultáneamente, se recolectaron plantas para la determinación taxonómica en el herbario y por otras fuentes20. Sin embargo, la topografía accidentada, la vegetación densa y la velocidad de movimiento de las cabras hicieron imposible recolectar todas las plantas consumidas.
Las cabras observadas individualmente no pueden ser réplicas verdaderas, ya que no toman decisiones de pastoreo de forma independiente unas de otras21. Por lo tanto, la información se agrupó considerando el rebaño como replicado. Se calculó la curva acumulativa del número de especies consumidas por las cabras durante las estaciones lluviosas y secas. Se empleó un método abreviado relativamente arbitrario del 75 % para determinar las principales especies de plantas y se utilizó una prueba de Ji cuadrada para evaluar las diferencias entre estaciones22.
Para determinar las similitudes entre los ocho rebaños en términos de las especies de plantas consumidas, se utilizaron métodos de agrupación jerárquica aglomerada a través de análisis de agrupación multivariada23. Para este propósito, las especies que representaron 75 % del total de plantas consumidas se emplearon para agrupar los rebaños. Este porcentaje de atajo es subjetivo, pero representa el punto en el que la curva acumulativa de la relación entre el número de especies consumidas comienza a alcanzar la asíntota. Los análisis se realizaron por separado para cada temporada. El índice de similitud Horn-Morisita se seleccionó para el número de plantas consumidas por las especies en este estudio. Se calcularon cuatro métodos de agrupamiento: enlace simple, enlace completo, aglomerante promedio (UPGMA) y varianza mínima de Ward23. Para examinar el contenido de especies de los grupos en función de las membresías del grupo, se utilizó el paquete vegano R23. Este paquete proporciona herramientas para la ecología de la comunidad descriptiva. Específicamente, tiene las funciones más básicas de análisis de diversidad, ordenación de la comunidad y análisis de disimilitud. Finalmente, los resultados de estos análisis se presentan como un mapa de color de la tabla doblemente ordenada de las plantas consumidas, con un dendrograma de sitios agrupados. Todos los análisis en este estudio se realizaron en la versión R 3.2.324.
Las cabras consumieron 82 y 65 especies durante la estación lluviosa y seca, respectivamente (Cuadro 1). Sin embargo, según la curva acumulativa, el 75 % de la dieta estaba constituida por 30 especies: 24 especies durante la temporada de lluvias y 20 especies en la estación seca (Figura 2). Las principales especies en ambas estaciones fueron Mimosa sp., Acacia cochiliacantha y Eleusine indica; durante la temporada de lluvias fue Dalea carthagenensis; mientras que en la estación seca fueron Prosopis leavigata, Opuntia sp. y Ceiba parvifolia, que difirió significativamente (Figura 3; P= 0.0001).
Cuadro 1 Lista de especies de plantas consumidas por cabras durante las estaciones de lluvia y seca en La Cañada, Oaxaca
| Especie | Abreviatura | Epoca lluviosa | Epoca seca | ||
|---|---|---|---|---|---|
| No. | % * | No. | % | ||
| Eleusine indica | Elin | 56 | 8.6 | 28 | 5.4 |
| Mimosa sp.1 | Misp | 51 | 7.8 | 50 | 9.6 |
| Acacia cochliacantha | Acco | 49 | 7.5 | 61 | 11.7 |
| Dalea carthagenensis | Daca | 27 | 4.2 | 10 | 1.9 |
| Agrostis stolonifera | Agst | 21 | 3.2 | 10 | 1.9 |
| Viguiera dentata | Vide | 16 | 2.5 | 18 | 3.4 |
| Cordia curassavica | Cocu | 16 | 2.5 | 5 | 1.0 |
| Eysenhardthia polystachya | Eypo | 14 | 2.2 | 8 | 1.5 |
| Senna wislizeni | Sewi | 14 | 2.2 | 10 | 1.9 |
| Aegopogon sp. | Aesp | 13 | 2.0 | 16 | 3.1 |
| Opuntia sp. | Opsp | 13 | 2.0 | 24 | 4.6 |
| Ceiba parvifolia | Cepa | 12 | 1.8 | 22 | 4.2 |
| Waltheria indica | Wain | 12 | 1.8 | 14 | 2.7 |
| Amphipterygium | Amad | 9 | 1.4 | 3 | 0.6 |
| adstringens | Ligr | 8 | 1.2 | - | - |
| Lippia graveolens | nd | 8 | 1.2 | - | - |
| nd | Phau | 8 | 1.2 | 2 | 0.4 |
| Phragmites australis | Papr | 7 | 1.1 | 16 | 3.1 |
| Parkinsonia praecox | Prle | 7 | 1.1 | 43 | 8.2 |
| Prosopis leavigata | Zipe | 7 | 1.1 | 11 | 2.1 |
| Ziziphus pedunculata | Buli | 7 | 1.1 | 2 | 0.4 |
| Bursera linanoe | Glgl | 7 | 1.1 | 2 | 0.4 |
| Glycyrrhiza glabra | nd | 6 | 0.9 | 5 | 1.0 |
| nd | Busp | 6 | 0.9 | 6 | 1.1 |
| Bursera sp. | Sapr | 5 | 0.8 | - | - |
| Sanvitalia procumbens | nd | 5 | 0.8 | 4 | 0.8 |
| nd | Crpr | 5 | 0.8 | - | - |
| Cyrtocarpa procera | Ledi | 5 | 0.8 | 12 | 2.3 |
| Leucaena diversifolia | nd | 5 | 0.8 | 6 | 1.1 |
| nd | Mame | 4 | 0.6 | - | - |
| Malpighia mexicana | Ipsp | 4 | 0.6 | 4 | 0.8 |
| Ipomoea sp. | Cili | 4 | 0.6 | 5 | 1.0 |
| Citrus limon | Pool | 3 | 0.5 | - | - |
| Portulaca oleracea | Brde | 3 | 0.5 | 3 | 0.6 |
| Brachiaria decumbens | Laca | 3 | 0.5 | 3 | 0.6 |
| Lantana camara | Sosp | 3 | 0.5 | - | - |
| Solanumzp | Agho | 3 | 0.5 | 2 | 0.4 |
| Agave horrida | Ages | 3 | 0.5 | 1 | 0.2 |
| Ageratina espinosarum | Lyac | 3 | 0.5 | 4 | 0.8 |
| Lysiloma acapulcense | Lyte | 3 | 0.5 | 4 | 0.8 |
| Lysiloma tergeminum | nd | 3 | 0.5 | - | - |
| nd | Pafo | 3 | 0.5 | - | - |
| Passiflora foetida | Plru | 3 | 0.5 | 7 | 1.3 |
| Plumeria rubra | Sotr | 3 | 0.5 | - | - |
| Solanum tridynamum | Tudi | 3 | 0.5 | - | - |
| Turnera diffusa | Maza | 2 | 0.3 | 2 | 0.4 |
| Manilkara zapota | Sila | 2 | 0.3 | - | - |
| Simsia lagascaeformis | Acfa | 2 | 0.3 | 12 | 2.3 |
| Acacia farnesiana | Anle | 2 | 0.3 | - | - |
| Antigonon leptopus | Busp1 | 2 | 0.3 | 2 | 0.4 |
| Bursera sp.1 | Caza | 2 | 0.3 | - | - |
| Calea zacatechichi | Guul | 2 | 0.3 | 7 | 1.3 |
| Guazuma ulmifolia | Lele | 2 | 0.3 | 9 | 1.7 |
| Leucaena leucocephala | Matr | 2 | 0.3 | 3 | 0.6 |
| Matelea trachyantha | Pawe | 2 | 0.3 | 3 | 0.6 |
| Pachycereus weberi | Pidu | 2 | 0.3 | 11 | 2.1 |
| Pithecellobium dulce | Plsp | 2 | 0.3 | - | - |
| Platanus sp. | Plbu | 2 | 0.3 | - | - |
| Plocosperma buxifolium | Posp | 2 | 0.3 | - | - |
| Polygonum sp. | Saal | 2 | 0.3 | 2 | 0.4 |
| Salix alba | Sppu | 2 | 0.3 | 11 | 2.1 |
| Spondias purpurea | Amhy | 1 | 0.2 | 4 | 0.8 |
| Amaranthus hybridus | Titu | 1 | 0.2 | 2 | 0.4 |
| Tithonia tuberformis | Alch | 1 | 0.2 | 2 | 0.4 |
| Allionia choisyi | Cnte | 1 | 0.2 | 1 | 0.2 |
| Cnidoscolus tehuacanensis | Acco | 1 | 0.2 | 1 | 0.2 |
| Acacia coulteri | Acme | 1 | 0.2 | 1 | 0.2 |
| Acrocomia mexicana | Agke | 1 | 0.2 | 1 | 0.2 |
| Agave kerchovei | Agpo | 1 | 0.2 | 1 | 0.2 |
| Agave potatorum | Bufa | 1 | 0.2 | 1 | 0.2 |
| Bursera fagaroides | Cesp | 1 | 0.2 | 1 | 0.2 |
| Ceiba sp. | Cepa | 1 | 0.2 | 2 | 0.4 |
| Celtis pallida | Cosc | 1 | 0.2 | - | - |
| Commicarpus scandens | Come | 1 | 0.2 | 1 | 0.2 |
| Condalia mexicana | Hete | 1 | 0.2 | 2 | 0.4 |
| Hechtia tehuacana | Mool | 1 | 0.2 | 1 | 0.2 |
| Moringa oleifera | Psan | 1 | 0.2 | 1 | 0.2 |
| Pseudosmodingium | Scba | 1 | 0.2 | 2 | 0.4 |
| andrieuxii | Soro | 1 | 0.2 | - | - |
| Schinopsis balansae | nd | 1 | 0.2 | 1 | 0.2 |
| Solanum rostratum | nd | 1 | 0.2 | 1 | 0.2 |
| nd | Asvi | - | - | 5 | 1.0 |
| nd | Pade | - | - | 2 | 0.4 |
| Astianthus viminalis | Stpr | 1 | 0.2 | 4 | 0.8 |
| Panicum decolorans | |||||
| Stenocereus pruinosus | |||||
(*) porcentaje del total en cada estación, (nd) no determinada.
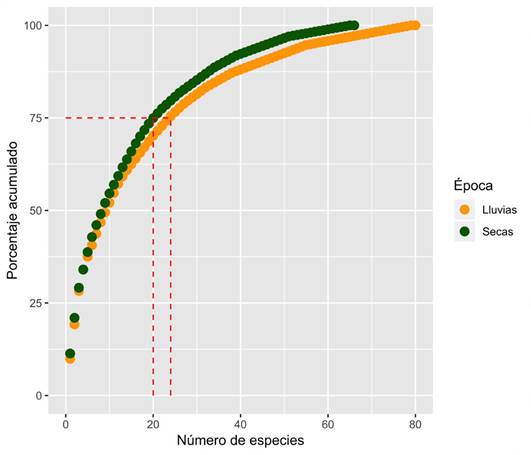
Figura 2 Curva acumulativa de la relación entre el número de especies consumidas por cabras durante las épocas de secas y de lluvias. Las líneas rojas punteadas muestran que, considerando un corte arbitrario del 75 %, 20 y 24 especies plantas fueron consumidas en cada época
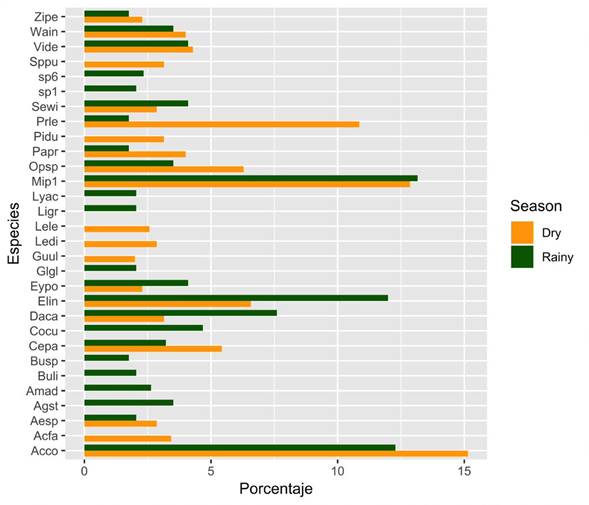
Figura 3 Porcentaje de las especies principales (75 % del total) consumida por cabras durante las estaciones secas y lluviosas
Los cuatro métodos de agrupamiento (enlace único, enlace completo, UPGMA y Ward) produjeron dendrogramas ligeramente diferentes. El cálculo del coeficiente de correlación de la distancia cofenética (r= 0.92 en la estación lluviosa y r= 0.86 en la estación seca) sugirió que UPGMA era el método de agrupamiento óptimo para los datos de la matriz. Los coeficientes de similitud de Horn-Morisita variaron entre las ubicaciones por pares y las estaciones (Cuadro 2). Mimosa sp. y Acacia cochiliacantha fueron las especies consumidas por todos los rebaños en ambas estaciones; mientras que Eleusine indica, Prosopis leavigata y Opuntia sp. fueron los siguientes más importantes, dependiendo de la temporada. Durante la temporada de lluvias, los rebaños de Tecomavaca y Teotitlán mostraron una menor similitud con respecto a los otros rebaños; mientras que, en la estación seca, los rebaños de Tecomavaca y Casa Blanca mostraron una menor similitud con respecto a las otras bandadas (Figura 4).
Cuadro 2 Coeficientes de similitud de Morisita-Horn entre pares durante las estaciones lluviosas y secas
| CB+ | CHI | COX | TOX | CUI | LCU | TEO | |
|---|---|---|---|---|---|---|---|
| Epoca lluviosa | |||||||
| CHI | 0.582 | ||||||
| COX | 0.707 | 0.72 | |||||
| TOX | 0.471 | 0.604 | 0.601 | ||||
| CUI | 0.536 | 0.640 | 0.694 | 0.685 | |||
| LCU | 0.549 | 0.723 | 0.664 | 0.800 | 0.499 | ||
| TEO | 0.353 | 0.547 | 0.401 | 0.481 | 0.401 | 0.495 | |
| TEC | 0.080 | 0.369 | 0.138 | 0 | 0.088 | 0.04 | 0.256 |
| Epoca seca | |||||||
| CHI | 0.610 | ||||||
| COX | 0.590 | 0.685 | |||||
| TOX | 0.480 | 0.678 | 0.611 | ||||
| CUI | 0.454 | 0.718 | 0.808 | 0.700 | |||
| LCU | 0.633 | 0.705 | 0.579 | 0.761 | 0.526 | ||
| TEO | 0.456 | 0.844 | 0.669 | 0.675 | 0.617 | 0.673 | |
| TEC | 0.381 | 0.477 | 0.35 | 0.463 | 0.615 | 0.275 | 0.511 |
Coxcatlán (COX), Casa Blanca (CB), Teotitlán (TEO), Toxpalan (TOX), Los Cues (LCU), Tecomavaca (TEC), Cuicatlán (CUI) and Chicozapotes (CHI).
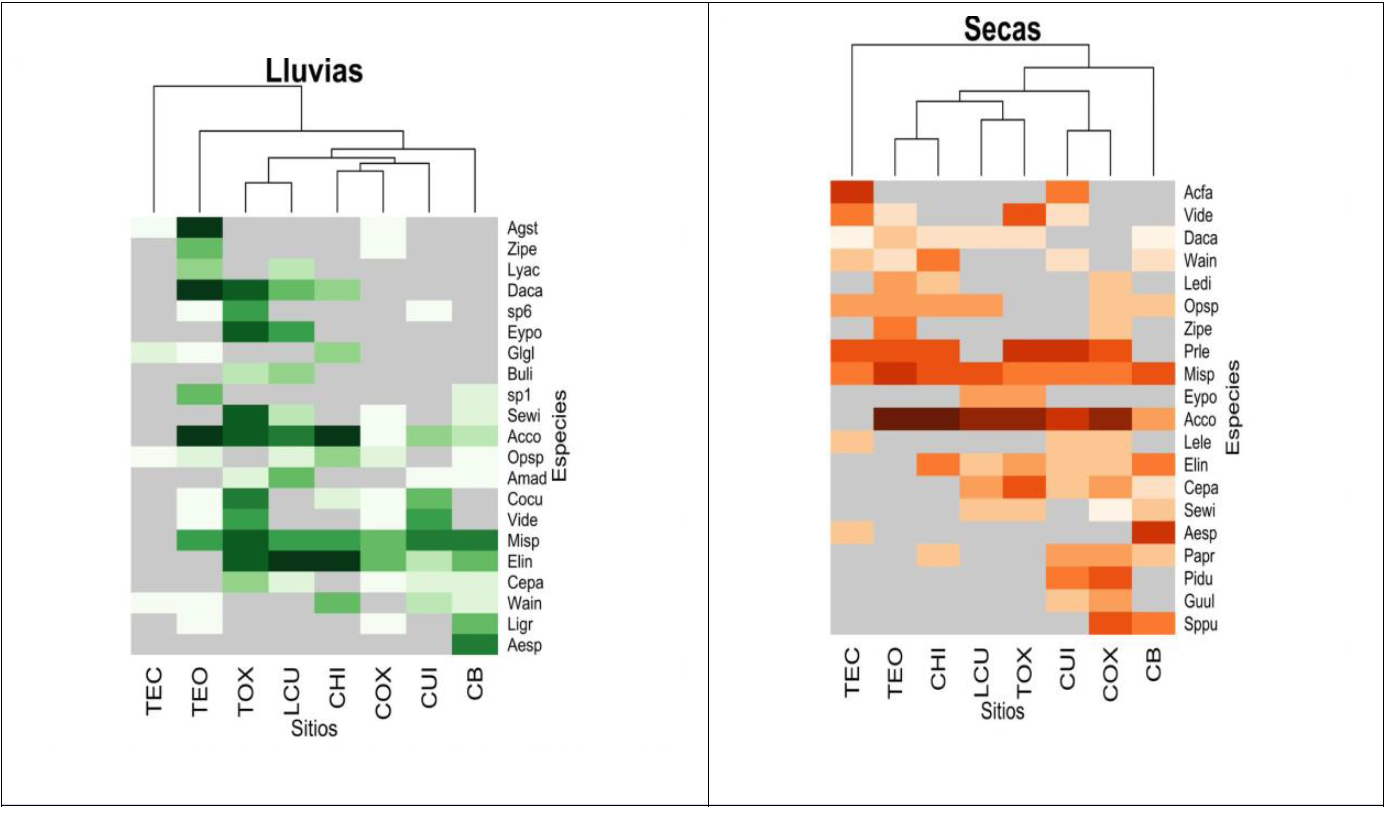
Figura 4: Clasificación de sitios de acuerdo con la similitud de las especies de plantas consumidas por las cabras durante las épocas de secas y de lluvias. El gradiente de color de intenso a ligero representa el grado de consumo de las especies. Un consumo muy bajo o nulo es representado por el color gris. En la parte superior se presenta el dendograma de los sitios estudiados clasificados por el método de agrupamiento UPGMA
La riqueza de especies de las plantas consumidas por las cabras en la región de La Cañada fue similar a la reportada en las regiones vecinas de la RBTC. Por ejemplo, en la región norte, entre 40 y 80 especies han sido consumidas por las cabras en las estaciones seca y lluviosa, respectivamente5,25. Entre los principales géneros consumidos por las cabras están Bursera, Jatropha, Fouquieria, Leucaena, Pithecellobium, Acacia guazuma y Prosopis25,26. En otra región tropical se ha informado que, de las 19 especies de árboles consumidas durante el año, Mimosa fue, con mucho, la especie seleccionada con mayor frecuencia; el pasto fue un componente importante de la dieta de la cabra en el período húmedo temprano, mientras que las hojas fueron una fuente importante de forraje durante los períodos secos28. En particular, la estación seca es la fase más crítica para el mantenimiento de los rebaños en esta región. Se ha documentado que las cabras pierden peso corporal significativamente durante este período debido a deficiencias en la proteína dietética y el fósforo29. Los animales ramonean, principalmente, las leguminosas durante la estación seca30.
Durante los períodos de escasez de forraje, las cabras suelen aumentar su esfuerzo de búsqueda a medida que disminuye la ingesta de nutrientes. El aumento del consumo de especies leñosas observado durante este período aumenta la presión de pastoreo sobre la vegetación local29. Por este motivo, como Opuntia spp. y Agave salmiana se han sugerido como suplementos dietéticos, junto con los frutos de Yucca periculosa y las vainas de Prosopis laevigata y Acacia subangulata combinadas con el tradicional rastrojo de maíz29. En otras regiones semiáridas, Prosopis laevigata y Opuntia sp. se utilizan como suplementos, teniendo en cuenta sus características nutricionales y su capacidad de crecimiento en condiciones de baja disponibilidad de agua31. En particular, los cladodios de los cactus y sus frutos se utilizan como fuente de alimentos de emergencia, proporcionando energía y agua en épocas de sequía, mientras que las plantas herbáceas proporcionan proteínas en la temporada de lluvias3.
Los rumiantes pequeños, como las cabras y ovejas, e incluso los animales silvestres como el venado de cola blanca, seleccionan su dieta de una amplia gama de especies de plantas, que difieren en términos de contenido de nutrientes y disponibilidad a lo largo del año19. Al final del otoño y principios del invierno, hay una falta de forraje de calidad, por lo que es necesario complementar la dieta de las cabras. La deficiencia de proteína cruda en la dieta de las cabras limita la digestión de fibra y minerales de los animales, lo que provoca un crecimiento lento, una función inmunológica reducida, anemia, edema y muerte32. De las especies de plantas consumidas, las que reúnen los mayores contenidos de proteínas (>20 %) son Ziziphus pedunculata, Prosopis laevigata y Ceiba parvifolia; otras especies que cumplen con los requisitos mínimos para las cabras son Mimosa sp., Viguiera dentata, Walteria indica y Solanum tridynamum33. La fibra contribuye significativamente a equilibrar los requerimientos nutricionales32,34. De las plantas analizadas, el mayor contenido de fibra lo presenta Agrostis stolonifera recolectado en la temporada de lluvias. De las plantas consumidas, aquellas con la mayor cantidad de fibra detergente neutro, la fibra detergente ácido fueron Mimosa sp., Opuntia sp., Viguiera dentata, Acacia farnesiana y Ziziphus pedunculata33. Las especies de arbustos de los géneros Prosopis, Mimosa y Acacia presentaron alta energía metabolizable en comparación con algunos árboles, cactus y plantas herbáceas3. La energía metabolizable en Prosopis y Acacia durante la estación seca superó los requerimientos de las cabras35.
Los métodos de agrupación jerárquica aglomerada a través de análisis de agrupación multivariable13 permitieron determinar similitudes entre los ocho rebaños en función de las especies de plantas consumidas. Estos métodos son comunes en estudios taxonómicos y ecológicos14. Con base en el 75 % de las principales especies consumidas y los mapas de calor, los ocho rebaños estudiados se clasificaron en diferentes grupos en cada temporada. Específicamente, el rebaño de Tecomovaca mostró una menor similitud en comparación con los otros rebaños. Las diferencias locales en la abundancia de especies de plantas y la presencia de algunas especies específicas explicaron el agrupamiento de los rebaños en las estaciones lluviosas y secas.
Finalmente, los resultados del presente estudio contribuyen a mejorar el conocimiento sobre los hábitos de pastoreo de las cabras en paisajes tropicales secos, donde la estacionalidad de los recursos es muy opuesta, como es el caso en la Cañada, que ha sido poco estudiada en comparación con las zonas áridas y semiáridas de México. Algunas de las plantas consumidas podrían ser utilizadas en la producción de ensilaje por microempresas familiares para alimentar a las cabras con plantas nativas. Debido a su disponibilidad en la zona, así como a su contenido nutricional, las especies Ceiba parvifolia, Waltheria indica, Prosopis leavigata, Solanum sp. y Sanvitalia procumbens podrían recolectarse en la temporada de lluvias para el henaje o el ensilaje y su posterior uso como complemento alimenticio en la estación seca o cuando los animales estén confinados. Estos resultados son valiosos para el manejo y la conservación de los hábitats estudiados, ya que fomentan la comprensión del hábitat de las cabras y la selección de la dieta en diferentes períodos.
Los rebaños de cabras estudiados consumieron de 65 a 82 especies de plantas durante las estaciones secas y lluviosas en la región de Cañada en el estado de Oaxaca. Sin embargo, las principales especies fueron Mimosa sp., Acacia cochiliacantha, Eleusine indica, Dalea carthagenensis, Prosopis laevigata, Opuntia spp. y Ceiba parvifolia. Algunas de estas especies han sido registradas en otras regiones. Los métodos de agrupación jerárquica aglomerada a través de análisis de agrupación multivariada permitieron la determinación de similitudes entre los ocho rebaños según la especie de planta consumida. Estos análisis muestran que las cabras de diferentes lugares en la región de Cañada consumieron especies de plantas relativamente similares.











 texto en
texto en 


