El clembuterol es un compuesto agonista de los receptores beta-adrenérgicos del músculo liso vascular, miometrial y bronquial, utilizado en la medicina veterinaria como broncodilatador y tocolítico1, y en algunos países está autorizado para su administración en el tratamiento de enfermedades respiratorias en humanos. Debido a que actúa como agente de repartición en animales mediante la eliminación de grasas y promoviendo la síntesis de proteínas, se provoca un acelerado crecimiento de la masa muscular, por lo cual este compuesto se utiliza de manera ilegal e indiscriminada con fines de producción cárnica de ganado bovino2-5. La ingesta de alimentos con residuos de clembuterol representa un riesgo para el consumidor, dado que puede derivar en graves intoxicaciones que se asocian con síntomas como palpitaciones, taquicardia, cefalea, temblor en extremidades, presión arterial elevada, ansiedad, nerviosismo, prurito, náuseas, dolor estomacal, fiebre, vómito, astenia y debilidad muscular, los cuales están acompañados de alteraciones de algunos parámetros hematológicos (leucocitosis) y bioquímicos, como electrolitos y glucosa6-10.
Con la finalidad de proteger a la población contra el riesgo por el consumo de alimentos contaminados por clembuterol, la Subsecretaría de Regulación, Control y Fomento Sanitario, dependiente de la Secretaría de Salud del Estado de Guerrero, ha implementado el Programa de Inocuidad Alimentaria (antes denominado Proyecto de Alimentos Potencialmente Peligrosos) desde el año 2005 basándose en la Norma Oficial Mexicana NOM-194-SSA1-200411, que consta de visitas de verificación en diversos establecimientos como mercados, rastros y tiendas de autoservicio, en las cuales se recolectan muestras de productos cárnicos para la detección de clembuterol por el Laboratorio Estatal de Salud Pública de Guerrero “Dr. Galo Soberón y Parra” (LESP-Guerrero) basado en el inmunoensayo enzimático Ridascreen Clenbuterol Fast (r-biopharm, Alemania)12. Este trabajo tuvo como finalidad evaluar los resultados de este programa para determinar su efectividad en la reducción del uso ilegal del clembuterol en la producción de ganado bovino para su consumo en el estado de Guerrero.
El estudio se realizó de manera retrospectiva, transversal, observacional y comparativa. Se llevó a cabo un análisis de los resultados del programa de vigilancia sanitaria del clembuterol en Guerrero implementado entre los años 2011 a 2015, para determinar la idoneidad del esquema de muestreo y establecer si existió una tendencia en los porcentajes de casos positivos a través de los años, además de la comparación entre los resultados obtenidos con respecto a la situación a nivel nacional. También, se aplicó un análisis regional y municipal del comportamiento del uso del clembuterol, así como un recuento de las intoxicaciones alimentarias derivadas de esta práctica ilegal.
De los establecimientos visitados por los verificadores sanitarios, se recolectaron muestras de hígado y músculo de bovinos, aproximadamente 250 g (de manera ocasional, se tomaron muestras de globo ocular y orina), para la detección de clembuterol. Las muestras se almacenaron en bolsas de polietileno y frascos de plástico con tapa de rosca (para muestras de orina), perfectamente identificadas y transportadas al LESP-Guerrero a una temperatura entre 2 y 8º C. La preparación de las muestras se realizó de la siguiente manera:
A) Hígado y músculo. Se depositaron 5 g de la muestra previamente triturada en un tubo para centrífuga de 50 ml (Corning, Estados Unidos de América), luego se agregaron 25 ml de HCl 0.05 M y se agitó mecánicamente por 20 min; posteriormente se centrifugó a 4,000 xg durante 15 min a una temperatura entre 10 y 15 ºC, y se transfirieron 18 ml de sobrenadante a otro tubo, al cual se le agregaron 2 ml de NaOH 0.5 M y se mezcló por 10 min. Finalmente, se adicionaron 4 ml de buffer de fosfatos (KH2PO4 0.5 M pH 3) y se homogenizó para dejarlo reposar otros 90 min a 2-8 ºC; posteriormente, se centrifugó y se tomaron 10 ml de sobrenadante y se pasaron a través de columnas de extracción en fase sólida tipo C18 (r-biopharm, Alemania).
B) Globo ocular. Las piezas se congelaron a -20 ºC durante 24 h para lisar el tejido. Después, se realizó la disección y el líquido obtenido se diluyó con agua destilada en una relación 1:2 y se centrifugó a 2,000 xg durante 5 min. Del sobrenadante se tomaron 20 µl para el inmunoensayo.
C) Orina. Estas muestras se analizaron directamente sin un tratamiento previo de extracción, y solamente cuando presentaron turbiedad se centrifugaron a 2,000 xg durante 5 min. El volumen adecuado para el análisis fue de 30 a 50 ml.
La extracción en fase sólida se llevó a cabo acondicionando la columna C18 con 3 ml de metanol y se agregaron 2 ml de un buffer de enjuague (KH2PO4 0.05 M pH 3); se aplicó el sobrenadante y se agregaron 3 ml de buffer de enjuague; la columna se secó y eluyó lentamente con 1 ml de metanol grado HPLC (Honeywell Burdick and Jackson, Estados Unidos de América); la concentración del extracto se realizó a 50 a 60 ºC bajo una corriente de aire; el residuo seco se reconstituyó con 400 µl de agua grado HPLC (Sigma Aldrich, Suiza).
El análisis de los extractos se realizó por medio de un inmunoensayo enzimático competitivo (Ridascreen Clembuterol Fast, r-biopharm, Alemania)12 con lectura en un espectrofotómetro UV-Vis iMark (Bio-Rad Laboratories Inc, Estados Unidos de América) a 450 nm; la concentración de clembuterol se expresó en ng/kg o ppt (partes por trillón). De conformidad con la NOM-194-SSA1-200411, se consideraron como muestras contaminadas, detectadas o positivas, aquéllas que presentaron concentraciones mayores a 2,000 ng/kg; las muestras con resultados inferiores se interpretaron como no detectadas con clembuterol. Sobre la calidad analítica del método, se cumplieron los criterios de aceptación descritos en el inserto del reactivo12; asimismo, en cada corrida se analizaron controles comerciales y muestras con concentraciones conocidas, obteniendo siempre los valores esperados. Cabe mencionar que este Laboratorio está facultado por la Comisión Federal para la Protección contra Riesgos Sanitarios (COFEPRIS) como Tercero Autorizado para la realización de pruebas analíticas en materia de regulación y control sanitario con base al cumplimiento de los requisitos técnicos y de gestión de calidad establecidos en la NMX-EC-17025-IMNC-200613.
Se analizaron estadísticamente los resultados obtenidos del programa mediante un estudio de correlación (coeficiente r de Pearson) entre el número de especímenes recolectados con variables como la población y el volumen de producción de carne en canal de los municipios visitados. Posteriormente, se calculó el porcentaje de muestras contaminadas de acuerdo a la Jurisdicción Sanitaria (JS) de procedencia y el año de estudio; se elaboraron gráficas que relacionaron los porcentajes anuales de muestras contaminadas en Guerrero versus los obtenidos a nivel nacional, así como con el número de personas intoxicadas durante el periodo estudiado. Los resultados calculados para las JS y los municipios se representaron en mapas temáticos. Estos análisis y gráficos fueron realizados con los programas SPSS versión 21 (IBM Corporation, Estados Unidos de América) y ArcGIS versión 9.3 (ESRI, Estados Unidos de América).
En el análisis de resultados se encontró que la recolección de muestras no fue uniforme en lo que se refiere a la cantidad, ya que en 2011 se analizaron más productos cárnicos que en cualquier otro año (n= 172), mientras que para el 2012 y 2013 disminuyeron de manera sustancial a 91 y 105, respectivamente. En el 2014 existió una recuperación de esta variable y tuvo una progresión en el año posterior (Cuadro 1). Este comportamiento puede deberse a que el presupuesto destinado para operar el programa de vigilancia sanitaria es diferente en cada año, y las actividades que se destinan implican gastos, lo que afecta directamente en la planeación de las visitas de verificación a las tiendas de autoservicio, rastros y expendios de carne. Además, la dinámica de aparición de muestras contaminadas con clembuterol provocan un rediseño de las estrategias para obtener mejores resultados que inhiban esta actividad ilegal en la producción pecuaria; esto significa poner énfasis en la vigilancia especialmente en las localidades que han presentado casos positivos, dejando en segundo término aquellas en las que no se ha observado este problema. Mediante la aplicación de este enfoque basado en riesgos se logra una eficacia del programa, y una reducción en la utilización de recursos tanto económicos como humanos.
Cuadro 1: Muestras contaminadas / recolectadas y porcentaje de muestras contaminadas por año (% anual) y jurisdicción sanitaria (JS)
| 2011 | 2012 | 2013 | 2014 | 2015 | Total | JS (%) | |
|---|---|---|---|---|---|---|---|
| Tierra Caliente | 4/25 | 0/9 | 6/26 | 2/24 | 1/23 | 13/107 | 12.1 |
| Norte | 4/22 | 2/12 | 0/10 | 6/19 | 4/30 | 16/95 | 16.8 |
| Centro | 2/36 | 1/8 | 0/19 | 0/21 | 4/32 | 7/116 | 6.0 |
| Montaña | 0/9 | 2/4 | 0/11 | 0/11 | 1/7 | 3/42 | 7.1 |
| Costa Grande | 4/28 | 1/16 | 0/11 | 0/13 | 0/24 | 5/92 | 5.4 |
| Costa Chica | 0/17 | 0/12 | 0/8 | 5/20 | 0/24 | 5/81 | 6.2 |
| Acapulco | 8/35 | 1/30 | 0/18 | 2/21 | 1/21 | 12/125 | 9.6 |
| 12.8 | 7.7 | 5.7 | 11.6 | 6.8 | 9.3 | ||
| Annual, % | n=172 | n=91 | n=105 | n=129 | n=161 | n=658 |
Con respecto al tipo de muestras, hubo cierta igualdad en la cantidad recolectada tanto de hígado (n= 329) como de músculo (n= 310) (Cuadro 2). La COFEPRIS a través de la Comisión de Operación Sanitaria establece en su Instrucción de trabajo14 que en las visitas de verificación sanitaria a los rastros, carnicerías y tiendas de autoservicio deben colectarse los productos cárnicos por triplicado, una muestra para su análisis en el Laboratorio Estatal, otra para resguardo de la Subsecretaría de Regulación Sanitaria y la tercera para el propietario del establecimiento regulado, por si tuviese alguna inconformidad con el resultado, pueda recurrir con base a su derecho, al análisis en otro laboratorio tercero autorizado del país (para que de esa manera se proceda a la emisión de un dictamen definitivo por parte de la autoridad sanitaria correspondiente).
Cuadro 2: Porcentaje de muestras detectadas con clembuterol por tipo de muestra y año correspondiente
| Año | Tipo de muestra |
Resultado | Total | % | |
|---|---|---|---|---|---|
| No detectado | Detectado | ||||
| 2011 | Hígado | 89 | 15 | 104 | 16.9 |
| Músculo | 61 | 7 | 68 | 11.5 | |
| 2012 | Hígado | 53 | 7 | 60 | 13.2 |
| Músculo | 31 | 0 | 31 | 0 | |
| 2013 | Hígado | 37 | 1 | 38 | 2.7 |
| Músculo | 56 | 4 | 60 | 7.1 | |
| Globo ocular | 6 | 1 | 7 | 16.7 | |
| 2014 | Hígado | 53 | 4 | 57 | 7.6 |
| Músculo | 61 | 11 | 72 | 18.0 | |
| 2015 | Hígado | 67 | 3 | 70 | 4.5 |
| Músculo | 74 | 5 | 79 | 6.8 | |
| Orina | 9 | 3 | 12 | 33.3 | |
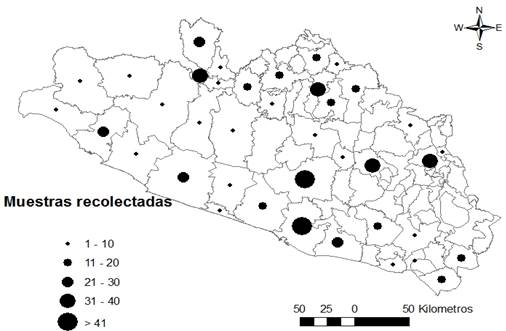
Entre las regiones, la recolección se llevó a cabo de manera similar con excepción de la Montaña, en la que se obtuvieron solamente 42 muestras (Cuadro 1). Las condiciones de difícil acceso a las localidades pueden ser un factor importante que limite la operación del programa en esta zona del Estado, tomando en cuenta además que el transporte y conservación de las muestras deben realizarse a una temperatura entre 2 y 8 ºC, y como los tiempos de traslado hacia el laboratorio suelen ser prolongados, es posible que la red fría se rompa en algún momento perjudicando así la calidad de la muestra, siendo éste otro factor que puede incidir en la escasa recolección observada en esta región. En lo que respecta a los municipios, se visitaron un total de 39 de los 81 que conforman el Estado (48.1 %), concentrándose la atención en aquellos con una mayor población e importancia, tanto turística como económica y política, como son Acapulco (n= 119), Chilpancingo (n= 73), Iguala (n= 39), Tlapa (n= 31), Ciudad Altamirano (n= 34) y Zihuatanejo (n= 29) (Figura 1). En un análisis de correlación entre el número de habitantes en los municipios visitados y la cantidad de productos cárnicos recolectados en estos, se obtuvo una alta relación entre estas dos variables (r= 0.912, P<0.001), lo cual es lógico, ya que en la medida que existen más consumidores la vigilancia sanitaria debe aumentarse con la finalidad de prevención y control de riesgos. No existió una relación entre los niveles de producción de carne en canal de los municipios, con las muestras obtenidas en estos (r= -0.045), es decir, la recolección de muestras no se vio influenciada por los altos volúmenes producidos en algunos municipios. Con base a lo anterior, es recomendable ampliar la cobertura del muestreo en los municipios y regiones para tener más posibilidades de detección de casos positivos, y así tener elementos para la toma de decisiones que coadyuven a lograr mejores resultados en la vigilancia sanitaria del clembuterol.
El porcentaje de muestras positivas, es decir, la relación entre la cantidad de productos cárnicos contaminados con clembuterol con respecto al total de los productos cárnicos recolectados, presentó una tendencia a la baja con el transcurso de los años (Cuadro 1). Dicha disminución se presentó de manera gradual, con la excepción del año 2014 en el que se obtuvo un ligero incremento (11.6 %). Al final, este porcentaje se vio reducido aproximadamente a la mitad de lo que se observó inicialmente (2011= 12.8 % vs 2015= 6.8 %). Lo anterior indica un logro importante del programa de vigilancia del clembuterol en la reducción de riesgos sanitarios para los consumidores de carne de ganado bovino de esta entidad federativa. El porcentaje global (9.3 %) fue menor a lo obtenido por Chávez et al15 en un estudio similar correspondiente a los años 2005-2010, cuyo porcentaje anual promedio fue de 13.1 %, con valores en 2005 de hasta casi 24 % de muestras contaminadas con este agente químico. No obstante, estas cifras siempre estuvieron por encima de lo obtenido a nivel nacional (media Guerrero= 9.5 %, media Nacional= 5.8%; P= 0.1) (Figura 2), y en algunos casos como en el 2011, el porcentaje de muestras positivas en Guerrero fue el doble con respecto al resto del país (12.8 vs 5.1 % respectivamente), por lo que debe plantearse una meta de revertir este comportamiento en el mediano o corto plazo para tener niveles de contaminación más acordes a la realidad nacional en torno a este problema.
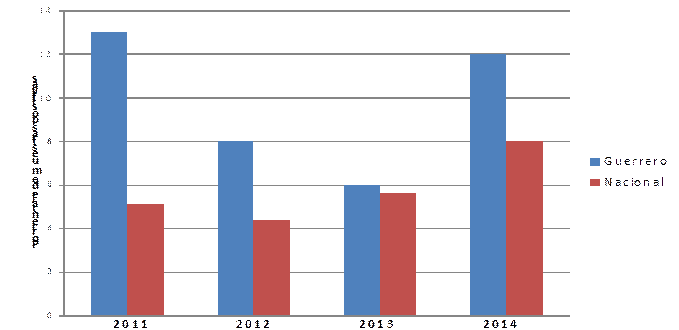
Figura 2: Comparación de los porcentajes de muestras positivas en Guerrero y a nivel nacional durante 2011-2014
El globo ocular y la orina no fueron las muestras de elección en el esquema de muestreo del programa, sin embargo, como se observa en el Cuadro 1, se tuvo más éxito en la detección de clembuterol en estas muestras biológicas, en las que sólo bastaron siete especímenes de globo ocular para encontrar residuos del fármaco en uno de estos, y del mismo modo, con tan sólo nueve muestras de orina se detectaron hasta tres de ellas con el compuesto de interés. Esto tiene su fundamento en la farmacocinética de la molécula, ya que se han reportado altas concentraciones de clembuterol en retina después de su administración a niveles terapéuticos, y por lo tanto, una alta permanencia16. De la misma manera, se excreta lentamente a través de la orina y puede encontrarse en los 10 días siguientes a la exposición a este agente17,18, en tanto que en sangre solamente puede ser detectado durante cinco días posteriores a su ingesta19. A pesar de la evidencia presentada en éste y otros estudios16,20, no se ha optado por recolectar muestras de globo ocular por no cumplirse la condición de obtener tres especímenes del mismo animal (por razones lógicas) tal como lo marca la Instrucción de trabajo de la COFEPRIS14. Asimismo, las muestras de orina únicamente se obtienen en operativos especiales de la autoridad sanitaria en los rastros, siendo esta actividad no muy frecuente, ya que responde a casos particulares en los que existe alguna queja pública o se tienen antecedentes de introducción de carne contaminada en estos establecimientos.
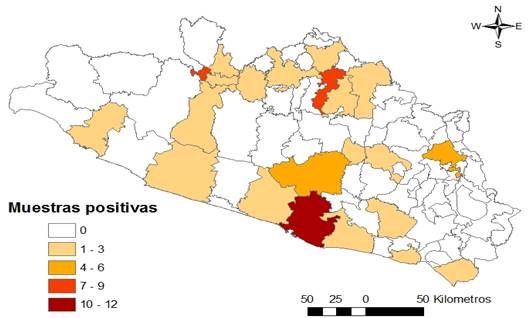
En el análisis regional, las principales JS que contribuyeron con mayores porcentajes de muestras positivas fueron la Norte y Tierra Caliente con 16.8 y 12.1 %, respectivamente, cuya presencia de este contaminante químico fue constante en casi todos los años estudiados. En Acapulco, a pesar de la intensa vigilancia realizada (fue el sitio en el que se recolectaron más muestras que en cualquier otra JS) también presentó casos positivos de manera reiterada, aunque en un menor grado que las jurisdicciones mencionadas, con 9.6 %. En las JS restantes, la situación se encontró más controlada y con aparición de casos positivos de manera esporádica. Se detectó el clembuterol en 22 municipios, entre los que se destacan aquellos que tienen una mayor población como Acapulco, Chilpancingo, Iguala, Ciudad Altamirano y Tlapa, y es justamente en estos donde se encontraron más casos de muestras contaminadas (Figura 3).
Se registraron algunos casos de intoxicaciones humanas por el consumo de productos cárnicos contaminados con clembuterol, con tres en 2011, cinco en 2012 y cuatro al año siguiente, mientras que para los demás años no ocurrieron eventos de esta naturaleza (Figura 4). De estos casos se registraron seis en Acapulco, tres en Iguala, dos en Chilpancingo y uno en Chilapa, municipios en los que, como se mencionó, se han detectado la mayor cantidad de muestras positivas, con excepción de Chilapa que sólo presentó una muestra positiva, la cual estuvo directamente relacionada con una intoxicación suscitada en 2012. Como en muchos de los padecimientos de salud en México y otros países, hay un sub-registro de las intoxicaciones alimentarias por clembuterol debido posiblemente a una falta de información en el primer nivel de atención para reconocer la sintomatología que implique un estudio más profundo de los casos para llegar a un adecuado diagnóstico21, a lo que se suma el hecho de que las personas no acuden a los centros de salud para recibir algún tipo de tratamiento, ya sea por falta de recursos económicos o por la escasa oferta de servicios médicos institucionales, por lo que se estima que la cantidad real de estos casos es de una mayor magnitud.
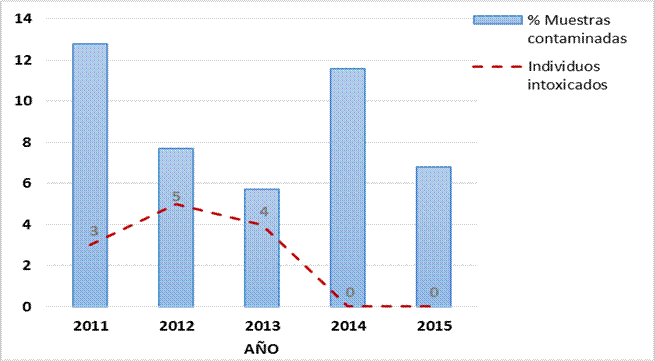
Figura 4: Porcentaje de muestras contaminadas (barras) y casos de intoxicaciones (línea punteada) en cada año estudiado
En virtud de que aún existe la presencia de este contaminante químico en los alimentos, es importante mantener y fortalecer el monitoreo mediante la ampliación de las visitas a los establecimientos, así como dar seguimiento a los casos de muestras contaminadas mediante la cadena de trazabilidad para ubicar a los productores de ganado y sensibilizarlos sobre las consecuencias negativas para la salud humana de estas prácticas inadecuadas de producción pecuaria.
Por último, es indispensable la coordinación intersectorial para combatir este problema; cada institución desde el ámbito de sus atribuciones y responsabilidades debe diseñar un esquema integral para la procuración de buenas prácticas de producción desde sus etapas iniciales, que inhiba las intenciones de los ganaderos de obtener mejores rendimientos a costa de la utilización de sustancias peligrosas para el consumidor. Del mismo modo, cuando exista evidencia suficiente sobre el uso ilegal del clembuterol, deben ejecutarse actos de autoridad con base a la legislación vigente y llegar hasta las últimas consecuencias, partiendo del hecho de que esta actividad supone un atentado contra la salud pública, y en ese tenor debe ser sancionada sin reserva ni excepción alguna.
A la luz de estos resultados, y en comparación con años anteriores, es justo mencionar el trabajo que ha realizado la Secretaría de Salud de Guerrero en torno a este fenómeno, con una disminución sustancial de los casos positivos, dando como consecuencia un número menor de intoxicaciones alimentarias. No obstante, debe mantenerse constante la operación del programa de vigilancia para tener como objetivo siguiente erradicar el uso ilegal de clembuterol para proteger a la población contra los riesgos sanitarios relacionados.











 text in
text in